Инфильтрация эпидермиса что это
Обновлено: 25.04.2024
Гистологическая картина солнечного кератоза. Виды солнечного кератоза.
Гистологически солнечный кератоз, по мнению W. Lever, — это дисплазия кератиноцитов или плоскоклеточный рак in situ. При микроскопическом исследовании наблюдается значительный гиперкератоз эпидермиса. Паракератоз выражен слабее и может вообще отсутствовать. Эпидермис — с папилломатозными и акантотическими разрастаниями, хотя рядом с последними могут наблюдаться участки резкой атрофии. Эти изменения, выраженные в различной степени и сочетаниях, приводят к чрезвычайному многообразию гистологических проявлений.
Дисплазия кератиноцитов также имеет различную степень выраженности и распространенности. В некоторых случаях могут наблюдаться изменения, захватывающие всю толщу эпидермиса и имитирующие болезнь Боуэна (плоскоклеточный рак in situ). В дерме наблюдается базофильная дегенерация, хронический воспалительный инфильтрат.
На ранних стадиях участки паракератоза лежат над слегка акантотичным эпидермисом, в котором отмечается атипия клеток базального и прилежащих к нему слоев в виде дискератоза и увеличения ядер. Проникновение в строму не выражено, отмечается очаговая лимфоидная инфильтрация, эластоз.
Более выраженный пара- и гиперкератоз с формированием структур кожного рога наблюдается при далеко зашедших случаях. В подобных наблюдениях клеточная атипия распространяется на всю толщину пидермиса, а в ряде случаев возможно и присутствие начальной дермальной инвазии.
Выделяют 5 гистологических типов солнечного кератоза: гиперпластический, атрофический, бовеноидный, акантолитический и пигментный, между которыми могут быть переходы и комбинации. При каждом типе солнечного кератоза на фоне выраженной атрофии эпидермиса обнаруживают очаг гиперкератоза ортокератозной структуры, под которым отмечается пролиферация атипичных базальных клеток, образующих участки в виде тяжей, проникающих в глубь дермы. В дерме выражена дегенерация соединительной ткани. В ее верхней части обычно присутствует довольно плотный воспалительный инфильтрат, состоящий, главным образом, из лимфоидных элементов с множеством плазматических клеток. В верхних участках дермы также обнаруживают явления солнечного эластоза. В эпидермисе — участки пролиферапии шиповатых клеток с выраженным ядерным полиморфизмом, диском-плексацией клеток, но сохраненной базальной мембраной.
Гиперпластический тип солнечного кератоза (син.: пролиферируюший гиперпластический кератоз, гипертрофический кератоз) выглядит как красный овальный шелушащийся очаг, клинически напоминающий типичный солнечный кератоз, но увеличивающийся в диаметре до 3-4 см, границы образования нечеткие. Гистологически отличается выраженными гиперпластическими и пролиферативными изменениями. При этом типе солнечного кератоза выраженный гиперкератоз обычно перемежается с участками паракератоза, может быть умеренный папилломатоз. Эпидермис неравномерно утолщен, с проникновением тяжей эпидермальных клеток в верхнюю часть дермы, но без признаков истинной инвазии. Некоторые кератиноциты демонстрируют плеоморфизм и атипию ядер. Ядра крупные, неправильной формы, гиперхромные. особенно в базальном слое.
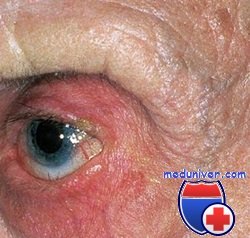
Солнечный кератоз век
Не которые кератиноциты в средней части эпидермиса проявляют незрелую кератинизацию, что приводит к формированию дискератотических клеток или апоптотических телец, характеризующихся гомогенной эозинофильной цитоплазмой с наличием ядер или без них.
В отличие от эпидермальных кератиноцитов, пенетрирующие в эпидермис клетки волосяных фолликулов и эккринных протоков не изменены и имеют нормальный характер кератинизации. Иногда эти клетки, подобно зонтику, располагаются над атипичными клетками эпидермиса. Однако в отдельных случаях атипичные кератиноциты распространяются вниз по наружной стороне фолликулярной воронки волоса до уровня протока сальной железы или, что бывает реже, вдоль протока экк-ринной железы.
Вариантом гипертрофического типа солнечного кератоза является лихеноидный солнечный кератоз. Лихеноидная форма солнечного кератоза представлена солитарными или множественными бессимптомными ороговевшими папулами, цвет которых варьируется от ярко-красного до фиолетового или коричневого; клинически напоминает элемент красного плоского лишая. Обычно встречается на разгибательных поверхностях предплечий и лиц
Гистологически отмечаются ядерная атипия. неправильный акантоз, гиперкератоз, вакуолизация базальных клеток, дегенерация базального слоя и лентовидный «лихеноидный» инфильтрат в тесной связи с эпидермисом; в верхней части дермы — множество эозинофильных гомогенных апоптотических телец (телец Civatte).
Подобная гистологическая картина солнечного кератоза элементов напоминает красный плоский лишай и доброкачественный лихеноидный кератоз. Важное диагностическое значение имеют результаты гистологического исследования: наличие проявлений солнечного кератоза, в первую очередь, диспластических изменений эпидермиса, позволяет поставить правильный диагноз.
В редких случаях гипертрофический тип солнечного кератоза, наряду с атипией ядер в нижней части эпидермиса, сопровождается участками эпидермолитического гиперкератоза в его верхних отделах. Подобные изменения описывают также при врожденной буллезной ихтиозиформной эритродермии, линейном эпидермальном невусе или могут присутствовать в различных очагах как случайный эпидермолитический гиперкератоз. В участках эпидермолитического гиперкератоза в верхней части дермы наблюдаются светлые пространства вокруг ядер и утолщенный зернистый слой с крупными неправильно очерченными кера-тогиалиновыми гранулами. Эпидермоли-тический гиперкератоз также встречается в участках солнечного хейлита.
Атрофический тип солнечного кератоза характеризуется атрофией эпидермиса, незначительным гиперкератозом, атипией клеток базального слоя, наличием узких акантолитических тяжей в поверхностных отделах дермы. Нередко над базальным слоем эпидермиса обнаруживаются щели и лакуны, что напоминает болезнь Дарье. Атипичный базальный слой может также окружать в виде клеточной мантии верхнюю часть пилосебо-цейных комплексов и потовых протоков, эпителий которых выглядит не измененным.
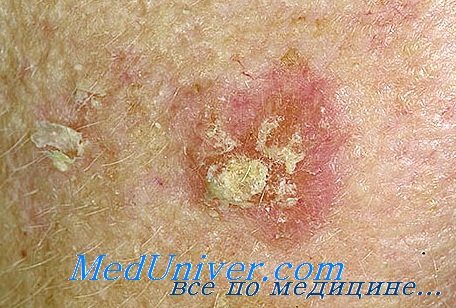
Солнечный кератоз (актинический кератоз)
Бовеноидный тип солнечного кератоза гистологически неотличим от болезни Боуэна. На этой стадии развития солнечный кератоз расценивается как рак in situ.
Акантолитический тип отмечен в 17-27% случаев солнечного кератоза. При этом типе заболевания непосредственно над атипичными клетками, формирующими базальный слой, имеются щели или лакуны, подобные описываемым при болезни Дарье. Они формируются в результате анапластических изменений в нижней части эпидермиса, приводящих к дискератозу и потере межклеточных мостиков. В щелях может присутствовать небольшое количество акантолитических клеток. Над акантолитическими шелями в эпидермисе выявляют различную степень атипии, но она менее выражена, чем в базаль-ном слое. Чаще измененные клетки от базаль-ного слоя распространяются в верхнюю часть дермы в виде коротких трубчатых структур,
Посколько акантолизу предшествуют клеточные изменения, он описывается как вторичный акантолиз, в отличие от первичного, наблюдаемого при акантолитической пузырчатке и болезни Дарье.
Акантолиз бывает фокусным или диффузным, эпидермальным или дермальным. Супрабазальный акантолиз также может отмечаться вокруг волосяных фолликулов и потовых протоков верхней части дермы.
При пигментном типе солнечного кератоза присутствует избыточное количество меланина особенно в базальном слое. Иногда увеличение содержания меланина отмечается и в атипичных кератиноцитах. В других случаях почти весь меланин скапливается в клеточных тельцах и дендритах мелано-цитов, что подтверждает наличие блока в передаче меланина. В верхней части дермы содержится также много меланофагов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
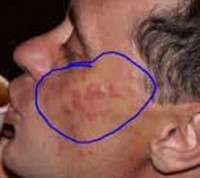
Лимфоцитарная инфильтрация Джесснера-Канофа – редкий хронический дерматоз, характеризующийся доброкачественной инфильтрацией кожи лимфоцитами. Заболевание имеет волнообразное течение, склонно к саморазрешению. Клинически проявляется высыпанием на неизменённой коже плоских гладких синюшно-розовых бляшек или папул, которые сливаются в очаги величиной с ладонь ребенка или взрослого. Первичные элементы имеют чёткие границы, шелушатся. Бляшки обычно единичные, располагаются на лице, шее, туловище, конечностях. Диагностируется клинически с гистологическим подтверждением, иногда проводят молекулярно-биологические исследования. Лечение – НПВС, гормональная терапия, препараты местного действия.
Общие сведения
Лимфоцитарная инфильтрация Джесснера-Канофа – доброкачественная псевдолимфома кожи с хроническим волнообразным рецидивирующим течением. Встречается редко. Чаще возникает у мужчин старше 20 лет. Сезонных, расовых различий не имеет, не эндемична. Иногда наблюдается улучшение в летний период. Впервые данная патология была описана в 1953 году, когда М. Джесснер и Н. Каноф рассмотрели ее как самостоятельное заболевание со сквозной инфильтрацией лимфоцитами всех слоёв дермы. Название «псевдолимфома» в 1965 году ввел К. Мач, объединивший инфильтрацию Джесснера-Канофа в одну группу с другими разновидностями лимфоцитарной инфильтрации.
В 1975 году О. Браун отдифференцировал тип заболевания, отнеся инфильтрацию лимфоцитами к В-клеточным псевдолимфомам, однако позже специалисты стали рассматривать патологию как Т-псевдолимфому. Именно Т-лимфоциты обеспечивают доброкачественное течение патологии и возможность спонтанной инволюции первичных элементов. Дальнейшие исследования показали, что в возникновении и течении лимфоцитарной инфильтрации Джесснера существенную роль играет иммунная система организма. Возможно, это связано с тем, что клетки иммунной системы располагаются в пищеварительном тракте, а он поражается в 70% случаев заболевания. Изучение лимфоцитарной инфильтрации Джесснера-Канофа продолжается и в настоящее время. Понимание причин возникновения и развития Т-лимфоидных процессов имеет большое значение в разработке патогенетического лечения псевдолимфом.

Причины лимфоцитарной инфильтрации
Наиболее вероятными причинами лимфоцитарной инфильтрации Джесснера-Канофа принято считать гиперинсоляцию, укусы клещей, инфекции, патологию желудочно-кишечного тракта, использование дерматогенной косметики и нерациональный приём лекарственных препаратов, провоцирующих системные иммунные нарушения, визуально представленные инфильтративными изменениями в коже. Механизм лимфоцитарной инфильтрации Джесснера-Канофа заключается в следующем: интактный эпидермис даёт Т-лимфоцитам возможность инфильтрировать глубокие слои дермы, располагаясь в сосочковых выростах и вокруг сосудистых сплетений по всей толще кожи. Триггеры заболевания запускают воспаление, на которое реагируют непосредственно клетки кожи и клетки иммунной системы. В процесс купирования воспаления включаются Т-лимфоциты, обеспечивающие доброкачественный ответ иммунной системы в виде пролиферации эпителиальных клеток дермы.
Одновременно в коже развивается банальное воспаление, проходящее три стадии: альтерации, экссудации и пролиферации с участием гистиоцитов – клеток ретикулярной ткани. Гистиоциты группируются и образуют островки, напоминающие лимфоидные фолликулы. На конечном этапе купирования воспаления два параллельных процесса пролиферации дополняют и усиливают друг друга. Так возникает очаг лимфоцитарной инфильтрации. Поскольку лимфоциты гетерогенны, оценка их гистохимических свойств с помощью иммунологических маркеров и моноклональных антител легла в основу иммунофенотипирования. Этот анализ имеет большое диагностическое значение в современной дерматологии.
Симптомы лимфоцитарной инфильтрации
Первичным элементом кожной сыпи при лимфоцитарной инфильтрации Джесснера-Канофа является крупная плоская розово-синюшная бляшка или папула с чёткими границами и гладкой поверхностью, имеющая тенденцию к периферическому росту. Сливаясь между собой, первичные элементы образуют кольцевидные или дугообразные «острова» с участками шелушения. Разрешение высыпавших элементов начинается с центра, поэтому сливные очаги могут иметь западание в центральной части. Типичной локализацией принято считать лицо, шею, околоушное пространство, затылок, лоб, щёки и скулы. Редко высыпания появляются на коже туловища и конечностях. Обычно первичный элемент одиночный, реже наблюдается тенденция к распространению процесса.
Лимфоцитарная инфильтрация Джесснера-Канофа характеризуется волнообразным рецидивирующим течением. Резистентна к проводимой терапии, способна спонтанно саморазрешаться. Рецидивы обычно возникают в местах прежней локализации, но могут захватывать и новые участки кожного покрова. Несмотря на длительное хроническое течение, внутренние органы в процесс не вовлекаются.
Диагностика лимфоцитарной инфильтрации
Заболевание диагностируется дерматологом на основании анамнеза, клиники, гистологии и люминесцентного микроскопирования (типичное свечение на границе дермоэпидермального соединения не определяется) с обязательной консультацией иммунолога и онколога. Гистологически при лимфоцитарной инфильтрации Джесснера-Канофа выявляется неизменённый поверхностный слой кожи. В толще дермальных слоёв обнаруживается группирование лимфоцитов и клеток соединительной ткани вокруг сосудов.
В сложных случаях проводят иммунотипирование опухоли, гистохимическое и молекулярное тестирование. К. Фан с соавторами рекомендуют основывать диагностику на результатах ДНК-цитофлюориметрии с анализом количества нормальных клеток (при лимфоцитарной инфильтрации Джесснера-Канофа более 97%). Дифференциальную диагностику проводят с саркоидозом, системной красной волчанкой, центробежной эритемой Биетта, кольцевидной гранулёмой, группой лимфоцитарных опухолей, токсикодермией и сифилисом.
Лечение лимфоцитарной инфильтрации
Лечение направлено на купирование острой фазы лимфоцитарной инфильтрации Джесснера-Канофа и увеличение продолжительности светлых промежутков. Терапия патологии неспецифическая. Отмечается хороший терапевтический эффект при назначении антималярийных препаратов (хлорохин, гидроксихлорохин) и нестероидных противовоспалительных средств (диклофенак, индометацин) после предварительного лечения сопутствующей патологии желудочно-кишечного тракта. Если состояние пищеварительной системы позволяет, применяют энтеросорбенты. Местно показаны гормональные кортикостероидные мази и кремы, а также инъекционные блокады очагов высыпаний триамцинолоном и бетаметазоном. При резистентности к проводимой терапии подключают плазмаферез (до 10 сеансов).
Инфильтративный туберкулез легких – вторичная туберкулезная инфекция, характеризующаяся распространенным поражением легких с экссудативным типом воспалительной реакции и формированием очагов казеозного распада. В клинической картине преобладает интоксикационный синдром, гипертермия, продуктивный кашель, боли в боку, кровохарканье. В диагностике инфильтративного туберкулеза легких информативны данные физикального, рентгенологического, лабораторного обследования, результаты туберкулиновых проб. Лечение стационарное, с проведением специфической химиотерапии противотуберкулезными препаратами.
МКБ-10

Общие сведения
Инфильтративный туберкулез легких – клинико-морфологическая форма туберкулеза органов дыхания, протекающая с образованием экссудативно-пневмонических очагов в легких с казеозным распадом в центре. Среди всех форм туберкулеза легких инфильтративная форма встречается наиболее часто - в 60-70% случаев. В этой связи организованное выявление более ранних форм туберкулеза является приоритетной задачей пульмонологии и фтизиатрии. Инфильтративный туберкулез легких относится к числу социально-опасных заболеваний. Болеют в основном взрослые (чаще - лица молодого возраста), имеющие неблагоприятные бытовые условия и низкие гигиенические навыки, страдающие вредными привычками. В структуре смертности от туберкулезной инфекции инфильтративная форма занимает около 1%.
Причины
В основе возникновения инфильтративного туберкулеза легких лежит один из двух механизмов: эндогенная реактивация либо экзогенная суперинфекция. Реактивация характеризуется прогрессированием старых или свежих очагов туберкулеза, появлением вокруг них зоны инфильтрации и развитием экссудативной тканевой реакции. Экзогенная суперинфекция, как причина инфильтративного туберкулеза легких, связана с наличием участков гиперсенсибилизации в легких (т. е. зон, ранее контактировавших с туберкулезной инфекцией). При повторном массивном попадании микобактерий туберкулеза в этих очагах развивается гиперергическая реакция, сопровождающаяся инфильтративным воспалением. В обоих случаях обязательным условием заболеваемости выступает наличие специфического противотуберкулезного (вторичного) иммунитете на момент заражения.
Категорию повышенного риска по развитию инфильтративного туберкулеза легких составляют лица, перенесшие контакт с бацилловыделителем, нервно-психическую травму; страдающие алкоголизмом, никотиновой зависимостью, ВИЧ-инфекцией, наркоманией; ведущие асоциальный образ жизни; имеющие хронические заболевания (сахарный диабет, ХНЗЛ и др.) и профессиональные заболевания; подвергающиеся гиперинсоляции и т. д.
Первоначально в легочной ткани образуется инфильтрат диаметром около 3 см, границы которого имеют тенденцию к расширению вплоть до поражения нескольких сегментов или целой доли легкого. Инфильтрат представляет очаг полиморфной экссудации, состоящей из фибрина, мононуклеаров, макрофагов, полиморфноядерных лейкоцитов, альвеолярного эпителия. При слиянии и расширении инфильтратов возникает специфическая долевая пневмония или бронхопневмония.
На следующем этапе участки инфильтрации подвергаются казеозному расплавлению. Лечение инфильтративного туберкулеза легких может способствовать полному рассасыванию инфильтрата, рубцеванию участков, инкапсуляции зоны инфильтрата с образованием туберкуломы легкого. В случае дальнейшего прогрессирования инфильтративного туберкулеза возможны два варианта развития: переход в казеозную пневмонию (устар. – «скоротечная чахотка») либо распад легочной ткани с формированием каверн (кавернозный туберкулез).
Классификация
В современной фтизиатрии принято выделять пять клинико-рентгенологических вариантов инфильтративного туберкулеза легких:
- Облаковидный инфильтрат – рентгенологически определяется в виде слабоинтенсивной гомогенной тени, имеющей расплывчатые контуры. Имеет склонность к быстрому распаду и формированию свежих каверн.
- Круглый инфильтрат – на рентгенограммах имеет вид округлого гомогенного фокуса (иногда с участком распада в виде просветления) с четко очерченными границами; чаще локализуется в подключичной области.
- Дольковый (лобулярный) инфильтрат – при рентгеновском исследовании выявляется негомогенное затемнение неправильной формы, образованное слиянием нескольких очагов, часто с распадом в центре.
- Краевой инфильтрат (перисциссурит) – обширная облаковидная инфильтрация, снизу ограниченная междолевой бороздой. Имеет треугольную форму с углом, обращенным в сторону корня легкого, а основанием – кнаружи. Нередко возникает поражение междолевой плевры, иногда с развитием туберкулезного плеврита.
- Лобит – обширный инфильтрат в легком, занимающий целую долю. Рентгенологически характеризуется негомогенным фокусом с наличием в нем полостей распада.
По размеру различают малые (1-2 см), средние (2-4 см), крупные (4-6 см) и распространенные (более 6 см) инфильтраты. Отдельно выделяют казеозную пневмонию, характеризующуюся инфильтративной реакцией с преобладанием некротических процессов. Казеозно-пневмонические очаги поражают долю или все легкое. Казеозная пневмония чаще развивается на фоне сахарного диабета, беременности, легочных кровотечений, сопровождающихся аспирацией крови, обсемененной микобактериями.
Симптомы инфильтративного туберкулеза легких
Вариант клинического течения зависит от типа инфильтрата. Острое начало характерно для лобита, перисциссурита, некоторых случаев облаковидного инфильтрата. Бессимптомное и малосимптомное течение наблюдается при наличии круглого, лобулярного и облаковидного инфильтратов. В целом же острая манифестация отмечается 15-20% пациентов, постепенная - у 52-60%, бессимптомная – в 25% случаев.
Осложнения
В числе осложнений инфильтративного туберкулеза легких можно встретить казеозную пневмонию, ателектаз легкого, пневмоторакс, плеврит, легочное кровотечение, туберкулезный менингит, реактивный миокардит, сердечную недостаточность. Начало казеозной пневмонии всегда острое: лихорадка достигает 40-41°С, типичны перепады между дневной и вечерней температурой, резко выражена туберкулезная интоксикация. Больных беспокоит одышка, кашель с гнойной мокротой, боли в грудной клетке, прогрессирующее похудание.
Диагностика
Поскольку клинические признаки инфильтративного туберкулеза легких малоспецифичны или отсутствуют совсем, основное значение в диагностике имеют объективные, инструментальные и лабораторные данные. Аускультативная картина характеризуется наличием звучных хрипов; перкуссия обнаруживает притупление звука над областью инфильтрата. Особенно эти изменения выражены при лобите и наличии распада инфильтрата с формированием каверны. Воспалительные изменения крови (сдвиги в лейкоформуле, ускорение СОЭ) незначительны.
Туберкулиновая проба у больных чаще положительная. Рентгенография легких позволяет не только обнаружить инфильтративные изменения, но и оценить характер тени, проследить динамику лечения. Выявить МБТ можно как с помощью микроскопического исследования, так и методом бактериологического посева мокроты или смывных вод бронхов, полученных при проведении бронхоскопии. Подтвердить наличие тубинфекции в организме позволяют новые, высоко достоверные исследования крови: T-SPOT.TB и квантиферон-тест.

КТ органов грудной клетки. Инфильтрация верхней доли правого легкого у пациента с верифицированным туберкулезом
Дифференцировать инфильтративный туберкулез легких приходится с очаговым туберкулезом, ОРВИ, неспецифической пневмонией, раком легкого, актиномикозом, эхинококкозом и кистами легкого, лимфогранулематозом.
Лечение инфильтративного туберкулеза легких
Пациенты с инфильтративным туберкулезом легких немедленно госпитализируются в противотуберкулезное учреждение, где находятся под наблюдением фтизиатра. Больным назначается патогенетическая терапия специфическими химиопрепаратами (изониазид, пиразинамид, рифампицин, этамбутол). Лечение продолжается в течение нескольких месяцев; критерий прекращения терапии - полное рассасывание инфильтративных изменений по рентгенологическим данным; в дальнейшем в амбулаторных условиях проводятся противорецидивные курсы противотуберкулезной терапии.
Одновременно назначаются иммуномодуляторы, антиоксиданты, кортикостероиды. В условиях рационального лечения клиническая симптоматика исчезает в среднем через 3-4 недели; бактериовыделение прекращается в сроки от 1 до 4-х месяцев; уменьшение и рассасывание инфильтрации, закрытие полостей происходит к 3-4 месяцу. При инфильтративном туберкулезе легких в фазе распада может ставиться вопрос о хирургическом лечении – оперативной коллапсотерапии.
Прогноз
Вариантом прогноза инфильтративного туберкулеза может быть благоприятный исход - рассасывание инфильтрата с остаточными фиброзноочаговыми изменениями легких; реже – полное рассасывание инфильтративного очага. К неблагоприятным исходам причисляют формирование туберкуломы легкого, переход в казеозную пневмонию или фиброзно-кавернозный туберкулез, смерть от нарастающей туберкулезной интоксикации или других осложнений. В современных условиях, при проведении противотуберкулезной терапии, неблагополучные исходы встречаются редко.
Профилактика инфильтративного туберкулеза легких не отличается от мер предупреждения заболеваемости другими формами туберкулезной инфекции. Поскольку больные с инфильтративной формой являются бацилловыделителями, необходимо как можно более раннее их выявление, изоляция и лечение.
2. Клинические проявления и эффективность лечения инфильтративного туберкулеза легких: Автореферат диссертации/ Назарова Н.В. – 2005.
3. Диагностика и дифференциальная диагностика инфильтративного туберкулёза лёгких в условиях высокоспециализированных противотуберкулёзных учреждений: Диссертация/ Посаженникова С. Ю. – 2015.
4. Особенности клинических проявлений заболевания и эффективность лечения больных инфильтративным туберкулезом легких, вызванным лекарственно-устойчивыми микобактериями: Автореферат диссертации/ Барламов О.П. – 2007.
Аппендикулярный инфильтрат — это одно из осложнений острого аппендицита. Представляет собой воспалительную опухоль, которая включает червеобразный отросток с окружающими его органами (слепой кишкой, сальником). Заболевание проявляется тупыми болями справа внизу живота, слабостью, субфебрильной температурой тела. Для постановки диагноза используют различные методы визуализации органов брюшной полости — УЗИ, КТ, диагностическую лапароскопию. Вспомогательное значение имеют клинический и биохимический анализы крови. коагулограмма. В типичных случаях аппендикулярного инфильтрата показано консервативное лечение с отсроченной аппендэктомией.
МКБ-10


Общие сведения

Причины
Аппендикулярный инфильтрат как осложнение аппендицита имеет такие же этиологические факторы. Его развитие связано с проникновением микробной флоры в червеобразный отросток и следующими за этим воспалительными изменениями в органе. Инфильтрат образуется при распространении патологического процесса за пределы аппендикса, вовлечении соседних петель кишечника, сальника. В хирургии выделяют три главные причины формирования АИ:
- Позднее обращение к врачу. Более трети больных с острым аппендицитом обращаются за медицинской помощью спустя сутки и более после появления симптомов. Этому способствуют проблемы с доступностью медицинской помощи, несознательное отношение к своему здоровью.
- Атипичное течение аппендицита. При снижении общей реактивности организма болевой синдром выражен незначительно, поэтому пациенты могут длительное время не осознавать факт наличия болезни. Это характерно для пожилых людей.
- Диагностические ошибки. Несмотря на высокий уровень развития современной медицины, по статистике ошибки в диагностике аппендицита на догоспитальном этапе выявляются в 25% случаев. Это обуславливает запоздалую госпитализацию и неадекватное лечение.
Патогенез
Аппендикулярный инфильтрат по структуре является воспалительной опухолью. Процесс воспаления затрагивает не только аппендикс, но и соседние ткани. На начальных этапах болезни формируется «рыхлый» инфильтрат, в котором органы не связаны между собой. По мере прогрессирования воспалительный процесс переходит в стадию пролиферации, на которой образуются соединительнотканные спайки. В таком случае возникает «плотный» АИ.
Симптомы аппендикулярного инфильтрата
Зачастую начало заболевания по клинической картине напоминает типичный острый аппендицит. Человек жалуется на сильные схваткообразные боли в правой подвздошной области, которые появляются внезапно. Болевые ощущения сопровождаются тошнотой, одно- или двукратной рвотой. Реже отмечаются диарея или болезненность при мочеиспускании. Характерно повышение температуры тела до 37-38 °С, слабость.
При атипичном начале характер и интенсивность болей меняется. В течение нескольких дней больного беспокоят ноющие или тупые боли справа в боку, которые имеют умеренную интенсивность. Болевой синдром в подобных клинических случаях может оказаться единственным проявлением аппендикулярного воспаления. Подобная клиническая симптоматика, как правило, встречается у людей пожилого и старческого возраста, ослабленных пациентов.
Спустя 2-3 дня после манифестации заболевания на фоне болевого синдрома начинает формироваться болезненная воспалительная опухоль. Больной может ее прощупать самостоятельно: инфильтрат представляет собой плотное и умеренно подвижное образование в правом нижнем квадранте живота. При этом постепенно уменьшаются боли в покое. Болезненность усиливается при наклонах туловища вперед и вправо. Температура тела при аппендикулярном инфильтрате держится на уровне 37-37,5 °С.

Осложнения
При несвоевременном лечении АИ есть высокая вероятность развития аппендикулярного абсцесса. При формировании гнойника вокруг воспаленного аппендикса самочувствие резко ухудшается. Наблюдается фебрильная лихорадка с периодами озноба, боли становятся постоянными и очень интенсивными. Такое состояние требует неотложной хирургической помощи, при отсутствии которой у 90-95% пациентов возникает перитонит.
Среди поздних осложнений аппендикулярного инфильтрата основную роль играет спаечная болезнь. После перенесенного воспаления формируются перемычки между петлями кишечника, которые нарушают нормальный транспорт каловых масс по кишечнику. Под действием провоцирующих факторов спайки приводят к механической кишечной непроходимости, некрозу участка кишечника.
Диагностика
Опытный хирург ставит предварительный диагноз уже на основании объективного осмотра. Обращает на себя внимание опухоль в области проекции аппендикса, которая имеет плотноэластическую консистенцию, болит при надавливании. Далее для диагностики аппендикулярного инфильтрата применяют следующие лабораторные и инструментальные методы:
- УЗИ брюшной полости. С помощью ультразвукового исследования врач оценивает состояние кишечных петель и червеобразного отростка, выявляет признаки аппендикулярного воспаления — инфильтрацию и утолщение стенок ЖКТ, наличие экссудата. При небольшом размере инфильтрата УЗИ может быть малоинформативным.
- КТ брюшной полости. Компьютерную томографию чаще проводят пожилым больным, чтобы дифференцировать аппендикулярный инфильтрат с доброкачественными и злокачественными опухолями. Исследование дает четкое и детальное изображение абдоминальных органов.
- Диагностическая лапароскопия. В затруднительных случаях прибегают к инвазивному методу визуализации. Благодаря введению видеохирургического инструментария в брюшную полость можно детально осмотреть патологический инфильтрат. При необходимости во время диагностики выполняют лечебные лапароскопические манипуляции.
- Анализы. Общеклиническое исследование крови показывает неспецифические воспалительные признаки — повышение уровня лейкоцитов и СОЭ. Показатели эритроцитов и гемоглобина помогают исключить токсико-анемический синдром. Обязательно назначают биохимический анализ крови, коагулограмму.

Лечение аппендикулярного инфильтрата
Консервативная терапия
Аппендикулярный инфильтрат — единственное из осложнений аппендицита, которое подлежит медикаментозной терапии. Лечение проводится только в условиях стационара. Подбираются этиотропные антибактериальные препараты широкого спектра. Местно на правую подвздошную область применяют холод, методы физиотерапии. Спустя 10-14 дней от начала проведения такой терапии инфильтрат рассасывается, аппендикулярные симптомы исчезают.
Хирургическое лечение
Если заболевание удалось купировать консервативным путем, спустя 3-4 месяца рекомендовано проведение плановой аппендэктомии. Операция предназначена для профилактики рецидивов воспалительного процесса. В абдоминальной хирургии для удаления аппендикса используют лапароскопическое оборудование. Операция проходит с небольшими разрезами кожи и минимальным повреждением тканей, что ускоряет реабилитационный период.
При нагноении аппендикулярного инфильтрата рекомендовано оперативное вмешательство в кратчайшие сроки. Производится вскрытие и дренирование гнойника, после чего самочувствие быстро улучшается. Обычно в таких ситуациях удаление червеобразного отростка не проводят, поскольку операция чревата осложнениями. Плановая аппендэктомия выполняется спустя 6 месяцев после первого этапа лечения.
Прогноз и профилактика
При своевременной комплексной терапии аппендикулярного инфильтрата пациенты полностью выздоравливают, никаких отдаленных осложнений болезни не возникает. Прогноз ухудшается при трансформации АИ в абсцесс или местный перитонит. Профилактика заболевания включает раннюю диагностику и адекватную хирургическую помощь при остром аппендиците, что особенно важно для ослабленных и пожилых больных.
Аппендикулярный инфильтрат - видео:
1. Аппендикулярный инфильтрат: диагностика и лечебная тактика/ Н.А. Майстренко, П.Н. Ромащенко, М.В. Ягин// Вестник хирургии. — 2016.
2. Некоторые диагностические ошибки и лечебные аспекты при аппендикулярных инфильтратах/ А.Г. Хасанов, И.Ф. Суфияров, Ф.Ф. Бадретинов, А.М. Меньшиков// Креативная хирургия и онкология. — 2019.
3. Особенности оперативного лечения у больных, перенесших плотный аппендикулярный инфильтрат/ В.В. Козлов, П.А. Гнилосыр, М.Б. Хмара, И.В. Гофринкель// Материалы межрегиональной научно-практической конференции «Молодые ученые — здравоохранению». — 2018.
4. Проблемы диагностики аппендикулярного инфильтрата у детей/ Н.В. Козулина, В.В. Паршиков, Ю.П. Бирюков // Современные проблемы науки и образования. — 2014.
Факторы определяющие степень злокачественности меланомы.
Количество митозов в дермальном компоненте опухоли, особенно их число на 1 мм2 площади, является важным прогностическим фактором для меланомы. Митотическая активность выше, чем 6 митозов на 1 ммг, измеренная в компоненте вертикальной стадии роста опухоли, является фактором высокой степени риска. Можно использовать прогностический индекс (pi) для меланомы, который вычисляется путем умножения числа митозов, приходящихся на 1 мм2 площади опухоли, на показатель толщины опухоли в миллиметрах. Это более точный показатель прогноза для пациента, чем любая из этих двух переменных в отдельности.
Изъязвление меланомы
Изъязвление эпидермиса над дермальной частью опухоли — важная прогностическая переменная. Фактически в нескольких исследованиях она была представлена как независимый фактор прогноза. Но не все исследователи согласны с этим выводом. Изъязвление появляется в опухолях с достаточной глубиной инвазии для появления метастазов, но в проведенных исследованиях этот факт не учитывался. Однако в тех случаях, когда изучались опухоли, согласованные по толщине, сокращение периода выживания у пациентов с изъязвленными опухолями снизилось с 80 до 55%, при этом прогностическое значение имели изъязвления диаметром более 3 мм.
Лимфоидная инфильтрация меланомы
В меланомах ответная реакция организма на неопластический процесс представлена, в основном, лимфоцитами. Опухоли с выраженным лимфоцитарной инфильтрацией имеют лучший прогноз. W.H. С1аrk с соавт. ввели термин TTLs («лимфоциты, инфильтрирующие опухоль»), чтобы учеств наличие лимфоцитов, фактически проникающих между клетками опухоли, что особенно важно для вертикальной стадии роста опухоли. В своих исследованиях они не относили к TILs лимфоциты, инфильтрирующие строму опухоли, и лимфоциты, связанные с радиальной стадией роста меланомы. Посредством многофакторного анализа эти ученые установили, что TILs является вторым наиболее важным прогностическим фактором для стадии I и II, а опухоль с оживленным TILs-ответом имеет более благоприятный исход. Отсутствие иммунного ответа в опухолях толщиной 3,65 мм и более служит отрицательным прогностическим фактором в отношении выживания больных и положительным в отношении вероятности развития костных и висцеральных метастазов.
Регрессия меланомы
Один из уникальных аспектов меланомы — способность опухоли к спонтанной регрессии. Регрессия может быть частичной или полной.
Сложившиеся противоречия вокруг понятия «спонтанной регрессии» в меланоме как прогностического фактора являются результатом использования различных определений самой «регрессии». Регрессия может проис-ходитв как в радиальной, так и в вертикальной стадии роста. Однако именно регрессия при радиальной стадии роста исторически была изучена как потенциальный прогностический признак меланомы. Эта регрессия была определена как отсутствие элементов опухоли в эпидермисе. Участок регрессии характеризовался фиброзом сосочкового слоя дермы, повышенной васкуляризацией и смешанной инфильтрацией лимфоцитами и меланофагами. Регрессия описывалась как «ак-ивная», когда присутствовали TILs, и как «прошлая», когда все клетки опухоли исчезали. Полное исчезновение клеток опухоли можно определить и как «истинную» регрессию. Несколько групп исследователей наблюдали неблагоприятные результаты у пациентов с частичной регрессией опухоли, в то время как другие не отмечали подобных результатов. W.H. Clark и соавт. предположили, что регрессия при радиальной стадии роста опухоли является важным независимым фактором прогноза выживания, но только у пациентов с наличием компонента вертикальной стадии роста. Невозможно предсказать прогноз у пациентов, если опухоль полностью регрессировала, или у пациентов, имевших только радиальную стадию роста опухоли, потому что статистически последние имеют выживание в 100% случаев, независимо от присутствия регрессии или любого другого прогностического фактора.

Гистологический подтип меланомы
Исторически сложилось, что подтип меланомы (злокачественное лентиго, поверхностно распространяющаяся или узловая меланома и т.д.) рассматривается как важный прогностический фактор, однако он не является независимым фактором прогноза. Так, неблагоприятный прогноз при узловой меланоме связан с толщиной опухоли, а не с гистологическим подтипом. Узловая меланома — по определению, опухоль в вертикальной стадии роста, в среднем ее толщина больше, чем при других гистологических подтипах, которые классифицируются на основании присутствия компонента радиальной стадии роста. Меланома типа злокачественного лентиго — единственная форма, имеющая лучший прогноз, чем другие подтипы.
Неточный состав компонента вертикальной стадии роста меланомы
Все меланомы имеют области, содержащие эпителиоидные и веретенообразные клетки, хотя в большинстве случаев отдельный клеточный тип преобладает. Меланомы, состоящие из веретенообразных клеток, имеют лучший прогноз, но при анализе клеточный состав редко рассматривается как независимый фактор прогноза. Плоидностъ
Проточная цитометрия для определения плоидности клеток применялась и при изучении меланом. В результате установлено, что анеуплоидность постоянно коррелирует с толщиной, уровнем инвазии и изъязвлением и является независимым фактором риска развития рецидива для опухолей толщиной более 1,5 мм и менее 3,0 мм. Анеуплоидность клеток также связана и с короткой ремиссией. Komino с соавт. выявили, что анеуплоидность может обнаруживаться в маленьких меланомах (и менее 6 мм) и уже на этой стадии связана с высоким риском рецидивирования и метастазирования.
Маркеры пролиферации меланомы
Митотическая активность в меланомах связана с рецидивами и выживанием. Иммуногистохимическое выявление высокого показателя пролиферации Ki-67 (MIBl) в меланомах коррелирует с толшиной опухоли. Толшина опухоли и максимальная числовая плотность Ki-67-положительных ядер является независимым фактором прогноза, более существенным по своему значению, чем толщина опухоли или число митозов по отдельности. Рецепторы эстрогена
Поскольку существуют явные различия в анатомическом местоположении и биологическом поведении меланом у мужчин и женщин, была исследована роль эстрогена и его рецепторов в меланомах. Меланомы имеют способность закрепления гормона стероида, однако не все исследования до настоящего времени сумели подтвердить наличие белка эстроген-рецептора в меланомах, даже в течение беременности. Тем не менее Walker с соавт. выявили наличие белка рецептора в 37-50% меланом как у мужчин, гак и у женщин и определили его как фактор прогноза, наряду с толшиной опухоли и уровнем инвазии. Присутствие и роль эстроген-рецепторов в меланомах требуют дальнейшего изучения.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

