Индифферентный эпителий эндометрия что это
Обновлено: 24.04.2024
Атипичная гиперплазия эндометрия матки. Аденокарцинома in situ матки.
Гиперплазия базального слоя (базальная гиперплазия) эндометрия — редкий вариант гиперплазии, встречающийся преимущественно после 35 лет, чаще имеет очаговый характер. Гиперплазированный утолщенный базальный слой имеет густую строму, в которой лежат клубками кровеносные сосуды с утолщенными склерозированными стенками.
При данной патологии отмечают замедленное отторжение части гиперплазированного базального слоя эндометрия, и потому для нее характерны длительные, обильные и болезненные менструации. При подозрении на замедленное отторжение эндометрия диагностическое выскабливание его рекомендуется делать на 6—7-й день менструальной фазы.
Малигннзация рассмотренных вариантов гиперплазии явление исключительно редкое, и нет оснований относить указанные процессы к предраку.
Атипическая гиперплазия и очаговый аденоматоз, как и аденоматозные полипы, относятся к предраковым процессам. Предрак эндометрия встречают в любом возрасте, чаще до 50 лет. Клинически проявляется, почти как правило, ановуляторными кровотечениями.
Атипическая гиперплазия (диффузный аденоматоз, атипическая железистая гиперплазия) функционального и/или базального слоя эндометрия в отличие от железистой гиперплазии, подобно аденоматозным полипам, характеризуется более выраженными пролиферативными процессами эпителиального компонента. В практике патологоанатома чаще обнаруживают очаговые разрастания с интенсивной пролиферацией желез и/или их эпителия (очаговый аденоматоз).
Очаговый аденоматоз обычно встречают на фоне железистой или железисто-кистозной гиперплазии, реже в полипах или в малоизмененном эндометрии.
Различия предраковых изменений в структурном отношении и в отношении степени риска малигнизации служат основой для выделения нерезкой и выраженной форм. Данную работу на высоком уровне выполняют гистологи Казани, поэтому работа в патологистолических отделениях больниц считается перспективной работой. Нерезкая форма предрака характеризуется наличием многочисленных мелких и более крупных желез, которые разделены сравнительно тонкими прослойками стромы. Цилиндрический эпителий нередко многорядный, ядра его чаще всего гиперхромны, палочковидной и овоидной формы.
Аналогичный эпителий имеется в расширенных и кистозно-измененных железах; уплощения эпителия в этих железах, как это наблюдают при железисто-кистозной гиперплазии, не отмечается. При выраженной форме предрака много ядерный железистый эпителий отличается некоторым полиморфизмом, образованием папиллоподобных выростов, направленных в просветы желез. Просветы желез обычно узкие. Железы иногда настолько тесно расположены друг к другу, что строма между ними практически отсутствует. В крупных ядрах железистого эпителия нередко обнаруживают мелкие ядрышки.
Термин «аденокарцинома in situ» (преинвазивная карцинома, нулевая стадия рака) эндометрия следует оценивать критически. Критерии для постановки такого диагноза на основании исследования соскоба эндометрия отсутствуют в отличие от хорошо известных критериев преинвазивпой карциномы шейки матки. Неудачен и термин «аденоакантома in situ», используемый по отношению к выраженной форме предрака эндометрия с участками плоскоклеточной метаплазии различной формы и величины.
Строма предрака нередко богата клетками; в некоторых наблюдениях среди них обнаруживают в разном количестве крупные пенистые светлые клетки, содержащие липиды. Существует мнение, что эти клетки (они могут встречаться в строме рака и при различных гиперпластических процессах, но чаще при предраке) содержат вещества эстрогенной природы. Неблагоприятная прогностическая роль их (чем больше таких клеток, тем быстрее развивается рак) не доказана. Эти клетки следует отличать от пенистых клеток (гисгиоцитов), содержащих гемосидерин и выполняющих роль макрофагов.
Развитие рака на фоне предракового процесса наблюдают в 12—14%. В трудных случаях дифференциальной диагностики отдельных форм предрака и рака эндометрия следует рекомендовать повторное его диагностическое выскабливание. В дифференциальной диагностие учитывают атипические изменения железистого эпителия, наблюдаемые во время беременности-— феномен Ариас-Стеллы.
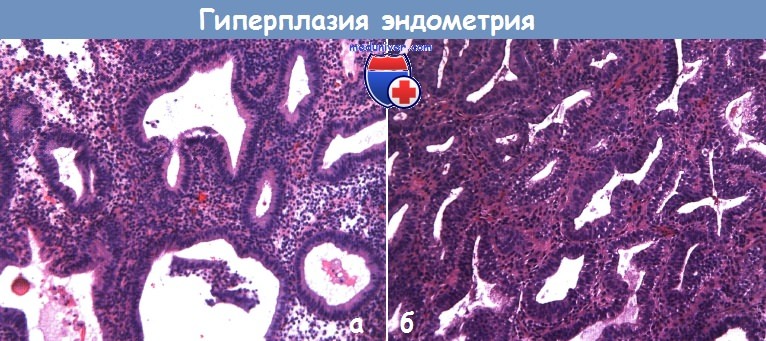
а - простая гиперплазия без атипии: эндометрий утолщен за счет железистого эпителия, что вызвано воздействием только эстрогенов, без прогестерона.
Железы характеризуются неравномерными, зачастую непредсказуемыми, очертаниями.
Строма обильная, поэтому соотношение железистая/стромальная ткань мало отличается от нормального.
Окраска гематоксилином и эозином, х10
б - сложная гиперплазия без атипии: соотношение железистая/стромальная ткань увеличено, при этом железы расположены тесно, имеют сложное строение, просветы часто неправильной формы.
Атипия ядер выражена незначительно. Окраска гематоксилином и эозином, х20
- Вернуться в оглавление раздела "гистология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Классификация гиперплазии эндометрия и их критерии
В настоящее время на основании предложенной в 1994 г. классификации Международного общества гинекологов-патологов (ISGYP), Международной федерации акушеров и гинекологов (FIGO) и Всемирной организации здравоохранения (WHO, ВОЗ) выделяют четыре вида гиперплазии эндометрия в зависимости от гистологического строения и цитологических характеристик. В зависимости от структурных изменений желез и железистого эпителия различают простую и сложную гиперплазию, а в зависимости от цитологических характеристик — с наличием или отсутствием атипии.
В связи с этим выделяют четыре разных диагноза: простая гиперплазия без атипии, сложная гиперплазия без атипии, простая атипическая гиперплазия, сложная атипическая гиперплазия.
От терминов «аденоматозная» и «железисто-кистозная гиперплазия» решено отказаться. Поэтому встречающаяся аббревиатура АГЭ относится к атипической гиперплазии эндометрия и объединяет два ее варианта: простая и сложная АГЭ, с атипией клеток эпителия маточных желез. Наличие атипии — это самый важный критерий последующей прогрессии в аденокарциному или одновременного наличия эндометриальной аденокарциномы. По имеющимся данным, сосуществование эндометриальной аденокарциномы и АГЭ отмечается не менее чем в 13 % и не более чем в 43 % случаев.
Классификация гиперплазии эндометрия:
- Простая гиперплазия
- Сложная гиперплазия (аденоматозная)
- Простая атипическая гиперплазия
- Сложная атипическая гиперплазия (аденоматозная с атипией)

а - простая гиперплазия без атипии: эндометрий утолщен за счет железистого эпителия, что вызвано воздействием только эстрогенов, без прогестерона.
Железы характеризуются неравномерными, зачастую непредсказуемыми, очертаниями.
Строма обильная, поэтому соотношение железистая/стромальная ткань мало отличается от нормального.
Окраска гематоксилином и эозином, х10
б - сложная гиперплазия без атипии: соотношение железистая/стромальная ткань увеличено, при этом железы расположены тесно, имеют сложное строение, просветы часто неправильной формы.
Атипия ядер выражена незначительно. Окраска гематоксилином и эозином, х20
Диагностика этих поражений обычно основана на гистологическом исследовании небольшого биоптата эндометрия, полученного в амбулаторных условиях с помощью специального гибкого стерильного пластикового устройства Pipelle. Онкогинекологическая исследовательская группа (GOG) выполнила проспективное исследование воспроизводимости результатов диагностики простой и атипической гиперплазии эндометрия. В исследование были включены женщины с диагностированной АГЭ в одном из 285 институтов GOG, которые дали согласие на выполнение гистерэктомии в течение ближайших 12 нед. Выборка данного исследования включала 302 соответствующих критериям включения женщины, медиана возраста составила 57 лет, при этом 31 % пациенток были моложе 50 лет.
Все микропрепараты эндометрия были пересмотрены 3 независимыми экспертами-патоморфологами-гинекологами в условиях слепого метода. Они согласились использовать следующие обозначения состояния эндометрия: нормальный (эндометрий стадии пролиферации, секреции, атрофичный, менструальный), неатипическая гиперплазия (беспорядочная пролиферация, простая или сложная гиперплазия), атипическая (простая или сложная) гиперплазия, аденокарцинома или неудовлетворительный для оценки биоптат. Для постановки диагноза требовалось, чтобы 2 из 3 экспертов выбрали один и тот же из пяти возможных диагнозов.
Правильный диагноз выставлялся на основании консенсуса специалистов после независимого гистологического исследования послеоперационного материала. Все 3 специалиста пришли к единому заключению в 40 % случаев. Воспроизводимость была наименьшей для диагноза АГЭ (к = 0,28), в отношении аде-нокарциномы показатель был лучше (к = 0,51). При раздельном выскабливании слизистой оболочки матки воспроизводимость была лучше (к = 0,47; доверительный интервал [ДИ] 0,41—0,53), чем при биопсии (к = 0,26—0,36). 2 из 3 экспертов согласились с установленным ранее диагнозом АГЭ в 38 % случаев. У 25 % пациенток согласительная комиссия изменила диагноз на менее тяжелый, при этом аденокарцинома была диагностирована в 29 % случаев. Наиболее важным результатом данной работы GOG стало доказательство того факта, что у 43 % пациенток во время выполнения гистерэктомии была аденокарцинома эндометрия.
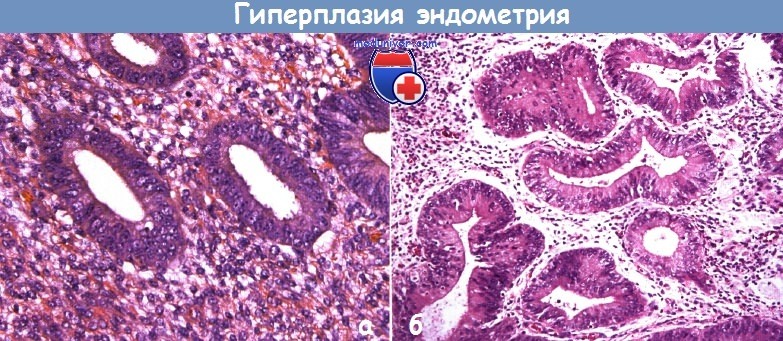
а - простая атипическая гиперплазия.
Редко диагностируемая форма гиперплазии, при которой железистый компонент преобладает над стромальным за счет простых желез, выстланных эпителием с атипичными ядрами.
Окраска гематоксилином и эозином, х40
б - сложная атипическая гиперплазия.
Значительное преобладание железистого компонента над стромальным, железы имеют сложное строение, клетки эпителия с атипией ядер.
Окраска гематоксилином и эозином, х20.
Другим серьезным итогом можно считать определение истинного процента аденокарцином в каждой группе больных с установленным до операции диагнозом: в группе нормального эндометрия и гиперплазии без атипии — 14/74 (18,9 %), в группе АГЭ — 45/115 (39,1 %) и в группе аденокарциномы — 54/84 (64,3 %). В 43 случаях исследование матки выявило такие факторы риска метастазирования, как инвазию в миометрий, умеренно- (G2) и низкодифферснцированные (G3) опухоли.
Простая гиперплазия без признаков атипии, как правило, протекает доброкачественно. Наиболее часто она встречается в период пременопаузы, характеризующийся появлением ановуляторных циклов. Устранение гиперэстрогении или терапия прогестагенами определяют исход заболевания. Большинство патологических изменений (60 %) исчезает без лечения, а при терапии прогестинами эффект будет достигнут у 84 % больных. Считается, что только в 3 % случаев происходит трансформация простой гиперплазии в РЭ.

а - высокодифференцированная аденокарцинома эндометрия (G1): железы расположены тесно, строма между ними скудная.
Железы выстланы высокими цилиндрическими опухолевыми клетками.
Окраска гематоксилином и эозином, х20
б - низкодифференцированная аденокарцинома эндометрия (G3) характеризуется утратой железистой структуры практически во всей опухоли.
По форме клетки округлые полигональные, но не цилиндрические. При данной патологии часто наблюдается некроз клеток (вверху справа).
Окраска гематоксилином и эозином, х20.
Сложная гиперплазия при отсутствии атипии клеток эпителия маточных желез также регрессирует в большинстве (56 %) случаев. Для АГЭ характерна трансформация в раку 36 % больных, причем в 27 % случаев заболевание прогрессирует даже на фоне терапии прогестинами, но при этом остается неясным, не отражает ли последний показатель синхронно протекающий РЭ. Подсчитано, что в 55 % случаев на фоне терапии прогестинами АГЭ регрессирует. Наилучший препарат из группы прогестинов для лечения данной патологии все еще не установлен. Точно так же необходимо уточнить схему назначения (циклический режим или непрерывный) и продолжительность лечения.
Считается, что при невозможности устранения гиперэстрогении показана пожизненная терапия прогестинами. В качестве альтернативного метода возможна гистерэктомия с целью предотвратить развитие наиболее часто встречающейся эстрогензависимой эндометриальной аденокарциномы I типа. Этот тип эстроген-индуцированного рака эндометрия (РЭ) — наиболее распространенный и менее агрессивный; поэтому и профилактика, и лечение должны бытьуспешными.
Внедрение современных научных разработок, в т. ч. молекулярных методов исследования поражений эндометрия и объективной компьютеризованной морфометрии, обещает увеличить точность и воспроизводимость диагностики новообразований эндометрия. В 2003 г. ВОЗ была предложена новая классификация, в которой в качестве предракового состояния описывается эндометриальная ин-траэпителиальная неоплазия (ЭИН). Первые данные свидетельствуют о лучшей прогностической значимости ЭИН при определении риска малигни-зации, однако этот термин до сих пор не используют в клинике.
На фоне атрофии эндометрия развивается серозно-папиллярный РЭ, который этиологически не связан с гиперэстрогенией; его классифицируют как РЭ II типа или эстрогеннезависимый. Гиперплазия эндометрия не относится к предшественникам серозного рака. Наиболее вероятно, что его предшественником считается интраэпителиальный рак эндометрия. Серозный рак эндометрия (РЭ) может быть мультифокальным по происхождению и поражать яичники и сальник, без признаков инвазии в миометрий. Учитывая, что при обычной ревизии органов брюшной полости и таза во время лапарото-мии невозможно определить инвазивный рост опухоли, рекомендуется тщательное хирургическое стадирование заболевания.
Вероятность выявления серозно-папиллярного рака на ранних стадиях заболевания ниже, чем при других гистологических типах РЭ. После получения результата гистологического исследования и установления стадии заболевания определяют характер послеоперационной терапии. Серозный вариант новообразования зачастую обусловлен нарушением функции гена-супрессора опухолевого роста ТР53, что ведет к накоплению белка р53 в клетке. Иммуногистохимическое исследование с применением антител к белку р53 дает положительный результат в большинстве случаев серозных опухолей в отличие от нормального эпителия эндометрия или РЭ.

а - интраэпителиальный рак эндометрия (ИРЭ) - поражение, предшествующее серозному раку эндометрия, с выраженным атипическим уплотнением эпителия и незначительным нарушением архитектоники.
ИРЭ обычно наблюдается на поверхности доброкачественных полипов эндометрия.
Окраска гематоксилином и эозином, х20.
б - иммуногистохимическое окрашивание интраэпителиального рака эндометрия на р53.
Мутации ТР53, ведущие к повышенному накоплению белка р53, характерны для серозного рака эндометрия.
В нормальных клетках содержание неизмененного белка р53 ниже порогового уровня и результат анализа отрицательный.
Иммунопероксидазное окрашивание на р53 с хромогеном DAB, х20.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
В современном мире неуклонно растет количество женщин постменопаузального возраста на фоне общего старения населения планеты, обусловленного увеличением продолжительности жизни. Полипы слизистой оболочки полости матки (ПЭ) выявляются у 50% женщин страдающих маточным кровотечением в менопаузе. Они могут протекать бессимптомно, но все чаще выявляются при УЗИ, гистероскопии. ПЭ отличаются многообразием форм гистологического строения, особенностями фоновых состояний, что, несомненно, влияет на течение болезни и прогноз. На фоне полипов в 1,39-15,74% могут развиваться злокачественные опухоли из эпителия – раки. Однако работы, посвященные этой проблеме единичны, сведения приводимые в них противоречивы.
В данной работе мы изучали особенности клинических проявлений, строения полипов у женщин с атрофией эндометрия в постменопаузе, возможности их озлокачествления, виды возникающих в них опухолей.
Материал и методы
Полипы на фоне атрофии эндометрия были обнаружены у 100 пациенток (78,13%). Согласно классификации предложенной Волошиным В.В. (2010) все они были отнесены к железисто-фиброзным атрофическим полипам (АП). АП отличали выраженная ножка со склерозированными сосудами, грубая коллагенизированная строма (площадь ее более 30%), преобладающая над железистым компонентом. Железистые ходы мелкие овальной формы или кистозно-расширенные были выстланы однорядным цилиндрическим эпителием с мелкими гиперхромными овальными ядрами не различимыми ядрышками. Такой эпителий называют «индифферентным», атрофическим. Митозы в клетках стромы и эпителии полипов отсутствовали. АП возникали на фоне атрофического эндометрия, в том числе кистозной атрофии – 35 наблюдений, и в этих случаях при УЗИ ставился диагноз гиперплазии слизистой оболочки полости матки.
В 52 (52,%) случаях они протекали бессимптомно, в 48 (48,0%) – проявились маточными кровотечениями. Ожирение у пациенток с АП отмечено в 24,0% наблюдений, сахарный диабет – в 19,0%, гипертензия – в 45,0% .
Рак на фоне АП был диагностирован в 4 (4,0%) случаях. Опухоль состояла из коротких с плотной стромой или длинных тонких папиллярных, или щелеподобных железистых структур покрытых одно – или многорядным цилиндрическим эпителием. Клетки его полиморфные с гиперхромными ядрами и крупными ядрышками. В них отмечалась выраженная экспрессия маркеров Ki 67 (32,7 + 1,7%) и p53 (35,4+3,2%). Экспрессия маркеров ER была низкой (2-3 – по Allred). РR в клетках опухоли не определялись. Морфологическая и иммуногистохимическая характеристика опухоли соответствовали серозной карциноме. В 1 наблюдении опухоль была ограничена полипом, в 3 – она прорастала в окружающий эндометрий и миометрий до 1/2 толщины, отмечалась инвазия в сосуды. У 2 больных карцинома прорастала железы и строму слизистой оболочки цервикального канала, т.е., соответствовала II B стадии. У всех пациенток новообразования проявились кровотечением. Лишь одна из этих больных страдала ожирением и артериальной гипертензией.
1. В постменопаузе чаще всего – 75,0%, на фоне атрофии эндометрия развиваются АП.
2.АП отличают выраженная сосудистая ножка, плотная склерозированная строма (площадью более 30%) и железы, выстланные «индифферентным» эпителием.
3. Развитие АП, видимо, не связано с нарушением гормонального статуса.
4. На фоне АП может развиваться серозная аденокарцинома – гормононезависимая опухоль с высокой степенью инфильтративного роста, неблагоприятным прогнозом.
5. Потому морфологическое исследование полиповидных образований развивающихся в менопаузе на фоне атрофии эндометрия является чрезвычайно важным и обязательным.
Циклические изменения в слизистой оболочке матки (эндометрии). Эндометрий состоит из следующих слоев.
1. Базальный слой, который не отторгается во время менструации. Из его клеток в течение менструального цикла образуется слой эндометрия.
2. Поверхностный слой, состоящий из компактных эпителиальных клеток, которые выстилают полость матки.
3. Промежуточный, или спонгиозный, слой.
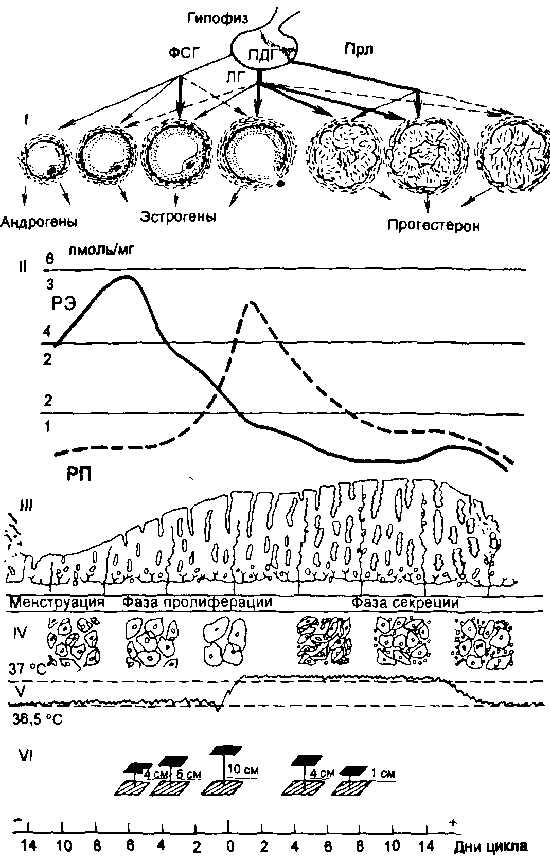
Рис. 2.15. Циклические изменения в органах репродуктивной системы в течение менструального цикла.
I — гонадотропная регуляция функции яичников;
ПДГ — передняя доля гипофиза;
II — содержание в эндометрии реиепторов к эстрадиолу — РЭ (1,2,3; сплошная линия) и прогестерону — РП (2,4,6; пунктирная линия);
III — циклические изменения эндометрия;
IV — цитология эпителия влагалища;
V — базальная температура;
VI — натяжение цервикапьной слизи.
Последние два слоя составляют функциональный слой, подвергающийся основным циклическим изменениям в течение менструального цикла и отторгающийся в период менструации.
В 1 фазе менструального цикла эндометрий представляет собой тонкий слой, состоящий из желез и стромы. Выделяют следующие основные фазы изменения эндометрия в течение цикла;
1) фаза пролиферации;
2) фаза секреции;
3) менструация.
Фаза пролиферации. По мере увеличения секреции эстрадио-ла растущими фолликулами яичников эндометрий претерпевает пролифера-тивные изменения. Происходит активное размножение клеток базального слоя. Образуется новый поверхностный рыхлый слой с вытянутыми трубчатыми железами. Этот слой быстро утолщается в 4—5 раз. Трубчатые железы, выстланные цилиндрическим эпителием, удлиняются.
Фаза секреции. В лютеиновую фазу яичникового цикла под влиянием прогестерона увеличивается извилистость желез, а просвет их постепенно расширяется. Клетки стромы, увеличиваясь в объеме, приближаются друг к другу. Секреция желез усиливается. В просвете желез находят обильное количество секрета. В зависимости от интенсивности секреции железы либо остаются сильно извитыми, либо приобретают пилообразную форму. Отмечается усиленная васкуляризация стромы. Различают раннюю, среднюю и позднюю фазы секреции.
Менструация. Это отторжение функционального слоя эндометрия. Тонкие механизмы, лежащие в основе возникновения и процесса менструации, неизвестны. Установлено, что эндокринной основой начала менструации является выраженное снижение уровней прогестерона и эстрадиола вследствие регрессии желтого тела.
Существуют следующие основные локальные механизмы, принимающие участие в менструации:
1) изменение тонуса спиральных артериол;
2) изменение механизмов гемостаза в матке;
3) изменения в лизосомной функции клеток эндометрия;
4) регенерация эндометрия.
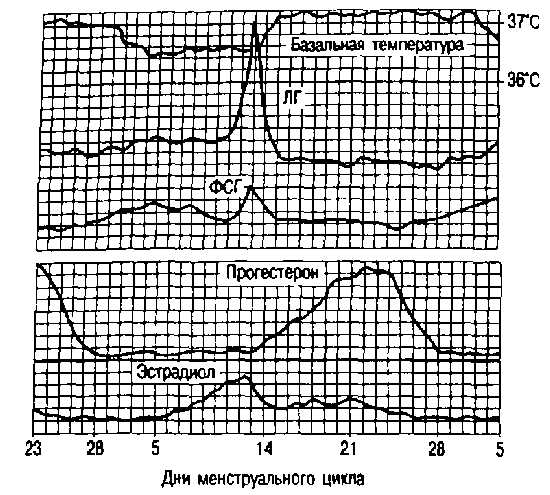
Рис. 2.13. Содержание гормонов в плазме крови в течение менструального цикла.
Установлено, что началу менструации предшествует интенсивное сужение спиральных артериол, приводящее к ишемии и десквамации эндометрия.
В течение менструального цикла изменяется содержание лизосом в клетках эндометрия. Лизосомы содержат ферменты, некоторые из которых участвуют в синтезе простагландннов. В ответ на снижение уровня прогестерона усиливается выделение этих ферментов.
Регенерация эндометрия наблюдается с самого начала менструации. К концу 24-го часа менструации отторгается 2/з функционального слоя эндометрия. Базальный слой содержит эпителиальные клетки стромы, являющиеся основой для регенерации эндометрия, которая обычно к 5-му Дню цикла полностью завершается. Параллельно завершается ангиогенез с восстановлением целости разорванных артериол, вен и капилляров.
Изменения в яичниках и матке происходят под влиянием двухфазной деятельности регулирующих менструальную функцию систем: кора большого мозга, гипоталамус, гипофиз. Таким образом, выделяются 5 основных звеньев репродуктивной системы женщины: кора большого мозга, гипоталамус, гипофиз, яичник, матка (рис. 2.14). Взаимосвязь всех звеньев репродуктивнои системы обеспечивается наличием в них рецепторов как к половым, так и к гонадотропным гормонам.
Атипическая гиперплазия эндометрия – это патологическое разрастание внутреннего слоя матки с появлением атипических клеток. Провоцируется избытком эстрогенов и недостатком прогестерона. Рассматривается, как предраковое заболевание. Может развиваться в любом возрасте, однако чаще выявляется после 45 лет. Сопровождается нарушениями менструального цикла и маточными кровотечениями (меноррагиями, метроррагиями). Диагноз устанавливается на основании жалоб, анамнеза и данных дополнительных исследований. Лечение – гормонотерапия, выскабливание или абляция слизистой оболочки.
МКБ-10


Общие сведения
Атипическая гиперплазия эндометрия – усиленная пролиферация эндометрия, сопровождающаяся изменением морфологии клеток. Данные о распространенности отсутствуют. Патология чаще выявляется у женщин в возрасте 45-55 лет. Длительная повторяющаяся гиперплазия в период климакса и менопаузы рассматривается как предраковое заболевание. Вероятность злокачественного перерождения в зависимости от формы болезни колеблется от 8 до 29%. Атипическая гиперплазия эндометрия нередко сочетается с другими заболеваниями репродуктивной системы. Тактика лечения определяется в зависимости от возраста больной, ее желания иметь детей, наличия или отсутствия сопутствующей генитальной и экстрагенитальной патологии. Лечение осуществляют специалисты в области клинической гинекологии и онкологии.

Причины
Развитие данного заболевания обусловлено увеличением уровня эстрогенов, уменьшением уровня прогестерона и наличием или отсутствием овуляции. Эстрогены и прогестерон участвуют в регуляции циклических изменений эндометрия. В первой фазе менструального цикла эстрогены обеспечивают пролиферацию клеток. Во второй фазе прогестерон подавляет пролиферацию и стимулирует секрецию. При отсутствии овуляции, относительной или абсолютной гиперэстрогенемии фаза секреции либо не наступает, либо проявляется недостаточно ярко. Клетки функционального слоя эндометрия продолжают разрастаться, возникает гиперплазия.
Факторы риска
Предрасполагающими факторами развития атипической гиперплазии эндометрия являются:
- возрастные изменения уровня половых гормонов;
- раннее начало менструаций;
- позднее начало климакса;
- заболевания и состояния, сопровождающиеся ановуляцией и нарушением функции яичников (синдром поликистозных яичников, гормонпродуцирующие опухоли яичников);
- соматические патологии: ожирение, гипертоническая болезнь, сахарный диабет и другие болезни эндокринной системы;
- воспалительные заболевания и врожденные аномалии репродуктивной системы;
- множественные аборты и диагностические выскабливания;
- наследственная предрасположенность;
- прием эстрогенсодержащих препаратов и тамоксифена.

Патогенез
Атипическая гиперплазия эндометрия характеризуется патологическим разрастанием функционального слоя слизистой оболочки матки, при этом железистая ткань эпителия подвергается более выраженным изменениям по сравнению с элементами стромы. В процессе гистологического исследования выявляется увеличение количества желез и отек стромы. Железы располагаются близко друг к другу. Сосуды расположены неравномерно. Клетки эпителия с гиперхромными ядрами. Определяются многочисленные патологические митозы.
В зависимости от особенностей расположения железистых клеток различают две формы атипической гиперплазии эндометрия: простую и аденоматозную. При простой форме наблюдается увеличение количества и избыточное разрастание клеток без изменения структуры слизистой оболочки. При аденоматозной форме из железистых клеток формируются особые структуры, отсутствующие в эндометрии здоровой матки. Эти структуры могут быть расположены на всем протяжении эндометрия (диффузная форма) или образовывать отдельные очаги (очаговая форма). Кроме того, участки аденоматозной гиперплазии могут обнаруживаться в области полипов матки.
Симптомы
Основным симптомом данного заболевания являются маточные кровотечения. У большинства пациенток такие кровотечения возникают на фоне задержки менструации сроком на 1-3 месяца. Реже (как правило, при отсутствии ожирения и явной эндокринной патологии) наблюдаются регулярные циклы при продолжительности меноррагии более 7 дней. Примерно у четверти больных с атипической гиперплазией эндометрия выявляются ановуляторные маточные кровотечения. В 5-10% случаев диагностируются метроррагии. Возможны скудные кровянистые выделения в середине менструального цикла либо при отсутствии менструаций.
Диагностика
Диагноз устанавливают на основании жалоб, данных анамнеза и результатов инструментальных исследований. В ходе опроса гинеколог выясняет возраст менархе, устанавливает длительность цикла, продолжительность и обильность менструаций, уточняет, были ли задержки цикла и кровянистые выделения. Затем врач осуществляет гинекологический осмотр и назначает на трансвагинальное УЗИ для оценки состояния эндометрия (его структуры, толщины, однородности) и выявления патологических изменений яичников (признаков опухоли, кисты или СПЯ).
Точность диагностики гиперпластических процессов при проведении УЗИ составляет 60-70%, однако подтвердить или опровергнуть атипию эндометрия с помощью ультразвукового исследования обычно не удается. Больную направляют на УЗИ на 5-7 день цикла. При длительных кровотечениях УЗИ назначают вне зависимости от фазы цикла. В норме в детородном возрасте толщина слизистой оболочки матки составляет не более 7 мм, при постменопаузе длительностью менее 5 лет – не более 5 мм, при постменопаузе длительностью более 5 лет – не более 4 мм. Увеличение толщины, неоднородность структуры и наличие эхогенных включений позволяют заподозрить гиперплазию эндометрия.
В ряде случаев после УЗИ осуществляют аспирационную биопсию с последующим гистологическим или цитологическим исследованием аспирата. Эта процедура относится к категории скрининг-тестов и выполняется в амбулаторных условиях. Однако золотым стандартом диагностики атипической гиперплазии эндометрия является гистероскопия и раздельное диагностическое выскабливание. Информативность исследования составляет более 90%.
При подозрении на СПЯ и метаболический синдром назначают анализы крови для определения уровня прогестерона, тестостерона, эстрадиола, ЛГ, ФСГ, гормонов надпочечников и щитовидной железы. Выполняют маммографию. При частых рецидивах проводят лапароскопию с биопсией или клиновидной резекцией яичников и последующим гистологическим исследованием материала.
Атипическую гиперплазию эндометрия дифференцируют с другими заболеваниями, провоцирующими маточные кровотечения:
- аденомиозом;
- полипозом;
- подслизистой фибромой матки;
- злокачественными опухолями слизистой оболочки матки (аденокарциномой, раком тела матки).

Лечение атипической гиперплазии эндометрия
Лечение данной патологии может быть как консервативным, так и оперативным, проводиться амбулаторно или в условиях стационара. Показанием к плановой госпитализации в репродуктивном возрасте являются кровотечения и кровянистые выделения, в постменопаузе – кровотечения, продолжительные водянистые или гнойные выделения. Экстренная госпитализация показана при обильных кровотечениях. Тактика лечения атипической гиперплазии эндометрия определяется с учетом возраста больной, ее желания иметь детей, наличия соматических заболеваний и болезней репродуктивной системы (особенно – аденомиоза или миомы), формы атипической гиперплазии эндометрия и количества рецидивов.
- Остановка кровотечения. При наличии метроррагии или меноррагии на первом этапе проводят мероприятия по остановке кровотечения и восполнению кровопотери. Выполняют выскабливание эндометрия, назначают окситоцин и холод на низ живота. Применяют препараты железа. При необходимости переливают кровь и кровезаменители. Осуществляют инфузионную терапию с использованием изотонического раствора, раствора глюкозы, желатиноля или декстрана для восстановления водно-электролитного баланса и улучшения реологических свойств крови.
- Фармакотерапия. Больным с атипической гиперплазией эндометрия в течение 3-6 месяцев проводят гормональную терапию, направленную на подавление пролиферации слизистой оболочки. В последующем назначают гормональные препараты для восстановления двухфазного менструального цикла или достижения стойкой менопаузы. Гормонотерапию осуществляют на фоне приема витаминов, гипосенсибилизирующих препаратов и гепатопротекторов.
- Хирургическое лечение. В качестве показаний к оперативному лечению рассматривают все случаи атипической гиперплазии эндометрия в постклимактерическом периоде, а также наличие противопоказаний к гормональной терапии, отсутствие эффекта от консервативной терапии и рецидивы заболевания у женщин репродуктивного возраста. Выполняют абаляцию эндометрия – малоинвазивное хирургическое вмешательство, целью которого является разрушение или удаление всей толщи слизистой оболочки. Операцию проводят гистероскопически с использованием высокочастотных токов.
Диспансерное наблюдение после консервативного лечения осуществляют в течение 5 лет, после хирургического вмешательства – в течение 6 месяцев.
Прогноз
Прогноз при атипической гиперплазии эндометрия зависит от возраста, склонности болезни к рецидивированию, наличия сопутствующей генитальной и экстрагенитальной патологии. Возможно полное выздоровление с сохранением репродуктивной функции, выздоровление с утратой репродуктивной функции или перерождение в злокачественную опухоль эндометрия. В последнем случае потребуется гистерэктомия или пангистерэктомия (удаление матки совместно с аднексэктомией). Прогностически неблагоприятными считаются сочетания атипической гиперплазии эндометрия с любыми обменными нарушениями и заболеваниями эндокринной системы, особенно – в возрасте старше 45 лет. Риск злокачественного перерождения при простой форме заболевания составляет 8%, при аденоматозной – 29%.
2. Лечение атипической гиперплазии эндометрия/ Е.Г. Новикова, О.В. Чулкова, С.М. Пронин// Практическая онкология. - 2004 - Т.5, №1.
3. Атипическая гиперплазия эндометрия (диагностика, клиника и лечение)/ Пушкарев В.А., Кулавский Е.В., Хуснутдинов Ш.М., Мустафина Г.Т.// Креативная хирургия и онкология. - 2010.
Читайте также:

