Индифферентный эпителий что это такое
Обновлено: 05.05.2024
Индифферентная стадия развития половых органов эмбриона. Происхождение гонад плода
Рассматривая вопрос о половой дифференциации, можно ожидать, что органы размножения, столь различные у взрослых особей мужского и женского пола, уже с самого момента своего появления должны резко отличаться друг от друга. В действительности это не так. Ранние эмбрионы имеют гонады, которые не обладают никакими признаками, позволяющими решить, превратятся ли они в семенники или в яичники. С этими индифферентными гонадами связаны две системы половых протоков.
Мужские протоки развиваются из протоков регрессирующих мезонефросов. Проток мезонефроса используется в качестве пути, по которому выделяются половые клетки. Некоторые из канальцев мезонефроса также связаны с развивающейся гонадой. Женские протоки — мюллеровы каналы — развиваются рядом с протоками мезонефросов, но независимо от них и в течение некоторого времени обе системы протоков присутствуют вместе.
У эмбрионов мужского пола, потенциальные женские протоки остаются рудиментарными, а протоки и соответствующие канальцы мезонефросов испытывают дальнейший рост и дифференцировку, приводящие к созданию системы протоков семенников. У развивающихся эмбрионов женского пола мюллеровы протоки образуют маточные трубы, матку и влагалище, а мужские протоки превращаются в рудименты.
Поэтому рассмотрение развития органов размножения следует начинать с индифферентной стадии у обоих полов.
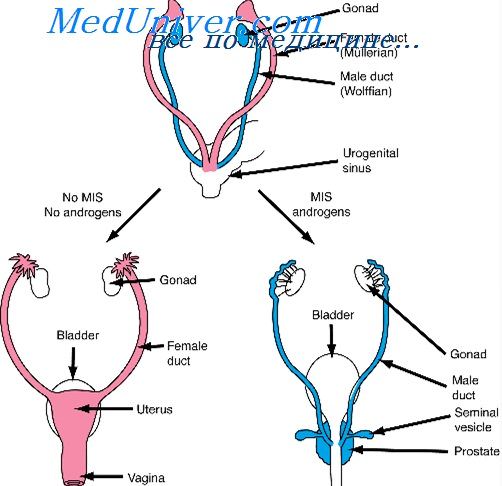
С самого момента своего появления гонады тесно связаны с мочевыделительной системой. В то время, когда мезонефрос является еще главным выделительным органом, гонады образуются в виде гребневидных утолщений (гонадные валики) на вентральных краях мезонефросов. Гистологически гонадные валики состоят в основном из тесно расположенных клеток, покрытых мезотелием. Мезотелиальная оболочка развивающейся гонады непосредственно переходит в мезотелиальную оболочку мезонефроса, являясь фактически лишь частью ее, распространившейся на развивающуюся гонаду.
Вскоре, однако, эта оболочка начинает обнаруживать свойства, отличающие ее от соседнего мезотелия. Она становится заметно толще, а клетки ее округляются и увеличиваются в размерах. Некоторые из клеток зачаткового эпителия, как теперь называется этот измененный слой мезотелия, становятся значительно крупнее, нежели соседние клетки, и опускаются под поверхностный слой. Эти большие клетки являются первичными половыми клетками гонады. Недавно были опубликованы данные, свидетельствующие о том, что первичные половые клетки не образуются in situ в результате дифференциации мезотелиальных клеток.
Установлено, что их можно обнаружить в организме задолго до того, как они появятся в зачатковом эпителии, и что они мигрируют с места своего образования (энтодерма желточного мешка), оседают в гонадах и здесь размножаются.
Позднее они хорошо видны в зачатковом эпителии и его разрастаниях в более глубоких частях гонад шестинедельных эмбрионов.
Независимо от того, развивается ли семенник или яичник, клетки зачаткового эпителия в обоих случаях вначале врастают в подлежащую мезенхиму и образуют тяжевидные массы. У эмбриона мужского пола эти тяжи начинают все более четко обособляться и в конце концов дифференцируются в семенные канальцы. Если же развивается яичник, примордиальные клеточные тяжи разбиваются на группы клеток и начинают дифференцироваться в первичные фолликулы. Дивергентная дифференциация гонад у обоих полов будет рассмотрена ниже.
- Вернуться в оглавление раздела "Акушерство."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
В современном мире неуклонно растет количество женщин постменопаузального возраста на фоне общего старения населения планеты, обусловленного увеличением продолжительности жизни. Полипы слизистой оболочки полости матки (ПЭ) выявляются у 50% женщин страдающих маточным кровотечением в менопаузе. Они могут протекать бессимптомно, но все чаще выявляются при УЗИ, гистероскопии. ПЭ отличаются многообразием форм гистологического строения, особенностями фоновых состояний, что, несомненно, влияет на течение болезни и прогноз. На фоне полипов в 1,39-15,74% могут развиваться злокачественные опухоли из эпителия – раки. Однако работы, посвященные этой проблеме единичны, сведения приводимые в них противоречивы.
В данной работе мы изучали особенности клинических проявлений, строения полипов у женщин с атрофией эндометрия в постменопаузе, возможности их озлокачествления, виды возникающих в них опухолей.
Материал и методы
Полипы на фоне атрофии эндометрия были обнаружены у 100 пациенток (78,13%). Согласно классификации предложенной Волошиным В.В. (2010) все они были отнесены к железисто-фиброзным атрофическим полипам (АП). АП отличали выраженная ножка со склерозированными сосудами, грубая коллагенизированная строма (площадь ее более 30%), преобладающая над железистым компонентом. Железистые ходы мелкие овальной формы или кистозно-расширенные были выстланы однорядным цилиндрическим эпителием с мелкими гиперхромными овальными ядрами не различимыми ядрышками. Такой эпителий называют «индифферентным», атрофическим. Митозы в клетках стромы и эпителии полипов отсутствовали. АП возникали на фоне атрофического эндометрия, в том числе кистозной атрофии – 35 наблюдений, и в этих случаях при УЗИ ставился диагноз гиперплазии слизистой оболочки полости матки.
В 52 (52,%) случаях они протекали бессимптомно, в 48 (48,0%) – проявились маточными кровотечениями. Ожирение у пациенток с АП отмечено в 24,0% наблюдений, сахарный диабет – в 19,0%, гипертензия – в 45,0% .
Рак на фоне АП был диагностирован в 4 (4,0%) случаях. Опухоль состояла из коротких с плотной стромой или длинных тонких папиллярных, или щелеподобных железистых структур покрытых одно – или многорядным цилиндрическим эпителием. Клетки его полиморфные с гиперхромными ядрами и крупными ядрышками. В них отмечалась выраженная экспрессия маркеров Ki 67 (32,7 + 1,7%) и p53 (35,4+3,2%). Экспрессия маркеров ER была низкой (2-3 – по Allred). РR в клетках опухоли не определялись. Морфологическая и иммуногистохимическая характеристика опухоли соответствовали серозной карциноме. В 1 наблюдении опухоль была ограничена полипом, в 3 – она прорастала в окружающий эндометрий и миометрий до 1/2 толщины, отмечалась инвазия в сосуды. У 2 больных карцинома прорастала железы и строму слизистой оболочки цервикального канала, т.е., соответствовала II B стадии. У всех пациенток новообразования проявились кровотечением. Лишь одна из этих больных страдала ожирением и артериальной гипертензией.
1. В постменопаузе чаще всего – 75,0%, на фоне атрофии эндометрия развиваются АП.
2.АП отличают выраженная сосудистая ножка, плотная склерозированная строма (площадью более 30%) и железы, выстланные «индифферентным» эпителием.
3. Развитие АП, видимо, не связано с нарушением гормонального статуса.
4. На фоне АП может развиваться серозная аденокарцинома – гормононезависимая опухоль с высокой степенью инфильтративного роста, неблагоприятным прогнозом.
5. Потому морфологическое исследование полиповидных образований развивающихся в менопаузе на фоне атрофии эндометрия является чрезвычайно важным и обязательным.
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
Биопсия эндометрия матки – процедура, во время которой производится забор образцов слизистой оболочки матки - эндометрия. Образцы ткани доставляют в лабораторию, где проводится гистологический анализ – изучение ткани слизистой оболочки и выявление атипичных признаков в клетках.
- причин бесплодия и самопроизвольного прерывания беременности;
- гормональных отклонений;
- причин маточных кровотечений не связанных с менструацией;
- гиперплазии эндометрия – разрастания слизистой оболочки матки;
- злокачественных изменений – рака матки.
- Пайпель биопсия – забор материала проводят с помощью тонкой пластиковой трубочки с боковым отверстием на конце. С помощью поршня в трубочке создается отрицательное давление, благодаря чему в цилиндр всасывается ткань маточных желез и эндометрия. Считается наименее травматичным методом взятия материала.
- Аспирационная биопсия – принцип проведения процедуры тот же, что и при Пайпель биопсии, но для создания отрицательного давления используется шприц или электрический вакуумный аппарат.
- Диагностическое выскабливание матки – забор материала с помощью хирургической ложки – кюретки. Гинеколог соскабливает верхний слой слизистой с отдельных участков или со всей поверхности матки. Слизистую выскабливают полностью или в виде штриховых соскобов – цугов.
- Биопсия во время гистероскопии– бразцы слизистой матки получают во время эндоскопического обследования с помощью гистероскопа – зонда, оснащенного миниатюрной видеокамерой и миниатюрным хирургическим инструментом.
Исследование биоптата. В лаборатории биоптат обезвоживают, делают жирорастворимым, а затем пропитывают парафином, превращая в специальных формах в твердый кубик. С помощью микротома его нарезают на пластины, толщиной 3-10 мкм. Эти тончайшие слои ткани размещают на предметное стекло, окрашивают и накрывают вторым предметным стеклом, что позволяет зафиксировать материал и хранить его долгое время.
Врачи гистологи и патоморфологи изучают образцы ткани, используя световой микроскоп. Весь процесс занимает 7-10 дней, по истечении которых выдается заключение, в котором описываются особенности строения эндометрия. Окончательный диагноз ставится только в явных случаях. Большинству пациенток клинический диагноз ставит гинеколог, с учетом результатов биопсии и других обследований (субъективных симптомов, результатов осмотра, гистероскопии, кольпоскопии).
Классификация гиперплазии эндометрия и их критерии
В настоящее время на основании предложенной в 1994 г. классификации Международного общества гинекологов-патологов (ISGYP), Международной федерации акушеров и гинекологов (FIGO) и Всемирной организации здравоохранения (WHO, ВОЗ) выделяют четыре вида гиперплазии эндометрия в зависимости от гистологического строения и цитологических характеристик. В зависимости от структурных изменений желез и железистого эпителия различают простую и сложную гиперплазию, а в зависимости от цитологических характеристик — с наличием или отсутствием атипии.
В связи с этим выделяют четыре разных диагноза: простая гиперплазия без атипии, сложная гиперплазия без атипии, простая атипическая гиперплазия, сложная атипическая гиперплазия.
От терминов «аденоматозная» и «железисто-кистозная гиперплазия» решено отказаться. Поэтому встречающаяся аббревиатура АГЭ относится к атипической гиперплазии эндометрия и объединяет два ее варианта: простая и сложная АГЭ, с атипией клеток эпителия маточных желез. Наличие атипии — это самый важный критерий последующей прогрессии в аденокарциному или одновременного наличия эндометриальной аденокарциномы. По имеющимся данным, сосуществование эндометриальной аденокарциномы и АГЭ отмечается не менее чем в 13 % и не более чем в 43 % случаев.
Классификация гиперплазии эндометрия:
- Простая гиперплазия
- Сложная гиперплазия (аденоматозная)
- Простая атипическая гиперплазия
- Сложная атипическая гиперплазия (аденоматозная с атипией)
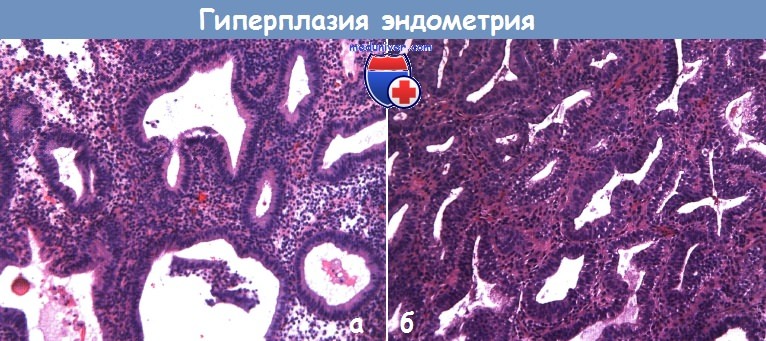
а - простая гиперплазия без атипии: эндометрий утолщен за счет железистого эпителия, что вызвано воздействием только эстрогенов, без прогестерона.
Железы характеризуются неравномерными, зачастую непредсказуемыми, очертаниями.
Строма обильная, поэтому соотношение железистая/стромальная ткань мало отличается от нормального.
Окраска гематоксилином и эозином, х10
б - сложная гиперплазия без атипии: соотношение железистая/стромальная ткань увеличено, при этом железы расположены тесно, имеют сложное строение, просветы часто неправильной формы.
Атипия ядер выражена незначительно. Окраска гематоксилином и эозином, х20
Диагностика этих поражений обычно основана на гистологическом исследовании небольшого биоптата эндометрия, полученного в амбулаторных условиях с помощью специального гибкого стерильного пластикового устройства Pipelle. Онкогинекологическая исследовательская группа (GOG) выполнила проспективное исследование воспроизводимости результатов диагностики простой и атипической гиперплазии эндометрия. В исследование были включены женщины с диагностированной АГЭ в одном из 285 институтов GOG, которые дали согласие на выполнение гистерэктомии в течение ближайших 12 нед. Выборка данного исследования включала 302 соответствующих критериям включения женщины, медиана возраста составила 57 лет, при этом 31 % пациенток были моложе 50 лет.
Все микропрепараты эндометрия были пересмотрены 3 независимыми экспертами-патоморфологами-гинекологами в условиях слепого метода. Они согласились использовать следующие обозначения состояния эндометрия: нормальный (эндометрий стадии пролиферации, секреции, атрофичный, менструальный), неатипическая гиперплазия (беспорядочная пролиферация, простая или сложная гиперплазия), атипическая (простая или сложная) гиперплазия, аденокарцинома или неудовлетворительный для оценки биоптат. Для постановки диагноза требовалось, чтобы 2 из 3 экспертов выбрали один и тот же из пяти возможных диагнозов.
Правильный диагноз выставлялся на основании консенсуса специалистов после независимого гистологического исследования послеоперационного материала. Все 3 специалиста пришли к единому заключению в 40 % случаев. Воспроизводимость была наименьшей для диагноза АГЭ (к = 0,28), в отношении аде-нокарциномы показатель был лучше (к = 0,51). При раздельном выскабливании слизистой оболочки матки воспроизводимость была лучше (к = 0,47; доверительный интервал [ДИ] 0,41—0,53), чем при биопсии (к = 0,26—0,36). 2 из 3 экспертов согласились с установленным ранее диагнозом АГЭ в 38 % случаев. У 25 % пациенток согласительная комиссия изменила диагноз на менее тяжелый, при этом аденокарцинома была диагностирована в 29 % случаев. Наиболее важным результатом данной работы GOG стало доказательство того факта, что у 43 % пациенток во время выполнения гистерэктомии была аденокарцинома эндометрия.
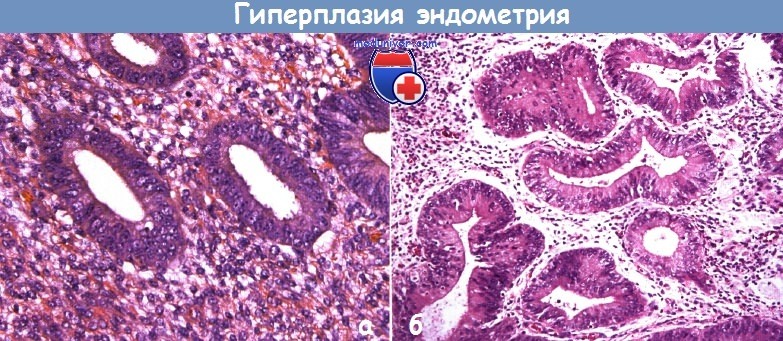
а - простая атипическая гиперплазия.
Редко диагностируемая форма гиперплазии, при которой железистый компонент преобладает над стромальным за счет простых желез, выстланных эпителием с атипичными ядрами.
Окраска гематоксилином и эозином, х40
б - сложная атипическая гиперплазия.
Значительное преобладание железистого компонента над стромальным, железы имеют сложное строение, клетки эпителия с атипией ядер.
Окраска гематоксилином и эозином, х20.
Другим серьезным итогом можно считать определение истинного процента аденокарцином в каждой группе больных с установленным до операции диагнозом: в группе нормального эндометрия и гиперплазии без атипии — 14/74 (18,9 %), в группе АГЭ — 45/115 (39,1 %) и в группе аденокарциномы — 54/84 (64,3 %). В 43 случаях исследование матки выявило такие факторы риска метастазирования, как инвазию в миометрий, умеренно- (G2) и низкодифферснцированные (G3) опухоли.
Простая гиперплазия без признаков атипии, как правило, протекает доброкачественно. Наиболее часто она встречается в период пременопаузы, характеризующийся появлением ановуляторных циклов. Устранение гиперэстрогении или терапия прогестагенами определяют исход заболевания. Большинство патологических изменений (60 %) исчезает без лечения, а при терапии прогестинами эффект будет достигнут у 84 % больных. Считается, что только в 3 % случаев происходит трансформация простой гиперплазии в РЭ.

а - высокодифференцированная аденокарцинома эндометрия (G1): железы расположены тесно, строма между ними скудная.
Железы выстланы высокими цилиндрическими опухолевыми клетками.
Окраска гематоксилином и эозином, х20
б - низкодифференцированная аденокарцинома эндометрия (G3) характеризуется утратой железистой структуры практически во всей опухоли.
По форме клетки округлые полигональные, но не цилиндрические. При данной патологии часто наблюдается некроз клеток (вверху справа).
Окраска гематоксилином и эозином, х20.
Сложная гиперплазия при отсутствии атипии клеток эпителия маточных желез также регрессирует в большинстве (56 %) случаев. Для АГЭ характерна трансформация в раку 36 % больных, причем в 27 % случаев заболевание прогрессирует даже на фоне терапии прогестинами, но при этом остается неясным, не отражает ли последний показатель синхронно протекающий РЭ. Подсчитано, что в 55 % случаев на фоне терапии прогестинами АГЭ регрессирует. Наилучший препарат из группы прогестинов для лечения данной патологии все еще не установлен. Точно так же необходимо уточнить схему назначения (циклический режим или непрерывный) и продолжительность лечения.
Считается, что при невозможности устранения гиперэстрогении показана пожизненная терапия прогестинами. В качестве альтернативного метода возможна гистерэктомия с целью предотвратить развитие наиболее часто встречающейся эстрогензависимой эндометриальной аденокарциномы I типа. Этот тип эстроген-индуцированного рака эндометрия (РЭ) — наиболее распространенный и менее агрессивный; поэтому и профилактика, и лечение должны бытьуспешными.
Внедрение современных научных разработок, в т. ч. молекулярных методов исследования поражений эндометрия и объективной компьютеризованной морфометрии, обещает увеличить точность и воспроизводимость диагностики новообразований эндометрия. В 2003 г. ВОЗ была предложена новая классификация, в которой в качестве предракового состояния описывается эндометриальная ин-траэпителиальная неоплазия (ЭИН). Первые данные свидетельствуют о лучшей прогностической значимости ЭИН при определении риска малигни-зации, однако этот термин до сих пор не используют в клинике.
На фоне атрофии эндометрия развивается серозно-папиллярный РЭ, который этиологически не связан с гиперэстрогенией; его классифицируют как РЭ II типа или эстрогеннезависимый. Гиперплазия эндометрия не относится к предшественникам серозного рака. Наиболее вероятно, что его предшественником считается интраэпителиальный рак эндометрия. Серозный рак эндометрия (РЭ) может быть мультифокальным по происхождению и поражать яичники и сальник, без признаков инвазии в миометрий. Учитывая, что при обычной ревизии органов брюшной полости и таза во время лапарото-мии невозможно определить инвазивный рост опухоли, рекомендуется тщательное хирургическое стадирование заболевания.
Вероятность выявления серозно-папиллярного рака на ранних стадиях заболевания ниже, чем при других гистологических типах РЭ. После получения результата гистологического исследования и установления стадии заболевания определяют характер послеоперационной терапии. Серозный вариант новообразования зачастую обусловлен нарушением функции гена-супрессора опухолевого роста ТР53, что ведет к накоплению белка р53 в клетке. Иммуногистохимическое исследование с применением антител к белку р53 дает положительный результат в большинстве случаев серозных опухолей в отличие от нормального эпителия эндометрия или РЭ.

а - интраэпителиальный рак эндометрия (ИРЭ) - поражение, предшествующее серозному раку эндометрия, с выраженным атипическим уплотнением эпителия и незначительным нарушением архитектоники.
ИРЭ обычно наблюдается на поверхности доброкачественных полипов эндометрия.
Окраска гематоксилином и эозином, х20.
б - иммуногистохимическое окрашивание интраэпителиального рака эндометрия на р53.
Мутации ТР53, ведущие к повышенному накоплению белка р53, характерны для серозного рака эндометрия.
В нормальных клетках содержание неизмененного белка р53 ниже порогового уровня и результат анализа отрицательный.
Иммунопероксидазное окрашивание на р53 с хромогеном DAB, х20.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Цитологическое исследование желудка. Гастрограммы.
При цитологическом изучении материала, полученного из желудка с помощью гастробиопсии, в препаратах отчетливо определяют клеточные элементы слизистой оболочки желудка: покровно-ямочный эпителий, главные и обкладочные клетки желез.
Соотношение в цитологических препаратах клеточных элементов слизистой оболочки желудка, различная степень их дифференцировки, появление признаков дегенерации и атипии, а также появление лейкоцитов, ретикулярных и гистиоидных элементов позволяют выявить типы гастроцитограмм. которые наиболее свойственны тому или другому заболеванию желудка.
Гастроцитограммы больных хроническим гастритом характеризуются наличием клеток покровно-ямочного эпителия, которые располагаются преимущественно небольшими пластами и скоплениями. Клетки имеют высоко- и низкоцилиндрическую форму, базально или центрально расположенное ядро. широкую,слабобазофильную цитоплазму. Ядра клеток отличаются некоторым полиморфизмом, имеются все переходы от незрелых относительно крупных, светлых с нежносетчатым рисунком хроматина до зрелых небольших размеров, интенсивно окрашенных ядер.
Главные и обкладочные клетки желез обнаруживают в различном количестве, расположены разрозненно, небольшими округлыми группами или ровными рядами, в которых отмечается правильное чередование главных и обкладочных клеток. В главных клетках отчетливо просматриваются окрашенные в сине-фиолетовый цвет грубые гранулы, заполняющие всю цитоплазму. Обкладочные клетки отличаются широкой светлой цитоплазмой, окрашенной в нежно-розовый цвет. В препаратах встречаются лимфоидные элементы и полиморфно-ядерные нейтрофильные лейкоциты.
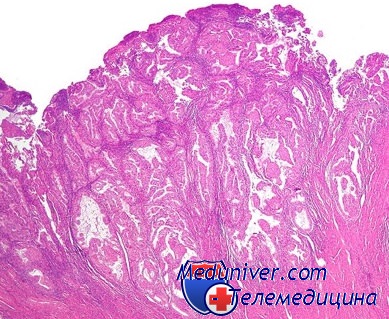
В цитограммах при полипах желудка большое количество пластов и больших скоплений покровно-ямочного эпителия, встречаются железисто-подобные структуры. По сравнению с цитограммами при гастрите можно отметить преобладание молодых, незрелых клеток с укрупненными ядрами и нежным рисунком хроматина в них.
При язвенной болезни желудка в гастроцитограммах преобладают сег менто-ядерные нейтрофилы, кроме того, обнаруживаются в значительном количестве лимфоциты, плазматические клетки, эозинофилы, клетки гистиоидного тина, скопления полиморфных эпителиальных клеток. В эпителии обычно отмечают признаки дегенерации в виде вакуолизации цитоплазмы и ядер, кариолизиса, кариорексиса и плазмолиза.
Однако необходимо отметить, что при цитологическом исследовании материала при неопухолевых и опухолеподобных поражениях желудка далеко не всегда возможно диагностировать эти заболевания. Последнее зависит от того, что изменения в клетках носят однотипный характер и часто можно обсуждать только степень клеточной пролиферации, атнпии и перестройки эпителия по кишечному типу.
Из злокачественных новообразований в желудке наиболее часто встречается аденокарцинома трех видов адеиокарцинома с высокой и низкой степенью дифференцировки, а также аденокарцинома с выраженным слизеобразованием. Реже встречаются перстневидноклеточный и недифференцированный рак, а также другие неэпителиальные опухоли.
Цитограммы больных раком желудка характеризуются наличием клеток с морфологическими признаками злокачественности. Клетки располагаются комплексами, в виде железисто-подобных или папиллярных структур, разрозненно. В комплексах и структурах отмечается беспорядочное нагромождение ядер. Клетки крупных размеров. Ядра занимают почтя всю клетку, преимущественно неправильной формы, гиперхромиые с грубым, неравномерно распределительным хроматином, гипертрофированными множественными нуклеоламн.
Гистологическую форму опухоли не всегда удается установить, чаше это возможно в случаях аденокарциномы, где, как правило, обнаруживаются железисто-подобные структуры. Коллоидный рак характеризуется наличием большого количества слизистых масс и перстневидных опухолевых клеток При малоднфференцированном раке резко анаплазированные клетки, с большим числом фигур деления, обычно располагающиеся разрозненно.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

