Группы инвалидности при дерматите дюринга
Обновлено: 19.04.2024
Герпетиформный дерматоз Дюринга – кожное проявление глютеновой энтеропатии. Различные проявления этой энтеропатии можно выявить у 90% больных герпетиформным дерматитом при изучении биоптатов кишечника, однако, клинические проявления отмечаются только у 20% пациентов. На сегодняшний день доказано, что у большинства пациентов существует генетическая предрасположенность, обусловленная генотипом HLA класса DQ2 [7].
Герпетиформный дерматит Дюринга был открыт в 1884 году Луисом Дюрингом, врачом из Пенсильвании.
Клинически заболевание проявляется везикулами и экскориированными папулами на разгибательных поверхностях конечностей. На данных клинической картины провести дифференциальный диагноз между линеарным IgA дерматитом и герпетиформным дерматитом Дюринга невозможно, так как единственным их отличием является расположение IgA в сосочковой дерме при прямой иммунофлюоресценции (при дерматите Дюринга – глыбками, а при линейном IgA дерматите – линейно). Небольшим различием между этими дерматозами является возраст начала заболевания. Герпетиформный дерматит Дюринга, как правило начинается в молодом возрасте, а линейный IgA дерматит может возникать в результате токсического действия препаратов в старшем возрасте.
Основными патогенетическими звеньями герпетиформного дерматита Дюринга на сегодняшний день общепризнанны:
1. Наследственная предрасположенность;
2. Глютеновая энтеропатия;
3. Гранулярное расположение IgA в сосочковой дерме;
4. Инфильтрация сочков дермы нейтрофилами;
5. Быстрый ответ на действие дапсона и ухудшение состояния при приеме препаратов йода [7].
Так, Скрипкин Ю.К. и Беренбейн Б.А. (1989, 1995) описывают диагностику герпетиформного дерматита Дюринга следующим образом:
«диагностика основывается на +++ эозинофилии пузыря и нередко крови» [2, 4].
Гистологическая картина герпетиформного дерматита Дюринга обусловлена отложениями нейтрофилов в сосочках дермы, вызванными скоплениями IgA. Лизосомальные ферменты нейтрофилов вызывают отслойку базальной мембраны и формирование субэпидермальных пузырьков (рис. 1).
Эозинофилы могут присоединяться вторично лишь при поздних высыпаниях герпетиформного дерматита, однако, патогенетической роли они не играют. По данным различных авторов частота встречаемости эозинофилов в пузырьках и инфильтрате различна. Одно из самых больших исследований инфильтрата 105 биоптатов кожи при герпетиформном дерматите Дюринга показало, что эозинофилы присутствуют в них лишь в 52% случаев [5].
Эозинофилы являются обязательным критерием гистологической диагностики буллезного пемфигоида, при котором формируются эозинофильные абсцессы [7, 8, 9]. Эозинофилия крови может отмечается у 50% больных буллезным пемфигоидом, а не дерматитом Дюринга [6, 7, 8, 9]. Однако, вследствие того, что эозинофилия крови является признаком многих процессов, считать этот признак диагностическим критерием нельзя. Поздние стадии герпетиформного дерматита Дюринга и буллезного пемфигоида при обычном гистологическом исследовании неотличимы, так как эозинофилы присутствуют в обоих случаях.
Таким образом, обнаружение эозинофилов в пузырьке ни в коем случае не может является критерием для диагностики герпетиформного дерматита Дюринга и не позволяет провести дифференциальный диагноз между этими заболеваниями. Наличие эозинофилов следует скорее считать признаком буллезного пемфигоида, хотя и это заключение только предположительно.
Мазок отпечаток возможно взять только со дна свежего вскрывшегося пузыря, наличие которых при герпетиформном дерматите Дюринга нехарактерно. Типичными высыпаниями для герпетиформного дерматоза Дюринга являются волдыри, папулы, бляшки и небольшие везикулы, взятие материала из которых практически невозможно.
Правильная диагностика буллезных заболеваний кожи является необходимой, поскольку терапия данных заболеваний различна. Для лечения герпетиформного дерматита Дюринга используют сульфоновые препараты, а для буллезного пемфигоида – кортикостероиды. Вместе с тем, на основании неверного метода больным зачастую устанавливается диагноз «герпетиформный дерматит», а терапия дапсоном оказывается неэффективной, и дерматологи вынуждены использовать системные кортикостероиды, трактуя данный факт как «резистентность герпетиформного дерматита Дюринга к терапии дапсоном».
К сожалению, причин столь длительно существующей ошибки несколько. «Золотым стандартом» диагностики буллезных дерматозов является прямая и непрямая иммунофлюоресценция, которая отсутствует во всех диспансерах Беларуси.
Патоморфологическая служба в Беларуси при описании воспалительных заболеваний кожи является описательной и редко позволяет точно диагностировать заболевания. Причиной тому незнание четких гистологических критериев заболеваний и алгоритмического метода их диагностики. К сожалению, общие патоморфологи не знакомы с патогенезом кожных заболеваний, а ведущие зарубежные издания по дермопатологии являются малодоступными. На сегодняшний день общеизвестными критериями гистологической картины герпетиформного дерматоза Дюринга и буллезного пемфигоида являются (Таблица 1) [8, 9]:
Раннее патоморфологическое исследование кожи является обязательным, несмотря на то, что она позволяет лишь ориентировочно определить диагноз. Биопсия при подозрении герпетиформного дерматита Дюринга должна проводиться в области эритемы или же края везикулярного поражения. При обнаружении большого количества нейтрофилов диагнозом является герпетиформный дерматит Дюринга или линеарный IgA дерматоз, а при обнаружении эозинофилов – буллезный пемфигоид. Более точная диагностика может основана только на результатах прямой иммунофлюоресценции.
На сегодняшний день, к сожалению, ни один из установленных в Беларуси диагнозов герпетиформного дерматита Дюринга или буллезного пемфигоида, как, впрочем, и других буллезных дерматозов, не может считаться правомочным из-за отсутствия прямой и непрямой иммунофлюоресценции. Буллезный пемфигоид и герпетиформный дерматит Дюринга редки, заболеваемость по данным литературы не превышает 10 новых случаев на 1 000 000 населения, однако, вследствие сильнейшего зуда оба заболевания вызывают значительное снижение качества жизни, и поэтому своевременная их диагностика и терапия необходимы.
2. Беренбейн, Б.А. Дифференциальная диагностика кожных болезней: руководство для врачей / Б.А. Беренбейн, А.А. Студницын и [и др.]; под. ред. Б.А. Беренбейна, А. А. Студницина. - 2 - е изд. - Москва: «Медицина», 1989. - с. 672.
3. Клинические протоколы диагностики и лечения больных с болезнями кожи и подкожной клетчатки, утвержденные приказом МЗ РБ № 142 от 25.02.2008 г. // Рецепт (специальный выпуск). – Минск, 2008.
4. Кожные и венерические болезни: руководство для врачей: в 4 - х т. / под. ред. Ю.К. Скрипкина. - М.: Медицина, 1995. - Т. 2: Пузырные дерматозы / Б.А. Беренбейн. - 1995. - С. 247 - 341.
5. Dermatitis herpetiformis / B.L. Connor at al. // Trans. St. Johns Hosp. Dermatol. Soc. – 1972. – Vol. 58. – P. 191.
6. Lever`s histopathology of the skin. – 9th edition / ed. D.E. Elder et al. – PA: “Lippincott WW”, 2005. – 1229 p.
7. Dermatology / J. Bolognia et al. – Mosby, 2003. – P. 2500.
8. Histologic diagnosis of inflammatory diseases. An algorithmic method based on pattern analysis / B. Ackerman et al. – A. Shribendi, NY. – 2005. – 522 p.
Ребенку пять лет. С рождения страдаем атопическим дерматитом. Детский сад не посещаем. т.к. постоянно-рецидивирующий атопический дерматит широкого распространения. Лечимся платно у аллергологов, дерматологов. В стационарах не лежали. Алерголог сказала что можно оформиться на инвалидность. Ребенок почти не спит ночами, сильный зуд. Днем вся нервная. Есть ли шанс у нас формить инвалидность?
Думаю, что нет.
Не все больные (в том числе и страдающие дерматитами) признаются инвалидами.
В настоящее время - основным документом, руководствуясь которым эксперты бюро МСЭ решают вопрос о наличии (или отсутствии) у больного признаков инвалидности - является вступивший в силу с 02.02.2016г. Приказ Минтруда России от 17.12.2015 N 1024н
К данному Приказу имеется Приложение в виде таблицы, в которой приведена количественная (в процентах) оценка степени тяжести различной патологии (заболеваний).
Инвалидность устанавливается при процентах от 40% и выше (при одновременном наличии ОЖД в установленных категориях).
Конкретная группа инвалидности - зависит от размера процентов по приложению к Приказу 1024н.
10-30% - инвалидность не устанавливается.
40-60% - соответствуют 3-й группе инвалидности.
70-80% - соответствуют 2-й группе инвалидности.
90-100% - соответствуют 1-й группе инвалидности.
40-100% - соответствует категории "ребенок-инвалид" (для лиц моложе 18 лет).
В приложении к Приказу 1024н применительно к дерматиту имеются следующие пункты:
12.3.3 Атопический дерматит
12.3.3.1 Ограниченный, обостряющийся до двух раз в году - 10%
12.3.3.2 Диффузный, обостряющийся более двух раз в году, требующий стационарного лечения - 40%
Проще говоря, безусловным основанием для установления инвалидности по дерматиту по ныне действующему законодательству является наличие за последние 12 мес. перед МСЭ более 2-х стационарных лечений по поводу обострений диффузного (распространенного) дерматита.
Сам по себе факт отсутствия у больного стационарного лечения свидетельствует о том, что тяжесть имеющегося у него обострения дерматита не настолько велика, чтобы были оснований для его госпитализации.
Кроме того, в соответствии с действующим законодательством:
"На медико-социальную экспертизу гражданина направляет организация, оказывающая лечебно-профилактическую помощь в соответствии с п.16 «Правил признания лица инвалидом» ПОСЛЕ проведения необходимых диагностических, лечебных и реабилитационных мероприятий, при наличии данных, подтверждающих СТОЙКОЕ нарушение функций организма, обусловленное заболеваниями, последствиями травм или дефектами."
Проще говоря, СНАЧАЛА больного надо пролечить в течении определенного периода (для каждой патологии этот период свой), и уже только ПОСЛЕ проведенного лечения - по его результатам решать вопрос о наличии (или отсутствии) у него признаков инвалидности.
При неэффективности проводимого амбулаторного лечения - больного лечат в условиях стационара.
И только при отсутствии эффекта не только от амбулаторного, но и от стационарного лечения, можно говорить о наличии у больного СТОЙКОЙ (т.е. - не поддающейся ни амбулаторному, ни стационарному лечению) патологии.
СТОЙКОСТЬ патологии (наряду с ее ВЫРАЖЕННОСТЬЮ) являются ведущими критериями установления больному инвалидности.
Cостояние и нозологическая структура инвалидности по причине заболеваний кожи
Пазина М.В., Малишевская Н.П., Торопова Н.П., Лаврик И.Г., Плотникова И.А., Татарева С.В., Попова С.Д.
ФГУ «УрНИИДВиИ Росмедтехнологий», Научно-практический центр детской дерматологии и аллергологии, г. Екатеринбург
Цель исследования: Изучение социальных последствий заболеваемости хроническими дерматозами.
Mатериалы и методы: Проанализированы показатели инвалидности по причине заболеваний кожи за 2002-2006 гг., представленные кожно-венерологическими учреждениями (КВУ) из 7 произвольно выбранных территорий РФ, преимущественно Урала, Сибири и Дальнего Востока. Изучение структуры инвалидности по нозологическому признаку взрослых по причине заболеваний кожи проведено по данным за 2006 год, представленным из 19 КВУ, среди детей 0–17 лет — по данным из 17 КВУ. Возрастная структура детей — инвалидов по причине заболеваний кожи изучена по данным Свердловской области за 2005-2006 гг.
Выводы: Проведенный анализ состояния инвалидности населения по причине заболеваний кожи свидетельствует о большой социальной значимости проблемы хронических дерматозов, актуальность которой на фоне увеличения показателей заболеваемости и инвалидности возрастает.
Выявленная при проведении исследования значительная вариабельность показателей инвалидности по причине заболеваний кожи в различных территориях, а также отсутствие их регистрации в ряде КВУ особенно по детской популяции свидетельствуют не только о некачественном их мониторинге, но и отсутствии систематического анализа причин и факторов, способствующих инвалидизации. Эта составляющая социальных последствий хронических дерматозов может служить, с одной стороны, одним из критериев результативности диспансерного наблюдения больных, с другой — объективным обоснованием для разработки и финансирования целевых программ, направленных на повышение качества и доступности специализированной помощи больным с тяжелыми хроническими дерматозами, в том числе по своевременному оказанию им необходимых высокотехнологичных видов медицинской помощи.
ФАКТОРЫ, ПРИВОДЯЩИЕ К ИНВАЛИДНОСТИ ДЕТЕЙ, БОЛЬНЫХ АТОПИЧЕСКИМ ДЕРМАТИТОМ. ДИФФЕРЕНЦИАЦИЯ ПОДХОДОВ К НАРУЖНОЙ ТЕРАПИИ И УХОДУ ЗА КОЖЕЙ.
Торопова Н.П., Пазина М.В., Сорокина К.Н.
ФГУ Уральский НИИ дерматовенерологии и иммунопатологии Росмедтехнологий, г. Екатеринбург
Атопический дерматит (АтД), отличающийся хроническим течением с рецидивами, является одной из главных причин как госпитализации детей и подростков в специализированные клиники, так и установления инвалидности с детства. Среди госпитализированных в детское отделение Ур НИИДВиИ в 2005-2008 гг. больные АтД составляли от 31,2 до 33,9%, в ОГУ НПЦ детской дерматологии и аллергологии за тот же период от 46,4 до 54,3% (при общем числе госпитализированных детей с дерматозами 1219-1330). Тяжелое течение АтД, требующее неоднократного стационарного лечения в течение года, приводящее к «нарушению той или иной психологической, физиологической или анатомической структуры и функции», является основанием для установления инвалидности с детства.
В Свердловской области среди детей — инвалидов с детства по рубрике «Кожа и подкожная клетчатка» за период 2005-2008 гг. удельный вес больных АтД составлял 76,5-79,6% от общего числа детей-инвалидов с заболеваниями кожи (абсолютное число больных — 317-279). Возрастной состав детей-инвалидов с АтД: от 1 до 3 лет — 14,7-16,2%, от 3 до 7 лет — 27,2-29,0%, от 8 до 14 лет — 46,6-48,3%, от 15 до 18 лет — 8,0-10,0% (данные за 2007-2008 гг.). Таким образом, более 70% детей с АтД с установленной инвалидностью — больные в возрасте 3-14 лет.
Ранжирование факторов, предрасполагающих и поддерживающих тяжелое течение АтД, позволяет выделить ведущие из них, в том числе их сочетания у одного и того же больного. Так, патология беременности выявлена у 72,0%, родоразрешения — у 58,3%, в том числе: кесарево сечения (28%), тазовое предлежание (6,7%), агрессивное ведение родов (прием Кристеллера) — 23,4%; что приводит к тяжелым вегетососудистым нарушениям, патогенетическим значимым для АтД. При обследовании больных АтД с инвалидизирующими формами выявлены: паразитозы (39,9%), болезни нервной системы у детей предшкольного и школьного возраста (86,3%); болезни органов пищеварения (у 60,9%), поддерживающие хроническое течение дерматоза.
Особые требования предъявляются к выбору средств наружной терапии и уходу за кожей в связи со значительной площадью поражения кожи, частым присоединением вторичной инфекции, что приводит к необходимости одновременного использования различных наружных средств на очаги поражения (например, Афлодерм, Белогент, смягчающие и увлажняющие кремы — локобейз РИПЕА, топикрем и другие).
Герпетиформный дерматит Дюринга — хроническое рецидивирующее поражение кожи, проявляющееся полиморфной сыпью в виде эритематозных пятен, пузырей, папул, волдырей и сопровождающиеся выраженным зудом и жжением. Заболевание получило свое название благодаря тому, что элементы сыпи при дерматите Дюринга группируются таким же образом, как высыпания при герпесе. Диагностика проводится при помощи гистологического исследования, анализа содержимого пузырей и реакции прямой иммунофлуоресценции. В лечении герпетиформного дерматита Дюринга эффективна сульфоновая группа препаратов и кортикостероиды.
Общие сведения
Герпетиформный дерматит Дюринга встречается в любом возрасте, но наиболее часто он развивается в 30-40 лет. Мужчины более подвержены этому заболеванию, чем женщины. В некоторых случаях герпетиформный дерматит Дюринга является кожной реакцией на имеющуюся в организме злокачественную опухоль внутренних органов, то есть выступает в качестве параонкологического дерматоза.

Причины возникновения
Причины и механизм развития герпетиформного дерматита Дюринга неизвестны. У многих пациентов выявляется непереносимость белка глютеина, содержащегося в злаковых растениях. В пользу аутоиммунного компонента в развитии заболевания говорит обнаружение IgA-антител на границе дермы и эпидермиса — в области базальной мембраны. Предполагают, что определенную роль в возникновении герпетиформного дерматита Дюринга играют повышенная йодная чувствительность, наследственность, аскаридоз, воспалительные процессы желудочно-кишечного тракта (гастрит, язвенная болезнь), вирусные заболевания (ОРВИ, герпетическая инфекция и др.).
Симптомы
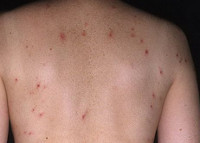
Обычно герпетиформный дерматит Дюринга имеет острое начало с появлением очагов полиморфной сыпи. Высыпаниям могут предшествовать умеренный подъем температуры тела, общая слабость, зуд и чувство покалывания. Элементы сыпи могут возникать на любом участке кожного покрова, кроме подошв и ладоней. Но наиболее частое их расположение — это разгибательные поверхности рук и ног, область лопаток, плечи, поясница и ягодицы. На ладонях могут возникать петехии и экхимозы — крупные (больше 3мм) пятна внутрикожных кровоизлияний. Высыпания сопровождаются выраженным дискомфортом: ощущением жжения, интенсивным зудом и парестезиями. Поражение слизистых оболочек при герпетиформном дерматите Дюринга, как правило, отсутствует. В редких случаях в полости рта могут возникать пузыри, быстро переходящие в эрозии.
Истинный полиморфизм сыпи при герпетиформном дерматите Дюринга связан с одновременным появлением на коже различного размера эритематозных пятен, волдырей, папул и пузырей. Со временем к истинному полиморфизму присоединяется ложный: образуются связанные с трансформацией высыпаний эрозии и корочки, а также вызванные сильным расчесыванием кожи экскориации. При заживлении элементов сыпи на коже остаются очаги гипо- и гиперпигментации, иногда рубцы.
Эритематозные пятна при герпетиформном дерматите Дюринга имеют четкий контур и округлую форму. Их гладкая поверхность часто покрыта расчесами, кровянистыми и серозными корочками. Со временем они пропитываются выпотом из расширенных сосудов и превращаются в похожие на волдыри (уртикароподобные) образования. Последние растут по периферии и сливаются, трансформируясь в розово-синюшные очаги, покрытые корочками, расчесами и пузырьками. Наряду с этим эритематозные пятна могут переходить в сочные розово-красные папулы. Кроме того, возникновение папул и уртикароподобных высыпаний может происходить без стадии эритематозного пятна.
Пузырные элементы сыпи при герпетиформном дерматите Дюринга могут быть небольшого размера — везикулы и диаметром более 2 см — буллезные высыпания. Они заполнены прозрачной жидкостью, помутнение которой говорит о присоединении инфекции. Пузыри вскрываются и подсыхают с образованием корки. Из-за расчесывания происходит снятие корки и на месте пузыря остается эрозия.
В зависимости от преобладания того или иного вида сыпи над остальными выделяют следующие виды герпетиформного дерматита Дюринга: папулезную, везикулезную, буллезную и уртикароподобную. Возможны атипичные варианты заболевания: трихофитоидные, экзематоидные, строфулоидные и др.
Острые периоды герпетиформного дерматита Дюринга сочетаются с довольно продолжительными ремиссиями (от нескольких месяцев до года и более). Обострения часто протекают с ухудшением общего состояния больного, подъемом температуры, нарушениями сна.
Диагностика
При подозрении на герпетиформный дерматит Дюринга проводят йодную пробу Ядассона. На здоровый участок кожи накладывают компресс с мазью, содержащей 50% йодида калия. Через 24 ч компресс снимают. Выявление на его месте покраснения, везикул или папул говорит в пользу герпетиформного дерматита Дюринга. Если проба отрицательна, то ее повторяют. Для этого через 48 ч накладывают такой же компресс на область пигментации, оставшейся после бывших высыпаний. Пробу Ядассона можно проводить с приемом препарата йода внутрь. Но такое исследование чревато резким обострением заболевания.
При герпетиформном дерматите Дюринга в клиническом анализе крови обнаруживается повышенное содержание эозинофилов. При цитологическом исследовании содержимого пузырей также выявляется большое количество эозинофилов. Однако эти данные, как и проба Ядассона, не являются обязательными или строго специфичными для заболевания.
Наиболее надежным способом диагностики герпетиформного дерматита Дюринга считается гистологическое исследование участков пораженной кожи. Оно выявляет расположенные под эпидермисом полости, скопления эозинофилов, нейтрофилов и остатков их разрушенных ядер. Реакция прямой иммунофлуоресценции (РИФ) обнаруживает на верхушках дермальных сосочков отложения IgA.
В диагностике буллезной формы герпетиформного дерматита Дюринга необходима дифференциация с другими буллезными дерматитами: буллезным пемфигоидом, вульгарной пузырчаткой и другими видами пузырчатки.
Поскольку герпетиформный дерматит Дюринга является параонкологическим заболеванием, для пациентов пожилого возраста желательно проведение дополнительных обследовании для исключения онкологической патологии внутренних органов: УЗИ органов брюшной полости и моче-половой системы, рентгенограмму легких, КТ почек и т. п.
Лечение герпетиформного дерматита Дюринга
Больным герпетиформным дерматитом Дюринга показано лечение у дерматолога. Назначают диету, исключающую злаки и йодосодержащие продукты (морская рыба, морепродукты, салат и др.). Медикаментозная терапия проводится препаратами сульфоновой группы: диафенилсульфон, сульфасалазин, солюсульфон и другие. Эти препараты обычно назначают внутрь циклами по 5-6 дней с перерывами в 1-3 дня. В случаях неэффективности сульфоновой терапии лечение проводят средними дозами кортикостероидов (преднизолон, дексаметазон и др.) Для купирования зуда применяют антигистаминные препараты: лоратадин, цетиризин, дезлоратадин.
Местное лечение герпетиформного дерматита Дюринга включает теплые ванны с раствором марганцовки, вскрытие пузырей и их обработку зеленкой или фукарцином, наложение кортикостероидных мазей или аэрозолей, применение 5% дерматоловой мази.
Читайте также:

