Гистология кожи при ожоге
Обновлено: 24.04.2024
В данной научной работе представлено гистологическое исследование степени тяжести дисплазии соединительной ткани на примере микроскопического исследования расщепленного кожного лоскута, взятого в ходе аутодермопластики у больных с глубокими ожогами. А также установлены корреляционные связи между выявленными гистологическими изменениями и степенью тяжести дисплазии соединительной ткани, выявленной в ходе клинического осмотра и оцененной по шкале Аббакумовой Л.Н. В тексте статьи также представлены ключевые моменты, такие как среднее количество койко-дней, проведенных в отделении, количество дней до аутодермопластики, выявлен наиболее часто выставляемый клинический диагноз, наиболее опасный с точки зрения получения ожогов сезон, препарат антибиотикопрофилактики, отдельно учитывались пациенты, которым требовалась некрэктомия и повторная аутодермопластика. В исследовании подробным образом дано гистологическое описание кожных лоскутов, взятых интраоперационно у больных с глубокими ожогами. Выявлено, какая степень дисплазии превалирует в данном исследовании. Сделаны выводы и даны рекомендации по ведению и послеоперационной реабилитации данной группы пациентов. Результаты данного исследования могут быть полезны в клинической практике для врачей таких специальностей, как хирурги, комбустиологи.

1. Яковлев В.М., Нечаева Г.И., Мартынов А.И., Викторова И.А. Дисплазия соединительной ткани в практике врачей первичного звена здравоохранения: Руководство для врачей. М.: КСТ Интерфорум, 2016. 520 с.
2. Rabkin E. Activated interstitial myofibroblasts express catabolic enzymes and mediate matrix remodeling in myxomatous heart valves. Circulation. 2001. Vol. 04 (21). P. 2525-32.
3. Кадурина Т.И., Корженевская М.А., Михеев В.С. Генетический анализ в семьях с генерализованной дисплазией соединительной ткани, включающей MASS-фенотип // Артер ги-перт. 1999. Vol. 5 (1). P. 26-7.
4. Нечаева Г.И., Мартынов А.И. Дисплазия соединительной ткани: сердечно-сосудистые изменения, современные подходы к диагностике и лечению. М.: ООО «Издательство «Медицинское информационное агентство», 2017. 400 с.
5. Нечаева Г.И., Дрокина О.В., Мартынов А.И., Логинова Е.Н., Друк И.В., Лялюкова Е.А., Вершинина М.В. Основы курации пациентов с дисплазией соединительной ткани в первичном звене здравоохранения // Терапия. 2015. № 1. С. 29-36.
6. Яковлев В.М., Нечаева Г.И., Мартынов А.И., Викторова И.А. Дисплазия соединительной ткани в практике врачей первичного звена здравоохранения: Руководство для врачей. М.: КСТ Интерфорум, 2016. 520 с.
8. Дедова В.О., Доценко Н.Я., Боев С.С., Шехунова И.А., Герасименко Л.В. Распространенность дисплазии соединительной ткани // Медицина и образование в Сибири. 2011. № 2. 11 С. 6.
9. Беленький А.Г. Гипермобильность суставов и гипермобильный синдром: распространённость и клинико-инструментальная характеристика: автореф. дис. … докт. мед. наук. Москва, 2004. 51 с.
10. Ляховецкий Б.И., Глазкова Л.К., Перетолчина Т.Ф. Кожные признаки недифференцированной дисплазии соединительной ткани // Современные проблемы дерматовенерологии, иммунологии и врачебной косметологии. 2012. № 1 (20). С. 30-35.
В наше время лечение ожоговой болезни является актуальнейшей проблемой комбустиологических центров по всей стране. Число людей, получивших ожоговые травмы различной этиологии, составляет более 350 000. На 10 000 населения приходится 300-350 случаев. Имеется склонность к увеличению количества пациентов с площадью поражения более 35%. Ожоги, помимо тяжелого травматического поражения, проявляются в виде местных и системных изменений в органах и тканях. Помимо риска обсеменения ожоговой раны, открытая ожоговая поверхность является местом выхода межтканевой жидкости, что усугубляет системные изменения. В настоящее время данная ситуация усугубляется увеличением антибиотикорезистентности у возбудителей ожоговой инфекции, что ведет к более длительному лечению и реабилитации [1].
Ожоговая травма является особой и требующей использования современных методов диагностики, лечения и реабилитации. В связи с этим лечение ожоговых травм проводится в специализированных учреждениях - комбустиологических отделениях. В нашей стране имеется также несколько крупных центров по лечению ожоговой травмы. Одно из лидирующих мест среди бытового травматизма занимают ожоговые травмы, помимо бытового способа получения ожоговая травма может быть получена на производстве, в условиях чрезвычайных ситуаций. Сложность в подходах диагностики, в оценке площади и глубины пораженной ткани, особенности этиопатогенеза, лечения и реабилитации пациентов, а также растущий уровень летальности и недееспособности делают ожоговую болезнь актуальнейшей проблемой современного общества [1].
Дисплазия соединительной ткани – это генетически обусловленное заболевание, которое характеризуется изменениями в основном веществе соединительной ткани, а также в его волокнистых структурах. Данное состояние характеризуется непрерывным течением, приводит к нарушению гисто- и органогенеза [1].
При синдроме дисплазии отмечают изменения в структуре коллагена и эластина, протеогликанов, гликопротеидов, нарушается роль фибробластов и других клеточных компонентов. Имеется группа заболеваний - «мукополисахаридозы», основной причиной которых является генетически детерминированное изменение метаболизма основного вещества и клеточных структур соединительной ткани. Разнообразные изменения генома, такие как точечные мутации, делеции и другие, вызывают формирование патологического коллагена и эластина, что приводит к нарушению гисто- и органогенеза и необратимому изменению функций [2].
В литературных источниках под термином «дисплазия соединительной ткани» часто встречаются такие понятия, как «слабость соединительной ткани», «мезенхимальная недостаточность», «мезенхимальная дисплазия», «соединительнотканная дисплазия со смешанным фенотипом», генерализованная дисплазия соединительной ткани, включающая в в себя изолированную соединительнотканную дисплазию и MASS-фенотип [3].
Синдром дисплазии соединительной ткани в нашей стране диагностируется достаточно часто (по данным Г.И. Нечаевой и соавторов, около 1:5), поэтому мы считаем, что данный синдром является одной из современных значимых проблем нашего общества [4; 5].
Детский и подростковый возраст являются тревожным периодом в отношении проявления дисплазии соединительной ткани. Появление признаков дисплазии соединительной ткани в данных возрастных группах может достигать 250-300%. Частота появления новых признаков дисплазии соединительной ткани у людей старше 30 лет практически невозможна, у людей старше 30 лет наиболее значимой проблемой является повышение рисков осложнений, связанных с дисплазией соединительной ткани. Для верификации и постановки диагноза, а также оценки степени тяжести и рисков применяют сводные таблицы, в которых каждому фенотипическому проявлению дисплазии соединительной ткани присуждается балл.
Суммарное количество баллов образовывает число, которое отображает степень тяжести и риски диспластического процесса [6].
Изучение литературных данных показало, что закономерности между гистологической характеристикой кожного лоскута у пациентов с ожогами средней степени тяжести и тяжестью диспластического процесса не отмечалось. Изучение данных связей представляет клинический интерес, так как больные с дисплазией соединительной ткани требуют особого подхода к лечению и более длительной и серьезной реабилитации.
Изучить гистологическую картину дисплазии соединительной ткани различной степени тяжести на примере микроскопического исследования расщепленного кожного лоскута, взятого в ходе аутодермопластики у больных с глубокими ожогами. Установить корреляционные связи между выявленными структурно-гистологическими проявлениями и степенью тяжести диспластического процесса. Определить актуальность полученных данных, а также возможность использования установленных закономерностей в деятельности врача-комбустиолога и врачей других специальностей.
Материал и методы исследования
Нами обследовано 100 больных с глубокими ожогами различной локализации. Средний возраст больных составил 53,57±3,52 года. В план обследования пациентов было включено: опрос, тщательный сбор анамнеза, данные лабораторных и инструментальных методов исследования. Пациенты были подвергнуты тщательному исследованию на предмет внешних проявлений диспластического процесса, проведен их подсчет и верификация по шкале Л.Н. Аббакумовой [7].
Морфологическое и цитологическое исследование кожного лоскута, взятого в ходе аутодермопластики во время операции; сопоставление полученных результатов.
Результаты исследования и их обсуждение
Средний возраст пациентов составил 53,52±3,89 года. 56% от всех пациентов приходилось на жителей районов республики. 42% пациентов являлись жителями г. Ижевска. 2% являлись жителями других территорий. 54% пациентов являлись пенсионерами, 46% пациентов являлись работающими.
Основное время получения ожогов приходилось на весенне-летний период, оно составило 56%, также наиболее часто ожоговую травму пациенты получали в период с ноября по февраль.
От момента получения ожога до момента обращения в лечебное учреждение в среднем проходило от 2 до 4 дней.
Среднее количество койко-дней составило 42,95±4,77. Нахождение пациентов с дисплазией выраженной степени тяжести составило 48,44±2,23 койко-дня. Пациенты с дисплазией средней и легкой степенью тяжести провели в стационаре 39,0±1,53 и 35,5±1,77 койко-дня соответственно.
Наиболее часто выставляемым диагнозом был «Ожог пламенем», он встречался в 59% случаев, вторым по встречаемости был диагноз «Контактный ожог», он встречался в 32% случаев. Наименее распространенным оказался диагноз «Ожог кипятком», частота его встречаемости составила 9%.
От момента поступление в ЛПУ до проведения аутодермопластики в среднем проходило 15,45± 3,74 койко-дня.
12% пациентов была необходима повторная аутодермопластика в связи с плохой приживаемостью аутотрансплантата.
Антибиотиком выбора был цефтриаксон. Он применялся в 63% случаев. Однако у пациентов с тяжелой степенью дисплазии имело место применение нескольких групп антибиотиков. Наиболее часто применялись: Цефтриаксон - 55%, Ванкомицин - 43%, Амикацин - 41%.
Выбор данной группы антибиотиков был обусловлен широтой спектра действия и высокой антимикробной активностью.
Из сопутствующей патологии наиболее часто встречались такие заболевания, как артериальная гипертония, хронический гастрит, сахарный диабет, вирусный гепатит В, вирусный гепатит С. Некоторые заболевания из сопутствующей патологии усугубляют тяжесть течения и увеличивают процесс регенерации и приживления аллотрансплантата кожной ткани, одним из таких заболеваний является сахарный диабет. У пациентов с сахарным диабетом увеличено количество койко-дней, проведенных на лечении и реабилитации в стационаре.
Нами обследовано 100 человек с диагнозом ожоги различной степени тяжести и локализации, находящиеся на лечении в комбустиологическом отделении БУЗ УР «Первая республиканская клиническая больница» МЗ УР. В исследовании было выделено 2 группы пациентов. В первую группу вошли те, у кого отсутствуют фенотипические проявления дисплазии, таких оказалось 57 человек. Во второй группе оказались 43 пациента с дисплазией соединительной ткани различной степени тяжести. Обе группы были подвергнуты общему осмотру.
Наиболее часто (в 57-94% случаев) встречающимся признаком, по которому происходит диагностика диспластического синдрома, является патология скелета, а именно: гипермобильность суставов, плоскостопие, деформации позвоночника, грудной клетки [8; 9].
Гипотонией мышц, расхождением прямых мышц живота, абдоминальными и паховыми грыжами, гипотрофией характеризуется диспластический синдром со стороны мышечного аппарата. Кожные проявления были в виде стрий, а также синдрома гиперэластической кожи. Несостоятельность коллагена кожи внешне проявляется в виде «папиросной бумаги» (дефект заживления кожных ран), данная патология отмечается достаточно часто [10].
Вторая группа пациентов была подвергнута тщательному осмотру, были обнаружены признаки синдрома дисплазии соединительной ткани. Данные признаки проявлялись врожденными пороками развития, а также малыми аномалиями.
Обнаружено 127 признаков, 2,95 признака на одного больного. Часто встречающимися признаками были неправильный рост зубов, гипертелоризм сосков, приросшая мочка, плоскостопие, готическое небо, нарушение зрения (диаграмма 1).
Оценивая степень тяжести синдрома дисплазии соединительной ткани по шкале Л.Н. Аббакумовой, выявили следующее: у 20 пациентов наблюдался синдром дисплазии соединительной ткани крайней степени, что соответствовало тяжелой дисплазии (пациенты данной группы набрали более 24 баллов), синдром дисплазии соединительной ткани проявлялся умеренно у 16 пациентов (по шкале Л.Н. Аббакумовой пациенты данной группы набрали 12-23 балла), в легкой степени тяжести синдром дисплазии соединительной ткани встречался у 7 пациентов (в данной группе пациенты набрали меньше 12 баллов по шкале Л.Н. Аббакумовой) (диаграмма 2).

Диаграмма 1. Частота встречаемости фенотипических признаков дисплазии

Диаграмма 2. Степень тяжести дисплазии
При патогистологическом исследовании расщепленного кожного лоскута, взятого в ходе аутодермопластики, выявлено, что у больных с глубокими ожогами с дисплазией соединительной ткани выраженной степени тяжести слабо развита аргирофильная сеть, отсутствие придатков кожи, атрофия эпидермиса, фиброз дермы. При патогистологическом исследовании биоптатов расщепленного кожного лоскута, взятого в ходе аутодермопластики у больных с глубокими ожогами с дисплазией соединительной ткани средней степени тяжести, отмечается: превалирование молодой грануляционной ткани, разная ориентированность коллагеновых волокон дермы, преобладает сглаженность сосочкового слоя дермы, а также слабая развитость аргирофильной сети. У пациентов с легкой степенью тяжести дисплазии соединительной ткани при микроскопическом исследовании в биоптате обнаруживается: преобладание грануляционной ткани, многослойный плоский ороговевающий эпителий.
Таким образом, по результатам нашего исследования можно сказать, что существует явная зависимость между степенью выраженности дисплазии соединительной ткани и гистологической картиной при ожогах. В нашем исследовании выявлено, что при тяжелой дисплазии и дисплазии средней степени тяжести отмечается слабая развитость аргирофильной сети и нарушение ориентированности коллагеновых волокон. Аргирофильная сеть является «преколлагеном» и дает начало коллагеновым волокнам, которые в свою очередь ответственны за упругость кожи. Также вместе с межуточным веществом дермы она образует базальную мембрану, которая имеет большое значение в обменных процессах между эпидермисом и дермой. Нарушение ее строения сказывается на базальном слое эпидермиса, который дает начало всем слоям эпидермиса. Имея представление об этом, можно говорить, что пациентам с тяжелой степенью дисплазии соединительной ткани может потребоваться повторное оперативное вмешательство, так как у пациентов с дисплазией заживление идет хуже, высок риск образования грубых келоидных и гипертрофических рубцов. Келоидные и гипертрофические рубцы, помимо косметического дефекта и психологического дискомфорта, вызывают зуд, болезненность, образование контрактур, которые ведут к нарушению функционирования тканей и органов. По сравнению с группой, в которой не выражены фенотипические признаки дисплазии, у пациентов с дисплазией средней и тяжелой степени наиболее часто происходит отторжение пересаженного кожного лоскута. Пациентам может потребоваться некрэктомия с повторной аутодермопластикой. Анализ послеоперационных осложнений показал, что у пациентов с отсутствием фенотипических признаков дисплазии соединительной ткани лизис аутотрансплантата наблюдался в 3,5% (2 человека) случаев. В группе пациентов с фенотипическими проявлениями дисплазии соединительной ткани лизис аутотрансплантата наступал в 16,3% (7 человек) случаев.
Желательно использование местных аппликаций с антигистаминным, противовоспалительным действием, а также гормонсодержащие препараты, протеолитические ферменты, местные анестетики, внутрирубцовые инъекции кортикостероидных препаратов. Патогенетически обоснованно применение ранозаживляющих средств, перевязочных материалов, раневых покрытий на основе природных полимеров, таких как коллаген, хитозан, гиалуроновая кислота. В послеоперационном периоде рационально применение высоких доз аскорбиновой кислоты. Аскорбиновая кислота участвует в гидроксилировании остатков пролина и лизина. В результате чего образуются более стабильные и пробные коллагеновые волокна.
Пациенты с выраженной степенью дисплазии соединительной ткани нуждаются в более длительном лечении, с использованием современных методов и технологий, а также в более длительной и серьезной реабилитации, включающей в себя психологическую статическую реабилитацию, физиотерапию, проведение реабилитации в специализированных медицинских центрах, а также санаторно-курортное лечение.
1. Проблема дисплазии соединительной ткани становится все более актуальной в связи с тем, что данная проблема очень активно изучается в настоящее время.
2. Установлено, что существует явная зависимость между степенью выраженности дисплазии соединительной ткани и гистологической картиной при ожогах.
3. Пациенты с выраженной степенью дисплазии нуждаются в более длительном лечении и серьезной реабилитации в стационарных условиях.
4. В данном исследовании выявлено, что преобладающей является тяжелая форма дисплазии соединительной ткани.
Коагуляционный некроз при ожоге. Морфология четвертой степени ожога
Вторая форма ожога является по своему характеру коагуляционным некрозом. На большем протяжении препарата эпидермис выпрямлен, плотно прилежит к собственно коже, местами незначительно приподнят, сохраняя с нею связь за счет резко вытянутых клеток базального слоя или образуя здесь щелевидные пустоты.
Клеточное строение эпидермиса сохранено. В цитоплазме многих клеток наблюдают базофильную зернистость, ядра уменьшены в размерах, гематоксилином окрашиваются интенсивно. В собственно коже волокнистое строение выражено отчетливо. В сетчатом слое коллагеновые волокна резко утолщены, гомогенизированы, но сохраняют петлистое расположение.
Обращают на себя внимание интенсивно выраженная базофилия, степень которой убывает в глубину собственно кожи, а также метахромазия коллагеновых волокон. Так, пикрофуксином соединительная ткань окрашивается в желтый цвет вместо ярко-красного, а гематоксилином по Шпильмейеру — в черный цвет (в норме она бесцветная).
Ядра соединительнотканных клеток, придатков кожи и эндотелия сосудов повсеместно определяются и окрашиваются интенсивно. В отличие от соединительной ткани эластические волокна утрачивают петлистое расположение, многие из них выпрямлены, истончены, фрагментированы. Сосудистые нарушения при указанной форме ожога в собственно коже выражены слабо, они преобладают в подкожной жировой клетчатке (полнокровие, кровоизлияния, тромбы).
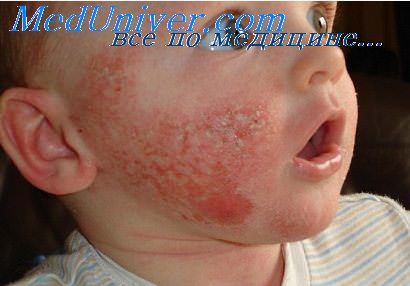
Границу коагуляционного некроза при быстрой смерти на месте происшествия определить трудно. Если смерть наступила в ближайшие часы посте ожога, то границу удастся отметить по реактивным изменениям в окружающей ткани Спустя 10—11 ч хорошо выражены отек и лейкоцитарная реакция; поздние изменения носят характер демаркационного воспаления с кровоизлияниями и тромбами.
Результатом этого воспаления является образование грануляционной ткани и отторжение некротического участка. Молодая грануляционная ткань богата гистиоцитами, эндотелиальными клетками, новообразованными сосудами. Постепенно она преобразуется в зрелую грануляционную ткань за счет появления фибробластов, коллагеновых волокон и уменьшения количества сосудов; при этом начинается процесс эпителизации ожоговой поверхности путем врастания сохранившеюся эпидермиса под лейкоцитарный вал.
При ожоге IV степени находят обугливание эпидермиса или верхних слоев собственно кожи, а также некроз подлежащих тканей. Микроскопически обугленный эпидермис имеет вид неровной однородной полосы черного цвета, которая местами приподнята над собственно кожей, сохраняя с нею связь за счет желто-бурых тканевых перемычек.
На коже ладоней или стоп обугливанию нередко подвергаются верхние слои эпидермиса; остальная его часть имеет бесструктурный вид ржаво-золотистого цвета. Собственно кожа представляется резко уплотненной, как бы спрессованной. Она имеет вид относительно гомогенного пласта, в котором лишь кое-где сохранился намек на волокнистое строение за счет преломляющих свет полос параллельных поверхности кожи.
Этот пласт окрашивается в сине-розовый цвет, имея в поверхностном слое буроватый оттенок. В его толще находят щелевидные пустоты. Ядра соединительнотканных клеток выявляются только в глубине собственно кожи. Они встречаются редко, имеют пикнотичный вид. Здесь же обнаруживают клеточные тяжи на месте спавшихся капилляров, сморщенных потовых, сальных желез и волосяных влагалищ. В просвете артерий и вен определяется гомогенная или зернистая масса, окрашенная в различные оттенки коричневого и зеленого цвета. Только в глубине подкожной жировой клетчатки находят сосуды, содержащие кровь обычного вида.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Ожоги. Местные проявления ожогов
Ожогом называется местный патологический процесс, который возникает при воздействии на кожу и слизистые оболочки высокой температуры — пламени, горячего газа и пара, нагретых предметов, раскаленного металла, кипятка. В судебно-медицинской практике чаще приходится встречаться со случаями смерти в пожаре, где нередко имеет место комбинированное воздействие различных термических факторов.
Местные изменения при ожоге носят различный характер, начиная от легкой степени нарушения кровообращения до некроза it обугливания мягких покровов тела. Макроскопически ожоги делят на четыре степени: покраснение и отек кожи — I степень, пузыри — II, некроз — III и обугливание — IV степень. При смерти в пожаре преобладают III и IV степени ожога.
Если пострадавший погибает спустя то или иное время после ожога, то па макроскопическую картину поражения оказывают влияние характер лечебных мероприятий и наслоение вторичных изменений, а во внутренних органах развиваются изменения, характеризуемые как ожоговая болезнь.
Для оценки характера и глубины повреждении мягких покровов тела, изменений во внутренних органах, установления прижизненности термического воздействия, а также при решении других вопросов, макроскопических данных при судебно-медицинском исследовании трупа часто недостаточно. Поэтому важное значение приобретает микроскопическое исследование мягких тканей и органов.
Микроскопическое исследование. Ожог I степени вызывает полнокровие капилляров, прекапилляров, артериол и мелких ар терий кожи, особенно подсосочкового сосудистого сплетения, разрыхление и небольшой серозный отек собственно кожи; клеточная реакция отсутствует или выражена слабо.
Для ожога II степени характерно образование пузырей. Пузыри могут располагаться в толще эпидермиса или между эпидермисом и собственно кожей. В толще эпидермиса и находят часто на коже ладоней и стоп, т. е. там, где эпидермис наиболее развит. В остальных отделах кожи пузыри преимущественно локализуются либо на границе с собственно кожей, либо на уровне базальною слоя клеток, который в этом случае образует дно пузыря.
Местами базальный слой может быть разорван, часть его клеток отходит вверх вместе с основной толщен эпидермиса, часть остается в углублениях между сосочками собственно кожи. Клетки при этом приобретают резко вытянутую волнообразную пли веретенообразную форму. Ядра интенсивно окрашиваются, иногда имеют вид частокола, цитоплазма окрашивается бтедно.
При любой локализации пузыря сег чатая структура рогового слоя утрачена, блестящий слой утолщен, эозином окрашивается ярко, клеточное строение зернистого и шиповатого слоев определяется слабо или вовсе неразличимо. Изменения в эпидермисе могут быть и более глубокими, вплоть до некроза. В этом случае он имеет вид бесструктурной, зернистой или сетчато-волокнистой ткани, окрашенной в бледно-розовый цвет.
Если цолость пузыря не нарушена, то в нем определяется гомогенное или нежно-зернистое содержимое, окрашенное эозином очень слабо. В нем встречаются отдельные эпителиальные клетки и небольшие их группы, нити фибрина и отдельные эритроциты. С увеличением давности ожога количество эритроцитов на растает, появляются клетки белой крови
Изменения в собственно коже могут быть выражены различно на месте пузыря и в участках, где пузыри отсутствуют и кожа имеет темно-красный цвет и пергаментную плотность.
На месте пузыря волокнистая структура собственно кожи хорошо сохранена, коллагеновые волокна гомогенизированы, эозином окрашены бледно с легким базофильным оттенком, сосуды расширены и заполнены кровью. Местами кровь в них имеет вид гомогеннои розово-желтой массы. Ядра соединительнотканных клеток неправильной формы. В потовых железах границы клеток определяются нечетко, цитоплазма базофильна. ядра окрашены настолько слабо, что местами железистые трубки представляют ся однородно гомогенными серо-зеленого цвета.
В эпителии волосяных влагалищ изменения клеток сходны с изменениями в ба зальном слое эпидермиса. В сальных железах выраженных изменений не наблюдают. В некоторых случаях, где дном пузыря является собственно кожа, изменения в ней могут быть выражены более значительно. Это касается сосочкового ее слоя, который бывает некротизирован и имеет вид аморфной полоски буро-голубого цвета.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Изменения кожи при ожоге. Эпидермис при ожоге
В коже темно-красного цвета пергаментной плотности (на месте бывших пузырей) верхние слои собственно кожи имеют вид компактной ткани желтоватого, зеленоватого или буроватого цвета, с почти неразличимым волокнистым строением. Эластичные волокна здесь не определяются. Сосочки в большинстве сво ем сглажены, соответственно им иногда различают группы деформированных ядер соединительной ткани и спавшихся капилляров.
В сохранившихся, но резко уплощенных сосочках на месте капилляров видна гомогенная масса желто-оранжевого или зеленоватого цвета, эндотелии обычно не определяется. В глубоких отделах собственно кожи коллагеновые волокна утолщены, гомогенизированы, многие из них выпрямлены параллельно поверхности кожи и сближены, имеют базофильный вид.
Поэтому количество ядер соединительнотканных клеток кажется уменьшенным. Эластические волокна утолщены и фрагментированы. Сальные и потовые железы сморщены, ядра клеток деформированы, в волосяных влагалищах ядра клеток нередко приобретают вид штрихов, окрашиваются интенсивно. Расширенные сосуды встречаются часто, в просвете их красно- или зелено-коричневая однородная масса. Кровоизлияния обнаруживаются редко, главным образом вблизи дериватов кожи.
Они имеют вид пятен коричневого цвета, в которых контуры эритроцитов не определяются.
В подкожной жировой клетчатке наблюдают выраженное полнокровие сосудов, кровоизлияния и тромбы. Мелкие кровоизлияния находят вблизи сосудов, крупные — на границе с собственно кожей. Излившаяся кровь красно-кирпичного цвета. эритроциты контурируются слабо и только по периферии кровоизлияния.
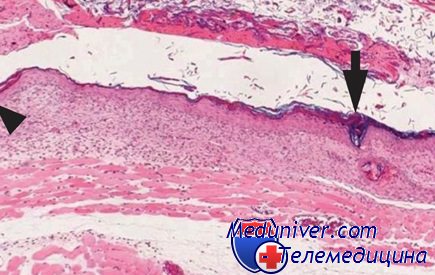
В мелких сосудах встречают гиалиновые и смешанные тромбы; в стенке сосудов можно видеть расщепление и фрагментацию эластических и аргирофпльных волокон. В нервах подкожной жировой клетчатки отмечают неравномерную импрегнацию и колбовидные утолщения. В поперечнополосатых мышцах изменения выражены незначительно.
В первые часы после ожога второй степени развиваются реактивные процессы: нарастает полнокровие сосудов кожи и подкожной жировой клетчатки, появляются лейкоциты и увеличивается их количество не только в содержимом пузыря, но и в толще эпидермиса и в собственно коже вблизи сосудов.
К концу первых суток инфильтрация лейкоцитами сосочкового слоя выражена отчетливо. Одновременно развивается отек, вначале в подкожной жировой клетчатке, затем в сетчатом слое. На 2— 3-й сутки обнаруживают демаркационное воспаление. Начало эпителизации ожоговой поверхности отмечают в краях пузыря по врастанию тяжей эпителиальных клеток под лейкоцитарный вал.
Микроскопическая картина ожога III степени характеризуется двумя формами: сочетанием некробиотических и некротических процессов либо чистой формой некроза как следствие фиксирующего воздействия высокой температуры (Науменко В. Г., 1955). Первая форма требует для своего развития некоторого промежутка времени и наблюдается при относительно постепенном действии температурного фактора, вторая форма указывает на прямое и, по-видимому, одномоментное термическое воздействие значительной интенсивности.
На месте ожога первой формы эпидермис в участках, где он сохранился, истончен. Под малым увеличением микроскопа он имеет вид бесструктурной волнистой ленты коричневого цвета. Под большим увеличением здесь иногда различаются контуры компактного рогового слоя и малинового или синего цвета зернистого слоя, а также очертания отдельных клеток шиповатого слоя.
В некоторых участках контуры клеток шиповатого и базального слоев бывают лучше сохранены, цитоплазма в них мутная, зернистая, ядра увеличены, окрашены бледно. Изредка наблюдают кариорексис и краевой гиперхроматоз. В собственно коже некротические и некробиотические изменения сходны с теми, которые наблюдают в красной пергаментно-плотной коже на месте ожоговых пузырей. Однако степень и глубина их распространения выражены в большей мере.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
ОЖОГ (combustio) - специфическое повреждение тканей и органов, вызванное воздействием термической, химической, электрической или лучевой энергии.
Этиология. По физической природе термические агенты можно разделить на твердые, жидкие и газообразные. По виду взаимодействия с тканями пострадавшего выделяют контактные поражения (при непосредственном взаимодействии с тканями пострадавшего: пламя, горячие жидкости и т. д. ) и дистантные (без непосредственного контакта: ультрафиолетовое, инфракрасное, тепловое излучение) поражения.
Патогенез местных изменений при ожогах кожи.
Температурный оптимум для активности многих биологически важных ферментов соответствует 36-37˚С, интервал температур от 37 до 41˚С для кожи является приемлемым, дальнейшее нагревание приводит к повреждению клеток. Продолжительность существования тканевой гипертермии многократно превосходит время действия самого термического агента.
При воздействии высоких температур на поверхности тела образуются ожоги различных степеней. При перегревании тканей свыше 520С коагуляционное свертывание белков невосстановимо. Последствия ожогов зависят от размеров и глубины повреждения тканей.
Различают 3 концентрические зоны поражения при глубоких ожогах в зависимости от степени нарушения кровообращения. Центральная область раны, наиболее тесно соприкасающаяся с источником тепла, носит название зоны коагуляции. Вокруг нее располагается зона паранекроза, названная Jackson D (1953) зоной стаза (ишемическая средняя зона) и эритемная периферическая зона. При микроскопии визуализируется сосудистый тромбоз в средней и периферической зонах.
Интенсивность нагревания тканей (глубина поражения) зависит от физических характеристик термического агента (низкотемпературные, высокотемпературные), способа теплопередачи (проведение, конвекция, испарение), теплозащитных свойств одежды. Объем поражения кожи зависит не только от фактической температуры, но и от времени ее воздействия, которое удлиняется за счет того, что кожа обладает достаточно высокой теплоемкостью и теплопроводностью. Степень тканевой гипертермии прямо пропорциональна продолжительности нагревания. Краткосрочное воздействие даже очень высоких температур может не приводить к развитию ожогов. Чем выше степень перегрева тканей, тем быстрее происходит гибель клеток.
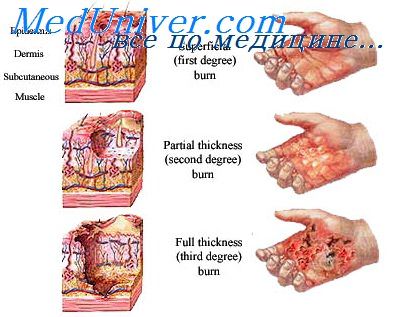
Классификация. В настоящее время в нашей стране используется классификация, принятая на XXVII Всесоюзном съезде хирургов. Выделяют следующие степени поражения (рис. 20. 1):
1 степень - поверхностный эпидермальный ожог
2 степень - ожог верхнего слоя кожи
3 степень - коагуляция и некроз всего сосочкового слоя или более глубоких слоев кожи.
3А степень - некроз эпителия распространяется на глубину эпителиального слоя до герминативного, но захватывает последний не полностью, а лишь на верхушках сосочков, сохраняются придатки кожи.
3Б степень - некроз распространяется на глубину всего эпителиального слоя и дермы.
4 степень - поражение глубжележащих тканей (подкожной клетчатки, фасций, мышц, сухожилий и костей).
За рубежом широко распространена классификация, выделяющая четыре степени поражения:
- первая степень – соответствует первой степени отечественной классификации;
- вторая поверхностная степень – соответствует II степени отечественной классификации;
- вторая глубокая степень – соответствует IIIа степени;
- третья степень – соответствует IIIб степени;
- четвертая степень – соответствует IV степени.
Клиническая картина.
Для ожоговых повреждений в зависимости от глубины (степени поражения) характерна различные местные клинические проявления (табл. 20. 1).
Ожог 1 степени характеризуются разлитой краснотой, отечностью и выраженной болезненностью кожи, местным повышением ее температуры. Термический агент за счет раздражения сосудистых нервов вызывает интенсивное расширение сосудов. Через несколько дней все проявления проходят, оставляя коричневую пигментацию кожи. Типичным примером ожога 1 степени является ожог солнечными лучами.
При ожоге 2 степени на различной глубине в толще эпидермального слоя образуются пузыри, наполненные прозрачной серозной жидкостью. Содержимым таких пузырей является бесклеточная серозная жидкость с высоким содержанием в ней белков. Заживление происходит за счет регенерации эпителия.
При ожоге 3а степени кожа местами покрыта пузырями, пятнистая, пятна бледного или темного оттенка, иногда даже черные. Нежизнеспособные ткани образуют струп, который отторгается от живых тканей с образованием демаркационной линии. Если в зоне ожога явно выражен отек, то можно рассчитывать на островковую эпителизацию и заживление без пересадки кожи. На месте ожога остаются нежные рубцы.
При ожогах 3б степени кожа поражается на всю толщину с вовлечением поверхностных слоев подкожной клетчатки. Кожа бледно-серого цвета, пятниста, чувствительность ее снижена или отсутствует. При заживлении на месте поражения образуются грубые рубцы.
Для ожогов 4 степени характерно глубокое поражение тканей, нередко их обугливание. Ткани превращаются в почерневшие ломкие массы. Самостоятельное заживление этих ожогов невозможно.
Тяжесть общего состояния больных главным образом зависит от площади обожженной поверхности и степени ожога, выраженность которых в конечном итоге и определяют прогноз заболевания. В первые дни тяжесть течения зависит в основном от площади обожженной поверхности. Глубина поражения сказывается главным образом на дальнейшем течении болезни.
Диагностика
При диагностике глубины поражения необходимо учитывать комплекс данных полученных при сборе анамнеза, осмотре пострадавшего и при проведении диагностических проб.
Анамнез позволяет установить вид и продолжительность воздействия повреждающего агента, факторы изменяющие интенсивность теплового воздействия, наличие сопутствующей патологии.
При осмотре оценивается изменение цвета эпидермиса и дермы, наличие и распространенность отека, наличие пузырей и характер их содержимого, наличие признаков нарушения кровообращения, наличие некроза тканей и его вид.
При физикальном обследование определяется состояние болевой чувствительности: уколы иглой, эпиляционный тест (выдергивание волосков), тесты с красителями.
Определение площади ожога.
Одной из важных составляющих диагноза при термической травме является определение площади поражения. Наиболее удобным является определение площади пораженной поверхности по Уоллесу (A. Wallace 1951г. ) – «правило девяток»: голова и шея - 9%, рука - 9%, нога - 18%, туловище сзади и спереди по 18%, промежность, гениталии - 1% (рис 20. 2).
Другим распространенным способом является «правило ладони». Согласно исследованиям J. Grazer (1997г. ) площадь ладони взрослого человека составляет 0, 78% от общей площади поверхности тела.
Местное лечение ожогов.
В качестве первой помощи при ожогах необходимо немедленно прекратить воздействие поражающего фактора, обеспечить доступ свежего воздуха охладить обожженные участки тела (холодная проточная вода, криопакеты «Comprigel» «Articare» и т. д. ), при обширных повреждениях ввести обезболивающие препараты (анальгин, морфин, омнопон, промедол, морадол), наложить на пораженные поверхности стерильные повязки. Следует отметить, что ключевым моментом оказания первой помощи является быстрое проведение охлаждения обожженной поверхности, правильное проведение которой снижает глубину (степень) ожога на единицу. Адекватно проведенная первая помощь на месте происшествия позволяет снизить риск ожоговой болезни и уменьшить количество осложнений.
Поверхностные ожоги не большой площади адекватно лечатся амбулаторно, поскольку в большинстве случаев, не требуют хирургического лечения. Местно применяются различные мазевые повязки, которые обладают местно охлаждающим действием, защищают раневую поверхность, стимулируют заживление, препятствуют присоединению вторичной инфекции. Наиболее часто используются мази-спреи «Олазоль», «Пантенол».
В последние годы при лечении пограничных ожогов IIIA степени и глубоких ожогов IIIБ-IV степени широко используются различные раневые покрытия, в течение многих лет успешно используется перфорированная свиная кожа - ксенокожа. Последняя помещается на ожоговые раны, обеспечивая их покой и защиту от инфекции, не препятствуя очищению ран и одновременному применению для местного лечения других препаратов.
В настоящее время существует два основных пути подготовки глубоких ожоговых ран к аутодермопластике (табл. 20. 3. ): химическая некрэктомия с отсроченной аутодермопластикой и хирургическая некрэктомия с одномоментной или отсроченной аутодермопластикой. Тактика местного лечения с использованием химической некрэктомии вполне оправдана при обширных глубоких ожогах более 40 % поверхности тела при условии крайне тяжелого общего состояния больных. Особенно при лечении больных пожилого и старческого возраста, у которых тяжелая сопутствующая патология делает оперативные вмешательства в ранние сроки невозможными.
В этих случаях с первых суток после травмы местное лечение должно быть направлено на быстрое формирование сухого ожогового струпа, профилактику инфицирования и углубления ожоговых ран. С этой целью применяют ватно-марлевые повязки с мазями на водорастворимой основе. Это способствует уменьшению потери жидкости с ожоговой поверхности, согреванию больного, формированию сухого струпа, не требует ежедневных перевязок.
В последующие дни формирование сухого ожогового струпа достигается применением влажно-высыхающих повязок. Оптимальными препаратами в этот период также являются 1 % растворы йодопирона или йодовидона, обеспечивающие высушивание струпа и обладающие широким спектром антимикробного и противогрибкового действия. Возможно также использование ватно-марлевых повязок с мазями на водорастворимой основе. Применение мази на жировой основе противопоказано.
Значительно ускоряет формирование сухого струпа лечение больного в условиях абактериальной среды. В этом случае используется открытый метод лечения с обработкой ожоговых ран два-три раза в день 1 % раствором йодопирона, йодовидона или препаратом "Наксол" и применением абактериальных изоляторов или кровати "Клинитрон". Способствует высушиванию струпа инфракрасное облучение ран. Образование сухого струпа уменьшает потери белка с ожоговой поверхности, способствует уменьшению интоксикации, улучшению общего состояния больного.
При глубоких циркулярных ожогах конечностей, когда высок риск сдавления и ишемии глубжележащих тканей формирующимся ожоговым струпом при циркулярных ожогах грудной клетки, ограничивающих еe экскурсию, в ближайшие дни после травмы показано выполнение некротомии.
После образования сухого "мумифицированного" струпа производится химическая некрэктомия с использованием 40 % салициловой мази. Толщина слоя мази должна составлять 1-2 мм. Одновременно применяется не более 200 граммов мази в связи с опасностью отравления салицилатами, уровень которых в крови может превысить допустимую норму. Через 48 часов ожоговый струп бескровно отделяется от подлежащих тканей. С учетом указанного обстоятельства химическую некрэктомию одномоментно можно осуществить на площади до 10-15% поверхности тела.
После очищения ожоговой поверхности от некроза для подготовки раны к аутодермопластике целесообразно применение мазей на водорастворимой основе, содержащих антибактериальные препараты, возможно и чередование с антисептическими растворами. Положительное влияние на раневой процесс оказывают ультрафиолетовое облучение, монохроматический красный свет лазера, низкочастотный ультразвук.
Если площадь глубоких ожогов пострадавших превышает 10-15 % поверхности тела целесообразно в это же время выполнить следующую, этапную химическую некрэктомию и подготовить гранулирующие раны к одномоментной аутодермопластике на площади до 20 % поверхности тела. Выполнение такой операции возможно только с использованием расщепленного перфорированного сетчатого кожного аутолоскута, позволяющего увеличить площадь трансплантата в соотношении 1: 2, 1: 4, 1: 6 и более.
В последние годы все большее число сторонников находит метод хирургического иссечения некротических тканей. Ведущим методом лечения является ранняя хирургическая некрэктомия ожоговых ран - радикальное иссечение всех пораженных тканей до развития воспаления и инфицирования с последующей одномоментной аутодерматопластикой кожных дефектов. Операция выполняется до 5-7 суток с момента травмы непосредственно по выведению больного из шока.
В структуре хирургических методов лечения так же применяются: раннее хирургическое очищение ожоговых ран - заведомо нерадикальное иссечение основного массива некроза с целью уменьшения интоксикации, отсроченная хирургическая некрэктомия - радикальное иссечение всех пораженных тканей при развившемся воспалении и инфицировании (выполняется на 5-14 сутки с момента травмы), поздняя хирургическая обработка раны (в т. ч. хирургическая обработка гранулирующей раны), ампутации и дезартикуляции конечностей и их сегментов.
При ожогах III степени хирургическая некрэктомия производится тангенциально (послойно) специальным инструментом (дерматом, нож Гамби) до появления мелкоточечного кровотечения из непораженного ожогом слоя кожи. При ожогах IV степени хирургическаяи некрэктомия выполняется чаще до фасции скальпелем или электроножом с последующим тщательным гемостазом. Ранняя хирургическая некрэктомия (тангенциальная или фасциальная) с одномоментной аутодермопластикой позволяет при глубоких ожогах IIIБ-IV степени восстановить целостность кожных покровов уже через 3-4 недели после травмы на площади до 20 % поверхности тела.
Следует отметить, что использование современных принципов и методов лечения тяжелой ожоговой травмы, включающих раннюю хирургическую некрэктомию с одновременной последующей аутодерматопластикой (непосредственно после выведения больного из состояния шока), позволяет у большинства пациентов избежать развития всех дальнейших периодов ожоговой болезни, либо уменьшить тяжесть ее проявлений и последствий.
В настоящее время разработан и применяется новый метод активного хирургического лечения обожженных с использованием культивированных аллофибробластов. Суть метода заключается в применении для пластического закрытия ожоговых ран искусственно выращенных в лабораторных условиях аллофибробластов - клеток соединительной ткани, определяющих активность процессов регенерации, в т. ч. эпителизации. Они могут быть получены из кожи донора или трупного материала, при культивировании неприхотливы и полностью утрачивают антигенспецифичность.
Метод предусматривает трансплантацию культивированных фибробластов на обширные ожоговые раны IIIA степени, донорские раны в т. ч. длительно не заживающие, или комбинированную аутодермопластику с использованием культуры фибробластов и сетчатых кожных аутолоскутов, перфорированных в соотношении 1: 6 и 1: 8 при глубоких ожогах IIIБ-IV степени. Операции предшествует выполнение химической или хирургической некрэктомии.
Источник: Н.А.Кузнецов в соавт. Основы клинической хирургии. Практическое руководство. Издание 2-е, переработанное и дополненное. - М.:ГЭОТАР-Медиа, 2009.
Читайте также:

