Генетическая болезнь кожи от солнца как
Обновлено: 19.04.2024
ГБУ РД "Республиканский кожно-венерологический диспансер", Махачкала
ГБОУ ВПО «Дагестанская государственная медицинская академия» Минздрава России, Махачкала, Россия, 367000
ФГБОУ ВО «Дагестанский государственный медицинский университет» Минздрава России, Махачкала, Россия
ФГБОУ ВО «Дагестанский государственный медицинский университет» Минздрава России, Махачкала, Россия
ГБУ РД "Республиканский кожно-венерологический диспансер", Махачкала
Представлены клинические наблюдения пигментной ксеродермии в пойкилодермической стадии у юноши М. 17 лет и девочки З. 7 лет, а также абортивной формы — пигментного ксеродермоида Юнга — у женщины 47 лет. У юноши отмечали деформацию и сужение ротового отверстия: многочисленные трещины, сухость и атрофические рубцовые изменения. Резко выражен кариес зубов. Органы зрения поражены с обеих сторон. У девочки отмечали зуд пораженных участков — предплечья, области тыла кистей и стоп, где выявлены мелкие бородавчатые разрастания. В результате терапии клиническая картина у пациентов не претерпела изменений, лишь у девочки зуд стал менее выраженным. Интересно развивались проявления пигментного ксеродермоида Юнга. Лицо, шея и слизистая оболочка полости рта у пациентки были поражены с рождения. С течением времени экзантема меняла яркость, несколько смещалась. Никаких субъективных ощущений пятна не вызывали. Год назад на них появились папилломатозные разрастания; 3 мес назад ухудшилась острота зрения левого глаза и появился шум в левом ухе. При ярком солнечном свете «рябило» в левом глазу, а затем возникали гул и боль в голове. Очаг поражения кожи имел темно-бордовый цвет, местами фиолетовый и темно-красный с участками здоровой кожи. Кожа подбородка, нижняя губа были гипертрофированы и инфильтрированы. Наблюдали участки здоровой кожи. Волосы на левой брови, волосистой части головы и пушковые в очаге поражения были сохранены. На фоне пигментного участка местами выявлены папилломатозные разрастания и черные милиарные узелки. Левая половина слизистой оболочки полости рта и язык имели насыщенно-красный цвет строго до средней линии. Отмечали инфильтрированность пораженной половины языка.
ГБУ РД "Республиканский кожно-венерологический диспансер", Махачкала
ГБОУ ВПО «Дагестанская государственная медицинская академия» Минздрава России, Махачкала, Россия, 367000
ФГБОУ ВО «Дагестанский государственный медицинский университет» Минздрава России, Махачкала, Россия
ФГБОУ ВО «Дагестанский государственный медицинский университет» Минздрава России, Махачкала, Россия
Пигментная ксеродерма (ПК; син.: прогрессирующий лентикулярный меланоз Пика, пигментная атрофия кожи Кроккера) — редкое наследственное заболевание, впервые описанное M. Kaposi [1] в 1870 г. Встречается дерматоз у предста-вителей всех рас с частотой 4:1 000 000 [2]. Тип наследования аутосомно-рецессивный. Известно восемь генетических субтипов ПК, каждый из которых соответствует определенному дефектному гену. При этом в коже выявлен дефект репаративных ферментов (отсутствуют или малоактивны) эндо- и экзонуклеаз полимераз, не позволяющий устранить повреждения, возникающие при мутагенном воздействии УФ-лучей, ионизирующей радиации в ДНК клеток кожи любого типа: кератиноцитах, фибробластах, лимфоцитах и т. д. [3]. По этой причине кожа таких пациентов чрезвычайно чувствительна к солнечному облучению, а манифестные проявления заболевания в ней являются облигатным предраком [4].
После рождения клинических признаков ПК не наблюдают. Манифестацию заболевания в 75% случаев отмечают в возрасте с 3 мес до 3 лет, однако дерматологический процесс может начаться и после 30 лет [5].
Для клинической картины ПК характерно поражение центральной нервной системы, органов зрения и кожи [6]. Первым дерматологическим признаком является эритема лица (открытые участки тела) с отечностью и иногда пузырьками после интенсивной инсоляции. Отмечается это у 60% больных с высокой чувствительностью к солнечному свету. У 40% пациентов без признаков фоточувствительности диагноз становится очевидным несколько позже — при появлении гиперпигментированных пятен (лентиго, веснушки) на подверженных инсоляции участках кожи. Такая же картина (гиперпигментация) вырисовывается после регресса воспалительных явлений. В комплексе вышеуказанные проявления идентифицируются как первая (воспалительная) стадия ПК [3]. Затем наступает вторая (пойкилодермическая) стадия. Для нее типичны телеангиэктазии, участки атрофии, сухости, истонченной кожи (появляются беловатые рубчики с гладкой блестящей поверхностью) и сохраняющаяся гиперпигментация, которые создают картину пойкилодермии [3]. На фоне гиперпигментации со временем появляются гипопигментированные пятна, часто на спинке носа и над подбородком [4].
Атрофия кожи приводит к деформации носовых ходов и ротового отверстия, истончению хрящей ушных раковин и носа. В 80% случаев одновременно наблюдается поражение органов зрения: светобоязнь, кератоконъюнктивит, эктропион, блефарит, изъязвление слизистой оболочки век, помутнение роговицы, ее васкуляризация, пигментные пятна на ней, птеригиум; также могут возникать эпителиумы на этих участках [3, 6].
На второй стадии у 20% больных отмечают неврологические нарушения: гипо- и арефлексию, атаксию, сенсорные нарушения, умственную отсталость, аномалии ЭЭГ [3, 6].
Для третьей (опухолевидной) стадии характерно возникновение доброкачественных (папилломы, кератоакантомы, ангиомы, ангиомиомы, фибромы) и злокачественных опухолей. Появляются такие новообразования на слизистой оболочке полости рта (лейкоплакия, хейлит актинический, рак языка и губ). На 8—10-м году болезни происходит малигнизация доброкачественных новообразований или сразу образуются базоцеллюлярные и спиноцеллюлярные эпителиомы, меланомы и саркомы [5]. Частота развития злокачественных новообразований коррелирует с тяжестью кожного процесса. Больные погибают после возникновения метастазов во внутренние органы [3]. В 70% случаев смерть наступает до 15 лет. Однако, по данным P. Bradford и соавт. [7], около 45% больных доживают до 40 лет.
Интересна публикация D. Tennstedt и J.-M. La-chapell [8], в которой они описывают спонтанное исчезновение четырех кератоакантом при ПК после удаления трех, предшествовавших им.
Заболевание обостряется весной и летом, а прогноз тем хуже, чем раньше оно начинается [5].
Комбинация ПК с идиотией и карликовым ростом носит название синдрома Де Санктиса—Каккьоне (идиотия ксеродермическая), описанного в 1932 г. [6]. В клинической картине доминируют умственная отсталость, микроцефалия, задержка роста (карликовый рост) и полового созревания, возможны потеря слуха, мозжечковая атаксия, параличи. На рентгенограмме отмечают малые размеры турецкого седла. Из-за недоразвития гипофиза и мозжечка нарушается порфириновый обмен. Кожные проявления резко выражены. У 70% больных развиваются злокачественные опухоли, которые метастазируют во внутренние органы и ведут к летальному исходу в детском возрасте [3].
Б.А. Бернбейн и соавт. [6] выделяли разновидности ПК: вариант ПК (форма без неврологических нарушений), форма II ПК (повышенная чувствительность к ионизирующей радиации, при которой отсутствуют злокачественные новообразования даже при тяжелом и длительном поражении кожи), пигментный ксеродермоид Юнга. Последняя разновидность является абортивной формой ПК, для которой характерны более позднее начало — в 3—4-м десятилетии, менее выраженные кожные изменения, легкое течение процесса. Предположительно при этой форме понижена чувствительность к солнечному облучению в сравнении с классической ПК (но она выше, чем у здоровых людей) [3].
Дифференциальный диагноз ПК проводят с синдромом Блума, наследственным лентигинозом, световой оспой Базена, пигментной крапивницей, врожденным дискератозом, врожденной пойкилодермией Ротмунда—Томсона, хроническим рентгеновским дерматитом, недержанием пигмента [3, 5].
Лечение ПК малоэффективно. Применяют витамины группы А, В1, В6, В12, РР, противомалярийные препараты, ароматические ретиноиды (этретинат, изотретиноин). Опухолевидные образования предпочтительно удалять (применяют методы иссечения, дерм-абразии, электроэксцизии, диатермокоагуляции, крио-деструкции). Назначают также проспидин по 100 мг внутримышечно (на курс 3000 мг), 5-флюорцитозиновую мазь. В качестве профилактики предохраняют кожу от солнечных лучей, применяя широкополые шляпы, зонты от солнца, фотозащитные кремы.
Приводим наши клинические наблюдения трех случаев ПК.
Больной М., 17 лет, обратился в ГБУ Республики Дагестан «Республиканский кожно-венерологический диспансер» (ГБУ РД РКВД) г. Махачкалы с жалобами на сухость, чувство стягивания и зуд кожи лица, шеи, кистей, стоп, появление там эффлоресценций, а также светобоязнь.
Анамнез. Со слов матери, болеет с годовалого возраста, когда на тыле кистей и лице появлялись шелушащиеся красные пятна, которые постепенно темнели, образовывались беловатые рубчики. Процесс сопровождался зудом и жжением кожи. Лечение (амбулаторное и стационарное) эффекта не давало. Отмечал обострение в летнее время года. Пациент несколько отстает в росте и массе тела от сверстников. Общее состояние удовлетворительное, питание пониженное. Родители не имеют дерматологических заболеваний и не являются родственниками между собой. Имеет старшего брата и сестру, которые не страдают подобной патологией.
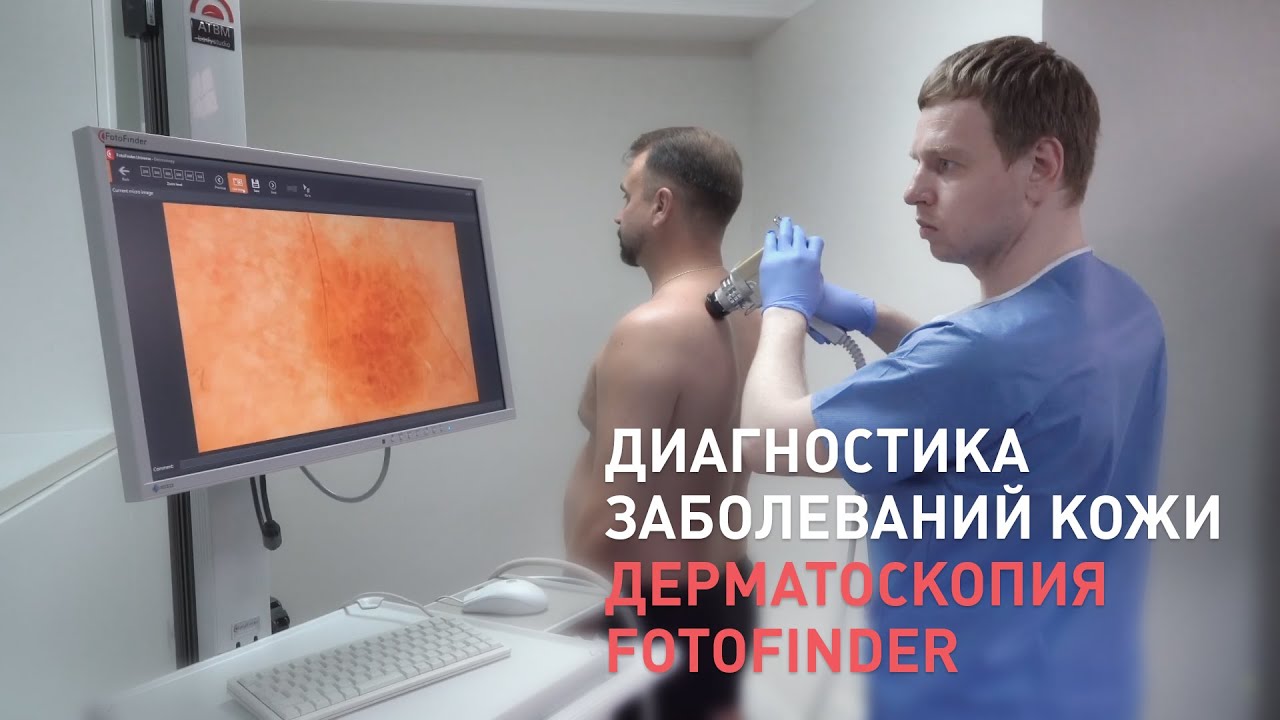
Status specialis: поражение кожи локализовано на лице, шее, тыле кистей и стоп. Кожа лица и шеи имеет пестрый вид: многочисленные темные пятна, белесоватые рубчики, крупнопластинчатые чешуйки (рис. 1). Рис. 1. Больной М. Область лица и шеи с многочисленными темными пятнами, белесоватыми рубчиками, крупнопластинчатыми чешуйками. На тыле кистей единичные коричневые пятна (рис. 2), Рис. 2. Больной М. Тыл кистей с единичными коричневыми пятнами и белесоватыми рубчиками. а на стопах воспалительные явления (рис. 3). Рис. 3. Больной М. Тыл стопы; воспалительные явления в области кожи первого и пятого пальцев. Отмечаются деформация и сужение ротового отверстия: многочисленные трещины, сухость и атрофические рубцовые изменения (рис. 4). Рис. 4. Больной М. Ротовое отверстие с многочисленными трещинами кожи, сухостью и атрофическими рубцовыми изменениями. Кариес. Резко выражен кариес зубов (см. рис. 4). Органы зрения поражены с обеих сторон: кератоконъюнктивит, блефарит, светобоязнь и слезотечение (рис. 5). Рис. 5. Больной М. Двусторонний кератоконъюнктивит, блефарит, светобоязнь и слезотечение. Диагноз: «пигментная ксеродермия, пойкилодермическая стадия».
Проведено лечение: дексаметазон по 4 мг внутримышечно 1 раз в день (10 дней), экстракт алоэ подкожно по 1 мл ежедневно в течение 14 дней, хлорохин (делагил) по 0,25 г 1 раз в день (14 дней), мебгидролин (диазолин) по 0,1 мг 2 раза в день (10 дней), силимарин (карсил) по 35 мг 3 раза в день в течение 9 дней, рибофлавин по 0,01 г 3 раза в день (10 дней), наружно крем солнцезащитный для светлой кожи (SPF-15). В результате терапии клиническая картина не претерпела изменений.
Больная З., 13 лет, с жалобами на гиперпигментированные высыпания и зуд кожи госпитализирован в ГБУ РД РКВД г. Махачкалы.
Анамнез. Родилась от первой беременности, протекавшей без осложнений. В возрасте 2 лет стали появляться эритематозные эффлоресценции на открытых участках кожи. В летнее время процесс обострялся. На момент осмотра пациентка адекватно отвечает на поставленные вопросы. Указывает на зуд пораженных участков. Других заболеваний кожи и внутренних органов не выявлено.
На предплечьях пойкилодермическая картина (рис. 6). Рис. 6. Больная З. Картина пойкилодермической стадии на коже предплечий. В области тыла кистей и стоп мелкие бородавчатые разрастания (рис. 7). Рис. 7. Больная З. На тыле кистей пигментированные пятна, белесоватые участки атрофии, мелкие бородавчатые разрастания с кор.
Диагноз: «пигментная ксеродермия, пойкилодермическая стадия».
Назначено лечение: мебгидролин (диазолин) по 0,1 мг 1 раз в день (утром) и хлоропирамина гидро-хлорид (супрастин) внутримышечно по 1 мл 1 раз в день (вечером) в течение 10 дней, 30% раствор тиосульфата натрия по 4 мл внутривенно через день (14 дней), энтеросгель по 15 г (столовая ложка) 3 раза в день в течение недели, местно на лицо мазь акридерм 2 раза в день в течение 14 дней, на тело и конечности крем солнцезащитный для светлой кожи (SPF-15). На фоне терапии зуд стал менее выражен, клиническая картина сохраняется.
Больная К., 47 лет, обратилась в ГБУ РД РКВД г. Махачкалы с жалобами на крупные пятна лица, шеи и слизистой рта.
Анамнез. Со слов пациентки, экзантема имелась на лице, шее и слизистой рта с рождения. В течение времени она меняла яркость, несколько смещалась. Никаких субъективных ощущений пятно не вызывало. Год назад на нем появились папилломатозные разрастания. Три месяца назад ухудшилась острота зрения левого глаза и появился шум в левом ухе. При ярком солнечном свете рябит в левом глазу, а затем возникают гул и боль в голове.
Status specialis. Состояние пациентки удовлетворительное. Поражение носит распространенный характер, локализовано на левой половине лица — на волосистой части головы, уха, шеи, а также на слизистой оболочке рта. Очаг поражения кожи имеет темно-бордовый цвет, местами фиолетовый, темно-красный с участками здоровой кожи. Кожа подбородка, нижняя губа гипертрофированы и инфильтрированы (рис. 8). Рис. 8. Больная К. Очаг поражения лица, шеи и волосистой части головы. Наблюдаются участки здоровой кожи. Волосы левой брови, волосистой части головы и пушковые в очаги сохранены (рис. 9). Рис. 9. Больная К. Пушковые волосы в очаге.
На фоне пигментного участка местами папилломатозные разрастания и черные милиарные узелки.

Левая половина слизистой оболочки рта и язык насыщенно-красного цвета строго до средней линии. Отмечается инфильтрированность пораженной половины языка (рис. 10). Рис. 10. Больная К. Гипертрофированная нижняя губа; пигментация и отечность левой половины слизистой оболочки рта и языка.
Диагноз: «ксеродермоид пигментный Юнга».
От госпитализации пациентка отказалась и повторно не обращалась.
Мы постарались ознакомить практикующих врачей с клиническими случаями пигментной ксеродермии и ее абортивной формы — пигментного ксеродермоида Юнга. Это должно способствовать свое-временной дифференциальной диагностике редкого генодерматоза, вторичной профилактике его об-острений и симптоматическому лечению, что должно повысить качество жизни таких пациентов.
Сведения об авторах
КАК ЦИТИРОВАТЬ:
Пигментная ксеродерма — одна из наследственных дерматологических болезней. Встречается она крайне редко: 2 случая на 1 миллион новорожденных. Симптоматика заболевания проявляется уже в раннем детском возрасте и неуклонно прогрессирует без комплексного лечения. Опасность пигментной ксеродермы заключается в ее высоком онкогенном потенциале. Кожные проявления болезни являются облигатным предраком, то есть склонны к злокачественному перерождению и практически во всех случаях переходят в рак.
Вместе с тем, первые дерматологические симптомы пигментной ксеродермы у ребенка чаще всего расцениваются родителями, как явления какого-либо аллергического дерматита и не вызывают излишнего беспокойства. Отсутствие настороженности приводит к позднему обращению за медицинской помощью и запоздалому лечению.
Причины и механизм развития
Пигментная ксеродерма относится к группе наследственных заболеваний и передается аутосомно-рецессивным путем. Под аутосомно-рецессивным понимают наследование, когда мутации происходят в любых хромосомах, кроме половых, и для проявления заболевания у ребенка необходимо, чтобы у обоих супругов был дефектный ген.
Основные звенья патогенеза пигментной ксеродермы — повышенная чувствительность к прямым солнечным лучам и невозможность организма устранять повреждения ДНК, вызванные ультрафиолетовым излучением. Нарушение процессов восстановления ДНК связано с отсутствием или низкой активностью в коже ферментов, отвечающих за репарацию: нуклеозидов и протеаз.
Необратимые повреждения генетического аппарата клеток приводят к ряду патологических процессов. Так, на ранней стадии заболевания в кожных покровах наблюдается:
- усиление скорости деления рогового слоя кожи и слущивание отмерших чешуек;
- истончение шиповатого (промежуточного) слоя;
- избыточное отложение меланина в базальном (ростковом) слое эпидермиса и в сосочковом слое дермы;
- инфильтрация лейкоцитами и другими клетками воспаления околососудистых пространств.
На более поздних стадиях пигментной ксеродермы на коже обнаруживают участки избыточного ороговения (гиперкератоз), акантоза (гиперпролиферативные очаги, нередко пигментированные) с элементами клеточной атипии, дегенеративные изменения в коллагеновых и эластиновых волокнах.
Терминальные стадии заболевания преимущественно характеризуются атрофией (истончением) и изъязвлением участков кожи, реже встречаются бородавчатые или папилломатозные разрастания. Особенно выражены эти процессы на открытых частях тела.
В зависимости от повреждённой хромосомы, выделяют 8 подвидов заболевания: A, B, C, D, E, F G и пигментный ксеродермоид Юнга. Первые 7 типов пигментной ксеродермы имеют схожее клиническое течение и определяются лишь после молекулярно-генетического анализа. Пигментный ксеродермоид Юнга имеет более благоприятный прогноз — симптоматика заболевания появляется позже, а сам патологический процесс имеет легкое течение.
Самостоятельной клинической формой заболевания является синдром Де Санктиса-Каккьоне. Он считается самой агрессивной разновидностью пигментной ксеродермы и характеризуется выраженными изменениями со стороны центральной нервной системы. Синдром может развиться при любом хромосомном варианте заболевания, но чаще всего встречается при подтипе A.
Клиническая картина
У новорожденных детей симптомов заболевания нет. Первые признаки пигментной ксеродермы начинают замечать в возрасте от 3 месяцев до 4 лет. В казуистических случаях дебют заболевания возможен в зрелом возрасте. В литературе имеются данные о появлении симптоматики у пациентов 25-30 лет.
Пигментная ксеродерма характеризуется сезонностью и стадийностью течения. Обострение заболевания происходит в солнечное время года (весна — ранняя осень). Первая стадия называется воспалительной и проявляется специфической триадой симптомов:
- фоточувствительность — непереносимость прямых лучей солнечного света;
- эритема — покраснение кожных покровов открытых участков тела после пребывания на солнце;
- очаги гиперпигментации — появление участков избыточной окраски.
Эритема кожных покровов носит стойкий характер. Она нередко сопровождается выраженной отечностью, шелушением и образованием небольших пузырьков с прозрачным содержимым. После стихания воспалительных процессов на месте эритемы появляются очаги гиперпигментации в виде светло- или темно-коричневых пятен разных размеров. В большинстве случаев они напоминают россыпь веснушек, но могут иметь большие размеры (лентиго).
Вторая стадия — пойкилодермическая. Она начинается в возрасте 3-7 лет и характеризуется выраженными изменениями кожных покровов в виде телеангиоэктазий (сосудистых «звездочек»), участков гиперкератоза с обильным шелушением, очагов атрофии и истончения кожи. Типичным проявлением второй стадии также является образование небольших гладких рубчиков белесоватого цвета с блестящей поверхностью. При внимательном осмотре участки атрофии кожи имеют неровный шероховатый вид и похожи на ожоговую поверхность.
Выраженные изменения кожных покровов приводят к ряду серьезных последствий:
- деформация наружного носа и носовых ходов, как следствие — затруднение дыхания;
- искривление рта;
- деформация ушей за счет атрофии хрящей;
- выпадение ресниц;
- выворот или заворот век.
У пациентов с пигментной ксеродермой сохраняются очаги гиперпигментации, а с прогрессированием заболевания появляются гипопигментированные пятна. Как правило, они локализуются на спинке и крыльях носа, на подбородке.
У 75-80% пациентов на второй стадии также определяются признаки поражения органа зрения: слезотечение и светобоязнь, блефарит, изъязвление конъюнктивы и ее воспаление, помутнение роговицы и появление на ней пятен. У 20% больных выявляются симптомы нарушения работы центральной нервной системы в виде снижения чувствительности, умственной отсталости, изменения согласованной работы мышц (атаксия) и снижения или отсутствия безусловных рефлексов (например, сухожильных).
В третью (опухолевидную) стадию заболевание переходит в подростковом возрасте. Для нее характерно появление на пораженных очагах доброкачественных или злокачественных новообразований различной формы и величины. Доброкачественные опухоли могут быть представлены папилломами, невусами, фибромами, ангиомами и имеют высокий риск онкологической трансформации. Нередко новообразования также выявляют на слизистой оболочке полости рта и носа.
Тяжелое клиническое течение имеет синдром Де Санктиса-Каккьоне. Его основные симптомы — нарушение умственного развития (идиотия) из-за уменьшения размеров головного мозга и черепа, карликовость и типичные кожные проявления пигментной ксеродермы. Дополнительными признаками синдрома является задержка полового развития и тяжелые нарушения работы нервной системы (парезы, параличи, атаксия). Кожные проявления у пациентов с синдромом Де Санктиса-Каккьоне появляются рано. Они ярко выражены, быстро прогрессируют и переходят в онкологические новообразования уже в детском возрасте.
Осложнения
Основное осложнение заболевания — появление кожных и висцеральных (внутренних) злокачественных опухолей. Наиболее высоким риском онкогенной трансформации обладают множественные бородавчатые новообразования. Частота возникновения злокачественных опухолей также коррелирует с тяжестью кожных патологических процессов. При раннем начале заболевания и его агрессивном течении онкологические новообразования появляются в подростковом возрасте (12-14 лет) и быстро метастазируют во внутренние органы.
Среди злокачественных опухолей чаще всего развивается плоско- или базальноклеточный рак, реже всего — меланома кожи или глаза. Описаны случаи возникновения более 50 различных вариантов онкологии: фибросарком, ангиосарком, гистиоцитом и других.
Заболевание также может приводить к выраженным деформациям лица (рта, носа, ушей). Как результат — социальная дезадаптация ребенка и психологические проблемы.
Диагностика
Большое значение в постановке правильного диагноза имеет детальный сбор анамнеза. Собранные данные (начало болезни в раннем детском возрасте, сезонность симптоматики, высокая фоточувствительность, кровные браки) позволяют предположить пигментную ксеродерму. Диагноз подтверждается после цитологического и гистологического исследования пораженных участков кожи.
Среди дополнительных обследований — осмотр стоматолога, оториноларинголога, офтальмолога и невролога для исключения поражения центральной нервной системы, ротового аппарата, органов зрения и слуха. При синдроме Де Санктиса-Каккьоне также проводится рентгенологическое исследование или компьютерная томография костей черепа, магнитно-резонансная томография головного мозга. При этом обнаруживают малые размеры турецкого седла, уменьшение объема черепной коробки и головного мозга, недоразвития мозжечка и гипофиза.
Методы лечения
Этиопатогенетического лечения пигментной ксеродермы не существует. По своей сущности, любые способы терапии являются симптоматическими и направлены на устранение имеющихся проявлений заболевания. В комплексное лечение заболевания входят:
- курсы витаминотерапии;
- противомалярийные препараты — отмечена эффективность лекарств этой группы в устранении воспалительного процесса и сенсибилизации организма;
- ароматические ретиноиды;
- цитостатические противоопухолевые препараты.
Пациентам также рекомендуется скорректировать образ жизни, максимально ограничить пребывание на солнце, а перед выходом на улицу позаботиться о защите кожных покровов от солнечных лучей.
Все доброкачественные кожные элементы подлежат обязательному удалению и гистологическому исследованию. При трансформации новообразования в злокачественное тактика лечения определяется, исходя из типа опухоли и стадии онкологического процесса.
Прогноз
Качество и продолжительность жизни зависят от нескольких факторов, в первую очередь, от сроков обращения за медицинской помощью, постановки правильного диагноза и раннего начала комплексного лечения. При своевременной диагностике заболевания и постоянном динамическом наблюдении врачом-дерматологом или онкодерматологом прогноз относительно благоприятный.
При бородавчатых разрастаниях на коже, около 35% пациентов не доживают до совершеннолетия и погибают в возрасте 13-15 лет. Это связано с высокой тенденцией к озлокачествлению и быстрым метастазированием опухоли во внутренние органы.
При синдроме Де Санктиса-Каккьоне прогноз неблагоприятный. Агрессивное течение заболевания приводит к летальному исходу от онкопатологии еще в детском возрасте у 70% пациентов.
Этиология и встречаемость пигментной ксеродермы. Пигментная ксеродерма — генетически разнородное, панэтническое, аутосомно-рецессивное заболевание репарации ДНК, вызывающее выраженную гиперчувствительность к ультрафилетовым лучам. В США и Европе распространенность составляет приблизительно 1 на миллион, но в Японии — 1 на 100 000.
Патогенез пигментной ксеродермы
Репарация ДНК, повреждаемой ультрафиолетовым излучением, происходит благодаря трем механизмам: эксцизионной репарации, пострепликационной репарации и фотореактивизации. Эксцизионная репарация устраняет повреждения ДНК восстановлением нуклеотида или одного основания. Пострепликационная репарация — аварийный механизм, обеспечивающий репликацию ДНК вдоль поврежденного шаблона. Фотореактивация возвращает поврежденную ДНК в нормальное химическое состояние без удаления или замены генетического материала.
Нуклеотидная эксцизионная репарация — сложный разносторонний процесс, в котором участвуют, по крайней мере, 30 белков. Основной принцип — удаление небольшого однонитевого участка ДНК, содержащего повреждение, разрезами с обеих сторон поврежденного сегмента, с последующим заполнением промежутка вновь синтезированной нитью на основе неповрежденной дополнительной нити, используемой как шаблон. В ходе транскрипции гена повреждение ДНК блокирует продвижение РНК-полимеразы II.
Остановленная РНК-полимераза II инициирует эксцизионную репарацию нуклеотидов (репарация, вызванная транскрипцией). В остальной части генома и в нетранскрибируемых генах комплекс нуклеотидной эксцизионной репарации выявляет повреждения ДНК по искажению скручивания ДНК (глобальная геномная репарация).
Пигментная ксеродерма вызвана мутациями, влияющими на геномную нуклеотидную эксцизионную репарацию или пострепликационную репарацию. В отличие от нее, синдром Коккейна — сходное заболевание, вызываемое мутациями, влияющими на связанный с транскрипцией путь нуклеотидной эксцизионной репарации. И пигментная ксеродерма, и синдром Коккейна подразделяют на 10 биохимических групп комплементации; каждая группа отражает мутации различных компонентов нуклеотидной эксцизионной или пострепликационной репарации.
Снижение или полное отсутствие возможности глобальной геномной репарации или пострепликационной репарации приводит к потере функций, необходимых для поддержания целостности генома, и вызывает накопление онкогенных мутаций. Новообразования у пациентов с пигментной ксеродермой имеют более высокий уровень мутаций генов-онкогенов и супрессоров опухолевого роста, чем опухоли в нормальной популяции, и эти мутации специфично вызывает ультрафиолетовое облучение.
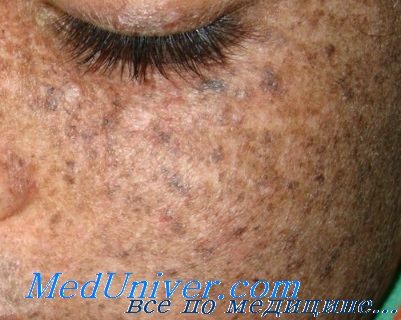
Фенотип и развитие пигментной ксеродермы
Симптоматика у пациентов с пигментной ксеродермой развивается в среднем в возрасте 1-2 года, хотя приблизительно у 5% пациентов описано начало после 14 лет. Первые симптомы обычно включают легкие ожоги, повышенную фоточувствительность, появление лентигинозной сыпи и фотобоязнь. Постоянное воздействие вызывает преждевременное старение кожи (истончение, морщины, веснушки, телеангиэктазии), фотокератоз и доброкачественные и злокачественные новообразования. Почти у 45% пациентов развиваются базальноклеточные или сквамозноклеточные карциномы, у 5% — меланомы.
Приблизительно 90% карцином появляется в местах сильного ультрафиолетового воздействия — на лице, шее, голове, кончике языка. До введения профилактических мероприятий средний возраст развития новообразований был 8 лет, на 50 лет раньше, чем в общей популяции, а их частота более чем в 1000 раз выше общепопуляционной.
Кроме кожных симптомов, у 60-90% пациентов отмечают нарушения со стороны глаз, включая фотобоязнь, конъюнктивиты, блефариты, эктропион и новообразования. Распределение патологии глаз и новообразований соответствуют участкам наибольшего влияния ультрафиолета.
Приблизительно у 18% пациентов развивается прогрессирующая дегенерация нейронов. Симптоматика представлена нейросенсорной глухотой, задержкой умственного развития, спастичностью, гипорефлексиией или арефлексией, сегментарной демиелинизацией, атаксиями, хореоатетозом и надъядерной офтальмоплегией. Тяжесть неврологических симптомов обычно пропорциональна степени нарушения нуклеотидной эксцизионной репарации. Нейродегенерация может быть вызвана неспособностью исправлять ДНК, повреждаемую эндогенными свободными радикалами.
Эксцизионная нуклеотидная репарация также исправляет повреждения ДНК, вызванные большинством химических канцерогенов, например сигаретным дымом, подгоревшей пищей или цисплатином (производное платины с противоопухолевой активностью, способное стимулировать механизмы клеточно-опосредованной цитотоксичности). В связи с этим у пациентов в 10-20 раз повышена частота опухолей внутренних органов, например опухолей мозга, лейкозов, рака легких и желудка.
Пациенты с пигментной ксеродермой имеют уменьшенный срок жизни; без профилактической защиты срок их жизни почти на 30 лет короче по сравнению с лицами без пигментной ксеродермы. Наиболее частые причины смерти — метастатические меланомы и сквамозноклеточные карциномы кожи.
Два сходных с пигментной ксеродермой заболевания, синдром Коккейна и трихотиодистрофия, также вызываются дефектами в различных компонентах клеточного механизма репарации нарушений ДНК, вызванных ультрафиолетом. Для обоих заболеваний характерны плохой постнатальный рост, уменьшение подкожной клетчатки, контрактуры суставов, тонкая кожа с фоточувствительностью, умственная задержка и неврологические симптомы.
У детей с синдромом Коккейна также развиваются дегенерация сетчатки и глухота; дети с трихотиодистрофией имеют ихтиоз и ломкие волосы и ногти. При обоих синдромах пациенты редко живут дольше 20 лет. Интересно, что ни тот, ни другой синдром не сопровождаются увеличением частоты опухолей кожи. Тем не менее дефекты в некоторых генах репарации ДНК (ERCC2, ERCC3 и ERCC5) приводят к фенотипам, имеющим общие симптомы между пигментной ксеродермой, синдромом Коккейна и трихотиодистрофией.
Особенности фенотипических проявлений пигментной ксеродермы:
• Возраст начала: детство
• Чувствительность к ультрафиолету
• Опухоли кожи
• Неврологическая дисфункция
Лечение пигментной ксеродермы
Подтверждение диагноза пигментной ксеродермы проводят функциональными тестами репарации ДНК и чувствительности к ультрафиолету; такие тесты обычно выполняют на зрелых фибробластах кожи. Подтверждение диагноза идентификацией мутаций в генах, связанных с пигментной ксеродермой, в настоящее время клинически недоступно.
Оказание помощи пациентам с пигментной ксеродермой состоит в исключении воздействия солнечного света, ношении защитной одежды, использовании физических и химических солнцезащитных кремов и тщательном наблюдении для своевременного выявления и удаления злокачественных новообразований. Исцеляющее лечение в настоящее время недоступно.
Риски наследования пигментной ксеродермы
Поскольку пигментная ксеродерма — аутосомно-рецессивное заболевание, семейный анамнез у большинства пациентов не отягощен. Для родителей, имеющих ребенка с пигментной ксеродермой, риск для последующих детей — 1 к 4. Пренатальная диагностика возможна путем определения функции репарации ДНК и чувствительности к ультрафиолету в культуре амниоцитов или клеток ворсин хориона.
Пример пигментной ксеродермы. B.C., 3-летний мальчик, направлен в клинику дерматологии в связи с выраженной чувствительностью к солнечным лучам и появлением множественных пятен. При клиническом осмотре выявлены фотобоязнь, конъюнктивит и значительная лентигинозная гиперпигментация в незащищенных от солнца областях; в остальном его развитие и данные осмотра оказались нормальными. Пациент — ребенок от неродственного брака родителей японского происхождения; никто в семье подобным образом не болел. Дерматолог сказал, что у ребенка классические проявления пигментной ксеродермы.
Для подтверждения диагноза проведена биопсия кожи с целью оценить репарацию ДНК и чувствительность к ультрафиолетовому излучению фибробластов кожи. Результаты этого теста подтвердили диагноз пигментной ксеродермы. Несмотря на соответствующие профилактические меры, в возрасте 15 лет у ребенка развилась метастатическая меланома, и через 2 года он умер. У его родителей есть два других ребенка; ни один из них не болен пигментной ксеродермой.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Синдромы хромосомной нестабильности. Пигментная ксеродерма.
В эту группу включен ряд синдромов, характеризующихся хромосомными повреждениями клеток в ответ на мутагенное действие ультрафиолетового излучения, ионизирующей радиации, химических канцерогенов и онкогенных вирусов. Высокий риск развития злокачественных новообразований при этих заболеваниях обусловлен характерными нарушениями репликации нуклеиновых кислот или дефектами репарации.
Следует учитывать, что ряд наследственных синдромов, которые могли бы рассматриваться в этой группе болезней, представлены в других разделах. В частности, атаксия-телеангиэктазия рассматривалась выше — в группе первичных иммунодефицитных заболеваний.
Хотя успехи биохимической и молекулярной генетики (по клонированию генов, получению сведений о локализации гена, первичном продукте мутантного гена и т.д.) позволили добиться значительного прогресса в понимании механизмов действия генов при целом ряде генетических заболеваний, связанных с высоким риском развития злокачественных новообразований, все же многие аспекты патогенеза опухолей при генетических синдромах пока остаются неясными. В частности, трудно объяснить, почему при пигментной ксеродерме повышается частота только кожного рака, а при синд роме Елума, врожденном дискератозе и анемии Фанкони в первую очередь возрастает частота развития злокачественных новообразований внутренних органов и лишь во вторую рака кожи, тогда как при синдроме Коккейна и триходистрофии. в некоторых случаях сопровождающихся тем же дефектом репарации ДНК, что и при пигментной ксеродерме, нехарактерно ни повышение риска развития рака кожи, ни возникновение злокачественных новообразований внутренних органов.
Ниже приводятся особенности ряда генетических кожных синдромов, ассоциирующихся со злокачественными новообразованями кожи и внутренних органов.
Пигментная ксеродерма
Пигментная ксеродерма (ПК) — редкое гетерогенное наследственное; аутосомно-рецессивное заболевание, одинаково частое у мужчин и женщин.
Самый ранний клинический признак пигментной ксеродермы — фотодерматит открытых участков кожи, возникающий даже при минимальной инсоляции и нередко сопровождающийся слезотечением и конъюнктивитом. Обычно эти изменения, соответствующие 1 клинической стадии ПК, возникают в период новорожденности или раннего детства (до 2-3 лет) и в дальнейшем (во II стадии) прогрессируют с развитием сухости кожи, образованием чешуек, гипо- и гиперпигментации (по типу лентиго и веснушек), рубцов, телеангиэктазий и участков атрофии, что создает картину пойкилодермии. Возможны также бородавчатые разрастания, трещины, изъязвления. Атрофия кожи лица сопровождается истончением кожи носа, ушных раковин, деформацией естественных отверстий, эктропионами, выпадением ресниц, изъязвлением слизистой носа.
При пигментной ксеродерме относительно часты неврологические расстройства — от умеренных, определяемых только с помощью тестирования, до тяжелых нарушений двигательных функций и задержки умственного развития или деменции. Наиболее тяжелые формы неврологической патологии наблюдаются при группе комплектации ПК-А (возникающей в молодом возрасте) и группе комплектации ПК-D (развивающейся в пожилом возрасте). При ПК-С, Е, F, V неврологические поражения нечасты. Тяжесть неврологических симптомов может отражать накопление в нейронах повреждений ДНК, не способной к репликации. Неврологическая симптоматика не коррелирует ни с наличием или длительностью солнечного облучения, ни с частотой кожного рака.
Кожный рак возникает на III стадии пигментной ксеродермы. Частота его развития в 5000 раз выше, чем в общей популяции. С первой опухолью обычно обращаются к врачу в детстве. При ПК развиваются все типы кожных раков: плоскоклеточный рак кожи, базалиома и др., а также меланома (часто множественная). Их анатомическая локализация подобна таковой в общей популяции, однако течение неблагоприятно и отличается высокой смертностью от метастазов. Известен лишь один случай спонтанного регресса у больного ПК множественной меланомы. Особенно высока предрасположенность к раку кожи при ПК групп А, С и D; наоборот, при ПК групп Е и F новообразования развиваются редко и в более позднем возрасте; ПК-В и G редки и проявляются синдромом Коккейна; ПК-V может сопровождаться как тяжелыми, так и легкими поражениями кожи. Характер злокачественного опухолевого процесса зависит от группы комплементации: при ПК-Е и ПК-V преимущественно развивается базалиома, при ПК-С — плоскоклеточный рак кожи, при ПК-D — меланома. Интересно, что у больных ПК лишь незначительно повышен риск развития опухолей внутренних органов.
При пигментной ксеродерме развиваются и доброкачественные опухоли кожи: фибромы, кератоакантомы, ангиомы, кератомы, нейрофибромы, невромы, обызвествленная эпителиома Малерба, атипичная фиброксантома и др.
Гистологические изменения при пигментной ксеродерме неспецифичны и зависят от стадии процесса: на ранней эритематозной стадии обнаруживаются гиперкератоз, неравномерное накопление пигмента в базальном слое эпидермиса, расширение поверхностных сосудов, отек сосочкового слоя дермы, периваскулярная лимфоцитарно-гистиоцитарная инфильтрация; со временем увеличивается выраженность пигментации, атрофия эпидермиса, развивается актинический эластоз с гомогенизацией, базофильной дегенерацией коллагена, фрагментацией эластических волокон; на опухолевой стадии гистологические изменения соответствуют типу новообразования.
Диагноз пигментной ксеродермы устанавливается на основании клинической картины и анамнеза заболевания (кровные браки). Пренатальная диагностика проводится у гомозиготных плодов путем обнаружения в клетках амниотической жидкости нарушения репарации ДНК после ультрафиолетового облучения.
Дифференциальный диагноз пигментной ксеродермы проводится с наследственным лентиго, врожденным дискератозом, синдромом Ротмунда—Томсона.
Тяжелый прогноз пигментной ксеродермы обусловлен высокой склонностью к возникновению злокачественных новообразований кожи.
Лечение пигментной ксеродермы. Любые опухоли, в том числе клинические доброкачественные, следует удалять на самых начальных этапах развития. Помимо хирургического удаления опухолей используют внутримышечные инъекции проспидина, длительный прием внутрь ароматических ретиноидов, криодеструкцию, лучи лазера, мази, содержащие цитостатики — флуороурацил (5-фторурацил), проспидин и др.
Профилактика пигментной ксеродермы — исключение кровных браков. Для профилактики кожного рака важны раннее выявление заболевания и защита от воздействия на кожу ультрафиолетовых лучей (солнцезащитные кремы и т.д.), рекомендуется также применение интерферонов.
Фотодерматозы — разнообразная группа кожных болезней, отличающихся по клинической картине, тяжести течения и прогнозу, в патогенезе которых важная роль принадлежит солнечному излучению.
Фотодерматозы — разнообразная группа кожных болезней, отличающихся по клинической картине, тяжести течения и прогнозу, в патогенезе которых важная роль принадлежит солнечному излучению.
Солнечный свет состоит из волн разной длины: ультрафиолетовое (УФ) излучение, инфракрасное и видимое излучение (рис. 1).
Самое серьезное из них в плане повреждения кожи — это УФ-излучение. Его делят на УФА (320–380 нм), УФВ (280–320 нм) и УФС (200–280 нм). Наиболее опасно УФС, но оно в основном поглощается озоновым слоем стратосферы и не достигает земной поверхности (рис. 2).
Высокие дозы УФ-радиации вызывают различные биологические реакции в человеческом организме. Единица измерения УФ-облучения — биодоза (минимальная эритемная доза) — это минимальная продолжительность облучения, при которой возникает четко очерченное покраснение кожи. Биодозу выражают в минутах или в количестве энергии на единицу площади мДж/см 2 (для УФВ) или Дж/см 2 (для УФА). Воздействие УФА-лучей наиболее глубокое. Они проникают в дерму и соединительную ткань и при длительном воздействии вызывают дистрофические изменения соединительной ткани, ускоряют процесс старения кожи (фотостарение, геродермия), могут способствовать развитию меланомы, вызывать повреждения ДНК и мутации в клетках кожи.
УФВ-излучение поглощается преимущественно клетками верхних слоев эпидермиса, вызывает загар и солнечные ожоги. В малых дозах УФВ-лучи индуцируют синтез витамина Д; посредством секреции эндотелиального фактора роста (endothelial growth factor — EGF) УФВ-излучение способствует развитию опухолей кожи, в том числе и меланомы. Доказано также иммуносупрессивное действие УФВ-излучения, что приводит к снижению иммунитета в отношении инфекционных и паразитарных заболеваний, подавлению отторжения опухолевых клеток и возникновению рака кожи.
Чувствительность кожи к воздействию УФ-лучей зависит от индивидуальных особенностей человека и цвета его кожи, в связи с чем выделяют несколько фототипов (светочувствительность) кожи (табл. 1).
Ввиду многообразия эндогенных и экзогенных факторов, способствующих этой патологии, единой классификации до настоящего времени нет.
Существует классификация по клинической характеристике патологического процесса (Штейнберг М. А., 1958; Нерадов Л. А., 1959); по патогенезу: генетические, метаболические, дегенеративно-атрофические и прочие фотодерматозы (Parrish J. A. et al., 1979); по фоточувствительности кожи и характеру обычной реакции на облучение; часто используют классификацию поражений кожи по длине волны света, вызвавшего поражения:
а) изменения, вызванные чрезмерной по интенсивности или длительности инсоляцией:
– солнечные ожоги;
– острые актинические дерматиты; или повторяющимся облучением:
– фотостарение кожи;
– солнечный эластоз;
– предопухолевые и опухолевые поражения кожи;
б) фотодерматозы, вызванные дефицитом естественных кожных протекторов (пигментная ксеродерма, альбинизм);
в) дерматозы, усиливающиеся или проявляющиеся после инсоляции (красная волчанка, дерматомиозит, болезнь Дарье, хлоазма);
г) дерматозы, обусловленные присутствием в коже веществ, способных усилить солнечные эффекты, или заставляющие реагировать иммунную систему кожи после фотоактивации.
Солнечные лучи в организме человека могут вызывать различные типы патологических реакций: фототравматические, фототоксические, фотоаллергические и идиопатические (причины которых неизвестны).
Фототравматические реакции возникают при избыточном по интенсивности или по времени облучения кожи или при дефиците естественных факторов защиты. По времени возникновения такие реакции могут быть острые и хронические.
К острой фототравматической реакции относится солнечный ожог, протекающий по типу острого воспаления кожи. Он развивается в короткое время при гиперинсоляции у лиц с повышенной фоточувствительностью (I–II фототип) на участках кожи, подвергшихся облучению. Солнечный ожог проявляется эритемой, зудом, а в тяжелых случаях — отеком, везикулами, пузырями и болью; сопровождается повышением температуры тела, недомоганием, головной болью. При легкой степени ожога воспалительные явления разрешаются самопроизвольно и переходят в загар. При тяжелых реакциях — через несколько дней наступает интенсивное шелушение кожи, гипер- и гипопигментация. Рубцы обычно не образуются.
Патогенез. Под действием УФВ-лучей происходит нарушение структуры ДНК эпидермальных клеток в результате поглощения энергии УФ-лучей. Медиатором воспаления служат гистамин, серотонин, простагландины, лизосомальные ферменты, кинины.
Прогноз. Тяжелые солнечные ожоги, сопровождающиеся пузырями, могут быть фактором риска развития меланомы. Повторные солнечные ожоги приводят к преждевременному старению кожи (геродермии, актиническому старению).
Лечение и профилактика. Лечение зависит от степени выраженности дерматита. При легкой степени — примочки с 2% раствором борной кислоты, Свинцовой воды, влажные обертывания с настоем лекарственных трав — ромашки, календулы, зеленого чая и др., мази с кортикостероидами.
При тяжелых реакциях — Аскорутин, Аспирин, Индометацин по 1 таблетке 3 раза в день, кортикостероиды 15–20 мг/сут, Делагил, Плаквенил.
Местно — влажные обертывания, кортикостероидные мази. Может потребоваться соблюдение постельного режима и даже госпитализация.
Профилактика — фотозащитные (солнцезащитные) средства — лосьоны, гели, кремы с высоким солнцезащитным индексом (SPF), особенно лицам I и II фототипов.
Актиническое старение кожи (фотостарение, солнечная геродермия) — возникает при многолетнем регулярном воздействии УФ-излучения и обусловлено его кумулятивным эффектом. УФА-излучение, действующее на кожу, повреждает белки, липиды клеточных мембран, нуклеиновые кислоты. Постепенно накапливаясь, эти повреждения вызывают дегенеративные изменения в эпидермисе, коллагеновых и эластических волокнах и межклеточном веществе дермы, в результате чего кожа становится более сухой и грубой, постепенно теряет тонус, появляются морщины, пигментные пятна (солнечное лентиго), телеангиоэктазии, участки кератоза (актинический кератоз).
Гистологически это проявляется гиперкератозом, атрофией эпидермиса, эластозом, увеличением содержания меланина, появлением атипичных меланоцитов, расширением капилляров. Эти признаки проявляются преимущественно на открытых участках кожи.
Патогенез. При поглощении квантов света молекулы переходят в нестабильное состояние, что делает их более реакционно-способными. В результате могут образовываться как вполне устойчивые, так и свободные радикалы и активные формы кислорода. Таким образом, УФ-излучение вызывает прямое повреждение молекул белков и нуклеиновых кислот, а также опосредованное свободными радикалами (рис. 3, рис. 4).
Белки и нуклеиновые кислоты первыми испытывают на себе вредное воздействие УФ-излучения, т. к. имеют максимальное поглощение в УФ-области. Затем, в результате свободнорадикальных реакций, повреждаются липидные структуры (липидные пласты эпидермиса и клеточные мембраны). Реакция окисления липидов с участием свободных радикалов (перекисное окисление липидов) имеет цепной неуправляемый характер и приводит к образованию большого количества активных форм кислорода, липидных гидроперекисей и других реакционно-способных молекул.
Дегенеративные изменения кожи под действием УФ-излучения могут быть связаны с повышением активности металлопротеаз — ферментов, разрушающих межклеточное вещество дермы. Еще одной причиной повреждения тканей при воздействии УФ-излучения является воспаление. Оно возникает как вследствие перекисного окисления клеточных мембран, так и в результате выработки воспалительных цитокинов кератиноцитами в ответ на УФ-излучение.
Течение и прогноз. Без соответствующего лечения процесс актинического старения прогрессирует. Фотостарение, в отличие от хроностарения, в значительной степени обратимо. Кожа, как и любая живая ткань, может не только защищать себя от повреждений, но и восстанавливать разрушенные структуры. Поддерживая и стимулируя репаративные системы, можно существенно улучшить внешний вид кожи, поврежденной УФ-излучением, и добиться ее видимого омоложения.
Лечение и профилактика. Первое, что нужно сделать для предотвращения фотостарения, — уменьшить количество фотонов, достигающих кожи. Для этого следует, по возможности, избегать солнца и использовать солнцезащитные средства. В связи с тем, что повреждающим действием обладает не только УФ-излучение, идущее с прямыми лучами солнца, но и отраженное от земли и окружающих предметов, проходящее сквозь облака, воду и легкую одежду, необходимо ежедневно, независимо от времени года, использовать косметику, содержащую УФ-фильтры.
Все УФ-фильтры делятся на химические (или органические) фильтры и физические, или экраны, содержащие частички, рассеивающие, отражающие и поглощающие УФ-излучение.
К органическим фильтрам относятся: УФВ-фильтры — цинкоматы, бензофенол, парааминобензойная кислота (РАВА) и ее производные салицилаты камфоры и др., УФА-фильтры — дибензоилметан, бензофенон, производные камфоры.
Природные солнцезащитные средства — экстракты алоэ, ромашки, кофейная кислота, масло каритэ, 1-, 3-бета-глюканы и др. В качестве неорганических УФ-фильтров используют диоксид титана (TiO2), оксид цинка (ZnO), оксиды железа (Fe2O3, Fe3O4) и т. д.
Помимо использования УФ-фильтров существуют другие меры защиты кожи от фотостарения.
В коже в процессе эволюции сформировались защитные механизмы, позволяющие снизить повреждающее действие УФ-лучей. Часть из них работает также по принципу фильтров и позволяет снизить число фотонов, достигающих уязвимых структур кожи. В качестве химических фильтров выступают вещества, поглощающие УФ-излучения, — меланин, уроканиновая кислота; роль физического фильтра берет на себя роговой слой, который утолщается в ответ на интенсивное УФ-излучение.
Прямое повреждающее действие УФ-излучения на биоткани лишь отчасти ответственно за фотостарение. Более серьезный вклад в этот процесс вносят реакции с участием свободных радикалов, образующихся как в результате прямого действия УФ-излучения, так и сопровождающих вызванную им воспалительную реакцию. Поэтому большую роль в защите кожи от УФ-излучения играют антиоксиданты — вещества, обезвреживающие свободные радикалы и блокирующие реакции с их участием.
В коже существует надежная антиоксидантная система, состоящая из жирорастворимых антиоксидантов, поступающих на поверхность кожи с кожным салом — альфа-токоферол, бета-каротин, сквален, и защищающая кератин и липиды эпидермиса от свободнорадикального окисления.
Кроме того, в клетках эпидермиса присутствует целый набор антиоксидантов, ферментной и неферментной природы. К первым относятся супероксиддисмутаза (СОД), каталаза, глутатионпероскидаза. В мембранах кератиноцитов много альфа-токоферола, блокирующего реакции перекисного окисления липидов. В цитоплазме клеток содержится аскорбиновая кислота, которая является восстановителем для альфа-токоферола.
Кроме того, антиоксидантными свойствами обладают также женские половые гормоны, серосодержащие аминокислоты, растворимые предшественники меланина, мелатонин. Однако антиоксиданты белковой природы, как и другие белки, повреждаются УФ-излучением и снижают свою активность. Другие антиоксиданты в процессе борьбы со свободными радикалами окисляются и требуют восстановления.
Поддержать естественную антиоксидантную систему кожи на должном уровне можно с помощью косметических средств, содержащих антиоксиданты.
Антиоксиданты в косметике, как и в коже, делятся на жирорастворимые (липофильные) и водорастворимые (гидрофильные).
Из жирорастворимых антиоксидантов чаще всего используют альфа-токоферол, каротиноиды, сквален, убихинон. Из водорастворимых — витамин С, а также растительные полифенолы (флавоноиды).
Источником флавоноидов, оказывающих антиоксидантное, противовоспалительное и сосудосуживающее действие, чаще всего является экстракт зеленого чая, виноградных косточек, коры приморской сосны, гинкго, ромашки приморской, календулы лекарственной, василька синего и др. растений.
В связи с тем, что реакции с участием свободных радикалов, вызванные УФ-излучением, разворачиваются в коже достаточно быстро, важно обеспечить надежную защиту до начала действия повреждающего фактора. Поэтому антиоксиданты и УФ-фильтры стали обязательным компонентом дневных и солнцезащитных кремов, а также средств декоративной косметики.
Постоянно используя косметические средства, содержащие антиоксиданты, и избегая солнечных ванн, можно существенно замедлить скорость старения кожи.
При имеющихся уже признаках фотостарения (морщины, пигментные пятна, телеангиоэктазии и т. д.) целесообразно применять не только защитные, но и лечебные средства.
Основным средством против фотостарения являются ретиноиды.
Еще в 1986 г. А. М. Клигманом была впервые продемонстрирована способность транс-ретиноивой кислоты (третиноина) устранять многие признаки фотостарения и восстанавливать нормальную структуру кожи. Впоследствии эта способность ретиноидов была многократно подтверждена другими авторами.
Ежедневное применение кремов, содержащих ретиноиды, в частности, третиноина 0,1%, заметно сокращает признаки фотостарения. Активация регенеративных процессов в коже является эффективным методом в борьбе с фотостарением. В этом ключе целесообразно использовать различные отшелушивающие средства — пилинги, как химические (фенолом, трихлоруксусной кислотой (ТСА), альфа-гидроксильными кислотами (АНА)), так и аппаратные — дермобразия, лазерная шлифовка (эрбиниевые и СО2-лазеры). Наряду со стимуляцией регенерации кожи эти методы являются высокоэффективными в борьбе с гиперпигментацией, которая является одним из характерных признаков фотостарения кожи и не поддается консервативной терапии 2–4% гидрохиноном, койевой, аскорбиновой, фитиновой, лимонной, гликолевой кислотами.
Актинический (солнечный) кератоз
Заболевание, возникающее в результате многолетнего регулярного воздействия солнечного света у людей І–ІІІ фототипов. В основе патогенеза лежит повреждение кератиноцитов. Основным травмирующим агентом является УФВ-излучение (длина волны 280–320 нм). Болеют взрослые, как правило, мужчины, работающие на открытом воздухе (фермеры, пастухи, моряки, альпинисты, теннисисты и др.).
Клиническая картина характеризуется появлением жестких ороговевающих чешуек, спаянных с подлежащей кожей, округлой или овальной формы, при насильственном удалении которых отмечается болезненность. Цвет чешуек варьирует от нормальной кожи до желто-коричневых, часто с красноватым оттенком, при пальпации жесткие, шероховатые. Размер, как правило, менее 1 см. Элементы располагаются изолированно, преимущественно на лице, ушных раковинах, боковых поверхностях шеи, тыльной поверхности кистей, предплечьях и голенях. Течение хроническое, возможны спонтанные ремиссии. Частота злокачественного перерождения примерно 1 на 1000 ежегодно. По современной классификации ВОЗ это заболевание отнесено к предраковым. Злокачественная трансформация очагов происходит медленно, метастазы наблюдаются очень редко.
Лечение и профилактика. Большинству больных помогает фторурацил (5% крем) в течение нескольких недель в сочетании с криодеструкцией, лазерной деструкцией, 30% проспидиновой мазью. Перед длительным пребыванием на солнце — солнцезащитные средства с высоким фактором защиты.
Продолжение читайте в следующем номере.
Н. Ф. Яровая, кандидат медицинских наук, доцент
Читайте также:

