Флегмона забрюшинного пространства при панкреонекрозе
Обновлено: 07.05.2024
1 ГБОУ ВПО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого Минздрава России»
Проведен анализ результатов лечения 26 больных с инфицированным деструктивным панкреатитом различной этиологии, первично оперированных как в условиях ККГСЦ КГБУЗ «Краевой клинической больницы», так и в районных больницах по месту жительства на территории Красноярского края. Учитывались следующие сравнительные параметры в зависимости от тяжести состояния: сроки выполнения первичной операции от начала заболевания, распределение по шкалам SAPSII и SOFA в динамике, продолжительность стационарного лечения, длительность пребывания в отделении реанимации и интенсивной терапии, наличие местных и системных осложнений, летальность. Полученные в ходе исследования данные показывают, что неоправданно раннее оперативное хирургическое вмешательство, недостаточный объём операций при панкреонекрозе, несвоевременность выполнения необходимого объёма лечения на ранних этапах формирования деструктивного панкреатита способствует увеличению доли гнойно-септических осложнений и, как следствие, повышению риску летального исхода. Наиболее частым осложнением у пациентов с тяжелым ПН является формирование тотальной флегмоны забрюшинного пространства. Риск летального исхода существенно повышается при центральном расположении забрюшинной флегмоны.

1. Арутунян А.В., Черданцев Д.В., Арутунян А.В. / Острый панкреатит: анализ заболеваемости в Красноярском крае. Сборник трудов краевой научно-практической конференции, посвященной юбилею ГКБСМП им. Н.С. Краповича.¬ – Красноярск, КрасГМУ, 2013. – С.33-38.
2. Белобородова Ю.С., Винник Ю.С., Белобородов А.А. и др. Значение методов лучевой визуализации в диагностическом алгоритме при остром панкреатите // Сибирское медицинское обозрение. – 2014. – № 1. – С. 66-70.
3. Данилов М.В., Федоров В.Д. / Хирургия поджелудочной железы. Руководство для врачей. – М.: Медицина, 1995. – 512 с.
4. Дюжева Т.Г., Джус Е.В., Рамишвили В.Ш. и др. Ранние КТ-признаки прогнозирования различных форм парапанкреонекроза // Анналы хирургической гепатологии. – 2009. – 14 (40). – С. 54-63.
5. Дюжева Т.Г. Хронический панкреатит. Как повысить эффективность лечения? // Cons. Med. Хирургия. – 2013. – № 1. – С. 20-24.
6. Зайнутдинов А.М. Профилактика и лечение гнойных осложнений у больных деструктивным панкреатитом / А.М. Зайнутдинов, И.С. Малков, А.П. Киршин // Казанский мед. журн. – 2009. – № 6. – С. 821–826.
7. Павликова Е.Ю. Диагностика панкреонекроза и его послеоперационных осложнений. Литературный обзор / Е.Ю. Павликова // Вестн. Рос. науч. центра рентгенорадиологии Федерального агентства по высокотехнологичной мед. помощи. – 2010. – № 10. – С. 30–38.
8. Первова О.В., Черданцев Д.В., Винник Ю.С. Деструктивный панкреатит: комплексное решение проблемы // Актуальные вопросы диагностики и лечения хирургической инфекции: материалы юбилейной конференции, посвященной 10-летию образования Красноярского краевого гнойно-септического центра.– Красноярск: ОИиПДККМИАЦ, 2011. – С.77–86.
9. Buchler М.W. Acute necrotizing pancreatitis: treatment strategy according to the status of infection / M.W. Buchler [et al.] // Ann. Surg. – 2014. – Vol. 232, N 5. – P. 619-626.
10. Spanier B.W. Epidemiology, and etiology and outcome of acute and chronic pancreatitis: an update / B.W. Spanier, M.G. Dijkgraaf, M.J. Bruno // Best Pract. Res. Clin. Gastroenterol. – 2013. – Vol. 1, № 22. – P. 45–63.
Актуальность. Острый панкреатит остается одной из наиболее важных проблем ургентной абдоминальной хирургии. На протяжении последних лет заболеваемость острым панкреатитом занимает второе, а в некоторых регионах – первое место в структуре острой хирургической патологии органов брюшной полости [3, 5, 9]. В 15–20 % наблюдений развитие острого панкреатита носит деструктивный характер. У 40–70 % больных происходит инфицирование очагов некротической деструкции. Именно эта категория больных является наиболее проблемной в диагностическом, лечебном и экономическом аспектах [2,4].
Cреди причин высокой летальности одно из важных мест занимает поздняя госпитализация пациентов, несвоевременная диагностика гнойно-септических осложнений, неадекватный выбор стартовой консервативной терапии, сроков и объема хирургического лечения [3, 8].
Цель исследования состояла в изучении особенностей характера течения и результатов лечения инфицированного панкреонекроза у больных на территории Красноярского края.
Материалы и методы. В исследование вошли 26 больных синфицированным деструктивным панкреатитом различной этиологии, которые находились на лечении в условиях ККГСЦ КГБУЗ «Краевая клиническая больница» г. Красноярска в период с 2013 г. по 2015 г. Мужчин было 16, женщин – 10, возраст больных варьировал от 19 до 77 лет, средний возраст составил 48,4±15,9 лет. Причинами развития заболевания у 55,4 % больных был алкогольный фактор, у 34,7 % – билиарный, и у 9,9 % пациентов причина осталась невыясненной.
Степень тяжести больных определяли по шкале SAPSII [8], наличие и степень выраженности полиорганной недостаточности (ПОН) определяли по шкале SOFA [8]. Кроме балльной оценки тяжести, нами учитывались критерии синдрома системного воспалительного ответа (ССВО), отражающие степень выраженности воспалительного процесса и свидетельствующие о наличии сепсиса. Для стратификации тяжести ПН использовали шкалу, предложенную в Санкт-Петербургском НИИ скорой помощи им. И.И. Джанелидзе [9]. В зависимости от степени тяжести панкреонекроза пациенты были распределены следующим образом: средняя степень тяжести выявлена у 7 больных (26,93 %); тяжелый панкреонекроз – у 19 пациентов (73 %).
Диагноз инфицированного ПН устанавливался на основании лабораторных исследований: клинический анализ крови с определением количества лейкоцитов, лейкоцитарной формулы; биохимический (уровень амилазы, липазы, мочевины, креатинина, общего белка); и инструментальных методов. Всем пациентам при поступлении выполнялось ультразвуковое исследование (УЗИ) и мультиспиральная компьютерная томография с внутривенным болюсным контрастированием (МСКТа).
При поступлении все пациенты были госпитализированы в отделение реанимации и интенсивной терапии (ОРИТ), для проведения комплексной интенсивной терапии, направленной на коррекцию витальных функций, водно-электролитного баланса, проведения интра- и экстрокорпоральной (по показаниям) деинтоксикации, антибиотикотерапии, секретолитической и стресспротекторной терапии.
При выборе хирургической тактики отдавали предпочтение открытым методам. Все пациенты оперированы из традиционного срединного доступа. В сомнительных случаях, при неподвижных, плотно фиксированных некрозах, наличии кровотечения из окружающих тканей, манипуляцию завершали санацией и тампонадой сальниковой сумки через сформированную оментобурсостому. При септических флегмонах забрюшинной клетчатки выполняли их вскрытие и проточно-промывное дренирование через люмботомические разрезы на соответствующей очагу поражения стороне. При наличии гнойного перитонита, кишечных свищей, признаков ишемии толстой кишки, операция завершалась наложением лапаростомы. Программированный контроль состояния брюшной полости выполняли через 48, реже – через 72 часа.
Результаты и обсуждение. Основная часть пациентов с деструктивным панкреатитом доставлялась в клинику в тяжелом и крайне тяжелом состоянии. Средняя давность заболевания до госпитализации в ККБ составила 7,4±6,2дней, причем для пациентов с ПН средней степени тяжести этот показатель был в среднем 6,1±5,1 дней, в то время как для больных с тяжелым ПН – 8,8± 6,4 суток (табл. 1).
Взаимосвязь тяжести ПН от давности заболевания
Давность заболевания (сутки)
ПН средней степени
Анализ сроков выполнения первичной операции показал, что в условиях ЦРБ было оперировано 10 (38,5 %) больных, причем во всех случаях оперативное вмешательство было выполнено в ранние сроки, в среднем, на 2,3± 1,7 сутки от начала заболевания. В послеоперационном периоде эти больные были транспортированы в ККГСЦ ККБ с клиникой тяжелого ПН (табл. 2). Из них 7 больным потребовалось повторное вмешательство в экстренном порядке в связи с необходимостью редренирования гнойно-некротических полостей. Остальные 16 (61,5 %) пациентов были госпитализированы в ККБ с клиникой прогрессирования средне-тяжелого и тяжелого ПН на фоне консервативной терапии. Первичное оперативное вмешательство им было выполнено в среднем на 10–14 сутки от момента заболевания. Распределение больных в зависимости от сроков операции и тяжести ПН представлено в таблице 2. Показанием к оперативному вмешательству было формирование гнойно-некротических осложнений деструктивного панкреатита.
Средние сроки выполнения первичной операции
ПН средней степени
В момент госпитализации в ККГСЦ инфицированные формы ПН были выявлены у 88,5 % (n=23) пациентов, по шкале SAPSII общее состояние больных средней и тяжелой степени соответствовало 2–3 и 4–6 баллам, соответственно. В дальнейшем отмечалось прогрессирование степени тяжести состояния больных, максимальные значения зафиксированы на 7–10 сутки госпитализации, затем у выживших больных наблюдалась тенденция к стойкому снижению этого показателя (табл. 3).
Распределение больных ПН по SAPSII в динамике
ПН средней степени
Исходно у всех больных были выявлены признаки ПОН. В зависимости от выраженности синдрома ПОН (по шкале SOFA), больные были распределены следующим образом (табл. 4). У больных с ПН средней степени тяжести значения шкалы SOFA варьировали в пределах 6–8 баллов, с тяжелым ПН – 10–12 баллов.
Распределение больных ПН по SOFA в динамике
ПН средней степени
При поступлении все пациенты были госпитализированы в ОРИТ Красноярского краевого гнойно-септического центра. Продолжительность пребывания, в котором зависела от сроков купирования клиники синдрома полиорганной недостаточности и сепсиса. Для больных с тяжелым панкреонекрозом этот показатель составил, в среднем, 20±17,3 суток, для больных с ПН средней степени тяжести - 8±3,2 суток. Продолжительность искусственной вентиляции легких составила, в среднем, 8±11,8 суток и 1,7±1,1 суток, соответственно.
Контроль за эффективностью проводимого лечения осуществляли с помощью лабораторных и инструментальных исследований в динамике. При поступлении у всех больных был выраженный лейкоцитоз, ферментемия с многократным превышением нормальных значений, повышение азотемических показателей и билирубина крови (табл. 5).
Данные лабораторных исследований
Лейкоциты (10 9 /л)
Всем больным при поступлении выполнялось УЗИ, которое носило характер скринингового исследования.
Для оценки адекватности хирургического вмешательства, функции дренажей и их положения, а также своевременного выявления не дренированных гнойных очагов, выполняли динамическое УЗИ и МСКТа.
Повторные хирургические вмешательства в ККБ были выполнены у 15 (57,7 %) больных с тяжелым ПН. Из них четырем больным (15,3%) – по программе, вследствие продолжающегося гнойного перитонита. Остальным 11 больным (42,4 %) повторные вмешательства выполнялись по требованию. Из них у 34,6 % (n=9) больных показанием к повторной операции было прогрессирование гнойно-деструктивного процесса забрюшинной клетчатки, наличие крупных секвестров. У одного больного с тотальным поражением забрюшинной клетчатки произошел некроз поперечно-ободочной кишки, еще у одного больного послеоперационный период осложнился аррозивным кровотечением сальниковой сумки.
Среднее количество операций на 1 больного у пациентов с ПН средней степени тяжести составило – 1,4, с тяжелым ПН – 2,6.
Анализ осложнений и летальности выявил следующие закономерности. Наиболее частым осложнением у пациентов с тяжелым ПН была флегмона забрюшинного пространства -61,5 % (n=16). Поражение забрюшинной клетчатки по левостороннему типу выявлено у 36,3 % (n=4), по правостороннему типу – у 9 % (n=1), по центральному – у 23 % (n=6), тотальное поражение забрюшинной клетчатки наблюдалось у 45,4 % (n=5) больных. Следует отметить, что в группе пациентов с летальным исходом у 62,5 % определялось центральное поражение забрюшинной клетчатки.
Системные осложнения выявлены у 72,1 % больных с тяжелым ПН. Распространенный гнойный перитонит осложнил течение тяжелого ПН у 23 % (n=6) больных.
У 84,2 % (n=16) больных выявлен сепсис, из них – тяжелый сепсис у 9 и септический шок у 7 пациентов. СПОН отмечен в 7 случаях с преобладанием дыхательной, сердечно-сосудистой и почечной недостаточности. У 22,2 % (n=2) больных с тяжелым сепсисом в программу комплексной консервативной терапии был включен метод экстракорпоральной детоксикации, что способствовало благоприятному течению заболевания.
Экссудативный плеврит диагностирован у 26,3 % (n=5) пациентов с тяжелым ПН, из них левосторонний в 60 % случаев, у остальных – двусторонний.
У 15,8 % (n=3) пациентов с ПН средней степени тяжести течение осложнилось одиночными панкреатогенными абсцессами сальниковой сумки. Этим больным проводилась чрескожная пункция жидкостного образования под УЗИ контролем с последующим дренированием и санацией растворами антисептиков полости абсцесса. Полное купирование гнойного очага производилось в среднем на 12±3,5 сутки. У одного больного при динамическом УЗИ контроле была выявлена дислокация дренажа, что потребовало повторного дренирования полости абсцесса сальниковой сумки.
Летальность в группе в целом составила 30,8 % (n=8), среди больных с ПН средней тяжести летальных исходов не выявлено. При анализе летальности выявлены следующие закономерности: у всех умерших больных объем поражения ПЖ носил тотальный характер, основными осложнениями течения ПН явились забрюшинная флегмона по центральному типу и тотальное поражение забрюшинной клетчатки, что в 25 % случаев приводило к формированию флегмоны мягких тканей грудной и брюшной стенки, с последующим развитием сепсиса; у 50 % больных способствовало некротическому мезоколиту, некрозу восходящей и поперечной ободочной кишки, еще у двух больных – стрессовой перфорации тонкой кишки. Несмотря на раннее выявление этих жизнеугрожающих осложнений, своевременную активную хирургическую тактику в комплексе с интенсивной консервативной терапией, летальный исход течения ПН у данной категории больных был обусловлен развитием сепсиса, септического шока.
Заключение
Течение деструктивного панкреатита в большинстве случаев осложняется формированием СПОН, сепсисом. Неоправданно раннее хирургическое вмешательство, недостаточный объём операций при панкреонекрозах, а также несвоевременность выполнения необходимого объёма лечения на ранних этапах формирования деструктивного панкреатита, способствует увеличению доли гнойно-септических осложнений и, как следствие, повышению риска летального исхода.
Несмотря на проведение комплексной интенсивной терапии в условиях специализированного учреждения КГСЦ, в группе пациентов с тяжелым ПН наблюдалась стойкая тенденция прогрессирования полиорганной недостаточности, тогда как в группе средней степени тяжести ПН наблюдалась положительная динамика в виде купирования явлений полиорганной недостаточности. Оценку эффективности комплексного лечения или ее отсутствия для максимальной объективности целесообразно проводить по современным шкалам оценки тяжести состояния.
Малоинвазивное лечение панкреонекроза включает в себя чрескожную пункцию отграниченных жидкостных образований ПЖ под УЗИ контролем с последующим дренированием и санацией, а при формировании флегмон забрюшинного пространства необходимо выполнение операции в объёме: лапаротомия, некрсеквестрэктомия, вскрытие, дренирование флегмоны забрюшинного пространства по традиционной методике.
Наиболее частым осложнением у пациентов с тяжелым ПН является формирование тотальной флегмоны забрюшинного пространства. Риск летального исхода существенно повышается при центральном расположении забрюшинной флегмоны.
Забрюшинный абсцесс – это обособленная полость в ретроперитонеальном пространстве, заполненная гнойным экссудатом. Проявления зависят от локализации и распространённости патологического процесса. Общими признаками являются недомогание, тошнота, лихорадка. Возникают боли на стороне гнойного поражения с иррадиацией в позвоночник, лопатку, тазобедренный сустав. Диагностика основывается на данных осмотра, рентгенографии органов брюшной полости, УЗИ и КТ забрюшинного пространства. Лечение комбинированное: чрескожное или оперативное дренирование абсцесса, антибиотикотерапия.
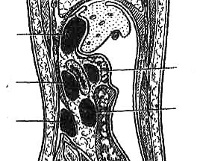
Общие сведения
Забрюшинный (ретроперитонеальный) абсцесс – ограниченное скопление гноя, расположенное между задним листком брюшины и внутрибрюшинной фасцией. Гнойники могут быть одиночными, при этом достигать значительных объемов, или множественными. Диагностика последних вызывает трудности в связи с малыми размерами образований и стёртой клинической картиной. Абсцессы могут образовываться вследствие травм, операций, перфорации полого органа, метастазирования инфекции из соседних структур. После плановых полостных операций гнойники возникают в 0,8% случаев, после экстренных - в 1,5%. Заболевание встречается преимущественно у лиц 20-40 лет.

Причины
Патогенная флора, участвующая в формировании гнойного процесса, представлена анаэробными и аэробными бактериями (стафилококк, стрептококк, кишечная палочка, клостридии и др.). Факторы, способствующие образованию гнойника, можно разделить на 2 группы:
- Первичные. Открытые ранения брюшной полости с загрязнением и недостаточной хирургической обработкой раны приводят к формированию ограниченной пиогенной полости. Закрытые травмы, сопровождающиеся повреждением забрюшинной части кишечника, могут способствовать развитию гнойного процесса и образованию абсцесса.
- Вторичные. Возникают вследствие гематогенного или лимфогенного (в 70% случаев) распространения инфекции из близлежащих органов. Ретроперитонеальный гнойник может возникать вследствие гнойного панкреатита, паранефрита, лимфаденита, абсцессов почек. Образование пиогенной полости может являться осложнением операций на органах забрюшинного пространства (мочеточнике, 12-перстной кишке, толстом кишечнике и др.). В этом случае инфекция развивается при недостаточной санации гнойного очага, нарушении правил асептики и антисептики, нерациональной АБ-терапии и неправильном уходе в послеоперационном периоде.
Классификация
В зависимости от местоположения гнойного процесса в ретроперитонеальном пространстве в абдоминальной хирургии выделяют:
1. Абсцессы переднего забрюшинного пространства. Расположены между париетальной брюшиной и предпочечной фасцией. К ним относятся:
- Панкреатические абсцессы. Образуются в результате деструктивного панкреатита, панкреонекроза.
- Околокишечные абсцессы. Формируются при перфорации 12-перстной кишки, восходящей и нисходящей части ободочной кишки в результате язвы, ранения или опухоли. Гнойник образуется при ретроперитонеальном расположении червеобразного отростка и затеке гноя в околоободочную клетчатку (параколон) при перитоните.
2. Абсцессы заднего забрюшинного пространства. Находятся между передней почечной фасцией и поперечной фасцией, выстилающей заднюю часть брюшной полости. Включают:
- Абсцессы околопочечного пространства. Располагаются с обеих сторон между передним и задним листками почечной фасции. Образуются при травмах паранефрона (околопочечной клетчатки), прорыве гнойников почек (пионефроз), при деструктивном ретроцекально расположенном аппендиците.
- Поддиафрагмальные абсцессы. Формируются непосредственно в клетчатке под диафрагмой. Отрицательное давление под куполом диафрагмы создает присасывающий эффект и способствует скоплению гнойного содержимого под диафрагмой при прободении аппендицита, разлитом перитоните, открытом и закрытом ранении брюшной полости.
Отдельно можно выделить псоас-абсцесс, образующийся при ограниченном гнойном воспалении поясничной мышцы. Формирование пиогенной полости происходит вследствие гематогенной передачи инфекции при остеомиелите позвоночника. Гнойники могут достигать больших размеров и вызывать расплавление мышцы.
Симптомы забрюшинного абсцесса
Клиническая картина заболевания зависит от размеров и локализации гнойника, длительности воспаления и этиологии патологического процесса. В начале болезни, при небольших размерах абсцесса, симптоматика может отсутствовать. По мере увеличения пиогенного образования нарастают симптомы интоксикации: озноб, лихорадка, недомогание, тошнота. Характер болей обусловлен локализацией воспалительного процесса и носит в основном разлитой характер. Болезненные ощущения чаще возникают в боку на стороне поражения. Боли могут иррадиировать в лопатку, грудной отдел позвоночника, ягодичную и ректальную область, тазобедренный сустав.
Неприятные ощущения возникают сначала во время движения (при ходьбе, попытках сесть, встать, перевернуться на бок), а затем и в покое. При забрюшинных абсцессах переднего отдела иногда пальпируется округлое образование живота. При околопочечных гнойниках боли отдают в спину, позвоночник и усиливаются при попытке согнуть ногу в тазобедренном суставе. Возникает нарушение мочеиспускания (дизурия). Затяжной характер болезни приводит к атрофии мышц поясничной и ягодичной областей. У пациентов возникает сколиоз, контрактура и внутренняя ротация бедра на стороне гнойника.
Осложнения
Длительное течение забрюшинного абсцесса может привести к прорыву гнойника в плевральную и брюшную полость. Это способствует развитию эмпиемы плевры и диффузного гнойного перитонита. Генерализация гнойного процесса с возникновением сепсиса представляет угрозу для жизни пациента. Летальность при ретроперитонеальных абсцессах варьирует от 10 до 30 %.
Диагностика
Диагностика забрюшинного абсцесса осуществляется абдоминальным хирургом, вызывает значительные трудности из-за отсутствия четко очерченной локализации боли и специфических признаков болезни. При предположении о наличие ограниченного гнойного образования ретроперитонеальной области проводят следующие обследования:
- Осмотр хирурга. Специалист проведет тщательный физикальный осмотр, сбор анамнеза жизни. Большое значение имеет наличие сопутствующей соматической патологии и оперативных вмешательств в прошлом. При подозрении на гнойный процесс в забрюшинной полости врач назначает дополнительное обследование.
- УЗИ брюшной полости и забрюшинного пространства. Выявляет воспалительные процессы в поджелудочной железе, почках, ретроперитонеальной клетчатке, жидкость в брюшной полости. При большом размере абсцесса удается визуализировать его как округлую гипоэхогенную тень.
- Обзорная рентгенография брюшной полости. Позволяет обнаружить округлое образование с уровнем жидкости.
- КТ забрюшинного пространства. Является наиболее современным и эффективным методом исследования. Позволяет определить местоположение, размеры абсцесса и выявить причину его образования.
- Лабораторные исследования. В ОАК определяются признаки бактериальной инфекции (лейкоцитоз, повышение СОЭ, сдвиг лейкоцитарной формулы влево). При поражении поджелудочной железы увеличивается уровень ферментов (амилаза, липаза) в биохимическом анализе крови. При заболеваниях мочевыделительной системы отмечается лейкоцитурия, пиурия. Для выявления возбудителя проводят анализ крови или мочи на стерильность.
Для дифференциальной диагностики имеет значение локализация забрюшинного абсцесса. Начальные этапы болезни схожи с течением инфекционных заболеваний различной этиологии (брюшной тиф, грипп, малярия). При гнойнике переднего ретроперитонеального пространства дифференциальную диагностику проводят с панкреонекрозом, острым панкреатитом, язвенной болезнью 12-перстной кишки. Околопочечные абсцессы следует отличать от параненефрита, острого пиелонефрита.
Лечение забрюшинного абсцесса
Тактика лечения зависит от размера и местоположения гнойника. При небольших одиночных абсцессах проводят чрескожное дренирование и введение в полость антибактериальных препаратов с помощью катетера. Манипуляцию выполняют под контролем УЗИ или КТ. При неполном опорожнении пиогенной полости возможен рецидив болезни. При множественных, крупных одиночных абсцессах показано хирургическое вмешательство. Операция заключается во вскрытии, дренировании гнойника, санации очага воспаления и ревизии забрюшинного пространства. Выбор доступа зависит от местоположения абсцесса.
Околопочечные абсцессы вскрывают заднелатеральным или заднемедиальным доступом. При показаниях к нефрэктомии удаление почки проводят вторым этапом (после купирования гнойного процесса). При поддиафрагмальных абсцессах используют внебрюшинный или чрезбрюшинный доступ, при околокишечных - переднелатеральный. Вскрытие псоас-абсцесса производят из внебрюшинного доступа (разрез над паховой связкой вдоль гребня подвздошной кости). При остеомиелите подвздошной кости выполняют удаление секвестров.
При забрюшинном абсцессе неуточненной локализации проводят вскрытие ретроперитонеального пространства косым поясничным разрезом по Пирогову, Израэлю, Шевкуненко. Во всех случаях до и после хирургического вмешательства назначают курс антибиотикотерапии с учетом возбудителя инфекции. После операции показана дезинтоксикационная, противовоспалительная и обезболивающая терапия.
Прогноз и профилактика
Прогноз болезни зависит от запущенности гнойного процесса, общего состояния пациента. При грамотной диагностике и комплексном лечении забрюшинного абсцесса прогноз благоприятный. При порыве гнойника могут возникнуть жизнеугрожающие состояния (сепсис, перитонит). Профилактика заболевания направлена на рациональное лечение и послеоперационное ведение пациентов с острой хирургической патологией. Важную роль играет своевременное обнаружение и дренирование гнойника. Пациентам рекомендовано при первых симптомах болезни обратиться к хирургу.
Забрюшинная флегмона – это разлитой гнойный процесс, локализованный в клетчатке ретроперитонеального пространства. Заболевание проявляется лихорадкой, недомоганием, тянущим умеренным или интенсивным болевым синдромом в пояснице и животе, усиливающимся при перемене положения тела. Для подтверждения диагноза проводят хирургический осмотр, УЗИ забрюшинного пространства, рентгенографию органов брюшной полости, анализ крови. Консервативное лечение предполагает назначение антибиотиков. Во время операции осуществляют вскрытие флегмоны и дренирование ретроперитонеального пространства.
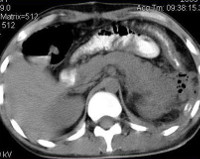
Общие сведения
Забрюшинная флегмона – острое гнойное поражение позадибрюшинной жировой клетчатки. Отличительной особенностью ретроперитонеальной флегмоны является отсутствие границ расплавления тканей и склонность к быстрому распространению воспалительного процесса на близлежащие структуры (фасции, мышцы, соседние органы). Рыхлое строение забрюшинной клетчатки способствует стремительному размножению гнилостной инфекции, более выраженной интоксикации, нежели при ограниченном нагноении (абсцессе). Заболевание преимущественно распространено среди людей молодого и среднего возраста (25-45 лет), в равной степени наблюдается у мужчин и женщин.

Причины
Флегмонозный процесс в забрюшинной клетчатке чаще имеет вторичный характер и возникает в условиях протекающей в организме инфекции (пиелонефрита, параколита и др.). Патогенная флора, способствующая развитию гнойного процесса, представлена преимущественно золотистым стафилококком, кишечной палочкой, зеленящим стрептококком и др. В абдоминальной хирургии выделяют две группы причин образования забрюшинной флегмоны:
- Первичные. Флегмона может возникать в результате нарушения принципов асептики и антисептики во время хирургических манипуляций на органах малого таза и брюшной полости или инфицирования ретроперитонеальной клетчатки при открытых ранениях живота.
- Вторичные. В этих случаях флегмона забрюшинной области развивается вследствие гематогенного, лимфогенного распространения инфекции из первичного очага воспаления при пионефрозе, гнойном панкреатите, флегмонозном аппендиците, остеомиелите костей таза и др. Патология может возникать при прорыве забрюшинного абсцесса и проникновении пиогенного содержимого в клетчатку, в результате нагноения забрюшинных гематом при закрытых травмах и ранениях крупных сосудов с переходом воспаления на ретроперитонеальную область.
Вероятность развития забрюшинной флегмоны возрастает при снижении резистентности организма (после перенесенных вирусных, бактериальных инфекций, химиотерапии, лучевой терапии), тяжелом течении хронических заболеваний (сердечной недостаточности, бронхиальной астмы, сахарного диабета и др.), авитаминозе, пожилом и старческом возрасте пациентов.
Патогенез
Толчком к началу заболевания служит проникновение возбудителя в забрюшинную клетчатку на фоне ослабленного общего иммунитета, декомпенсации хронических заболеваний и т. д. Под воздействием токсинов, которые выделяются патогенными микроорганизмами, развивается серозный отек, воспалительная инфильтрация клетчатки с последующим образованием гнойного экссудата и расплавлением жировой ткани. Особенности строения ретроперитонеального пространства определяют быстрый переход воспаления на окружающие анатомические области. Распространение инфекции происходит через естественные промежутки в фасциях, которые способствуют проникновению гнойного экссудата из одного пространства в другое.
Классификация
Выделяют острое и хроническое течение забрюшинной флегмоны. Острая флегмона развивается внезапно и сопровождается интенсивной болью и интоксикацией. Хроническое течение возникает на фоне сниженной вирулентности патогенной флоры и быстрой активации защитных сил организма и проявляется слабовыраженной симптоматикой с периодами обострения и ремиссии. По характеру экссудата абдоминальные хирурги различают серозную, гнойную, некротическую и гнилостную формы заболевания. Исходя из локализации пиогенного процесса в ретроперитонеальном пространстве, выделяют следующие виды флегмоны:
- Поясничная. Наиболее распространённый вариант заболевания. При данной локализации флегмона, расположенная над гребнем подвздошной кости, распространяется по наружному краю поясничной мышцы до края длинных мышц спины.
- Подвздошная. Инфильтрат локализуется в среднем и верхнем отделах подвздошной ямки, начинаясь вблизи тела лобковой кости, проходит вдоль наружного края поясничной мышцы и достигает передней верхней ости подвздошной кости. Верхний край флегмоны обычно хорошо определяется при пальпации живота.
- Паховая. Данный тип забрюшинной флегмоны встречается редко. Инфильтрат расположен в позадибрюшинной клетчатке в проекции наружной подвздошной артерии и вены.
Симптомы забрюшинной флегмоны
Клинические проявления на начальной стадии не имеют специфических черт. Появляются общие признаки воспалительного процесса: повышение температуры тела до фебрильных значений, слабость, повышенная утомляемость, озноб, тошнота, головокружение. По мере прогрессирования патологии возникает боль. Болезненные ощущения вначале носят периодический тянущий, пульсирующий характер и локализуются в зависимости от расположения флегмоны в поясничной области, левой и правой половинах живота.
Боли постепенно нарастают, становятся постоянными, интенсивными и не имеют четкой локализации. Болевой синдром усиливается при попытке встать, сесть, повернуться на бок, значительно ухудшая уровень жизни пациента и мешая ему нормально передвигаться. При пальпации спины и живота отмечается резкая болезненность в поясничной области. При поясничном расположении инфильтрата можно заметить сглаженность контуров на пораженной половине поясницы, при глубокой пальпации живота определяется утолщение клетчатки в зоне воспаления.
Осложнения
Распространение гнойного процесса на окружающие ткани может стать причиной гнойного перитонита, пиелонефрита, эмпиемы плевры. Попадание инфекции в кровоток приводит к развитию тромбофлебита, лимфаденита, артериита. Поражение артерии может осложняться ее расплавлением и артериальным кровотечением. Генерализация инфекционного процесса приводит к возникновению сепсиса, выраженной интоксикации вплоть до септикопиемии, инфекционно-токсического шока и летального исхода.
Диагностика
Диагностика патологии часто вызывает трудности в связи с отсутствием патогномоничных симптомов и четкой клинической картины. В некоторых случаях заболевание удается обнаружить только на поздних стадиях, при развитии осложнений. Для установления диагноза проводятся следующие виды исследований:
- Осмотр хирурга. При сборе анамнеза специалист обращает внимание на травмы, операции и инфекционные заболевания в прошлом. Во время физикального осмотра отмечается напряжение мышц живота и спины на стороне поражения, наличие инфильтратов различной локализации, болезненных при пальпации.
- УЗИ брюшной полости и забрюшинного пространства. Позволяет визуализировать патологический инфильтрат в забрюшинной области. При наличии первичного очага инфекции (в почках, поджелудочной железе, кишечнике) удается выявить изменения в органах и жидкость в брюшной полости.
- Обзорная рентгенография брюшной полости. На рентгенограммах отмечается исчезновение контуров поясничной мышцы в области поражения. В зоне флегмоны в пределах ограниченного участка кишки определяется выраженный метеоризм, который не исчезает после использования клизм.
- Анализ крови. Лабораторное исследование крови выявляет наличие общего инфекционного процесса в организме, при котором повышается уровень лейкоцитов, ускоряется СОЭ, наблюдается сдвиг лейкоцитарной формулы влево. Анализ крови на стерильность выполняют для верификации возбудителя инфекции и назначения грамотной антибиотикотерапии.
В сомнительных и трудных случаях назначают КТ забрюшинного пространства. Данное исследование с большей точностью помогает определить этиологию болезни, местоположение флегмоны и изменения со стороны соседних органов. Дифференциальную диагностику забрюшинной флегмоны проводят с гриппозной инфекцией, тифом, паратифом, пиелонефритом, остеомиелитом костей таза. На начальных этапах симптомы болезни часто ошибочно принимают за проявления дегенеративных заболеваний позвоночника (остеохондроза поясничного отдела позвоночника, протрузии позвоночных дисков).
Лечение забрюшинной флегмоны
Тактика лечения зависит от локализации и величины флегмоны, а также наличия осложнений. Все пациенты с данным заболеванием подлежат госпитализации в хирургическое отделение. В настоящее время существует два основных подхода к лечению патологии:
- Консервативный. Применяется на начальных этапах болезни, при малых размерах флегмоны и отсутствии осложнений со стороны других органов и систем. Этиотропная терапия представлена антибактериальными препаратами широкого спектра действия. Наряду с основным лечением назначают дезинтоксикационную терапию, противовоспалительные и обезболивающие средства, витамины и иммуномодуляторы.
- Хирургический. При отсутствии эффекта от консервативной терапии, больших флегмонах и выраженной интоксикации применяют оперативное лечение. Выполняют вскрытие нагноения и санацию забрюшинного пространства, после чего устанавливают дренажную систему с целью активной аспирации гнойного экссудата из ретроперитонеальной области. При поясничной локализации применяют доступ Симона, при паранефритах – задний латеральный или медиальный доступы. При отсутствии данных о точном расположении флегмоны выполняют косые поясничные разрезы по Израэлю, Пирогову, Шевкуненко. До и после операции назначают антибактериальную и противовоспалительную терапию.
Прогноз и профилактика
Прогноз зависит от расположения, размеров флегмоны и выраженности интоксикационного синдрома. При своевременном обнаружении заболевания и адекватной антибиотикотерапии течение благоприятное. Поздняя диагностика, развитие перитонита, инфицирование других органов может повлечь за собой серьезные последствия (шок, сепсис и др.) вплоть до смертельного исхода. Основу профилактики заболевания составляет строгое соблюдение медицинским персоналом правил асептики во время инвазивных вмешательств, рациональное назначение антибиотиков и грамотное послеоперационное наблюдение за больными с хирургической патологией. Важную роль играет раннее распознавание и лечение хронических заболеваний брюшной полости и ретроперитонеального пространства (пиелонефрит, колит и др.).
Панкреонекроз – деструктивное заболевание поджелудочной железы, являющееся осложнением острого панкреатита и приводящее к развитию полиорганной недостаточности. К проявлениям панкреонекроза относят острую опоясывающую боль в животе, упорную рвоту, тахикардию и энцефалопатию. Лабораторная диагностика предполагает определение уровня альфа-амилазы; инструментальная – проведение обзорной рентгенографии брюшной полости, УЗИ, КТ и МРТ поджелудочной железы, РХПГ, диагностической лапароскопии. Лечение включает в себя консервативные мероприятия (угнетение протеолитических ферментов, восстановление оттока соков поджелудочной железы, дезинтоксикацию и обезболивание) и оперативное вмешательство.
МКБ-10

Общие сведения
Панкреонекроз является наиболее тяжелым осложнением панкреатита, поражает в основном молодых трудоспособных людей, составляет 1% всех случаев острого живота. В основе патогенеза панкреонекроза лежит сбой механизмов внутренней защиты поджелудочной железы от разрушающего действия панкреатических ферментов.
В последнее время в России увеличивается количество острых панкреатитов – данная патология выходит на второе место после острого аппендицита в хирургических стационарах. Также растет и число деструктивных форм панкреатита, в частности панкреонекроза - до 20-25%. В разных клиниках летальность при деструкции поджелудочной железы достигает 30-80%. Ведущий способ снижения летальности при некрозе поджелудочной железы – своевременная диагностика, госпитализация и раннее начало патогенетического лечения.
Причины панкреонекроза
Причинами развития, как панкреатита, так и панкреонекроза, обычно являются нарушения диеты и эпизодический прием алкоголя. Исследования в области гастроэнтерологии показали, что панкреонекрозами обычно страдают люди, не склонные к постоянному употреблению алкоголя. Тем не менее, в подавляющем большинстве случаев началу панкреонекроза предшествует эпизод употребления спиртного в больших количествах. У пациентов, страдающих хроническим алкоголизмом, практически всегда развивается хронический панкреатит, редко осложняющийся панкреонекрозом. Первые признаки заболевания могут появиться спустя часы или сутки после действия провоцирующих факторов.
Патогенез
В основе патогенеза панкреонекроза лежит нарушение местных защитных механизмов поджелудочной железы. Обильный прием пищи и алкоголя приводит к значительному усилению внешней секреции, перерастяжению протоков поджелудочной железы, нарушению оттока панкреатических соков. Повышение внутрипротокового давления провоцирует отек паренхимы, разрушение ацинусов поджелудочной железы, преждевременную активацию протеолитических ферментов, которые и приводят к массивному некрозу ткани железы (самоперевариванию).
Активация липазы вызывает некроз жировых клеток, эластазы – разрушение сосудистой стенки. Активированные ферменты и продукты распада тканей, благодаря воздействию эластазы, попадают в кровоток, оказывая токсическое действие на все органы и ткани. В первую очередь страдают печень, почки, сердце, головной мозг.
Классификация
В зависимости от того, какие повреждающие механизмы лидируют в патогенезе, выделяют жировую, геморрагическую и смешанную формы панкреонекроза.
- Жировая форма. Если преобладает повышение активности липазы, происходит разрушение жировой ткани поджелудочной железы. Липаза попадает за пределы панкреатической капсулы, вызывая появление очагов некроза в большом и малом сальнике, листках брюшины, брыжейке, внутренних органах. Жировая форма панкреонекроза обычно оканчивается развитием тяжелейшего химического асептического перитонита, полиорганной недостаточности.
- Геморрагическая форма. В случае же преобладания микроциркуляторных нарушений развивается спазм сосудов поджелудочной железы, приводящий к быстрому нарастанию отека паренхимы. В течение нескольких часов или дней токсемия постепенно приводит к парезу сосудистой стенки, расширению сосудов и замедлению кровотока в тканях железы. Все это способствует повышенному тромбообразованию, а в дальнейшем – развитию ишемического некроза. Активация эластазы вызывает разрушение сосудистой стенки сначала в толще поджелудочной железы, затем и в других органах. В конечном итоге это ведет к геморрагическому пропитыванию панкреас, кровоизлияниям во внутренние органы и забрюшинную клетчатку. Признаком геморрагического панкреонекроза является выпот в брюшную полость с примесью крови.
- Смешанная форма. Если активность эластазы и липазы находятся примерно на одном уровне, развивается смешанная форма панкреонекроза. В этом случае явления жирового некроза и геморрагической имбибиции выражены одинаковы. При панкреонекрозе также значительно повышается уровень альфа-амилазы, однако в патогенезе этот факт не играет никакой роли. Измерение уровня амилазы имеет только клиническое значение.
Симптомы панкреонекроза
Развитие клиники панкреонекроза происходит в три этапа. Этому состоянию может предшествовать гнойный панкреатит, острый алкогольный панкреатит, билиарный панкреатит, геморрагический панкреатит. На первом этапе активное размножение бактерий в поджелудочной железе вызывает выраженную токсинемию и усиление панкреатической ферментативной активности. Пациента беспокоят лихорадка, рвота, неустойчивость стула. На втором этапе заболевания происходит гнойное и ферментативное расплавление тканей железы с формированием одной или нескольких каверн. На последней стадии воспалительный процесс распространяется на окружающие ткани, приводя к полиорганной недостаточности и смерти больного.
Заболевание имеет острое начало, обычно пациенты четко связывают появление первых симптомов с погрешностями в диете и приемом алкоголя. Около 70% больных поступают в стационар в состоянии сильного алкогольного опьянения, что говорит об очень быстром развитии патологических изменений в поджелудочной железе.
Первым симптомом обычно выступает острая опоясывающая боль, иррадиирующая в левую половину живота и поясницы, левое плечо. Безболевых форм панкреонекроза не бывает. Между выраженностью болевого синдрома и тяжестью некроза поджелудочной железы существует прямая зависимость. Распространение деструктивных изменений на нервные окончания приводит к постепенному уменьшению болевого синдрома, в сочетании с сохраняющейся интоксикацией это является плохим прогностическим признаком.
Через некоторое время после появления боли развивается неукротимая рвота, не связанная с приемом пищи и не приносящая облегчения. В рвотных массах содержится желчь, сгустки крови. Из-за рвоты развивается дегидратация, проявляющаяся сухостью кожи и слизистых, язык обложен, постепенно снижается темп диуреза. Развивается метеоризм кишечника, перистальтика ослаблена, отмечается задержка газов и стула. Интоксикация и дегидратация сопровождаются лихорадкой.
Токсемия, колебания уровня глюкозы в крови, гиперферментемия приводят к поражению головного мозга и развитию энцефалопатии, которая выражается спутанностью сознания, возбуждением, дезориентацией, вплоть до развития комы (примерно у трети пациентов).
Прогрессирование воспалительного процесса приводит к значительному увеличению поджелудочной железы в размерах, формированию инфильтрата в брюшной полости. Уже к пятым суткам от начала заболевания инфильтрат можно не только пропальпировать, но и увидеть невооруженным глазом. В проекции поджелудочной железы появляется гиперестезия кожи.
Осложнения
Указанные патологические сдвиги в организме приводят к формированию полиорганной недостаточности на фоне тяжелого токсического гепатита, нефрита, кардита, дыхательных нарушений. Панкреонекроз может осложняться шоком, перитонитом, абсцессом брюшной полости, желудочно-кишечными кровотечениями.
Из местных осложнений часто встречаются абсцесс, киста или ложная киста поджелудочной железы, ферментная недостаточность, фиброз поджелудочной железы, флегмона забрюшинной клетчатки, язвы ЖКТ, тромбоз воротной и мезентериальных вен.
Диагностика
Осмотр пациента должен осуществляться совместно гастроэнтерологом, хирургом, реаниматологом. Наличие панкреонекроза предполагает крайнюю тяжесть состояния пациента, поэтому во всех случаях рекомендуется госпитализация в отделение интенсивной терапии. В отделении производится постоянное определение ферментов поджелудочной железы в крови и моче. Плохим прогностическим признаком является прогрессирующий рост уровня амилазы либо резкий скачок данного показателя.
При физикальном осмотре отмечается вздутие живота, на боковых поверхностях передней брюшной стенки и пояснице появляются синюшные пятна (проявление внутренних гематом, кровоизлияний в мягкие ткани). Кожные покровы землисто-бледные или желтушные, мраморные, холодные. Тахикардия, артериальная гипотония, учащенное поверхностное дыхание являются признаком тяжелой интоксикации. Диагноз подтверждается с помощью:
- Рентгенодиагностики. Обзорная рентгенография органов брюшной полости позволяет выявить косвенные признаки воспалительного процесса. Введение контрастного вещества может дать возможность визуализировать фистулы поджелудочной железы. Исследовать состояние выводящих протоков поджелудочной железы, выявить причину застоя панкреатического сока позволяет ретроградная холангиопанкреатография.
- УЗИ-диагностики.Ультрасонография поджелудочной железы и желчных путей указывает на наличие камней в желчевыводящих протоках, увеличение и изменение структуры железы, анэхогенные очаги некроза в полости живота.
- Томографической диагностики. Более детально визуализировать патологические изменения можно с помощью МРТ поджелудочной железы, МРПХГ, компьютерной томографии.
- Диагностической операции. В сложных случаях проводится диагностическая лапароскопия – наиболее точный способ визуализации и постановки диагноза, оценки состояния поджелудочной железы и окружающих тканей и органов.
Дифференциальный диагноз проводят с кишечной непроходимостью, острыми воспалительными заболеваниями аппендикса, желчного пузыря, желчной коликой, перфорацией полого органа, тромбозом мезентериальных сосудов, инфарктом миокарда, разрывом аневризмы брюшной аорты.

КТ ОБП. Панкреонекроз. Диффузный отек и нарушение структуры поджелудочной железы, отсутствие накопления контраста в ее паренхиме.
Лечение панкреонекроза
Консервативная терапия
Лечение панкреонекроза начинают с обеспечения полного покоя воспаленной поджелудочной железе. Исключаются физические нагрузки, энтеральное питание, может назначаться промывание желудка прохладными растворами. Основными направлениями лечения являются обезболивание, обезвреживание протеолитических ферментов, дезинтоксикационная терапия.
- Аналгезия. Адекватное обезболивание включает в себя введение анальгетиков (при необходимости - наркотических), спазмолитиков, рассечение капсулы поджелудочной железы, новокаиновые блокады. Уменьшение отека железы под влиянием диуретиков приводит к угасанию болевого синдрома (так как ведет к ослаблению натяжения панкреатической капсулы).
- Инфузионная терапия. Дезинтоксикация проводится большим количеством инфузионных растворов под контролем диуреза. В инфузионный раствор добавляют апротинин. Обязательно назначаются антигистаминные препараты.
- Антибиотикотерапия. С целью профилактики гнойных осложнений проводится антибактериальная терапия антибиотиками широкого спектра действия. Симптоматическое лечение включает в себя противошоковые мероприятия, восстановление функции других органов и систем.
Хирургическое лечение
Практически во всех случаях развития панкреонекроза требуется проведение хирургического лечения для восстановления оттока панкреатических соков, удаления некротических масс (некрэктомия поджелудочной железы). В первые пять суток от начала патологического процесса проводить оперативное вмешательство не рекомендуется, так как в эти сроки еще невозможно оценить уровень некроза, зато повышается риск вторичного инфицирования и послеоперационных осложнений.
На этапе гнойного воспаления в брюшной полости могут использоваться разнообразные методики (пункционные, лапароскопические, лапаротомные) восстановления оттока из протоков поджелудочной железы; устранения некротических масс, воспалительного и геморрагического экссудата; остановки внутрибрюшного кровотечения. Для улучшения состояния внутренних органов может потребоваться дренирование брюшной полости.
Прогноз и профилактика
Составление прогноза для пациентов с панкреонекрозом является очень сложной задачей, так как зависит от многих обстоятельств. Значительно ухудшается прогноз при наличии одного или нескольких из следующих факторов: возраст более пятидесяти пяти лет, лейкоцитоз более 16х10 9 /л, гипергликемия, гипокальциемия, метаболический ацидоз, артериальная гипотензия, повышение уровня мочевины, ЛДГ и АСТ, значительные потери жидкости из кровеносного русла в ткани. Наличие семи из указанных критериев обеспечивает 100% летальность пациента. Профилактика панкреонекроза заключается в своевременном обращении за медицинской помощью, раннем начале лечения, в том числе и хирургического.
Острый панкреатит имеет различные степени тяжести – от клинически самоограничивающегося до быстрого смертельного течения. Как самостоятельное заболевание, он является полиэтиологическим, но монопатогенетическим. Панкреонекроз – самое тяжелое состояние, развивающееся как следствие острого панкреатита. Для него характерен неблагоприятный прогноз: смертность составляет приблизительно от 15 и до 30-39% в случае инфицирования некроза, который является основной причиной смерти. Некротическая форма острого панкреатита характеризуется тяжелым и продолжительным течением. Распространенные некрозы поджелудочной железы могут быть геморрагическими, жировыми или смешанными. Клинические наблюдения и секционные находки показывают, что в первые часы и дни (3-5 дней) заболевания граница между некротизированными и жизнеспособными тканями в поджелудочной железе является нечеткой, а связь между ними достаточно прочной. Хирургическое вмешательство обычно требуется при инфицированном панкреонекрозе, реже при стерильном. Его цель заключается в удалении некротических очагов не только из поджелудочной железы, но и из забрюшинной клетчатки. Наиболее распространенным подходом при инфицированном панкреонекрозе является открытая хирургическая некрэктомия, но она отягощена высокими показателями заболеваемости (34-45%) и смертности (11-39%). Попытка удалить омертвевшие участки поджелудочной железы и забрюшинной клетчатки сопровождаются кровотечением, поэтому более безопасно осуществлять некрэктомию не ранее, чем через 10 дней, так как в это время граница между мертвыми и живыми тканями становится четкой. Сосуды некротизированных тканей оказываются тромбированными и некрэктомию можно выполнить почти бескровно. Объем определяется степенью патологических изменений и тяжестью состояния больного. За последние два десятилетия лет лечение панкреонекроза значительно эволюционировало от открытой хирургии к малоинвазивным методам. Следует отметить, что раннее интенсивное консервативное лечение, иногда в сочетании с вышеописанными оперативными вмешательствами является эффективным методом для ведения больных с острым панкреатитом.

1. A.C. de Beaux, K.R. Palmer, D.C. Carter Factors influencing morbidity and mortality in acute pancreatitis; an analysis of 279 cases // Gut . 1995 Jul. №37. pp. 121-126.
2. Banks, P. A., Bollen, T. L., Dervenis, C., Gooszen, H. G., Johnson, C. D., Sarr, M. G.,Vege, S. S. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by international consensus // Gut. 2012. №62. С. 102-111. doi:10.1136/gutjnl-2012-302779
3. Bugiantella, W., Rondelli, F., Boni, M., Stella, P., Polistena, A., Sanguinetti, A., & Avenia, N Necrotizing pancreatitis: A review of the interventions // International Journal of Surgery. 2016. №28. pp. 163-171. doi:10.1016/j.ijsu.2015.12.038
5. Ismail O. Z., & Bhayana V. Organ failure and infection of pancreatic necrosis as determinants of mortality in patients with acute pancreatitis // Clinical Biochemistry. 2017. №50 (18). pp. 1275-1280. doi:10.1016/j.clinbiochem.2017.07.003
6. Ситкин С.И., Силаев В.Н., Бозова Е.Ю., Токарева С.И. Современные подходы к лечению острого панкреатита (обзор международных рекомендаций) // Тверской медицинский журнал. 2015. №2. С. 14-24.
7. Э.Э. Топузов, В.К. Балашов, Б.Г. Цатинян, Э.А. Аршба, А.В. Петряшев, М.А. Бобраков Хирургическое лечение острого панкреатита: возможности чрескожного дренирования // Хирургия. 2017. №8
Актуальность: Острый панкреатит (ОП) среди острых хирургических заболеваний является причиной 5-10% госпитализаций в хирургические стационары [7]. Общая смертность от ОП в мире составляет от 5-10% [6]. Примерно у 80% пациентов острый панкреатит является лёгким и самоограничивающимся, но у 20% он может иметь тяжелое течение с некрозом паренхимы поджелудочной железы и / или перипанкреатической ткани, ведущее к тяжелой заболеваемости и смертности до 27% [1,3]. Основной причиной смерти является инфицирование некротизированной ткани, которое связано с неблагоприятным прогнозом: смертность составляет приблизительно 15% у пациентов с панкреонекрозом и до 30-39% с инфицированием панкреонекроза (оно возникает примерно у трети пациентов) [4]. На сегодняшний день так и не удалось снизить летальность от гнойно ‑ септических осложнений, уменьшить длительность стационарного лечения, что непосредственно связано с особенностями течения заболевания [7]. Лечение больных с панкреонекрозом – одна из актуальных проблем в хирургии. Раннее распознавание острого панкреатита и выбор адекватного метода лечения являются основными задачами успешного лечения. Это обусловлено частой встречаемостью данного заболевания, а также высокой летальностью от осложнений.
Панкреонекроз – деструктивное заболевание поджелудочной железы, являющееся осложнением острого панкреатита и приводящее к развитию полиорганной недостаточности.
Этиология. Острый панкреатит – это воспаление поджелудочной железы; иногда оно связано с системным воспалительным ответом, который может нарушать функцию всех органов или систем. Воспаление может стихать самопроизвольно или прогрессировать до некроза поджелудочной железы и / или окружающей жировой ткани.
К развитию острого панкреатита может привести любая причина, вызывающая гиперсекрецию панкреатического сока и затруднение его оттока с развитием гипертензии в панкреатических протоках; заброс в протоки цитотоксических и активирующих панкреатические ферменты веществ, прямое повреждение секретирующих панкреатоцитов. Этиологическую характеристику острого панкреатита определяют условия его развития. Основными условиями действия пусковых факторов являются [2]:
‑ заболевания внепеченочных желчевыводящих путей с нарушением желчетока;
‑ заболевания ДПК и большого дуоденального сосочка (БДС);
‑ избыточная пищевая нагрузка и медикаментозная стимуляция панкреатической гиперсекреции;
‑ прием алкоголя и его суррогатов резко усиливает секреторную активность поджелудочной железы, а длительное употребление крепких алкогольных напитков приводит к дуодениту с отеком БДС, создавая затруднение оттоку панкреатического секрета и желчи;
‑ острые и хронические нарушения кровообращения с расстройствами микроциркуляции в поджелудочной железе приводят к развитию ишемического острого панкреатита.
Патогенез. Первым по значимости фактором является собственное переваривание вследствие сочетанного влияния всех ферментов поджелудочной железы, причем в остром периоде каждый из них выступает самостоятельно [10]. В здоровом организме пищеварительные ферменты начинают свою работу после того, как вступят в контакт с желчью, которая поступает в полость кишечника из печени. В том случае, если они активизируются слишком рано, не в кишечнике, а в протоках поджелудочной железы, они начинают разрушать ее.
Существуют механизмы защиты, которые предотвращают при нормальных условиях самопереваривание поджелудочной железы:
‑ ферменты секретируются преимущественно в неактивном состоянии (трипсиноген, химотрипсин и др.);
‑ эпителий протока защищен выстилающим его поверхность мукополисахаридом (слой слизи);
‑ в крови находятся ингибиторы, которые инактивируют ферменты, если им удается оказаться вне системы протока;
‑ обмен веществ, присущий ацинарной клетке, предотвращает проникновение выделенных ферментов назад в клетку.
Если у человека имеется стеноз большого дуоденального сосочка, то в протоках поджелудочной железы повышается давление, что приводит к их растяжению, а это, в свою очередь, является причиной снижения количества слизи, защищающей поверхность протоков от ферментов. Также в данной ситуации имеет место поступление желчи в протоки поджелудочной железы в больших количествах. Перерастяжение сначала возникает на ограниченном участке крупных протоков, по мере повышения давления, процесс распространяется до самых мелких протоков. Поэтому повреждения железы возникают, прежде всего, в пределах регионарной протоковой системы, когда происходит разрыв мелких протоков с выходом протеолитических ферментов в интерстиций. Ингибиторы крови инактивируют ферменты и, вместе с тем, в крови повышается количество амилазы. Однако, повышение амилазы еще не означает наличие острого панкреатита, т.к. это возникает чаще, чем определяется клиническое тому соответствие.
Вторым по значимости фактором повреждения панкреатоцитов является расстройство кровообращения в поджелудочной железе. Недостаточное кровообращение железы снижает обмен веществ до критической границы, что может привести к отдельным местным некрозам [9]. Причинами могут быть:
‑ микротромбозы и др.
На возникшие некротические ткани воздействуют протеолитические ферменты. Продукты разложения всасываются в лимфатические сосуды и через них попадают в кровь. Они представляют большую опасность для паренхиматозных органов, в частности, для почек. В случае излечения, на периферии железы поврежденные ткани замещаются соединительной, а внутри железы, при определенных обстоятельствах, формируются ложные кисты [5].
В последние годы наблюдается увеличения частоты затяжного острого панкреатита, это объясняется двумя факторами:
- Ранним поступлением больных в стационар, улучшением диагностики и, как следствие, ранним проведением интенсивной противошоковой терапии;
- Частным поражением периферии поджелудочной железы, когда некроз располагается по наружной поверхности, в то время как центральная часть железистой ткани, расположенная вокруг главного панкреатического протока, остается неповрежденной.
Диагностика острого панкреатита обычно основывается на наличии боли в животе и увеличении уровня сывороточной амилазы и / или липазы.
Методы лучевой диагностики панкреонекроза.
- Ультразвуковое исследование
Данный метод является наиболее доступным, в связи с отсутствием инвазивности, простотой выполнения, высокой специфичностью и чувствительностью в определении основных проявлений панкреонекроза. - Компьютерная томография
КТ с болюсным контрастным усилением является приоритетным методом диагностики при определении тактики хирургического лечения.
КТ позволяет оценить размеры любого отдела железы в аксиальной, сагитальной и фронтальной плоскостях, а также плотность ткани в единицах Хаунсфилда. Кальцинаты и конкременты в ПП хорошо видны на фоне паренхимы ПЖ без контрастного усиления.
Противопоказанием к назначению данного исследования является непереносимость пациентом йодсодержащих контрастных препаратов, почечная недостаточность.
Ограничивающим фактором является значительная лучевая нагрузка на пациента. - Магнитно-резонансная томография
Выполнение МРТ целесообразно у пациентов с непереносимостью йодсодержащих контрастных препаратов, метод является наиболее информативным в дифференциальной диагностике причин билиарной и панкреатической гипертензии. - Эндоскопическая ретроградная панкреатохолангиография
Эндоскопическую ретроградную панкреатохолангиографию (ЭРПХГ) в настоящее время применяют редко. Несмотря на высокую диагностическую информативность ЭРХПГ не исключает возможности развития серьезных осложнений (острого панкреатита, холангита, сепсиса, ретродуоденальной перфорации). Недостатком является также невозможность оценить изменения непосредственно паренхимы железы. ЭРПХГ позволяет детально оценить состояние протока ПЖ и его ветвей.
Некрэктомия и резекция поджелудочной железы.
Наиболее безопасно осуществлять некрэктомию не ранее, чем через 10 дней от начала заболевания, так как в первые 3-5 дней при некрэктомии высок риск развития значительных кровотечений и повреждения прилежащих жизнеспособных тканей. Через 10 дней и более от начала заболевания граница между мертвыми и живыми тканями становится четкой, сосуды некротизированных тканей оказываются тромбированными и некрэктомию можно выполнить почти бескровно. В сроки 6-14 дней от начала заболевания некрэктомию относят к операциям, выполняемым в фазе расплавления и секвестрации, то есть ко второй группе операций при остром панкреатите. Третья группа – это поздние отсроченные операции, с 3 недели заболевания и далее, т.е. в фазе септического воспаления. Операции могут быть одно -, двух- и многоэтапные.
- Абсолютные:
‑ инфицированный панкреонекроз;
‑ панкреатогенный абсцесс;
‑ деструктивный холецистит;
‑ септическая флегмона забрюшинной клетчатки;
‑ гнойный перитонит. - Относительные:
‑ стерильный некроз более 50% ткани поджелудочной железы (по данным КТ);
‑ абактериальный некроз забрюшинной клетчатки (по данным УЗИ и КТ);
‑ холедохолитиаз, механическая желтуха (ЭРПХГ, эндоскопическая папиллотомия, эндоскопическая литоэкстракция);
‑ прогрессирующее ухудшение состояния в виде полиорганной недостаточности.
Предоперационная подготовка. Подготовка больных к операции должна включать коррекцию алиментарных и водно-электролитных нарушений. У больных, страдающих сахарным диабетом, необходимо проводить терапию с участием эндокринолога. При наличии дуоденальной дистрофии с нарушением дуоденальной проходимости требуется интенсивная терапия с элементами гипералиментации [8].
Возможные ошибки и осложнения.
1. Осложнения во время операции:
a. несоблюдение основных принципов ревизии брюшной полости, что не позволяет выявить или исключить разнообразные формы «острого живота»;
b. недостаточно широкий разрез желудочно-ободочной связки;
c. за некротизированную или секвестрированную ткань поджелудочной железы принимаются очаги некроза окружающей орган клетчатки, что дает хирургу основание сделать заключение о более распространенной деструкции железы, чем это есть на самом деле;
d. рассечение капсулы поджелудочной железы при отечном панкреатите. Это вмешательство неизбежно сопровождается повреждением сосудов и паренхимы органа, в то же время, оно не снижает напряжения в ткани железы и не улучшает кровоснабжения.
2. Осложнения в послеоперационном периоде:
‑ внутрибрюшные кровотечения: кровотечения после резекционных операций на ПЖ следует классифицировать согласно рекомендациям международной группы исследователей в области хирургии ПЖ (ISGPS) , при этом учитываются следующие факторы:
a. время начала кровотечения - 24 часа после завершения операции, разграничивают ранние и поздние кровотечения;
b. тяжесть кровотечения - показатель гемоглобина и необходимость переливания компонентов крови;
c. источник и локализация кровотечения – внутрипросветное (в просвет желудочно-кишечного тракта), либо внутрибрюшное кровотечение (уровень доказательности А).
3. разлитой перитонит;
4. распространение панкреонекроза;
5. нагноение в операционной ране и эвентрация;
6. образование кист, наружных свищей поджелудочной железы, свищей желудка и кишечника;
7. развитие гнойных форм острого панкреатита;
8. флегмона забрюшинного пространства;
9. абсцесс (поддиафрагмальный, подпеченочный, межкишечный);
10. некрозы брыжейки тонкой и толстой кишок;
11. острые эрозии и язвы пищевода, желудка и кишечника;
12. геморрагический гидроторакс;
13. печеночно-почечная недостаточность.
Выводы. Таким образом, проанализировав литературу по данному вопросу можно сделать вывод о том, что панкреонекроз является полиэтиологичным заболеванием, но имеет один патогенетический механизм, что обусловливает тактику лечения данного заболевания. Хирургическое лечение панкреонекроза должно проводиться в определенные сроки от начала заболевания, это будет способствовать увеличению скорости восстановления пациентов после операции и развитию меньшего количества осложнений в послеоперационном периоде.
Читайте также:

