Эпителиальный сидеропенический синдром при анемии проявляется
Обновлено: 01.05.2024
Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.).
Сидеропенический синдром проявляется многочисленными симптомами:
- извращение вкуса - непреодолимое желание употреблять в пищу что-либо необычное и малосъедобное (мел, зубной порошок, уголь, глину, песок, лед), а также сырое тесто, фарш, крупу; этот симптом чаще встречается у детей и подростков, но достаточно часто и у взрослых женщин; пристрастие к острой, соленой, кислой, пряной пище;
- извращение обоняния - пристрастие к запахам, которые большинством окружающих воспринимаются как неприятные (бензин, ацетон, запах лаков, красок, гуталина и др.);
- выраженная мышечная слабость и утомляемость, атрофия мышц и снижение мышечной силы в связи с дефицитом миоглобина и ферментов тканевого дыхания;
- дистрофические изменения кожи и ее придатков (сухость, шелушение, склонность к быстрому образованию на коже трещин; тусклость, ломкость, выпадение, раннее поседение волос; истончение, ломкость, поперечная исчерченность, тусклость ногтей; симптом койлонихии - ложкообразная вогнутость ногтей);
- ангулярный стоматит - трещины, «заеды» в углах рта (встречаются у 10-15% больных);
- глоссит (у 10% больных) - характеризуется ощущением боли и распирания в области языка, покраснением его кончика, а в дальнейшем атрофией сосочков («лакированный» язык); часто наблюдается склонность к пародонтозу и кариесу;
- атрофические изменения слизистой оболочки желудочно-кишечного тракта - это проявляется сухостью слизистой оболочки пищевода и затруднениями, а иногда болями при глотании пищи, особенно сухой (сидеропеническая дисфагия); развитием атрофического гастрита и энтерита;
- симптом «синих склер» характеризуется синеватой окраской или выраженной голубизной склер. Это объясняется тем, что при дефиците железа нарушается синтез коллагена в склере, она истончается и через нее просвечивает сосудистая оболочка глаза.
- императивные позывы на мочеиспускание, невозможность удержать мочу при смехе, кашле, чихании, возможно даже ночное недержание мочи, что обусловлено слабостью сфинктеров мочевого пузыря;
- «сидеропенический субфебрилитет» - характеризуется длительным повышением температуры до субфебрильных величин;
- выраженная предрасположенность к острым респираторно-вирусным и другим инфекционно-воспалительным процессам, хронизации инфекций, что обусловлено нарушением фагоцитарной функции лейкоцитов и ослаблением системы иммунитета;
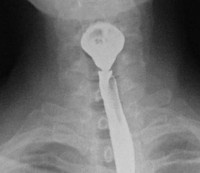
Синдром Пламмера-Винсона — патологическое дисфагическое состояние, обусловленное сужением пищевода и атрофией эпителия верхних отделов ЖКТ на фоне железодефицитной анемии. Проявляется затруднениями глотания в сочетании с бледностью кожи и слизистых, головокружениями, болезненностью и покраснением языка, трещинами в углах рта, сухостью кожи, деформацией ногтевых пластин. Диагностируется с помощью общего анализа крови, определения уровней железа, ферритина, проведения эзофагоскопии, рентгенографии пищевода. Для лечения используют препараты, содержащие железо, В-витаминные комплексы. При стойкой обструкции выполняют баллонную дилатацию, бужирование пищевода.
МКБ-10
Общие сведения
Сидеропеническую дисфагию (болезнь Пламмера-Винсона, синдром Келли-Паттерсона) в 1911-1919 годах независимо друг от друга описали американские физиологи Г.С. Пламмер, П.П. Винсон и британские ларингологи Д.Р. Паттерсон, А. Браун-Келли. Заболеванию более подвержены белые женщины климактерического возраста, хотя известны случаи диагностики синдрома у подростков и даже детей. Патология выявляется крайне редко, самые высокие показатели заболеваемости отмечались в XX столетии на территории скандинавских стран. Уменьшение распространенности сидеропенической дисфагии связано с улучшением питания и эффективной медикаментозной коррекцией железодефицитных состояний. Актуальность своевременной диагностики расстройства обусловлена высоким риском развития сопряженного рака пищевода.

Причины синдрома Пламмера-Винсона
Хотя заболевание стойко ассоциировано с железодефицитной анемией и гипосидерозом, его этиология на сегодняшний день окончательно не установлена. С учетом характерных патоморфологических и клинических проявлений специалистами в сфере гастроэнтерологии, гематологии, иммунологии предложено несколько теорий происхождения сидеропенической дисфагии:
- Железодефицитная теория. Атрофия слизистых ЖКТ — одно из проявлений сидеропенического синдрома. Из-за нехватки миоглобина и несостоятельности ферросодержащих ферментных систем при гипосидерозе развивается мышечная слабость, возникают нарушения акта глотания, характерные для дисфагии Пламмера-Винсона.
- Теория системного гиповитаминоза. У некоторых пациентов снижены уровни рибофлавина, фолиевой кислоты. Клинически гиповитаминозы обычно проявляются анемией, поражением слизистых, что послужило основанием для их рассмотрения в качестве этиологического фактора сидеропенической дисфагии.
- Аутоиммунная теория. Заболевание часто сочетается с аутоиммунным тиреоидитом, ревматоидным артритом, целиакией. Из-за преимущественного выявления у женщин климактерического возраста и несостоятельности железистого эпителия часть авторов рассматривает заболевание как легкий вариант синдрома Шегрена.
В качестве предпосылок к развитию расстройства рассматривается неполноценное питание, наследственная несостоятельность ферментов, участвующих в метаболизме железа, заболевания, сопровождающиеся хронической кровопотерей (метроррагии, геморрой, язвенная болезнь и др.), нарушение всасывания макроэлементов, витаминов при ахилии, энтеритах, другой патологии ЖКТ. У пожилых пациентов определенную роль могут играть инволюционные нарушения утилизации железа.
Патогенез
Механизм развития синдрома Пламмера-Винсона продолжает изучаться. Считается, что патогенез сидеропенической дисфагии основан на системных изменениях в тканях, связанных с железо-витаминной недостаточностью. В эпителиальной оболочке пищеварительных органов происходят гиперкератические и атрофические процессы, приводящие к сухости и истончению слизистых. Ситуация усугубляется повреждением железистой ткани с апоптозом секретирующих клеток, эпителиоцитов выводных протоков желез, выделением более густого секрета. В результате в верхнем отделе пищевода образуются небольшие липкие пленки (пищеводные мембраны), которые задерживают продвижение твердой части пищи и провоцируют спастическое сокращение мускулатуры. Атония дистальной части пищеводной трубки, вызванная низким содержания миоглобина в мышечных клетках, нарушает эзофагеальную перистальтику и препятствует нормальному прохождению пищевого комка.
Симптомы синдрома Пламмера-Винсона
Клиническая картина заболевания развивается постепенно. Вначале возникают признаки анемического синдрома: бледность кожи, слизистых оболочек, быстрая утомляемость, головные боли и головокружение, нечеткость зрения, учащение пульса, снижение артериального давления. Типичные симптомы сидеропенической дисфагии — воспалительная атрофия слизистой оболочки языка, которая проявляется его покраснением, жжением, сглаженностью, сухостью, болезненностью при пережевывании пищи. Характерно выделение небольшого количества вязкой слюны, появление чувствительных трещин в углах губ (ангулярный хейлит). У многих пациентов выявляется кератоконъюнктивит, кожа становится сухой, ногти — ложкообразными, отмечаются признаки себореи. При прогрессировании заболевания обнаруживается дисфагия (нарушение глотания) вначале твердой, а затем и жидкой пищи. Возможны боли и тяжесть в левом подреберье, обусловленные увеличением селезенки. Типично сезонное обострение синдрома в весенний период.
Осложнения
При тяжелом течении симптомокомплекса Пламмера-Винсона у пациентов наблюдается стремительная потеря массы тела вплоть до кахексии, что вызвано невозможностью проглатывания пищи из-за значительного сужения пищевода. Длительное белково-энергетическое голодание ведет к дистрофическим изменениям в мышцах и внутренних органах. При выраженном снижении уровня гемоглобина может возникать анемическая кома, вызванная недостаточным поступлением кислорода в структуры головного мозга. При вовлечении в атрофический процесс слизистой желудка развивается гастрит с пониженной кислотностью, усугубляющий расстройства пищеварения. Наиболее опасное осложнение синдрома, выявляющееся у 3-15% больных, — плоскоклеточный рак пищевода, глотки, реже наблюдаются злокачественные неоплазии дыхательных путей.
Диагностика
Постановка диагноза может представлять затруднения вследствие неспецифичной клинической картины и низкой распространенности заболевания. О возможном наличии синдрома Пламмера-Винсона свидетельствует сочетание дисфагии с сидеропенической анемией и сужением пищевода. Наиболее информативными в диагностическом плане являются:
- Общий анализ крови. Выявляется анемический синдром: снижение количества гемоглобина и эритроцитов, появление большого количества микроцитов, уменьшение среднего объема эритроцита. Для болезни Пламмера-Винсона характерна сидеропения — падение уровня ферритина и железа в крови, повышение железосвязывающей способности сыворотки.
- Эзофагоскопия. С помощью гибкого эндоскопа, введенного в пищевод, в проксимальном отделе органа удается обнаружить тонкие гладкие стриктуры с эксцентричным входом. При подозрении на развитие злокачественной опухоли осуществляется эндоскопическая биопсия измененного участка эпителия для гистологического анализа.
- Рентгенография пищевода. Метод рекомендован больным с выраженными стриктурами пищевода, препятствующими продвижению эндоскопа. Выполнение серии рентгенограмм после перорального введения контрастного вещества эффективно обнаруживает участок сужения органа. Рентгенография также позволяет оценить состояние пищеварительного тракта.
Для исключения других причин анемического синдрома может назначаться исследование клеточного состава костного мозга (миелограмма). Для обнаружения структурных изменений при выраженной спленомегалии производят УЗИ селезенки. Дифференциальную диагностику проводят с дивертикулами и злокачественными опухолями пищевода, кардиоспазмом, эзофагоспазмом, ахалазией пищевода, склеродермией, стриктурами органа после термических или химических ожогов, грыжей пищеводного отверстия диафрагмы, новообразованиями средостения, наследственными формами анемий, синдромом функциональной дисфагии, болезнью Меллера-Гунтера. Кроме осмотра гастроэнтеролога пациенту рекомендованы консультации онколога, хирурга, оториноларинголога, терапевта, гематолога, невролога, иммунолога, ревматолога.
Лечение синдрома Пламмера-Винсона
Тактика ведения пациента основана на вероятных причинах и механизмах развития заболевания. Обычно стойкого терапевтического эффекта удается достичь консервативными методами и изменением рациона с употреблением достаточного количества белка, продуктов, содержащих витамины группы В. Рекомендованная схема лечения включает следующие лекарственные средства:
- Препараты железа. Коррекция сидеропенического синдрома позволяет уменьшить или полностью купировать дисфагию. Для улучшения усвоения железа применяют лекарственные формы с большей биодоступностью, комбинированные средства с аскорбиновой кислотой.
- Витаминные комплексы. С учетом патогенетической роли рибофлавина и фолиевой кислоты в возникновении расстройства Пламмера-Винсона пациентам показаны монопрепараты витаминов В2, В9. Еще более эффективно назначение поливитаминных препаратов.
При наличии сведений о патологических состояниях, осложнившихся анемией и сидеропенией, этиопатогенетическая терапия основного заболевания проводится по соответствующим протоколам лечения. Пациентам со стойкой дисфагией и выраженной эзофагеальной обструкцией для разрыва пленок, устранения спазма выполняется бужирование или баллонная дилатация пищевода.
Прогноз и профилактика
Исход заболевания зависит от выраженности структурных изменений пищевода и наличия функциональных расстройств других органов. Прогноз относительно благоприятный, после проведения комплексного лечения у большинства пациентов с расстройством Пламмера-Винсона наступает выздоровление. Меры профилактики заболевания неспецифичны, предусматривают соблюдение сбалансированной диеты, употребление продуктов с высоким содержанием железа и витамина С, посильные физические нагрузки, отказ от вредных привычек. Для предупреждения развития осложнений все больные, перенесшие синдром сидеропенической дисфагии, после выздоровления подлежат длительному диспансерному наблюдению.
1. Синдром Пламмера-Винсона/ Черноусов А.Ф., Ветшев Ф.П., Хоробрых Т.В., Рогаль М.М.// Хирургия. Журнал им. Н.И. Пирогова – 2013 - №10.
Сидеробластная анемия – это приобретенное или наследственное заболевание крови, характеризующееся гипохромией эритроцитов, высоким уровнем сывороточного железа с отложением в тканях органов. Клиническая картина представлена анемическим синдромом (головокружение, утомляемость, бледность кожи), гемосидерозом внутренних органов (гепатомегалия, кардиомегалия, ХПН), изменением картины крови. Диагноз выставляется на основании клинических и биохимических анализов (ОАК, сывороточное Fe, ферритин, трансферрин, витамин В6), генодиагностики, исследования миелограммы. Лечение может включать гемотрансфузии, витамино-, гормонотерапию, хелаторную терапию.
МКБ-10
Общие сведения
Сидеробластные (сидероахрестические) анемии включают несколько гетерогенных синдромов, которые протекают с нарушением синтеза гема, несмотря на повышенное содержание железа в плазме. Популяционная частота сидеробластных анемий (СБА) не выяснена ввиду их клинической неоднородности, однако известно, что приобретенные формы встречаются чаще наследственных. Врожденные анемии обычно манифестируют в детстве, но могут оставаться нераспознанными вплоть до зрелого возраста. Первичная приобретенная сидеробластная анемия диагностируется преимущественно у лиц среднего и пожилого возраста.

Причины
Врожденная сидеробластная анемия
Врожденные СБА связаны с мутациями в генетическом материале. Они различаются по типу наследования и патогенетическому механизму:
- Х-сцепленные сидеробластные анемии. Один вариант обусловлен дефектами гена ALAS2 ‒ синтазы дельта-аминолевуленовой кислоты II типа (локус Хр11.21). Другой тип болезни связан с трансгенациями hABC7 (Xp13.1-q13.3), кодирующего белок, участвующий в транспорте гема.
- Аутосомно-рецессивная сидеробластная анемия. Генетически гетерогенная группа. Может возникать при дефекте гена WFS1 (4p16.1), отвечающего за экспрессию трансмембранного белка вольфрамина. В этом случае СБА диагностируется в рамках синдрома Вольфрама (DIDMOAD). Другая форма развивается при дефектах в гене SLC25A38, кодирующем белок-транспортер глицина, необходимый для синтеза гема.
- Митохондриальная цитопатия. Вызвана делециями митохондриальной ДНК, клинически проявляется развитием синдрома Пирсона.
- Спорадические сидеробластные анемии. Обусловлены появлением вновь возникших генетических мутаций, которые отсутствуют у родителей и других членов семьи.
Приобретенная сидеробластная анемия
Идиопатические (первичные) СБА ‒ рефрактерные анемии с кольцевыми сидеробластами ‒ рассматриваются как разновидность миелодиспластического синдрома (МДС) и занимают в его структуре 5-15%. Чаще возникают как следствие лучевой или цитостатической терапии, проводимой по поводу коллагенозов, гемобластозов, различных онкопроцессов. Риск развития МДС повышен у курильщиков, лиц, контактирующих с химическими веществами (бензином, растворителями, инсектицидами).
Вторичная сидеробластная анемия может быть этиологически связана со следующими факторами:
- прием антибактериальных и туберкулостатических препаратов (хлорамфеникол, линезолид, изониазид, циклосерин);
- интоксикация свинцом;
- хронический алкоголизм;
- нарушение баланса витаминов и микроэлементов: дефицит пиридоксина (витамина В6), недостаток меди, избыток цинка;
- коллагенозы;
- болезни крови (полицитемия, гемолитическая анемия).
Патогенез
Независимо от многообразия причин все они тем или иным путем приводят к нарушению образования гема. Гем является соединением, состоящим из протопорфирина и атома железа (Fe2+). При его связывании с белком глобином образуется гемсодержащий хромопротеин гемоглобин, главная функция которого заключается в транспорте кислорода к тканям, а углекислоты из тканей.
При СБА в результате дефектов ферментных систем, дефицита пиридоксальфосфата, токсического влияния или других факторов нарушается биосинтез протопорфирина, что делает образование гема невозможным, несмотря на достаточный уровень Fe в сыворотке крови. Развивается гипохромная анемия. В условиях, когда железо не используется клетками, оно начинает накапливаться в тканях и внутренних органах с развитием их дисфункции.
Классификация
Сидеробластные анемии делятся на 2 большие группы – наследственные и приобретенные, внутри которых выделяют конкретные клинические формы, связанные с определенными этиофакторами:
1. Наследственные сидеробластные анемии:
- Х-сцепленные;
- аутосомные (могут быть пиридоксин-рефрактерными и пиридоксин-зависимыми);
- митохондриальные болезни.
2. Приобретенные сидеробластные анемии:
- первичные ‒ клональные СБА в рамках миелодиспластического синдрома;
- вторичные ‒ обратимые СБА (лекарственные, токсические, алиментарные);
- на фоне других заболеваний (системных, гематологических и пр.)
Симптомы сидеробластной анемии
В клинической картине сидероахрестических анемий преобладают две группы симптомов: циркуляторно-гипоксические и недостаточность органов, обусловленная гемосидерозом. Гематологические изменения выявляются при диагностическом исследовании крови и костного мозга.
Гипоксический синдром сопровождается недомоганием и слабостью, тахикардией, снижением АД. Характерны жалобы на головокружение, ноющие боли в сердце, появление «мушек» перед глазами, одышку при движениях. Отмечается сухость и бледность кожи, ломкость ногтей. У детей ухудшается запоминание учебного материала, снижается успеваемость.
Депонирование железа приводит к развитию гепатоспленомегалии, а в поздних стадиях – циррозу печени. Поражение поджелудочной железы сопровождается манифестацией сахарного диабета. Гемосидероз миокарда проявляется кардиомегалией, нарушением ритма, сердечной недостаточностью. Отложение железа в тканях мужских половых желез вызывает вторичный гипогонадизм. При поражении легких возникает дыхательная недостаточность, почек – ХПН.
Осложнения
Перегрузка железом вызывает необратимые органные поражения, приводящие к стойкой функциональной недостаточности сердца, печени, почек, эндокринных органов. Таким пациентам требуется пожизненная заместительная и поддерживающая терапия, у них снижена общая продолжительность жизни. Течение идиопатической формы сидеробластной анемии у 5-10% пациентов осложняется острым лейкозом, рефрактерным к полихимиотерапии.
Диагностика
Основанием для выставления диагноза «сидеробластная анемия» служат клинические и лабораторные данные. Больных консультирует врач-гематолог, при необходимости – генетик, токсиколог, ревматолог, нарколог. Опорными диагностическими критериями выступают:
- Гемограмма. Характерные изменения периферической крови включают снижение Hb и ЦП, возможна ретикулоцитопения. В мазке крови обнаруживается базофильная зернистость эритроцитов, тельца Паппенгеймера. Эритроциты часто уменьшены в размерах (микроцитарная анемия), имеют аномальную форму.
- Биохимические исследования. Сывороточное железо, уровни ферритина и трансферрина повышены, ОЖСС – снижена. Отмечается непрямая гипербилирубинемия, повышение ЛДГ. Может выявляться дефицит витамина В6. При токсической СБА показано исследование содержания свинца в крови.
- Генодиагностика. Осуществляется при подозрении на наследственную форму сидеробластной анемии. Диагноз считается достоверным при выявлении мутаций в причинных генах.
- Исследование мочи. Исследование порфиринов в суточной моче показывает их повышенную экскрецию. Результаты десфералового теста демонстрируют выведение с мочой значительного количество железа.
- Миелограмма. Цитологическая картина пунктата костного мозга указывает на гиперплазию эритроидного ростка миелопоэза. Более 40% предшественников эритроцитов представлены кольцевидными сидеробластами.
- Биопсия внутренних органов. При биопсии печени в гепатоцитах обнаруживаются депозиты железа, иногда – признаки цирроза. Возможно проведение биопсии селезенки, поджелудочной железы.
Лечение сидеробластной анемии
При токсических и лекарственных формах СБА в первую очередь устраняют провоцирующий фактор (отменяют ЛС, проводят дезинтоксикационную терапию и т.д.). Лекарственная терапия сидеробластной анемии включает назначение следующих препаратов:
- Витамин В6. Пиридоксинзависимые формы (некоторые наследственные, алиментарные, алкогольные) поддаются терапии пиридоксина гидрохлоридом или пиридоксальфосфатом. При положительном отклике проводят длительные курсы большими дозами вит. В6 с последующей поддерживающей витаминотерапией.
- Гормонотерапия. Показана пациентам с пиридоксин-резистентной формой сидеробластной анемии. Назначаются анаболические гормоны, андрогены, эритропоэтин.
- Хелаторная терапия. Введение дефероксамина направлено на удаление избытка железа из организма, уменьшение степени выраженности гемосидероза. Для коррекции перегрузки железом также может быть использована флеботомия.
- Вспомогательная терапия. Включает назначение фолиевой кислоты, антиоксидантов (вит. Е, липоевой кислоты), гепатопротекторов.
Прогноз и профилактика
Прогноз при сидеробластной анемии обусловлен ее этиологией. Лучше поддаются коррекции пиридоксин-зависимые и некоторые приобретенные формы (лекарственные, алиментарные). Существенно снижена продолжительность жизни у лиц с СБА, трансфузионно-зависимыми, рефрактерными к лечению, ассоциированными с лейкемией, синдромом Пирсона. Профилактика, прежде всего, касается вторичных сидеробластных анемий: следует полноценно питаться, принимать витаминные комплексы, не допускать интоксикаций (этанолом, свинцом) и контакта с вредными веществами. Для исключения наследственных СБА рекомендуется генетическое консультирование.
3. Клинический случай X-сцепленной сидеробластной анемии с новой миссенс-мутацией cd518 ttg-ttt (leu518phe) в гене alas2. и соавт.// Гематология и трансфузиология. – 2020.
4. Морфология анемий и гемобластозов/ Макаров И.Ю., Меньщикова Н.В., Дубяга Е.В., Левченко Н.Р. – 2018.
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
МКБ-10



Общие сведения
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Причины
Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями:
Кровопотери
Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др.
Особую группу составляют лица с болезнями крови - геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин - у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе.
Нарушение поступления, всасывания и транспорта железа
К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей - искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени).
Повышенное расходование железа
Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях.
Патогенез
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% - в состав миоглобина, 1% - в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.).
Классификация
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Симптомы
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.

Осложнения
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
Диагностика
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям - гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний - сидеробластной анемии, талассемии.

Лечение
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.

Прогноз и профилактика
В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
3. Федеральные клинические рекомендации по диагностике и лечению железодефицитных анемий/ Румянцев А.Г. и соавт. - 2015.
4. Железодефицитная анемия у женщин молодого возраста: аспекты качества жизни и оптимизация лечения: Автореферат диссертации/ Абдуллина Л.Р. - 2007.
ЖДА – приобретенное заболевание из группы дефицитных анемий, возникает при дефиците железа, сопровождающееся микроцитарной, гипохромной, норморегенераторной анемией, клиническими проявлениями которой являются сочетание сидеропенического и анемического синдромов [6, 8, 15].
Название протокола - Железодефицитная анемия у детей
Код протокола:
Код(-ы) по МКБ-10
D50 Железодефицитная анемия
D50.0 Хроническая постгеморрагическая анемия
Сокращения, используемые в протоколе:
АХБ анемия при хронических болезнях
ВОЗ Всемирная организация здравоохранения
ГПК гидросидполимальтозный комплекс
ЖДА железодефицитная анемия
ЖКТ желудочно-кишечный тракт
ЛДЖ латентный дефицит железа
МСНС средняя концентрация гемоглобина в эритроците
НТЖ коэффициент насыщения трансферрина железом
ОЖСС общая железосвязывающая способность
СЖ сывороточное железо
СФ сывороточный ферритин
ЦП цветовой показатель
МСН содержание гемоглобина в эритроците
MCV средний объем эритроцитов
RDW степень анизоциотоза эритроцитов
Дата разработки протокола: 2013 год
Категория пациентов: дети, подростки с диагнозом «Железодефицитная анемия»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация:
I степень (легкая) – уровень Hb 110-90 г/л;
II степень (средняя) – уровень Hb 90-70 г/л;
III степень (тяжелая) – уровень Hb менее 70 г/л.
Диагностика
Перечень основных и дополнительных диагностических мероприятий:
- Развернутый ОАК, ретикулоциты
- Концентрация сывороточного железа
- Общая железосвязывающая способность сыворотки
- Содержание сывороточного ферритина
- Перечень дополнительных диагностических мероприятий:
- MCV
- MCH
- MCHC
- RDW
- коэффициент насыщения трансферрина железом
- определение растворимых трансферриновых рецепторов
Диагностические критерии:
Клинические проявления ЖДА представляют совокупность двух синдромов: сидеропенического и анемического.
Для сидеропенического синдрома характерны следующие симптомы:
- изменения кожи: сухость, появление маленьких пигментных пятен цвета «кофе с молоком»;
- изменения слизистых оболочек: «заеды» в углу рта, глоссит, атрофический гастрит и эзофагит;
- диспептические явления со стороны ЖКТ;
- изменения волос – раздваивание кончика, ломкость и выпадение вплоть до гнездной алопеции;
- изменения ногтей – поперечная исчерченность ногтей больших пальцев рук (в тяжелых случаях и ног), ломкость, расслаивание на пластинки;
- изменение обоняния – пристрастие больного к резким запахам лака, краски ацетона, выхлопных газов автомобиля, концентрированных духов;
- изменения вкуса – пристрастие больного к глине, мелу, сырому мясу, тесту, пельменям и др.;
- боли в икроножных мышцах.
Считается, что наличие 4-х симптомов и более из перечисленных выше патогномонично для латентного дефицита железа (ЛДЖ) и ЖДА.
Для анемического синдрома характерны следующие симптомы:
- снижение аппетита;
- шум в ушах;
- мелькание мушек перед глазами;
- плохая переносимость физических нагрузок;
- слабость, вялость, головокружение, раздражительность;
- обмороки;
- одышка;
- снижение работоспособности;
- снижение когнитивных функций;
- снижение качества жизни;
- бледность кожи и видимых слизистых оболочек;
- изменение тонуса мышц в виде тенденции к гипотонии, гипотония мышц мочевого пузыря с развитием недержания мочи;
- расширение границ сердца;
- приглушенность сердечных тонов;
- тахикардия;
с- истолический шум на верхушке сердца.
Критерии лабораторной диагностики заболевания
Имеется 3 возможности лабораторной диагностики ЖДА:
- ОАК, выполненный «ручным» методом - снижение концентрации Hb (менее 110 г/л), небольшое снижение количества эритроцитов (менее 3,8 х 1012/л), снижение ЦП (менее 0,85), увеличение СОЭ (более 10-12 мм/час), нормальное содержание ретикулоцитов (10-20‰). Дополнительно врач-лаборант описывает анизоцитоз и пойкилоцитоз эритроцитов. ЖДА это микроцитарная, гипохромная, норморегенераторная анемия.
- ОАК, выполненный на автоматическом анализаторе клеток крови - снижаются средний объем эритроцита – MCV (менее 80 фл), среднее содержание Hb в эритроците – MCН (менее 26 пг), средняя концентрация Hb в эритроците – МСНС (менее 320 г/л), повышается степень анизоцитоза эритроцитов – RDW (более 14%).
- Биохимический анализ крови - снижение концентрации сывороточного железа (менее 12,5 мкмоль/л), повышение общей железосвязывающей способности сыворотки (более 69 мкмоль/л), снижение коэффициента насыщения трансферрина железом (менее 17%), снижение сывороточного ферритина (менее 30 нг/мл). В последние годы появилась возможность определения растворимых трансферриновых рецепторов (рТФР), количество которых в условиях дефицита железа увеличивается (более 2,9 мкг/мл).
Лечение
Цели лечения:
- нормализация показателей крови;
- купирование анемического, сидеропенического синдромов
Тактика лечения
Немедикаментозное лечение
- Устранение этиологических факторов;
- Рациональное лечебное питание (для новорожденных – грудное естественное вскармливание, а при отсутствии молока у матери – адаптированные молочные смеси, обогащенные железом. Своевременное введение прикорма, мяса, субпродуктов, гречневой и овсяной круп, фруктовых и овощных пюре, твердых сортов сыра; уменьшение приема фосфатов, танина, кальция, которые ухудшают всасывание железа).
Медикаментозное лечение
В настоящее время в нашей стране используется терапевтический план лечения ЖДА пероральными препаратами железа, суточные дозы которых представлены в таблице.
Возрастные терапевтические дозы пероральных препаратов железа для лечения ЖДА у детей (ВОЗ, 1989)
| Возраст ребенка | Суточная доза элементарного железа |
| Солевые препараты железа | |
| Дети до 3-х лет | 3 мг/кг |
| Дети старше 3-х лет | 45-60 мг |
| Подростки | до 120 мг |
| Препараты железа на основе ГПК трехвалентного железа | |
| Любой возраст | 5 мг/кг |
Принципы рациональной терапии ЖДА у детей
- Лечение препаратами железа рекомендуется проводить под наблюдением врача. Детям препараты железа рекомендуется назначать после консультации педиатра.
- Не следует назначать препараты железа детям на фоне воспалительных процессов (ОРВИ, ангина, пневмония и др.), так как в этом случае железо аккумулируется в очаге инфекции и не используется по назначению.
- Лечить железодефицитную анемию следует в основном препаратами для внутреннего применения.
- Железо должно быть двухвалентным, поскольку всасывается именно двухвалентное железо.
- Применение препаратов железа следует сочетать с оптимизацией пищевого рациона, с обязательным введением в меню мясных блюд.
- Для максимального всасывания железа препарат следует принимать за 0,5-1 час до еды, запивая водой. Если появляются побочные эффекты, можно принимать лекарство во время еды. Хуже всего всасывается железо, если препарат принимается после еды.
- Пероральные препараты железа следует принимать с интервалом не менее 4-х часов.
- Таблетки и драже, содержащие железо, не разжевывать!
- Включение в комплексные препараты железа аскорбиновой кислоты улучшает усвоение железа (в качестве антиоксиданта аскорбиновая кислота препятствует превращению ионов Fe-II в Fe-III, не всасывающихся в ЖКТ) и позволяет уменьшить назначаемую дозу. Всасывание железа также увеличивается в присутствии фруктозы, янтарной кислоты
- Нельзя сочетать прием препарата железа с веществами, ингибирующими его всасывание: молоко (соли кальция), чай (танин), растительные продукты (фитаты и хелаты), ряд лекарственных препаратов (тетрациклин, антациды, блокаторы, Н2-рецепторов, ингибиторы протонной помпы).
- Прием комбинированных препаратов, которые наряду с железом содержат медь, кобальт, фолиевую кислоту, витамин В12 или экстракт печени, чрезвычайно затрудняет контроль эффективности железотерапии (за счет гемопоэтической активности этих веществ).
- Средняя продолжительность курса лечения ЖДА составляет от 4-х до 8 недель. Лечение препаратом железа следует продолжать и после купирования ЖДА для восстановления тканевого и депонированного железа. Длительность поддерживающего курса определяется степенью и давностью дефицита железа (ДЖ), уровнем СФ.
- В лечении ЖДА не должны применяться витамин В12, фолиевая кислота, витамин В6, патогенетически никак не связанные с дефицитом железа.
- Неэффективность терапии ЖДА пероральными препаратами железа требует пересмотра диагноза (нередко диагноз ЖДА устанавливается боьным с анемией хронического заболевания, при котором лечение препаратами железа неэффективно), проверки исполнения больным назначений врача в дозировке и сроках лечения. Очень редко встречается нарушение всасывания железа.
- Парентеральное введение препаратов железа показано только: при синдроме нарушенного кишечного всасывания и состояних после обширной резекции тонкого кишечника, неспецифическом язвенном колите, тяжелом хроническом энтероколите и дисбактериозе, непереносимости пероральных препаратов железа. Ограничение парентерального введения связано с высоким риском развития местных и системных побочных реакций. Кроме того, парентеральное применение препаратов железа значительно дороже, чем пероральная терапия, за счет трудозатрат медицинского персонала и большей стоимости лекарственной формы. Парентеральное введение препаратов железа следует производить только в стационаре!
- Одновременное назначение препаратов железа внутрь и парентерально (внутримышечно и/или внутривенно) должно быть полностью исключено!
- Трансфузии эритроцитарной массы в лечении ЖДА применяться не должны. Донорское железо не реутилизируется организмом реципиента и остается в гемосидерине макрофагов. Возможен перенос опасных инфекций через донорскую кровь. Исключениями, допускающими трансфузии донорских эритроцитов, являются: 1) выраженные гемодинамические нарушения; 2) предстоящие дополнительные кровопотери (роды, операция) при выраженной анемии (гемоглобин менее 70 г/л); 3) отвечающий современным требованиям препарат железа должен быть доступным и дешевым.
Препараты, содержащие трехвалентное железо Fe (III)
Трехвалентное железо практически не всасывается в желудочно-кишечном тракте. Однако комплексные органические соединения Fe (III) с рядом аминокислот, мальтозой существенно менее токсичны, чем Fe (II), но не менее эффективны. Иммобилизация Fe (III) на аминокислотах обеспечивает его стойкость к гидролизу в ЖКТ и высокую биодоступность, благодаря медленному высвобождению лекарственного вещества и более полной его абсорбции, а также отсутствие диспептических явлений.
Осложнения лечения
Применение солевых препаратов железа может сопровождаться осложнениями в виде токсичности для ЖКТ с развитием таких симптомов как боли в эпигастральной области, запор, понос, тошнота, рвота. Это приводит к низкой комплаентности лечения ЖДА солевыми препаратами железа – 30-35% больных, начавших лечение, отказываются от его продолжения. Возможны передозировка и даже отравления солевыми препаратами железа из-за пассивного неконтролируемого всасывания.
Другие виды лечения - нет
Хирургическое вмешательство - нет
Профилактика
Первичной профилактикой дефицита железа является правильное, полноценное питание.
Вторичная профилактика дефицита железа – это активное выявление ЛДЖ и ДЖА в процессе диспансеризации, медицинских осмотров, при посещении врача.
Дальнейшее ведение: прогноз заболевания благоприятный, излечение должно наступать в 100% случаев.
Так называемые «рецидивы» заболевания возможны при:
- использовании низких доз препаратов железа;
- неэффективности пероральных препаратов железа, которая встречается редко;
- уменьшение длительности лечения больных;
- лечении больных хронической постгеморрагической анемией с невыявленным и неустраненным источником кровопотери.
Информация
Источники и литература
- Протоколы заседаний Экспертной комиссии по вопросам развития здравоохранения МЗ РК, 2013
- Список использованной литературы: 1. Международная статистическая классификация болезней и проблем, связанных со здоровьем. Десятый пересмотр (МКБ-10). Женева: ВОЗ; 1995. т. 1-2 2. WHO, UNICEF, UNU.IDA: prevention, assessment and control: report of a joint WHO/UNICEF/UNU consultation. Geneva: WHO, 1998. 3. World Health Organization. Iron deficiency anemia: assessment, prevention and control. A guide for programme managers. Geneva; 2001; (WHO/NHD/01.3). 4. Хертл М. Дифференциальная диагностика в педиатрии. М.: Медицина; 1990. т.2. 510 с. 5. Конь И.Я., Куркова В.И. Роль алиментарного фактора в развитии железодефицитной анемии у детей раннего возраста. В кн.: Кисляк Н.С. и др. (ред.) Дефицит железа и железодефицитная анемия. М.: Славянский диалог; 2001. 87-98. 6. Румянцев А.Г., Коровина Н.А., Чернов В.М. и др. Диагностика и лечение железодефицитной анемии у детей. Методическое пособие для врачей. М.; 2004. 45 с. 7. Доклад о состоянии здоровья детей в РФ. М.; 2003. 96 с. 8. Ожегов Е.А. Оптимизация лечения железодефицитной анемии у детей и подростков. Автореф.дисс… канд.мед.наук. М.; 2005. 9. Красильникова М.В. Железодефицитные состояния у подростков: частотные характеристики, структура и вторичная профилактика. Автореф.дисс. канд.мед.наук. М.; 2006. 10. Анемия – скрытая эпидемия. Пер. с англ. М.: Мега Про; 2004. 11. Recommendations to prevent and control iron deficiency in the United States. Centers for Disease Control and Prevention. MMWR Recomm Rep 1998; 47 (RR-3): 1-29. 12. Омарова К.О., Базарбаева А.А., Курманбекова С.К. Железодефицитные анемии у детей. Методические рекомендации. Алматы. 2009. 13. Стандарты оказания специализированной помощи детям и подросткам с гематологическими и онкологическими заболеваниями. Москва. 2009. 14. Кривенок В. Необходимое составляющее лечение железодефицитной анемии // Провизор. – 2002. - № 18. – С.44. 15. Коровина Н.А., Заплатников А.Л., Захарова И.Н. Железодефицитные анемии у детей. Москва, 1999, с.25-27. 16. Справочник Видаль. Лекарственные препараты в Казахстане: Справочник М.: Астра Фарм Сервис, 2008. – 944 с. 17. Ужегова Е.Б. Железодефицитная анемия. Учебно-методическое пособие. – Алматы. 2008. – С.22-24. 18. Fairbanks V.F., Beutler E.: Iron deficiency // In Williams Hematology, Fifth Editor, New York, McGraw-Hill; 1999, P.490-510.
Информация
Список разработчиков протокола
Омарова К.О. – доктор медицинских наук, профессор, Научный центр педиатрии и детской хирургии МЗ РК.Конфликт интересов
Разработчик протокола не имеет финансовой или другой заинтересованности, которая могла бы повлиять на вынесение заключения, а также не имеет отношение к продаже, производству или распространению препаратов, оборудования и т.п., указанных в протоколе.Рецензенты
Курманбекова С.К. - профессор кафедры интернатуры и резидентуры по педиатрии Казахского национального медицинского университета им.С.Д.АсфендияроваУсловия пересмотра протокола: по истечению 3 лет с момента публикации
Читайте также:

