Диагностируется ли ихтиоз биопсией
Обновлено: 23.04.2024
Аутосомно-рецессивный врожденный ихтиоз (Autosomal recessive congenital ichthyosis - ARCI) – клинически и генетически гетерогенная группа заболеваний кератинизации, характеризующаяся шелушением кожи на всем теле, часто ассоциированном с эритемой. Существуют две несиндромальные формы ихтиоза: ламеллярный ихтиоз (lamellar ichthyosis – LI, ARCI 1, MIM 242300) и небуллезная врожденная эритродермия (Nonbullous congenital ichthyosiform erythroderma – NCIE, ARCI 2, MIM 242100). Частота обеих форм заболевания 1:300-500 тысяч новорожденных.
Клинически ламеллярный ихтиоз отличается от небуллезной врожденной эритродермии характеристикой чешуек (они крупные, темные) и отсутствием эритемы. При небуллезной врожденной эритродермии чешуйки тонкие, серебристые, располагаются на фоне эритемы, на конечностях они больше и темнее. Существуют перекрывающиеся фенотипы как у одного больного, так и у разных больных из одной семьи. Гистопатологические изменения и структурные особенности четко не разделяют ламеллярный ихтиоз и небуллезную врожденную эритродермию. Кроме того, мутации в одних и тех же генах приводят к обоим фенотипам. Поэтому в 2009 году был введен термин Autosomal recessive congenital ichthyosis – ARCI для объединения LI, NCIE, а также «плода Арлекина» (harlequin ichthyosis). Harlequin ichthyosis – редкая тяжелая форма врожденного ихтиоза, при которой дети обычно умирают в течение первой недели жизни.
Аутосомно-рецессивный врожденный ихтиоз ARCI 1, L1 (MIM 242300): дети с этим типом заболевания или умирают в течение первых месяцев жизни от сепсиса, потери белков и электролитов, или кожное заболевание может быть полностью вылечено. При рождении тело ребенка покрыто коллодиоподобной мембраной, затем на коже образуются большие коричневые чешуйки, покрывающие все тело. Больные могут иметь ладонный и подошвенный гиперкератоз и значительное натяжение кожи лица, которое может быть ассоциировано с эктропионом (выворачиванием век) и выворачиванием губ.
При аутосомно-рецессивном врожденном ихтиозе ARCI 2, NCIE, (MIM 242100), больные имеют ладонно-подошвенный кератоз, часто с болезненными трещинами, контрактурами. У половины больных встречается дистрофия ногтей. При небуллезной врожденная эритродермии чаще, чем при ламеллярном ихтиозе встречается эктропион, вовлечение кожи головы, потеря бровей и ресниц. Большинство больных рождается с коллодиоподобной мембраной.
У большинства детей, рожденных с коллодиоподобной мембраной, затем развиваются различные типы ARCI. Однако около 10% из них спонтанно вылечиваются в течение первых недель. Это мягкое клиническое течение назвали «self-healing collodion baby».
Аутосомно-рецессивный врожденный ихтиоз делится на несколько типов. К ARCI 1 (MIM 242300) приводят мутации в гене TGM1 (MIM 190195), к ARCI 2 (MIM 242100) приводят мутации в гене ALOX12B (MIM 603741), к ARCI 3 (MIM 606545) – в гене ALOXE3 (MIM 607206). Кроме того выделяют следующие типы ARCI: ARCI4A (MIM 601277) и ARCI4B (harlequin ichthyosis; MIM 242500), вызываемые мутациями в гене ABCA12 (MIM 607800), локализованном на хромосоме 2q35. ARCI5 (MIM 604777): неламеллярный неэритродермический ихтиоз, при котором образуются тонкие белые чешуйки в основном на ногах и на коже головы, гиперисчерченность ладоней и подошв похожа на такую при вульгарном ихтиозе, к заболеванию приводят мутации в гене CYP4F22 (MIM 611495) на хромосоме 19p13. При ARCI6 (MIM 612281) часть больных имеет фенотип, похожий на NCIE, часть – на ламеллярный ихтиоз, у всех больных имеется ладонно-подошвенный кератоз, часто желтоватый с трещинами, а также у некоторых больных наблюдается утолщение ногтей, заболевание обусловлено мутациями в гене NIPAL4 (ichthyin; MIM 609383) на хромосоме 5q33. ARCI7 (MIM 615022) был картирован на хромосоме 12p11. ARCI8 (MIM 613943) вызван мутацией в гене LIPN (MIM 613924) на хромосоме 10q23. ARCI9 (MIM 615023) обусловлен мутациями в гене CERS3 (MIM 615276) на хромосоме 15q26. К ARCI10 (MIM 615024) приводят мутации в гене PNPLA1 (MIM 612121) на хромосоме 6p21.
При ARCI большинство мутаций найдено в гене TGM1 – 32%; в 12% случаев мутации идентифицированы в гене ALOX12B, в 16% - в ихтине (NIPAL4), в 8% - в CYP4F22, по 5% мутаций найдено в генах ALOXE3 и ABCA12.
В Центре Молекулярной Генетики проводится поиск мутаций во всех экзонах генов TGM1, ALOX12B, ALOXE3 и NIPAL4 методом прямого автоматического секвенирования.
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Татьяны Алексеевны, гинеколога со стажем в 14 лет.
Над статьей доктора Игнатенко Татьяны Алексеевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Причины дисплазии шейки матки
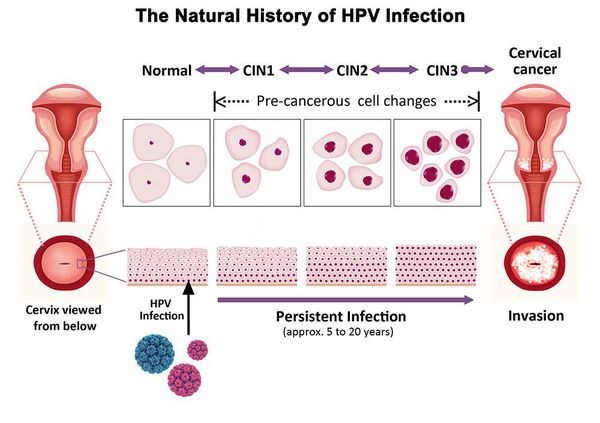
Папилломавирусная инфекция (ВПЧ) — основная причина дисплазии и рака шейки матки. К болезни приводит длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
К факторам риска дисплазии шейки матки относится длительный приём контрацептивов и курение. Выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Другие факторы риска — раннее начало половой жизни, большое число и частая смена половых партнеров, употребление алкоголя, сопутствующие половые инфекции, много беременностей и родов. Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
- нормальные мазки, без изменений клеток шейки матки (NILM, Negative for intraepithelial lesion or malignancy);
- «непонятные» мазки без определенного значения, по которым нельзя определить характер поражения, однако они при этом не являются нормой (ASC-US, Atypical Squamous Cells of Undetermined Significance) или, что хуже, ASC-H, Atypical squamous cells cannot exclude HSIL, обнаружение атипичных клеток плоского эпителия, не исключающее SIL высокой степени);
- предраки низкой (LSIL, Low Grade Squamous Intraepithelial Lesion) и высокой (HSIL, High Grade Squamous Intraepithelial Lesion) степени.
Классификация Папаниколау
- 1-й класс — нормальная цитологическая картина (отрицательный результат);
- 2-й класс — изменение морфологии клеток, которое обусловлено воспалением во влагалище и (или) шейке матки;
- 3-й класс — единичные клетки с аномалией ядер и цитоплазмы (подозрение на злокачественное новообразование);
- 4-й класс — отдельные клетки с явными признаками озлокачествления;
- 5-й класс — много типично раковых клеток (злокачественное новообразование).
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
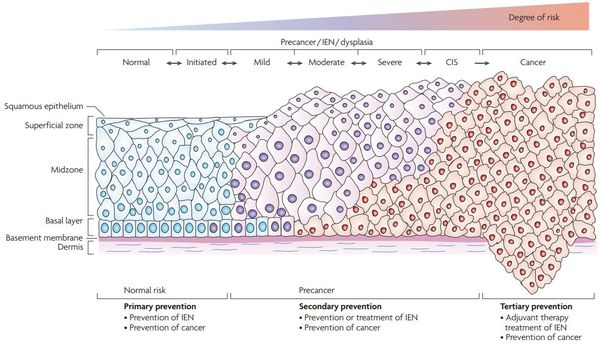
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя выделяют три степени дисплазии шейки матки:
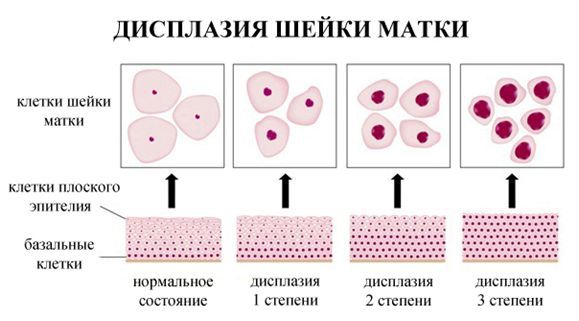
- ЦИН 1 (дисплазия слабой степени) — признаки папилломавирусной инфекции (койлоцитоз и дискератоз). Поражение до 1/3 толщины клеточного пласта;
- ЦИН 2 (дисплазия средней степени) — поражена 1/2 толщины клеточного слоя;
- ЦИН 3 (дисплазия тяжелой степени) — поражение более 2/3 клеточного слоя. [8]
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
| Система Папаниколау | Описательная система ВОЗ | CIN | Терминологи- ческая система Бетесда (ТСБ) |
|---|---|---|---|
| Класс 1 (норма) | Отсутствие злокачественных клеток | Отсутствие неопластических изменений | Норма |
| Класс 2 (метаплазия эпителия, воспалительный тип) | Атипия, связанная с воспалением | Реактивные изменения клеток ASC: ASC - US, ASC - H | |
| Класс 3 ("дискариоз") | Слабая дисплазия | CIN 1 койлоцитоз | LSIL |
| Умеренная дисплазия | CIN 2 | HSIL | |
| Тяжелая дисплазия | CIN 3 | ||
| Класс 4 (клетки, подозрительные на рак или карцинома in situ | Карцинома in situ | ||
| Класс 5 (рак) | Инвазивная карцинома | Карцинома | Карцинома |
Осложнения дисплазии шейки матки
Последствия дисплазии шейки матки
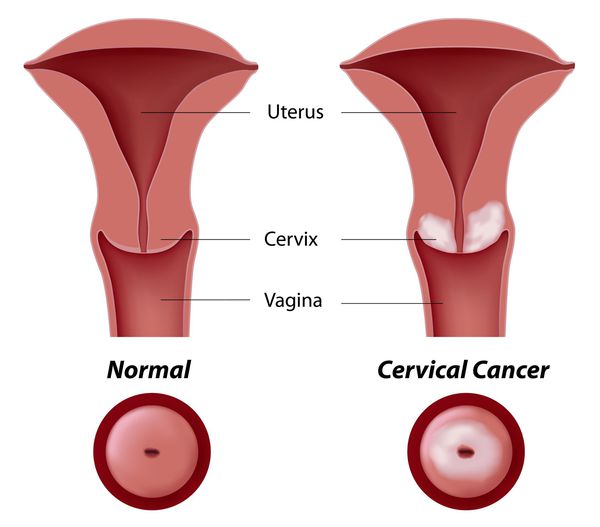
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
Методы диагностики дисплазии шейки матки
В России система цервикального скрининга включает последовательность действий:
- Цитологическое исследование: РАР-тест;
- ВПЧ-тестирование: в США и странах Евросоюза ВПЧ-тест применяется для первичного скрининга рака шейки матки (РШМ). В России его использование вариативно: при первичном скрининге в сочетании с РАР-тестом, в качестве самостоятельного теста, при ведении пациенток с неясными результатами РАР-теста (ASCUS) и для наблюдения паценток после лечения HSIL;
- Кольпоскопия: показаниями к исследованию являются положительные результаты РАР-теста (класс 2-5). Метод основан на осмотре шейки матки при помощи увеличивающих оптических систем и проведения диагностических проб с растворами уксусной кислоты и йода (Люголя). С помощью кольпоскопии определяют локализацию поражения, его размер, выбирают участок для проведения биопсии, определяют тактику лечения.
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
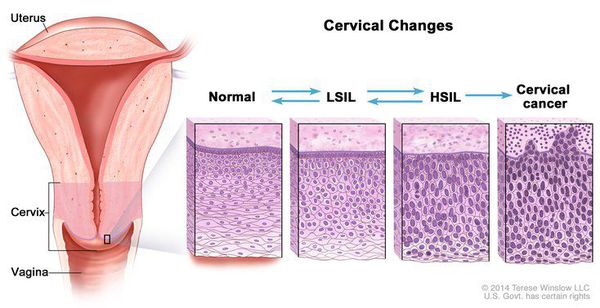
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
- Зона трансформации 1 типа — переходная зона видна полностью. Это самый оптимальный и прогностически «благоприятный» вариант кольпоскопического заключения.
- Зона трансформации 2 типа — переходная зона частично скрыта в канале шейки матки. Адекватно оценить такую картину сложно, так как наиболее измененные участки могут быть не видны и пропущены.
- Зона трансформации 3 типа — переходная зона находится глубоко в канале шейки матки и оценить её кольпоскопически невозможно. Кольпоскопия в этом случае считается неинформативной, поскольку глубина залегания патологического очага остается неизвестной.
- Биопсия: прицельная или расширенная биопсия (конизация) всегда должна выполняться под контролем кольпоскопии. Выбор метода биопсии зависит от типа поражения, возраста пациентки и зоны трансформации. Важной информацией, которую дает биопсия, является возможность иммуногистохимического определения маркера ранней диагностики дисплазии с высокой степенью риска озлокачествления: p16INK4a.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии.
Хирургическое лечение дисплазии
При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
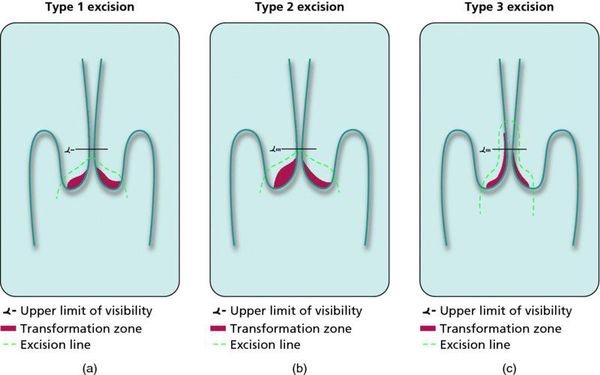
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
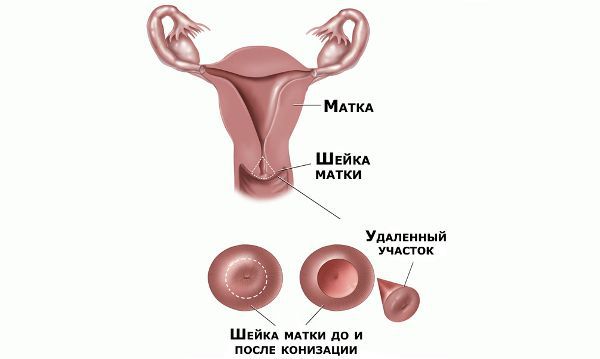
Реабилитация после хирургического лечения
В течение месяца после операции следует воздержаться от спринцеваний, половых контактов и не пользоваться тампонами. На 2–3 недели исключают тяжёлые физические нагрузки и тепловые процедуры. Незначительные сукровичные выделения, усиливающиеся иногда до менструальноподобных, в течение 10–20 дней после операции — это нормальное явление.
При реабилитации после хирургического лечения шейки матки эффективны препараты, содержащие антисептик и стимулятор регенерации эпителия.
После лечения возможен рецидив, поэтому необходимо пожизненное наблюдение: цитологический мазок через 6 и 12 месяцев после операции, затем раз в год в течение 10 лет, далее раз в 3 года.
Планировать беременность после операции на шейке матки можно не ранее, чем через 3–6 месяцев. Эти сроки будут зависеть от глубины эксцизии или конизации и длины шейки матки [9] .
Лечение дисплазии при беременности
В большинстве случаев лечение должно быть отложено на послеродовый период. При беременности на фоне дисплазии шейки матки каждые три месяца проводится кольпоскопический и цитологический контроль. При выявлении рака шейки матки пациентку консультирует онкогинеколог. Доктор подбирает тактику лечения, может потребоваться прервать беременность по онкологическим показаниям [9] .
Прогноз. Профилактика
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
- курение;
- длительное использование гормональных контрацептивов;
- многократные травматичные роды;
- ВИЧ-инфекция.
- У пациенток с ЦИН часто обнаруживают вирус простого герпеса 2 типа, цитомегаловирусную инфекцию, хламидийную урогенитальную инфекцию, бактериальный вагиноз, ассоциированный с резким снижением или отсутствием вагинальной лактофлоры, повышенным ростом во влагалище Gardnerella vaginalis и Atopobium vaginae, повышение концентрации в бакпосеве грибов рода Candida, Mycoplasma hominis.
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения", осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Врожденный ихтиоз – гетерогенная группа наследственных заболеваний, для которых характерны мутации генов, отвечающих за правильное развитие кожи, следствием чего являются специфические поражения дермы и другие системные патологии. Основные симптомы – очаги усиленного шелушения кожи, образование плотных чешуек с болезненными бороздками между ними, склонность к гиперпирексии, системное поражение внутренних органов, дефекты лица. Врожденный ихтиоз диагностируется клинически, подтверждается результатами биопсии кожи. В лечении используются препараты ретиноидов и кератолитики, также проводится неспецифическая терапия.
МКБ-10
Общие сведения
Врожденный ихтиоз – наследственный дерматоз, характеризующийся нарушением процессов ороговения. Точное описание болезни дал Роберт Виллан в 1808 году, термин «ихтиоз» предложен В. Вилсоном в 1852 году и используется в настоящее время. Частота встречаемости врожденного ихтиоза варьирует в зависимости от формы заболевания и составляет в среднем 1:2000 для простого ихтиоза, 1:4000 для Х-сцепленного ихтиоза, 1:100000 для эпидермолитического ихтиоза, 1:300000 для ламеллярного ихтиоза. Половых различий не выявлено, кроме Х-сцепленной формы врожденного ихтиоза, которая диагностируется только у мальчиков. Актуальность проблемы в педиатрии связана с часто запоздалой диагностикой и временным эффектом от лечения. Врожденный ихтиоз – одна из причин детской инвалидности.

Причины врожденного ихтиоза
Врожденный ихтиоз всегда является следствием мутаций в генах, отвечающих за правильное развитие эпителия. Мутировавшие гены передаются из поколения в поколение, то есть заболевание наследуется. Первичные причины самих мутаций достоверно неизвестны, но могут быть связаны с тератогенными факторами и факторами внешней среды. Простой и эпидермолитический ихтиоз наследуются по аутосомно-доминантному типу, ламеллярный – по аутосомно-рецессивному типу. При Х-сцепленном ихтиозе мутация происходит в гене, сцепленном с половой хромосомой, механизм наследования рецессивный.
В случае простого ихтиоза нарушен синтез филаггрина – белка, отвечающего за соединение нитей кератина между собой. Именно кератин способствует удержанию влаги кожей, и в данном случае нарушается эта его функция. Х-сцепленный врожденный ихтиоз характеризуется недостаточностью стеролсульфатазы, вследствие чего кератиноциты оказываются прочно связанными с подлежащими слоями кожи, ввиду чего нарушается их своевременное отторжение. Ламеллярный ихтиоз связан с недостаточностью трансглутаминазы-1, которая принимает участие в ороговении оболочек клеток кожи, и ускоренным продвижением кератиноцитов к поверхности кожи, то есть быстрой их сменой. Следствием являются обширные воспалительные процессы, нарушения терморегуляции и высокий риск вторичных инфекций.
В основе эпидермолитического ихтиоза – нарушение синтеза кератина, из-за чего клетки кожи становятся нестабильными. Это способствует образованию буллезных пузырей, характерных для этого типа врожденного ихтиоза. Редко встречающийся ихтиоз плода развивается внутриутробно и обусловлен нарушением транспорта липидов, вследствие чего нарушается барьерная функция кожи.
Классификация врожденного ихтиоза
Существует несколько классификаций заболевания по различным признакам. В зависимости от типа наследования врожденный ихтиоз может быть:
- Аутосомно-доминантным (простой и эпидермолитический ихтиоз);
- Аутосомно-рецессивным (ламеллярный ихтиоз, ихтиоз плода);
- Х-сцепленным (Х-сцепленный ихтиоз).
Различаются условия, необходимые для проявления заболевания. Первые два типа не связаны с полом, мутировавший ген должен быть представлен в доминантной и рецессивной форме соответственно. Х-сцепленный ихтиоз наследуется рецессивно, проявляется у мальчиков, в то время как девочки являются носителями мутации.
Клинически выделяют следующие типы врожденного ихтиоза: простой (вульгарный), ламеллярный, Х-сцепленный, эпидермолитический, ихтиоз плода. В зависимости от тяжести клинических проявлений ихтиоз может быть тяжелым, средней тяжести и поздним (проявляется не сразу после рождения). Врожденный ихтиоз может быть не только самостоятельным заболеванием, также он присутствует в структуре некоторых синдромов, таких как синдром Нетерсона, синдром Рефсума, синдром Руда, синдром Шегрена-Ларссона и некоторые другие. Также существуют ихтиозиформные заболевания, например, гиповитаминоз А, сенильный ихтиоз и др. В этих случаях клиника схожа, но причины другие.
Симптомы врожденного ихтиоза
Симптоматика напрямую зависит от формы заболевания. В клинике простого ихтиоза всегда имеет место выраженная сухость кожи и шелушение. Зоны поражения располагаются на разгибательных поверхностях суставов, особенно ног. Лицо остается нетронутым, за редким исключением, когда в процесс вовлекается кожа лба и щек. Также характерен фолликулярный гиперкератоз – скопление кератина в фолликулах волос. Возникает почти на всей поверхности кожи, где растут волосы. Обнаруживается при пальпации в виде так называемого симптома «тёрки». Кожа на ладонях и подошвах утолщена, усилен кожный рисунок, выделяются бороздки между участками утолщенной кожи. У больных отмечается снижение потоотделения, что является причиной частой гипертермии.
Основные симптомы врожденного ихтиоза проявляются с 3-12 месяцев жизни ребенка. Шелушение кожи часто практически нивелируется к 20-25 годам. При этом остаются характерные для этой формы заболевания изменения ладоней и подошв. Часто врожденный ихтиоз данного типа сопровождается аллергическими заболеваниями в виде ринита, крапивницы, бронхиальной астмы. В большинстве случаев характерно поражение желудочно-кишечного тракта: гастрит, колит, дискинезия желчных путей, гепатоспленомегалия. На клеточном уровне изменения идентичны таковым в клетках кожи.
Х-сцепленный врожденный ихтиоз проявляется в первые месяцы жизни и только у мальчиков. Характерное поражение кожи – крупные, грязно-коричневого цвета чешуйки без шелушения. Локализация подобных участков может быть практически любой, кроме области ладоней и стоп. Такой цвет чешуек обусловлен высокой концентрацией меланина в нижних слоях эпидермиса. Из других признаков часто обнаруживается специфическое помутнение роговицы в форме цветка без влияния на остроту зрения. У пятой части пациентов диагностируется крипторхизм. В отличие от простого ихтиоза, поражения кожи при данном типе заболевания практически не уменьшаются с возрастом.
Ламеллярный ихтиоз проявляется с рождения. Кожа новорожденного покрыта тонкой, но плотной пленкой - это патогномоничный симптом врожденного ихтиоза данного типа. Постепенно пленка трансформируется в крупные толстые чешуйки от светлого до коричневого цвета. Вследствие закупорки потовых желез нарушено потоотделение, поэтому часто наблюдается гиперпирексия. На ладонях и подошвах – глубокие трещины и кератодермия. Бороздки между чешуйками болезненны и являются воротами для вторичной бактериальной инфекции, включая сепсис. Ламеллярный врожденный ихтиоз сопровождается дефектами развития: часто отмечается выворот век (эктропион) и губ (экслабион), деформация или отсутствие ушных раковин, деформация хрящей носа, сращение фаланг пальцев либо отсутствие концевых фаланг и др.
Эпидермолитический врожденный ихтиоз проявляется обширной влажной эритродермией с формированием буллезных пузырей. На месте вскрытия пузырей остаются эрозии, которые бесследно проходят. Со временем присоединяется грубое ороговение, часто образуются бородавки. Ороговевшие чешуйки темные, с неприятным запахом (следствие вторичной инфекции). Слизистые оболочки при данном типе врожденного ихтиоза не поражаются, потоотделение также не нарушено. Тем не менее, эта форма заболевания очень опасна и может сопровождаться смертельным исходом.
Врожденный ихтиоз плода – самая редкая форма заболевания, развивается внутриутробно на 16-20 неделе беременности. Дети рождаются недоношенными, кожа их напоминает панцирь, который вскоре трескается с образованием крупных пластинчатых чешуек, чаще темных. Характерно почти полное отсутствие волос на голове, кератодермия ладоней и подошв. Из-за сильного ороговения кожи лица рот постоянно открыт, выражены эктропион и экслабион, ушные раковины деформированы. При врожденном ихтиозе плода часто диагностируется нейросенсорная тугоухость. Сниженный иммунитет способствует развитию бактериальных инфекций уже в первые дни жизни; часто встречаются отиты, пневмония, подкожные абсцессы. Высока смертность в первые дни и недели жизни.
Диагностика врожденного ихтиоза
Во время беременности с целью диагностики можно использовать амниоцентез с последующим анализом амниотической жидкости, а также биопсию ворсин хориона. Однако инвазивные методы повышают риск самопроизвольного прерывания беременности, поэтому на практике используются крайне редко. Показанием для пренатальной биопсии является отягощенный анамнез по врожденному ихтиозу. УЗИ в III триместре позволяет диагностировать ихтиоз плода. Заметно фиксированное положение рук и открытый рот, можно увидеть гипоплазию носовых хрящей и неспецифические признаки в виде многоводия и повышенной эхогенности амниотической жидкости. Остальные формы врожденного ихтиоза можно лишь заподозрить.
После рождения ребенка диагноз ставится педиатром, в первую очередь, на основании клинических симптомов, характерных для врожденного ихтиоза. Это специфическое шелушение кожи, локализация пораженных участков, симптом «тёрки» при простом ихтиозе, выраженная эритродермия при эпидермолитическом ихтиозе и др. Изменения в анализах неспецифичны, но могут выявить аллергические процессы (часто сопутствуют ихтиозу), высокий уровень холестерола и одновременно сниженный уровень эстриола в крови (при Х-сцепленном ихтиозе). Имеет значение анамнез родителей: выявленные прежде случаи врожденного ихтиоза, в том числе его синдромные формы.
Часто клиническая картина заболевания неспецифична, поэтому обязательно проведение дифференциальной диагностики. Необходимо исключать приобретенные формы ихтиоза, дерматозы (псориаз, экзема, контактный дерматит, врожденный сифилис и др.), атопический дерматит. Так, для дерматитов характерно наличие воспалительного процесса, зуда, экземы и др. Однако часто врожденный ихтиоз также сопровождается дерматитом. Дерматозы имеют свои патогномоничные симптомы, отсутствующие при ихтиозе, например, зубы Гетчинсона при врожденном сифилисе, специфические папулы с излюбленной локализацией при псориазе и т. д. Приобретенные формы ихтиоза развиваются вследствие аутоиммунных, инфекционных заболеваний, опухолей и др., в этом случае нужно искать причину, способную вызвать патологию уже после рождения.
Лечение врожденного ихтиоза
Лечение заболевания проводится в стационаре, в случае тяжелых форм врожденного ихтиоза – в отделении реанимации. В помещении должна поддерживаться высокая влажность и пониженная температура воздуха. Обычно показана гипоаллергенная диета, в тяжелых случаях – питание через зонд. Рекомендуется принимать ванны от 2 раз в день. Это позволяет увлажнить кожу, уменьшить шелушение и провести профилактику вторичных инфекций. В случае эпидермолитического врожденного ихтиоза во время купания часто используются антисептики. После купания, как правило, проводят механическое отшелушивание с последующим нанесением увлажняющего крема.
Применяется системная терапия врожденного ихтиоза препаратами витамина А и ретиноидами, которые облегчают отшелушивание ороговевших клеток и снижают скорость пролиферации клеток, иными словами, тормозят их усиленный рост. Кроме того, ретиноиды оказывают противовоспалительное и иммуномодулирующее действие. В педиатрической практике в настоящее время используется тигазон, неотигазон. Очевидна высокая клиническая эффективность данных препаратов, однако эффект от лечения временный, а терапия проводится курсами ввиду множества побочных эффектов: сухость и кровоточивость слизистых, гиперостоз, нарушений функций печени, фотосенсибилизация кожи и высокая чувствительность к свету и др.
К современным препаратам относятся блокаторы метаболизма ретиноевой кислоты, например, лиарозол. При лечении отмечается тот же клинический эффект, но безопасность намного выше. Основу наружной терапии врожденного ихтиоза составляют кератолитики: растворы хлорида натрия и мочевины, декспантенол, салициловая кислота, топические ретиноиды. Средства наносятся на пораженные участки кожи и оказывают местное действие, способствуя отшелушиванию, смягчению кожи, уменьшению воспаления и др. При назначении кератолитиков необходимо учитывать возраст ребенка, поскольку некоторые из них (мочевина, салициловая кислота) токсичны для детей первого года жизни.
В лечении тяжелых форм врожденного ихтиоза применяются системные кортикостероиды, иммуноглобулины, а также антибиотики в случае необходимости. Обязательна консультация детского офтальмолога при диагностике эктропиона, детского оториноларинголога – при деформации и отсутствии ушной раковины, а также для диагностики и лечения нарушений слуха, в частности нейросенсорной тугоухости. При синдромальных формах врожденному ихтиозу часто сопутствуют неврологические нарушения, в этих случаях обязательна консультация детского невролога. Также к лечению подключается генетик для планирования последующих беременностей и расчета вероятности заболевания у будущих поколений.
Прогноз и профилактика врожденного ихтиоза
Прогноз зависит от формы заболевания. Клинические проявления простого ихтиоза минимизируются после 20-25 лет, однако качество жизни все равно снижается из-за наличия системных патологий желудочно-кишечного тракта. Тяжелые формы врожденного ихтиоза часто являются причиной смерти и детской инвалидности.
Генетическое консультирование – единственный способ профилактики врожденного ихтиоза. Необходимо планировать беременность в случае отягощенного анамнеза по данному заболеванию, то есть, если один и тем более оба родителя больны, либо кто-то из них является носителем мутации. В этом случае рекомендуется отказ от беременности, но в любом случае окончательно решение принимает семья. Как вариант, парам предлагается ЭКО и усыновление.

Следствием мутации некоторых групп генов становится тяжелая болезнь – ихтиоз. Так называют патологическую трансформацию эпидермиса, в результате которой поверхность кожи покрывается твердыми чешуйками. Степени и формы ороговения варьируют от легкой шероховатости до образования плотного слоя ороговевшего эпидермиса.
Почему развивается заболевание
Патология носит наследственный характер, а главной причиной ихтиоза является мутация некоторых групп генов, которая передается детям от родителей. В редких случаях заболевание является приобретенным и становится следствием недостатка витаминов, проявлением некоторых болезней крови и др.
У больных отмечается нарушение метаболизма белков и аминокислот, в эпидермисе усиливается активность окислительных ферментов, понижается концентрация иммуноглобулинов. Этиология и патогенез до сих пор недостаточно изучены, но многие исследователи отмечают важную роль недостаточности витамина А и функции некоторых желез – щитовидной, надпочечников.
У пациентов с генетической формой ихтиоза, как правило, замедляются обменные процессы, нарушается терморегуляция, плохо работают потовые железы. Высокий уровень ферментов приводит к существенному усилению кожного дыхания. Клеточный и гуморальный иммунитет часто понижен. Нередко гиперкератоз сопровождается эндокринными заболеваниями, болезнями надпочечников и репродуктивной сферы, глазными заболеваниями. Часто у больных усиливается ломкость волос и ногтей, зубы легко поражаются кариесом.
В кожных покровах присутствует чрезмерное количество структурно измененного кератина. Из-за замедления метаболических процессов старые клетки кожи отторгаются недостаточно быстро, что приводит к образованию на поверхности кожи твердых чешуек. Между слоями клеток кожи скапливаются аминокислотные комплексы, ускоряющие процесс затвердения и ороговения, а также скрепляющие чешуйки между собой.
Клинические проявления

Основной симптом ихтиоза – характерные твердые чешуевидные образования на сухой коже – проявляется уже на первом году жизни, гораздо реже – в течение нескольких последующих лет. Кожа ребенка становится шершавой, на ней появляются прозрачные, белесые или сероватые чешуйки, прилегающие друг к другу. Чистыми остаются только локтевые сгибы, впадины под коленями и подмышечные зоны, а также область паха. Ладони и стопы шелушатся, на них ярко выделяется рисунок кожи. В наиболее легких случаях болезнь проявляется лишь небольшим шелушением и сухостью кожи.
В настоящее время насчитывается более пятидесяти клинико-морфологических форм заболевания, однако во всех случаях присутствуют следующие проявления:
- роговой слой эпидермиса утолщен, на нем формируются чешуйчатые образования и зоны ороговения;
- кожа сухая и шелушащаяся, сальные железы практически не работают;
- ногтевые пластины расслаиваются или ломаются, в ряде случаев деформированы и напоминают птичьи когти, отслаиваются от мягких тканей;
- кожный рисунок становится более глубоким и выразительным;
- присутствуют высыпания разной формы и окраски.
Ихтиоз кожи, как правило, обостряется с наступлением холодов. В теплое время обычно наступает ремиссия. Во время полового созревания у подростков болезненные проявления уменьшаются, чтобы вновь вернуться во взрослом возрасте.
Разновидности патологии
Более чем у 90% пациентов развивается вульгарный ихтиоз – заболевание, которое впервые проявляется уже на втором или третьем месяце жизни. В зависимости от характера поражения кожи выделяют следующие клинические формы:
- ксеродермию, или абортивную форму – наиболее легкий вариант болезни, при котором кожа становится сухой и шершавой, но чешуйчатые наслоения отсутствуют;
- простую форму с небольшими чешуйками, тонкими по краям и с уплотненным центром, которыми покрывается все тело вплоть до волосистой части головы;
- блестящую форму с прозрачными чешуйками, расположенными в виде мозаики преимущественно на ногах;
- белую форму с белыми либо слегка желтоватыми чешуйками, внешне похожими на асбестовые волокна;
- змеевидную форму с грубыми ороговениями коричневого, бурого или серого цвета, напоминающими змеиную чешую.
Намного реже встречается ламеллярная форма заболевания (коллодийный плод), фетальная (плод Арлекина), линеарная и т. д. Некоторые из них несовместимы с жизнью – так, фетальный ихтиоз формируется еще во втором триместре внутриутробного развития, и ребенок гибнет в первые дни жизни либо рождается уже мертвым.
Как определяют заболевание
Для первичной диагностики ихтиоза, как правило, бывает достаточно внешних проявлений заболевания. Чтобы отличить его от других кожных заболеваний, назначают гистологическое исследование эпидермиса.
При наличии случаев заболевания в семье проводится пренатальная диагностика: между 19 и 21 неделями развития у плода забирают биопсию эпидермиса.
Можно ли излечить?

На текущем этапе развития медицина еще не умеет справляться с генетическими заболеваниями, поэтому современное лечение ихтиоза направлено на уменьшение клинических проявлений и облегчение состояния пациента. Для этого назначают:
- витаминные комплексы, железосодержащие составы, иммуноглобулин;
- переливания плазмы крови;
- гормонотерапию (в сложных случаях);
- ванны с добавлением различных препаратов, смягчающие мази и кремы;
- физиопроцедуры, курортное лечение по показаниям.
Выбор лечебных методик зависит от степени поражения кожи и особенностей протекания болезни.
Часто возникающие вопросы
Как наследуется ихтиоз от больных родителей?
Заболеванию одинаково подвержены как мужчины, так и женщины, но некоторые формы развиваются преимущественно у детей одного пола. Генная мутация наследуется в 97% случаев, если хотя бы один из родителей болен ихтиозом.
Передается ли ихтиоз при контактах с больным?
Ихтиоз – заболевание генетического характера, поэтому люди, которые им болеют, абсолютно не заразны и не могут передавать свою патологию иначе, чем наследственным способом, т.е. собственным детям.
Как живется людям с ихтиозом?
При ихтиозе показано пребывание в теплом и влажном климате, здоровое разнообразное питание с большим количеством витаминов. Чтобы уменьшить проявления болезни и продлить ремиссию, необходимо:

Гиперкератоз – общее название для группы патологий, основным признаком которых служит неумеренное ороговение кожи. Клетки внешнего, рогового слоя под действием определенного фактора активизируют процесс деления, при этом слущивание отмерших клеток замедляется. В результате кожа покрывается роговым слоем, толщина которого варьирует от долей миллиметра до нескольких сантиметров. Ороговению могут подвергаться любые участки тела, в зависимости от причин патологии.
Разновидности процесса ороговения
Различают наследственный и приобретенный гиперкератоз кожи. В зависимости от клинических проявлений, патология может принимать различные формы:
- фолликулярную – чешуйки отслаивающейся кожи закупоривают протоки фолликулов, из-за чего на коже появляются многочисленные мелкие бугорки, похожие на прыщики;
- лентикулярную – на волосяных фолликулах нижних конечностей появляются роговые папулы, при их удалении на коже остаются небольшие углубления;
- диссеминированную – на коже появляются образования, напоминающие короткие и утолщенные волоски;
- себорейную – на волосистой части головы, иногда на коже лица образуются участки шелушения в виде жирной, легко удаляемой корки, под которой обнаруживаются красноватые пятна кожи;
- диффузную – поражаются большие участки кожи на любых частях тела, иногда даже вся кожа полностью, сальные железы перестают работать, кожа иссушается и шелушится;
- бородавчатую – на коже появляются образования, напоминающие бородавки, но без участия папилломавируса, причем иногда они перерождаются в опухоли;
- старческую – на коже пожилых людей появляются темные ороговевшие пятна.
Диссеминированная и лентикулярная формы, как правило, развиваются у пожилых мужчин. Женщин и молодежь они поражают крайне редко.
Симптоматика

Основным симптомом гиперкератоза служит появление на каких-либо участках тела утолщений кожного покрова с пониженной чувствительностью, нередко с измененным цветом, отличающимся от основного оттенка. В начальной стадии кожа производит впечатление огрубевшей, затем толщина ороговевшего слоя увеличивается, иногда до такой степени, что начинает доставлять дискомфорт. В частности, запущенный гиперкератоз стоп может привести к изменению походки. Ороговевшая кожа шелушится или частично отслаивается, на наиболее утолщенных и сухих участках могут появляться болезненные трещины, которые долго заживают и становятся местами проникновения инфекции. Часто патология сопровождается сухостью кожи, снижением функции сальных желез.
Причины развития патологии
Все вызывающие развитие кератоза причины можно разделить на две группы. В первую входят внешние воздействия – тесная обувь или натирающая определенные участки кожи одежда, интенсивный физический труд, постоянный контакт с химическими реагентами или другими веществами, негативно воздействующими на кожу, несоблюдение правил гигиены и т. д.
Вторая группа включает заболевания и патологические состояния, которые приводят к чрезмерному образованию рогового слоя:
- системные нарушения, врожденные либо приобретенные – ихтиоз, сахарный диабет, псориаз, кератодермия и др.;
- нарушения кровообращения, наиболее часто возникающие в нижних конечностях, – варикозная болезнь, облитерирующий атеросклероз;
- недостаток витаминов;
- грибковые заболевания кожи (лишай) и стоп;
- желудочно-кишечные заболевания;
- стрессы;
- лишний вес, патологии стопы, хромота.
Под влиянием тех или иных факторов в верхнем слое кожи нарушается капиллярное кровоснабжение, ухудшается иннервация. Из-за этого активизируется процесс деления клеток рогового слоя с одновременным замедлением их слущивания и образованием утолщенных ороговевших участков.
Диагностические методы
Как правило, при гиперкератозе диагностика заключается в выявлении заболевания, которое привело к образованию ороговевших участков. Дерматолог проводит наружный осмотр и опрос пациента, проверяет, нет ли признаков кожных заболеваний. Как правило, квалифицированный специалист может распознать заболевание по внешним признакам. Для уточнения может понадобиться дифференциальная диагностика, которая необходима при сходстве проявлений патологии с другими кожными заболеваниями, для которых тоже характерны шелушение и сухость кожи. При затруднениях с определением диагноза проводят биопсию пораженного участка кожи с гистологическим исследованием ткани.
Лечение
Метод лечения гиперкератоза зависит от формы заболевания и от причины, которая его вызвала. Как правило, в периоды обострения показано местное применение кортикостероидных мазей, которые снимают воспаление и отшелушивают ороговевшую кожу. Мягкий кислотный пилинг при помощи специальных кремов помогает освободиться от затвердевших слоев кожи. Механическое удаление огрубевших участков не рекомендуется, так как из-за него образование рогового слоя может усилиться. Хороший эффект дают теплые ванны с добавлением соли, пищевой соды либо крахмала, после которых на кожу наносят увлажняющий крем.
Гиперкератоз кожи головы лечат при помощи смягчающих компрессов, для которых используют касторовое масло, вазелин или глицерин, рыбий жир и т. д. При необходимости могут быть назначены мази с содержанием гормонов. При фолликулярной форме заболевания наружное лечение пне приносит большой пользы, поэтому терапия направлена на устранение нарушений в работе организма.
При гиперкератозе кожи стоп необходимо вначале устранить фактор, вызывающий патологию. Часто в роли патологического фактора выступает грибок кожи, от которого избавляются при помощи специальных противогрибковых мазей. Хороший эффект дают ножные теплые ванночки с поваренной солью, после которых распаренный ороговевший слой снимают при помощи пемзы, а кожу смазывают смягчающим кремом. Необходимо выбрать удобную обувь, которая не сдавливает и не натирает стопу. Если пациент страдает косолапостью или плоскостопием, следует позаботиться о выборе специальной обуви.
Профилактика
Чтобы не допустить повторного развития гиперкератоза, необходимо ухаживать за кожей, обеспечивать ее питание и гигиену. Предупредить рецидивы заболевания помогут:
- нормализация питания, обеспечение разнообразного сбалансированного рациона;
- отказ от длительного пребывания на солнце или переохлаждения кожи;
- соблюдение гигиены, уход за кожей;
- использование защитных средств при работе с химическими реагентами.
Некоторые формы заболевания крайне тяжело поддаются лечению и остаются с человеком в течение всей жизни. В этом случае особенно важно уделять внимание профилактическим мерам, которые снижают риск рецидивов.
Вопросы и ответы
Какой врач лечит гиперкератоз?
По поводу диагностики и лечения гиперкератоза следует обратиться к дерматологу. Если речь идет о заболевании стоп, то желательно проконсультироваться у подолога. В ходе лечения, возможно, придется обратиться к флебологу, эндокринологу или другим специалистам, в зависимости от выявленных заболеваний.
Как лечить гиперкератоз народными методами?
Домашние рецепты народной медицины при гиперкератозе помогают только на начальных стадиях и при легкой форме заболевания. Неплохой эффект дают смягчающие кожу аппликации с листьями алоэ, компрессы с прополисом или с отваром луковой шелухи. Можно использовать березовый деготь – действенное противовоспалительное средство, а также барсучий жир для смягчения потрескавшейся кожи.
Чем опасен гиперкератоз?
При отсутствии лечения могут развиться осложнения. Так, при ороговении кожи стоп у пациента нередко появляются трещины и натоптыши, а также высок риск заражения грибком. Бородавчатая форма патологии может оказаться предраковым состоянием кожи. Фолликулярная форма часто сопровождается пиодермией.
Читайте также:

