Что такое плоский эпителий в бронхах
Обновлено: 18.04.2024
Перестройка бронхиального эпителия при хроническом бронхите.
Определение непрямым методом Кунса иммуноглобулинов классов A, G, М показало их определенную динамику и изменение взаимоотношений между ними. Для первой формы, где взаимоотношения между клетками бронхиального эпителия относительно сохранены и имеются лишь признаки гиперсекреции, в инфильтрате преобладают лимфоциты, лазмоциты и гистиоциты. В плазматических клетках выявляется Ig A. Секреторный иммуноглобулин А локализуется в апикальных отделах реснитчатых клеток. Клетки, синтезирующие Ig M и Ig G, встречаются редко.
Вторая форма характеризуется нарастанием альтеративных изменений в бронхиальных клетках, изменением соотношения между ними в пользу гиперплазированных и гипертрофированных бокаловидных клеток, при интактных пока базальных клетках, сопровождается изменениями местного иммунитета. В инфильтрате, помимо лимфоцитов и плазматических клеток, появляются эозинофилы, тучные клетки, по-линуклеарные нейтрофилы. Число глобулинопродуцирующих клеток, с преобладанием Ig А, значительно увеличивается. В капиллярах активируются эндотелиоциты, которые выглядят гипертрофированными, в них появляются пиноцитозные пузырьки, цитоплазматические выросты. В процесс вовлекается железистый аппарат БВБ, где также отмечается гиперплазия и гипертрофия клеток с накоплением ШИК-положительной слизи в концевых отделах и выводных протоках, лимфоплазмоклеточная инфильтрация стромы желез. В слизистых клетках желез и в апикальной зоне реснитчатых клеток выявляется секреторный иммуноглобулин А.
В дальнейшем, при третьей форме, процесс гиперсекреции бокаловидных клеток переходит в их дистрофию. Практически полностью нарушается реснитчатый покров. Частично реснитчатые и бокаловидные клетки замещаются эпителиоцитами полигональной формы. В эпителии редки клетки, содержащие Ig А, в собственной пластинке слизистой оболочки доминируют плазмоциты, маркированные Ig G. В стенках мелких вен выявляются иммунные комплексы, Ig G и М. Авторы трактуют эти изменения как смену "первой линии защиты" - второй, где ситуацию контролирует Ig G, заменяющий Ig А. Способность Ig G комплексироваться с антигеном с активацией комплемента по классическому пути создает предпосылки для развития иммунокомплексной реакции. В этих условиях нарушение микроокружения базальных клеток, фиксируемое авторами, с изменением дифференцировки и регенерации покровного эпителия, является "существенным звеном в самоподдержании воспалительного процесса".
При четвертой форме у больных находят метаплазию эпителия бронхов в многослойный плоский, инфильтрат собственной пластинки слизистой оболочки - скудный, основу его составляют фибробласты, плазматические клетки и лимфоциты. Собственная пластинка слизистой оболочки бронхов склерозирована. Имеется периваскулярный склероз. Единичные плазматические клетки маркированы Ig А, превалируют клетки с Ig G в цитоплазме, в бронхиальном эпителии секреторный иммуноглобулин А отсутствует.
Таким образом, перестройка бронхиального эпителия при хроническом бронхите сопровождается утратой способности синтезировать секреторный иммуноглобулин А. Это снижает свойства слизистой оболочки (БВБ), тем самым создается порочный круг, в котором важную роль играет состояние местного иммунитета и иммуннопатологические реакции. Развитие работ этого направления внесло некоторые уточнения в характер распределения иммуноглобулинов, в целом подтвердив, что недостаточность местных гуморальных факторов связана с нарушением взаимоотношений в эпителиальном компоненте БВБ.
Не вступая в дискуссию по поводу некоторой условности деления описанного процесса на формы, следует отметить, на наш взгляд, важный факт системной перестройки бронховаскулярного барьера, всех его компонентов при развитии хронического воспаления.
Количественные и качественные изменения в представительстве иммунокомпетентных клеток, заселяющих стромальный компонент БВБ, являются отражением общих системных нарушений иммунитета, предваряющих и сопровождающих развитие и течение хронического бронхита. Убедительно показано наличие дисфункции центральных звеньев иммунитета, наличие тимической недостаточности со снижением количества Т лимфоцитов и их пролиферативной активности, обнаруживаемой тестами с фитогемаглютинином и конканавалином А, особенно при наличии обструктивного синдрома.
Недостаточность неспецифических механизмов, в частности фагоцитарного, определяется исходно сниженной функциональной активностью про- и моноцитов костного мозга у этих больных. Снижены фагоцитарная активность и индекс миграции лейкоцитов на фоне угнетенного энергетического метаболизма. Изменения затрагивают и трахеобронхиальные лимфатические узлы. Тяжелое течение хронического бронхита сопровождается меньшим содержанием плазматических клеток, маркированных иммуноглобулинами классов А и М.
Наши результаты по подсчету различных типов клеток-эффекторов иммунной системы, локализованных в БВБ на уровне дольки при хроническом бронхите без клинических признаков обострения показали, что инфильтрат формируется не только из лимфоцитов. Суммарно - до 15-20% от общего числа клеток приходится на плазматические, тучные клетки, нейтрофильные и эозинофильные лейкоциты. Изменен не только качественный состав хронической воспалительной реакции, меняется характер взаимоотношений, между клетками - эффекторами.
Анализ межклеточных корреляционных связей показал, что при хроническом воспалении бронхов утрачиваются одни и появляются новые варианты кооперативных отношений между клетками иммунной системы. В макрофагах и нейтрофилах высока активность ферментов пентозного шунта и снижена - ферментов гликолиза. В лимфоцитах регистрируется низкая активность одного из ключевых ферментов цикла Кребса - СДГ, более высокая, чем у здоровых людей, активность лизосомального фермента - кислой фосфатазы.
Реактивность организма и ферментативная активность иммунокомпетентных клеток коррелируют, по некоторым данным, с формой и степенью дыхательной недостаточности. Согласно иммунологическим тестам возможны три варианта течения хронического бронхита: с нормальной иммунологической реактивностью - катаральная форма; с селективным увеличением числа циркулирующих "ноль" лимфоцитов в сочетании с недостаточностью антител классов А и G - обструктивная форма; с Т иммунодефицитом, увеличением продукции "ноль" лимфоцитов и антител класса М при недостаточности иммуноглобулина А - длительно текущая обструктивная и гнойно-обструктивная форма.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Плоскоклеточный рак легкого – гистологический тип бронхопульмонального рака, возникающий в результате плоскоклеточной метаплазии бронхиального эпителия. Клинические проявления зависят от локализации опухоли (центральный или периферический рак легкого). Заболевание может протекать с кашлем, кровохарканьем, болью в груди, одышкой, пневмонией, плевритом, общей слабостью, метастазированием. Рак легкого диагностируется по данным рентгена, томографии, бронхоскопии; морфологическая диагностика основывается на результатах цитологического и гистологического анализа бронхоальвеолярных смывов, биоптатов. Лечение плоскоклеточного рака легкого – хирургическое и/или химиолучевое.
МКБ-10
Общие сведения
Плоскоклеточный (эпидермоидный) рак легкого – злокачественная опухоль, развивающаяся из метаплазированных клеток плоского эпителия бронхов. В норме в выстилке здоровых бронхов плоские эпителиальные клетки отсутствуют, поэтому развитию плоскоклеточного рака предшествует эпидермоидная метаплазия – процесс трансформации мерцательного эпителия в плоский. Плоскоклеточный рак легкого составляет более половины (около 60%) всех гистологических форм рака легкого. Он поражает преимущественно мужчин старше 40 лет. До 70% опухолей этого типа локализуется в корне легкого, в трети случаев выявляется периферический рак легкого. Актуальность плоскоклеточного рака легкого для клинической пульмонологии заключается, прежде всего, в его высокой распространенности и потенциальной устранимости факторов риска заболевания.
Причины
Причиной плоскоклеточной метаплазии и последующего развития опухолевого процесса является воздействие токсических веществ на слизистую оболочку бронхов. Большинство пациентов, заболевающих плоскоклеточным раком легкого, страдают многолетней никотиновой зависимостью, поэтому курение (в т. ч., пассивное) считается основным фактором риска данной патологии. В повреждении бронхов велика роль аэрогенных поллютантов, вдыхаемых с атмосферным воздухом (двуокиси серы, окиси углерода, диоксида азота, кислот, формальдегида, твердых частиц и пр.). К числу фоновых патологий, нередко предшествующих плоскоклеточному раку легких, относятся пневмокониозы, хронический бронхит, пневмония, туберкулез. Известно, что инфицированность некоторыми вирусами (цитомегаловерусом, вирусом папилломы человека) может вызывать атипическую метаплазию эпителия бронхов.
В норме стенки бронхов выстланы цилиндрическим мерцательным эпителием, на ресничках которого оседают мельчайшие примеси, содержащиеся во вдыхаемом воздухе. Движение (мерцание) ресничек обеспечивает удаление, изгнание вредных частиц из дыхательных путей, т. е. с их помощью реализуется механизм самоочищения бронхов. Под влиянием вредных аэрогенных нагрузок бронхиальный эпителий начинает видоизменяться, приспосабливаться к постоянным агрессивным воздействиям. Происходит постепенное исчезновение ресничек, изменение формы (уплощение) эпителиальных клеток и их кератинизация. В новых условиях легкие становятся открыты для проникновения инородных частиц, а постоянное скопление мокроты в бронхах способствует развитию хронических фоновых заболеваний. Некоторые исследователи рассматривают эпидермоидную метаплазию эпителия как раннюю, преинвазивную стадию плоскоклеточного рака легкого.
Классификация
Определяющими микроскопическими критериями плоскоклеточного рака легкого служат: признаки кератинизации, наличие межклеточных мостиков и формирование роговых жемчужин. На основании выраженности данных признаков судят о степени дифференцировки опухоли, выделяя высокодифференцированный (ороговевающий), умеренно дифференцированный (неороговевающий) и низкодифференцированный плоскоклеточный рак легкого.
Гистологически высокодифференцированная опухоль представлена пластами крупных клеток, с четко очерченными ядрами, выраженной кератинизацией клеток, межклеточными мостиками и роговыми жемчужинами. Умеренно дифференцированная форма рака также представлена крупными полигональными клетками, хорошо контактирующими друг с другом, имеющими развитую цитоплазму, но с меньшим количеством межклеточных мостиков; кератин определяется лишь в некоторых клетках. Низкодифференцированный плоскоклеточный рак легкого характеризуется преобладанием мелких клеток со слабо развитыми ядрами, органеллами и десмосомальными контактами.
Согласно анатомической классификации, различают периферический и центральный плоскоклеточный рак легкого; реже встречаются атипичные формы (диссеминированная, медиастинальная).
Симптомы
Клинические проявления в большей степени зависят не от гистологического типа и степени дифференцировки рака легкого, а от анатомической локализации опухоли, ее размера, характера роста и скорости метастазирования. Поэтому симптомы плоскоклеточного рака легкого в целом схожи с другими типами рака (крупноклеточным, мелкоклеточным, аденокарциномой).
У 5-15% пациентов ранние стадии рака протекают клинически бессимптомно; в этом случае опухоль может случайно обнаруживаться при флюорографическом обследовании. Все симптомы плоскоклеточного рака легкого делятся на первичные (местные), вторичные (вызванные осложнениями, метастазированием или раковой интоксикацией). Первичные симптомы, как правило, являются относительно ранними и связаны с ростом первичного опухолевого узла. Наиболее постоянные жалобы включают кашель, боли в грудной клетке, одышку. Кашель вначале сухой, надсадный; у половины больных с центральной формой рака легкого наблюдается кровохарканье, в поздних стадиях переходящее в легочное кровотечение.
По мере распространения опухолевого процесса к местным проявлениям плоскоклеточного рака легкого присоединяются вторичные симптомы. Они связаны как с местными осложнениями (осложнениями воспалительной природы, прорастанием или сдавлением соседних структур), так и с отдаленным метастазированием, а также общим воздействием на организм злокачественной опухоли. При развитии обтурационной пневмонии у больных возникает фебрильная лихорадка, влажный кашель с отхождением слизисто-гнойной мокроты. При компрессии или прорастании рядом расположенных органов может беспокоить дисфагия, осиплость голоса, синдром Горнера, интенсивные боли в шее и плече, аритмия.
Общие симптомы включают общую слабость, анорексию, снижение массы тела, кахексию. При эпидермоидном раке легкого могут развиваться гиперкальциемия и гипофосфатемия, обусловленные эктопической продукцией паратгормона и простагландинов. Экстраторакальные метастазы (в печень, кости, надпочечники, головной мозг) выявляются у половины пациентов, умерших от плоскоклеточного рака легкого.
Диагностика
Первичный комплекс диагностики включает в себя оценку анамнеза, жалоб, физикальное и рентгенологическое обследование. Рентгенография легких позволяет обнаружить рак легких в 80% случаев, установить размер опухоли и ее расположение, вовлеченность внутригрудных лимфоузлов. Для изучения распространения бронхопульмонального рака используется КТ органов грудной клетки.
С помощью бронхоскопии визуально подтверждаются или исключаются признаки опухолевого роста. Более детальное изучение клеточного состава производится при цитологическом анализе мокроты и бронхоальвеолярного смыва. Окончательная верификация гистологического статуса возможна только после проведения щипковой или трансбронхиальной биопсии опухоли и морфологического исследования биоптата. Плоскоклеточный рак требует дифференцирования от других видов злокачественных опухолей легкого, а также метастазов плоскоклеточного рака другой локализации.
Лечение
Планирование лечебной тактики при плоскоклеточном раке легкого основывается на знании локализации и распространенности процесса. При возможности радикального удаления опухоли прибегают к иссечению первичного очага и пораженных метастазами лимфатических узлов и клетчатки средостения. Объем резекции обычно составляет от лобэктомии до расширенной пневмонэктомии.
Химиолучевое лечение плоскоклеточного рака легких может осуществляться в рамках радикальной программы или с паллиативной целью. Облучению подвергаются как зоны расположения опухоли, так и зоны метастазирования. Полихимиотерапия (циклофосфан, винкристин, метотрексат) обычно используется в дополнение к лучевой терапии у неоперабельных пациентов. Симптоматическая терапия (дезинтоксикация, обезболивание, психологическая помощь) диктуется состоянием больного. Иммунохимиотерапия с использованием ингибиторов факторов роста и ангиогенеза является новым, но достаточно перспективным методом лечения плоскоклеточного рака легких.
Прогноз
Пятилетняя выживаемость после предпринятого лечения по поводу плоскоклеточного рака легкого составляет 60-80 %. При выявлении рака легкого на второй стадии этот показатель уменьшается до 40%, на третьей – до 15-18%. На прогноз существенно влияет степень дифференцировки плоскоклеточного рака легких – чем она ниже, тем меньше чувствительность опухоли к химиолучевому воздействию и раньше происходит ее метастатическое распространение. Медиана выживаемости больных при отсутствии лечения в среднем равняется 6-8 месяцам.
3. Плоскоклеточный рак легкого (значение клинико-морфологических и молекулярно-генетических характеристик опухоли в прогнозировании результатов хирургического лечения): Автореферат диссертации/ Лактионов К. К. – 2004.
Плоскоклеточный рак – это разновидность немелкоклеточного рака. На него приходится около 30% случаев злокачественных опухолей легких. Новообразование развивается из плоского эпителия, который образует слизистую оболочку бронхов. Плоскоклеточный рак встречается не только в легких, но и в других органах: коже, слизистой оболочке кишечника и др.
Ищете, где можно получить современное и эффективное лечение при раке легких? Обратитесь за помощью к специалистам Центра Комплексной Медицины: мы поможем подобрать подходящую клинику и врача. Свяжитесь с нами:8 (495) 215-50-60
Почему развивается плоскоклеточный рак легких?
Причины большинства онкологических заболеваний неизвестны, и рак легкого – не исключение. Опухоли дают начало клетки, в которых произошли некоторые мутации, но что именно к этому привело, сказать очень сложно. Известны лишь факторы, которые повышают вероятность развития заболевания. Их так и называют – факторы риска.
Из всех видов немелкоклеточного легких рака именно плоскоклеточный сильнее всего связан с курением. Вредно воздействие табачного дыма в любых формах: в виде сигарет, сигар, кальянов, трубок. Риск напрямую зависит от того, как долго человек является курильщиком, и сколько сигарет выкуривает ежедневно. Пассивное курение тоже опасно.
Другие факторы риска:
- Возраст. Чем старше человек, тем выше вероятность заболеть.
- Семейный анамнез: случаи заболевания у близких родственников.
- Воздействие пыли, асбеста, радона (газ, который образуется в почве при распаде урана и может накапливаться в помещениях) и некоторых других веществ.
Стадии плоскоклеточного рака легких
Стадию определяют в зависимости от размеров первичной опухоли, наличия раковых клеток в регионарных лимфатических узлах, отдаленных метастазов. При плоскоклеточном раке легкого выделяют четыре основные стадии:
- На первой стадии опухоль не больше 4 см в диаметре, не распространяется в регионарные лимфатические узлы, нет отдаленных метастазов.
- При плоскоклеточном раке легкого 2 стадии опухоль крупнее (до 7 см в диаметре), может распространяться на регионарные лимфоузлы.
- На 3 стадии опухоль сильнее прорастает в окружающие ткани, поражает большее количество лимфатических узлов.
- Четвертая стадия рака характеризуется наличием отдаленных метастазов.
Симптомы
На ранних стадиях рак зачастую не проявляется какими-либо симптомами. Позже начинает беспокоить упорный хронический кашель, во время которого может отходить мокрота с примесью крови, боли в грудной клетке, одышка, повышенная утомляемость. По мере прогрессирования рака и образования отдаленных метастазов присоединяются такие симптомы, как желтуха, нарушение пищеварения, тошнота и рвота, потеря веса (при метастазах в печени), боли в костях и патологические переломы (при метастазах в костях), головные боли и неврологические расстройства (при метастазах в головном мозге).
Зачастую из-за отсутствия симптомов рак легких диагностируется на поздних стадиях, когда лечить его уже сложно. В ранней диагностике помогают скрининговые исследования: флюорография, некоторым курильщикам с большим стажем стоит периодически проходить компьютерную томографию (этот вопрос нужно решить с врачом).
Методы диагностики
Обнаружить опухоль в легких помогает рентгенография грудной клетки. Более детальную картину помогают получить такие методы диагностики, как КТ, МРТ. Для того чтобы осмотреть слизистую оболочку бронхов, прибегают к эндоскопическому исследованию – бронхоскопии. Обнаружить метастазы помогают: ПЭТ-сканирование, рентгенография и радиоизотопное исследование костей, УЗИ органов брюшной полости и другие методы диагностики.
Для того чтобы подтвердить наличие раковых клеток в новообразовании, прибегают к биопсии, цитологическому исследованию мокроты.
Лечение плоскоклеточного рака легких
Выбор лечения зависит от многих факторов, один из самых главных – стадия рака. Чем ниже стадия, тем выше риск ремиссии. К сожалению, поздняя диагностика – весьма актуальная проблема при плоскоклеточном раке легкого. Зачастую, когда человек обращается за медицинской помощью, опухоль уже успевает сильно прорасти за пределы легких, дать метастазы. Но даже если ремиссия невозможна, это еще не означает, что больному нельзя помочь. Зачастую врачи могут существенно продлить жизнь пациента, сделать так, чтобы он не испытывал мучительных симптомов.
Хирургическое лечение
Цель радикальных операций при плоскоклеточном раке легкого – полностью удалить опухоль, так, чтобы в организме не осталось раковых клеток, которые могли бы привести к рецидиву.
Объем вмешательства напрямую зависит от того, насколько сильно успела вырасти опухоль. Но при этом нужно учитывать и состояние функции легких: чем она лучше, тем больше тканей может удалить врач, не боясь серьезных осложнений. Иногда нужно удалить все легкое целиком. В других случаях удаляют его долю, сегмент или небольшую часть – новообразование с некоторым количеством окружающей ткани.
Применяют при раке легкого и миниинвазивные методики. В некоторых случаях можно прибегнуть к видеоассистрированной торакальной хирургии (VATS), если это позволяет техническое оснащение и квалификация врачей клиники.
Лучевая терапия и химиотерапия при плоскоклеточном раке легких
Часто лучевая терапия и химиотерапия по отдельности или в сочетании дополняют хирургическое лечение. Терапия, которую проводят до операции, называется неоадъювантной. Она помогает уменьшить опухоль, что позволяет сократить объем хирургического вмешательства. Адъювантную терапию назначают после операции, она помогает предотвратить рецидив, так как убивает оставшиеся в организме раковые клетки.
При раке на поздних стадиях химиотерапию и лучевую терапию применяют в паллиативных целях. Они помогают затормозить рост опухоли, улучшить состояние больного, продлить жизнь. С помощью лучевой терапии можно уничтожать единичные метастатические очаги.
Новые методы лечения плоскоклеточного рака легких
Два современных направления в лечении онкологических заболеваний:
- Таргетные препараты. Они блокируют определенные молекулы-мишени, которые нужны для роста и выживания злокачественных опухолей.
- Иммунопрепараты также воздействуют на молекулярные механизмы, помогают снять блок с иммунной системы, который мешает ей атаковать опухолевую ткань.
Оба эти вида лечения применяются при раке легких. В некоторых случаях они помогают на поздних стадиях, когда другие методы лечения неэффективны.
Прогноз при плоскоклеточном раке легких
Основной показатель для оценки прогноза – пятилетняя выживаемость или количество пациентов, которые остаются живы спустя пять лет после того, как установлен диагноз. Пятилетняя выживаемость при плоскоклеточном раке легкого, как и при других онкологических заболеваниях, зависит от стадии:
Роль эпителия бронхов при воспалении.
Этот фрагмент не претендует на полноту, поскольку некоторые вопросы, рассматриваемые в других разделах сайта, в частности, роль лимфоцитов в воспалении, описывается в статьях, посвященных роли иммунной системы.
Эпителий бронхов. Большую роль в развитии воспаления бронхов играет повреждение эпителия. Функции его многообразны: во-первых, в эпителии находятся наиболее эффективные антиген-презентирующие дендритные клетки, которые после поглощения антигена мигрируют в региональные лимфоузлы, где контактируют со специфическими Т-лимфоцитами; во-вторых, клетки эпителия экспрессируют разнообразные рецепторы, благодаря которым с эпителиоцитами связываются различные БАВ, клетки воспаления, бактерии и; в-третьих, эпителиоциты активно продуцируют медиаторы, в частности, провоспалительные цитокины, поддерживающие хроническое воспаление.
Велика роль эпителия в регуляции экссудации плазмы в просвет бронхов: клетки эпителия, как и другие типы клеток, продуцируют вазоактивные медиаторы экссудации, включая различные лейкотриены (ЛТ), прежде всего ЛТД4, и фактор активации тромбоцитов (ФАТ), причем, первоначальная экссудация имеет защитное действие, поскольку плазма образует гель, который защищает обнаженную мембрану, поэтому имеется связь между степенью повреждения эпителия (аллергеном, поллютантом, бактерией) и выраженностью плазменной экссудации.
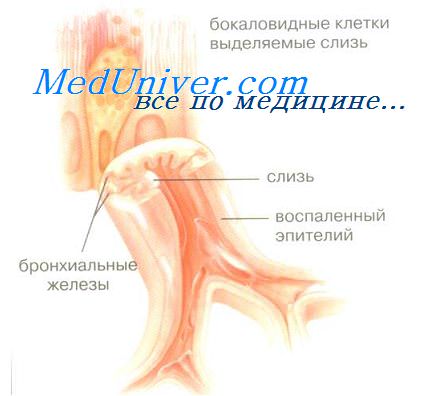
Эпителий продуцирует много провоспалительных цитокинов благодаря выраженной метаболической активности, в частности, метаболит арахидоновой кислоты 15-НЕТЕ (15-гидроксиейкозатетраеновая кислота), который стимулирует продукцию слизи и активирует 5-липоксигеназный путь обмена в тучных клетках, простагландины Е, и F2a, GM-CSP (гранулоцитарно-макрофагаяьный колониестимулируюший фактор), активирующий альвеолярные макрофаги, гранулоциты и базофилы, GCSP (гранулоцитарный колониестимулирующий фактор), интерлейкины (ИЛ), в частности ИЛ-1, ИЛ-6 и ИЛ-8 - хемоаттрактант и активатор эозинофилов и нейтрофилов. Одним из главных хемоаттрактантов, выделяемых эпителием со специфическим привлечением моноцитов - МСР-1 (моноцитарный хемоаттрактантный пептид-1). Эпителий бронхов выделяет также другие медиаторы воспаления: эндотелии-1,- активный вазо- и бронхоконстриктор и активатор фибробластов, цитокины группы RANTES из подсемейства полипептидов В или "С-С" (Regulated on Activation, Normal T-cell Expressed and Secreted), привлекающие эозинофилы, различные факторы роста (PDGE - пластиночный фактор роста, BFGF - основной фактор роста фибробластов, IGE - инсулиноподобный фактор роста),- все из них способны принимать участие в ремоделировании дыхательных путей.
В последнее время большое внимание уделяется выделению эпителием бронхов окиси азота (N0), которая обладает вазо- и бронходилатирующим действием и ее концентрация по-разному изменяется при различных легочных болезнях.
Важным в генезе воспаления является экспрессия различных молекул, прежде всего, молекул адгезии ICAM-I (intercellular adhesion molecnle-I), необходимая для транспорта нейтрофилов и эозинофилов через слизистую в просвет дыхательных путей, а также рецепторов автономной нервной системы, что указывает на влияние автономной нервной системы на функции эпителия и формирование нейрогенного воспаления. Помимо адренорецепторов, мускариновых холинорецепторов (в основном, М3), в последнее время интенсивно изучаются VIP-рецепторы (рецепторы вазоинтестинального пептида), возбудитель которых - VIP -сходен по действию с агонистами и дефицит которого может играть важную роль в патогенезе БА; тахикининовые рецепторы, которые с высокой плотностью находятся на эпителии и опосредуют действие мощных провоспалительных медиаторов - вещества П и нейрокинина А; а также большое количество медиаторных рецепторов, посредством которых различные БАВ модулируют метаболическую активность эпителиоцитов, стимулируют экспрессию других видов рецепторов или, наоборот, тормозят ее.
Таким образом, эпителиоциты действуют как трансдукторы между различными сигналами, возникающими в просвете бронха и на поверхности эпителия, и воспалительными событиями в стенке бронха, причем в нормальных условиях эпителий поддерживает баланс между про- и противовоспалительными эффектами.
При нарушении эпителиального покрова этот баланс нарушается в пользу преобладания провоспалительных эффектов, в просвет бронхов выходят клетки воспаления и жидкая часть плазмы, и при определенных условиях процесс может принять хроническое персистирующее течение.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Лабораторная диагностика легочных и бронхиальных заболеваний основана на исследовании мокроты, бронхиального аспирата, материала щеточной и катетерной биопсии, трансбронхиальной и трансторакальной пункционной аспирационной биопсии, которые составляют обширный раздел практической цитологии [1]. Клиническая цитология - признанный полноценный метод морфологического анализа, основанный на изучении и оценке клеточного материала, полученного различными способами из патологического очага. К преимуществам цитологического исследования мокроты в амбулаторной практике относят ее простоту, быстроту, легкую повторяемость. Последнее позволяет использовать цитологический анализ для изучения динамики морфологических изменений в течение заболевания и в процессе лечения. Кроме того, цитологическое исследование не требует больших материальных затрат, недороги реактивы и оборудование. Все вышеизложенное позволяет широко использовать метод как для морфологической верификации в условиях поликлиники, так и для проведения массовых профилактических осмотров, выбора групп риска с последующим систематическим наблюдением за лицами входящими в группы риска.
Слизистый характер бронхиального секрета обусловлен сочетанным функционированием желез подслизистой оболочки бронхов и бокаловидных клеток эпителия. В ответ на инвазию инфекционными агентами эпителий бронхов выделяет цитоки- ны IL-8, IL-6, колониеобразующие факторы гранулоцитов, моноцитов, и др. Так, тучные клетки выделяют хемотаксические факторы «быстрого реагирования»: эозинофильный хемотаксический фактор анафилаксии; хемотаксический фактор нейтрофилов высокой молекулярной массы; хемотаксические факторы, направленные на лимфоциты, базофилы, моноциты; фактор, активирующий тромбоциты (ФАТ). Усиливается синтез и выделение простогландинов, простациклинов, Т-хелперов. Также увеличивается содержание альвеолярных макрофагов. Они осуществляют фагоцитоз, переработку антигена и «передачу» информации лимфоцитам, предотвращают развитие аллергических реакций. Иммунная защита, секреторная активность являются индукторами микроваскулярного просачивания и секреции слизи.
Цитологическое исследование мокроты позволяет выявить болезнетворные микроорганизмы (в том числе микобакте- рию туберкулеза), клетки злокачественных опухолей, примеси (кровь, гной и т.п.), характерные для определенных болезней, а также определить чувствительность бактериальной флоры к антибиотикам.
Возможно обнаружение в мокроте следующих клеток: эпителиальные клетки, или клетки цилиндрического мерцательного эпителия (при бронхитах, бронхиальной астме или злокачественных новообразованиях легких); бокаловидные клетки (при усиленной секреции); базальные или промежуточные клетки; альвеолярные макрофаги из нижних респираторных отделов. Плоский эпителий попадает в мокроту из полости рта и не имеет диагностического значения. Наличие в мокроте более 25 клеток плоского эпителия указывает на то, что данный образец мокроты загрязнен отделяемым из ротовой полости. Альвеолярные макрофаги локализуется в основном в межальвеолярных перегородках. Поэтому анализ мокроты, где присутствует хотя бы 1 макрофаг, указывает на то, что поражены нижние отделы дыхательной системы. При инфаркте легкого, застое в малом кругу кровообращения обнаруживаются «клетки сердечных пороков», т.е. альвеолярные макрофаги с включениями гемосидерина [2].
Встречаются также и макрофаги с липид- ными включениями (липофаги) при туберкулезе, хроническом заболевании легких. Отмечают повышение в мазке мокроты количества нейтрофилов, лимфоцитов, эозинофилов, моноцитов, «гигантских» клеток Пирогова-Лангерганса. Обнаружение более 25 нейтрофилов в поле зрения свидетельствует об инфекции (пневмония, бронхит). Единичные эозинофилы могут встречаться в любой мокроте; в большом количестве (до 50-90% всех лейкоцитов). Они обнаруживаются при бронхиальной астме, эози- нофильных инфильтратах, глистных инвазиях легких и т.п. Эритроциты появляются в мокроте при разрушении ткани легкого, пневмонии, застое в малом круге кровообращения, инфаркте легкого и т.д. Мокрота может содержать клетки злокачественных опухолей, особенно если опухоль растет эндобронхиально или распадается. Определять клетки как опухолевые можно только в случае нахождения комплекса атипичных полиморфных клеток, особенно если они располагаются вместе с эластическими волокнами.
В мазке мокроты могут встречаться волокнистые образования: эластические волокна, фибриновые волокна и спирали Куршмана (при туберкулезе, абсцессе легкого,раке). Эластические волокна имеют вид тонких двухконтурных волоконец одинаковой на всем протяжении толщины, дихотомически ветвящихся. Эластичные волокна исходят из легочной паренхимы. Выявление в мокроте эластичных волокон свидетельствует о разрушении легочной паренхимы (туберкулез, рак, абсцесс). Иногда их присутствие в мокроте используют для подтверждения диагноза абсцедирую- щей пневмонии.
Кристаллические образования также встречаются в мазке мокроты. Это кристаллы Шарко-Лейдена - бесцветные октаэдры различной величины, напоминающие по форме стрелку компаса, состоящие из белка, освобождающегося при распаде эозинофилов(при бронхиальной астме, эмфиземе, глистных инвазиях); кристаллы гематоидина - ромбы, иголки, звезды от желтого до оранжевого цвета (при некрозе ткани, кровоизлияниях при инфаркте легкого кристаллы холестерина (при распаде ткани - туберкулез, абсцесс легкого, рак); друзы актиномицетов [3]. Мокрота в норме не содержит паразитов и яйца гельминтов. Выявление паразитов позволяет установить природу легочной инвазии, а также диагностировать кишечную инвазию и ее стадию [2].
Читайте также:

