Что такое персистенция вируса герпеса
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Генитальный герпес: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Генитальный герпес – хроническое рецидивирующее заболевание вирусной этиологии, передающееся преимущественно половым путем. Герпес считается крайне распространенным эрозивно-язвенным заболеванием половых органов - ежегодно в мире регистрируется 500 000 новых случаев обращений по этому поводу. В Российской Федерации у лиц старше 18 лет инфицированность вирусом, вызывающим генитальный герпес, составляет 17,2 случая на 10 000 населения.
В 70% случаев заболевание протекает бессимптомно, что и обусловило широкое распространение этой патологии.
Причины появления генитального герпеса
Генитальный герпес вызывает вирус простого герпеса (ВПГ) I и/или II типов. Вирус герпеса I типа чаще всего поражает слизистую оболочку рта и носит название орального (лабиального) герпеса. При заражении этим вирусом очаги поражения локализуются на лице в области губ.
Вирус герпеса II типа чаще вызывает генитальный герпес, однако оба типа могут провоцировать развитие патологии оральной и генитальной локализации. Для ВПГ II типа более характерно рецидивирующее течение, чем для ВПГ I.
- Половой путь – самый часто встречающийся путь передачи генитальной герпетической инфекции.
- Передача вируса бытовым путем является самой редкой.
- Аутоинокуляция – перенос вируса с зараженных участков слизистой на здоровые самим больным.
- Трансплацентарный – через плаценту от инфицированной матери плоду.
- Перинатальный – в процессе родов.
- Контактно-бытовой (при несоблюдении правил ухода и гигиены).
- Аутоинокуляция (см. выше).
- Беспорядочная половая жизнь без использования барьерной контрацепции (презервативов).
- Нарушение правил личной и бытовой гигиены.
- Снижение иммунитета (в силу наличия длительно текущих хронических заболеваний, несбалансированного питания, подверженности частым стрессам, нарушения режима сна).
- Первый эпизод развития клинической симптоматики генитального герпеса.
- Рецидивирующая герпетическая инфекция.
- Инфекция мочеполовых органов.
- у мужчин,
- у женщин.
- Инфекция прямой кишки и перианальной кожи.
- Герпес с типичной клинической картиной.
- Атипичное течение.
Если иммунная система справляется с вирусом на этом этапе, то формируется иммунитет и носительство вируса, не исключающее рецидива заболевания при ослаблении защитных функций организма.
Если у организма нет ресурсов противостоять ВПГ, то вирус проникает во внутренние органы и фиксируется на них. При снижении иммунитета, прочих вирусных инфекциях или при обострениях хронических заболеваний ВПГ из органов вновь выходит в кровь и с ее током разносится по организму.
Симптомы генитального герпеса
При первичном инфицировании инкубационный период составляет от 1 до 10 дней, а клинические проявления длятся от 18 до 24 дней с нарастанием симптоматики в течение недели. До возникновения очагов повреждения у 50% больных появляются продромальные симптомы - парестезии, чувство жжения в генитальной области, невралгии в ягодичной, паховой бедренной областях, дизурия - и продолжаются до 24 часов. В последующем вирусное повреждение эпителия проявляется в виде везикул на эритематозном фоне с дальнейшим характерным разрешением (образованием корочек). Симптомы общей интоксикации, свойственные любой вирусной инфекции, – недомогание, слабость, субфебрилитет, головная боль - развиваются, как правило, при первичном инфицировании, при рецидиве они минимальны.
Непервичная генитальная герпетическая инфекция протекает менее выраженно: длительность клинических проявлений составляет до 15 дней, реже наблюдается бессимптомное выделение вируса, длительность слущивания поврежденного эпителия составляет всего 4-5 дней.
Высыпания на половых органах и/или в перианальной области всегда носят пузырьковый характер, содержимое прозрачное, основание пузырьков гиперемировано (красного цвета); могут быть множественными и единичными.
Пораженная область слизистой оболочки отечная. У мужчин самая частая локализация высыпаний – мошонка, половой член, лобок, промежность, перианальная область.
У женщин – клитор, влагалище, вульва, лобок, шейка матки, перианальная область. В случае присоединения вторичной (чаще бактериальной) инфекции появляются гнойные и слизисто-гнойные выделения.
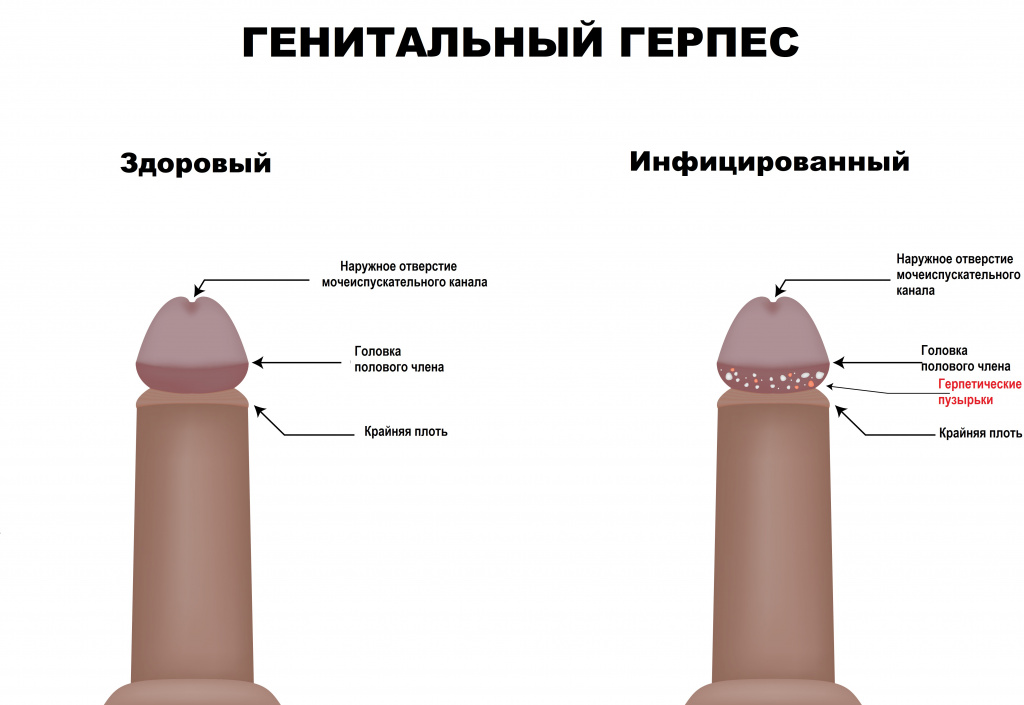
В случае обострения генитального герпеса присутствует боль при половом контакте.
Диагностика генитального герпеса
Диагностика этого заболевания строится на характерной клинической картине высыпаний и на выявлении ДНК вируса в крови или в отделяемом с пораженных тканей.
Необходимо сдать анализы крови для подтверждения инфицированности вирусом герпеса и определения активности процесса, для выявления ДНК вируса в эякуляте, секрете простаты, в соскобе клеток урогенитального тракта, а также в соскобах с конъюнктивы, кожи, слизистой оболочки носа, ротоглотки.
Раздельное определение ДНК-вируса простого герпеса 1 типа (губного или лабиального) и 2 типа (генитального) в сыворотке крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме реального времени. Термин "герпес" (от древнегреч. – ползти, ползучи.
В последние годы в инфекционной патологии все большее значение приобретают герпес-вирусы (от греч. herpes — ползучий). Внимание, которое вирусологи и клиницисты проявляют в последние 25 лет к герпес-вирусным заболеваниям человека, связано
В последние годы в инфекционной патологии все большее значение приобретают герпес-вирусы (от греч. herpes — ползучий). Внимание, которое вирусологи и клиницисты проявляют в последние 25 лет к герпес-вирусным заболеваниям человека, связано с их значительной эпидемиологической ролью и социальной значимостью в современном мире. Неуклонный рост числа герпетических заболеваний у взрослых и детей обусловливает необходимость всестороннего изучения герпетической инфекции и разработки эффективных методов профилактики и лечения разнообразных форм этой инфекции. Среди вирусных инфекций герпес занимает одно из ведущих мест в силу повсеместного распространения вирусов, многообразия клинических проявлений, как правило, хронического течения, а также различных путей передачи вирусов.
Он входит в число наиболее распространенных и плохо контролируемых инфекций человека. Герпес-вирусы могут циркулировать в организме с нормальной иммунной системой бессимптомно, но у людей с иммуносупрессией вызывают тяжелые заболевания со смертельным исходом. По данным ВОЗ, смертность от герпетической инфекции среди вирусных заболеваний находится на втором месте (15,8%) после гепатита (35,8%).
Герпес-вирусы объединены в обширное семейство Herpesviridae и в настоящее время наиболее четко классифицированы. Семейство Herpesviridae включает в себя более 80 представителей, 8 из которых для человека наиболее патогенны (human herpes virus-HHV). Герпес-вирусы — филогенетически древнее семейство крупных ДНК-вирусов — подразделяются на 3 подсемейства в зависимости от типа клеток, в которых протекает инфекционный процесс, характера репродукции вируса, структуры генома, молекулярно-биологических и иммунологических особенностей: α, β и γ (табл. 1, по данным Н. Г. Перминова, И. В. Тимофеева и др., Государственный научный центр вирусологии и биотехнологий).
α-герпес-вирусы, включающие HSV-1, HSV-2 и VZV, характеризуются быстрой репликацией вируса и цитопатическим действием на культуры инфицированных клеток. Репродукция α-герпес-вирусов протекает в различных типах клеток, вирусы могут сохраняться в латентной форме, преимущественно в ганглиях.
β-герпес-вирусы видоспецифичны, поражают различные виды клеток, которые при этом увеличиваются в размерах (цитомегалия), могут вызывать иммуносупрессивные состояния. Инфекция может принимать генерализованную или латентную форму, в культуре клеток легко возникает персистентная инфекция. К этой группе относятся CMV, HHV-6, HHV-7.
Герпес-вирусы ассоциированы с малигнизацией и способны (по крайней мере, EBV и HVS) трансформировать клетки in vitro. Все герпес-вирусы сходны по морфологическим признакам, размерам, типу нуклеиновой кислоты (двухцепочечная ДНК), икосадельтаэдрическому капсиду, сборка которого происходит в ядре инфицированной клетки, оболочке, типу репродукции, способности вызывать хроническую и латентную инфекцию у человека.
Клонирование герпес-вирусов происходит по следующей схеме: спонтанная случайная адсорбция исходного «материнского» вируса на поверхности клетки-мишени, «раздевание вириона» — расщепление оболочки и капсида, инфильтрация вирусной ДНК в ядро клетки-мишени, формирование и созревание «дочерних» вирионов путем почкования на ядерной мембране. После инфицирования клетки, например вирусом простого герпеса 1 или 2 типов, синтез новых вирусных белков начинается через 2 ч, а число их достигает максимума примерно через 8 ч. В процессе созревания «дочерних» вирионов их оболочки капсиды и ДНК формируются из имеющихся внутри инфицированной клетки аминокислот, белков, липопротеидов и нуклеозидов. Эти молекулы поступают в инфицированную клетку из межтканевых пространств по мере истощения внутриклеточных резервов. В этом отношении вирусы зависят от интенсивности внутриклеточного обмена, который, в свою очередь, определяется природой клетки-мишени. Наиболее высокий темп обмена веществ характерен для короткоживущих клеток эпителиоидного типа, поэтому герпес- вирусы особенно хорошо колонизируют клетки эпителия и слизистых оболочек, крови и лимфатических тканей. Полностью сформированные и готовые к последующей активной репродукции «дочерние» инфекционные вирионы появляются внутри инфицированной клетки через 10 ч, а их число становится максимальным примерно через 15 ч. Количество вирионов в определенной степени влияет на темп распространения инфекции и площадь поражения.
Первая генерация «дочерних» герпес-вирусов начинает поступать в окружающую среду (межклеточные пространства, кровь, лимфу и другие биологические среды) примерно через 18 ч. Это можно пронаблюдать в клинической практике при неконтролируемых процессах (например, при ветряной оспе, опоясывающем герпесе, генерализации цитомегаловирусной инфекции) — элементы герпетической сыпи возникают на коже или слизистых оболочках волнами. В свободном состоянии герпес-вирусы находятся в течение весьма непродолжительного периода (от 1 до 4 ч) — именно такая продолжительность характерна для периода острой интоксикации при герпес-вирусных инфекциях. Срок жизни каждой генерации образовавшихся и адсорбированных герпес-вирусов в среднем составляет 3 сут.
В эпидемиологическом плане наиболее интересны следующие сведения о герпес-вирусах: вирионы чрезвычайно термолабильны — инактивируются при температуре 50–52°С в течение 30 мин, при температуре 37,5°С — в течение 20 ч, устойчивы при температуре 70°С; хорошо переносят лиофилизацию, длительно сохраняются в тканях в 50-процентном растворе глицерина. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) герпес-вирусы выживают в течение 2 ч, на пластике и дереве — до 3 ч, во влажных медицинских вате и марле — до их высыхания при комнатной температуре (до 6 ч).
Уникальными биологическими свойствами всех герпес-вирусов человека является тканевой тропизм, способность к персистенции и латенции в организме инфицированного человека. Персистенция представляет собой способность герпес-вирусов непрерывно или циклично размножаться (реплицироваться) в инфицированных клетках тропных тканей, что создает постоянную угрозу развития инфекционного процесса. Латенция герпес-вирусов — это пожизненное сохранение вирусов в морфологически и иммунохимически видоизмененной форме в нервных клетках регионарных (по отношению к месту внедрения герпес-вируса) ганглиев чувствительных нервов. Штаммы герпес-вирусов обладают неодинаковой способностью к персистенции и латенции и чувствительностью к противогерпетическим препаратам в связи с особенностями их ферментных систем. У каждого герпес-вируса свой темп персистенции и латенции. Среди изучаемых наиболее активны в этом отношении вирусы простого герпеса, наименее — вирус Эпштейна-Барр.
По данным многочисленных исследований, к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами по меньшей мере 7 клинически значимых герпес-вирусов (простого герпеса 1 и 2 типов, варицелла зостер, цитомегаловирусом, Эпштейна-Барр, герпеса человека 6 и 8 типов). В большинстве случаев первичное и повторное инфицирование происходит воздушно-капельным путем, при прямом контакте или через предметы обихода и гигиены (общие полотенца, носовые платки и т. п.). Доказаны также оральный, генитальный, орогенитальный, трансфузионный, трансплантационный и трансплацентарный пути передачи инфекции.
Герпес-вирусные инфекции широко распространены в мире и имеют тенденцию к неуклонному росту. Особенностью герпес-вирусной инфекции является возможность вовлечения в инфекционный процесс многих органов и систем, чем и обусловлено многообразие вызываемых герпес-вирусами заболеваний, варьирующих от простых кожно-слизистых до угрожающих жизни генерализованных инфекций. Важное свойство герпес-вирусов — это способность после первичного инфицирования в детском возрасте пожизненно персистировать в организме и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов.
Инфицирование человека указанными герпес-вирусами сопровождается клиническими симптомами соответствующего острого инфекционного заболевания в среднем не более чем у 50% людей, в основном у детей: внезапная эритема (вирус герпеса человека 6 типа), афтозный стоматит (вирусы простого герпеса 1 или 2 типов), ветряная оспа (вирус варицелла зостер), инфекционный мононуклеоз (вирус Эпштейна-Барр), мононуклеозоподобный синдром (цитомегаловирус). У остальных пациентов инфекция протекает бессимптомно, что особенно характерно для подростков и взрослых людей. Помимо биологических свойств штамма герпес-вируса, влияние на течение острых и рецидивирующих герпес-вирусных заболеваний оказывают индивидуальные (возрастные, половые, фило- и онкогенетические) особенности иммунного ответа инфицированного человека на многочисленные антигены вируса.
Часто, особенно при снижении иммунореактивности организма, герпес-вирусы выступают в качестве вирусов-оппортунистов, приводя к более тяжелому, с необычными клиническими проявлениями, течению основного заболевания. Вирусы простого герпеса 1 и 2 типов, а также ЦМВ входят в число возбудителей TORCH-инфекций. Они играют важную роль в нарушении репродуктивной функции человека, развитии серьезных заболеваний матери, плода, новорожденного и детей младшего возраста.
Вызываемые вирусами ВПГ, CMV, ВЭБ заболевания рассматриваются как СПИД-индикаторные в связи с их частым обнаружением при данной патологии. В 1988 г. они включены в расширенное определение случаев, подлежащих эпидемиологическому надзору по поводу СПИДа. Результаты исследований последних лет свидетельствуют о роли некоторых герпес-вирусов (ВГЧ-8, ЦМВ, ВЭБ и др.) в развитии ряда злокачественных новообразований: назофарингеальной карциномы, лимфомы Беркитта, В-клеточной лимфомы, рака груди, аденокарциномы кишечника и простаты, карциномы цервикального канала шейки матки, саркомы Капоши, нейробластомы и др.
Наибольшую угрозу для здоровья представляют герпетические нейроинфекции (летальность достигает 20%, а частота инвалидизации — 50%), офтальмогерпес (почти у половины больных приводит к развитию катаракты или глаукомы) и генитальный герпес.
По-видимому, все известные герпес-вирусные инфекции могут рецидивировать, однако порог и причины трансформации острой формы в рецидивирующую для каждого типа герпес-вируса свои. В целом герпес-вирусные инфекции принимают рецидивирующее течение не более чем у 8–20% больных. Рецидивирующие герпес-вирусные заболевания у некоторых людей могут восприниматься как «хронические», когда они развиваются в течение многих лет, не только разрушая физическое здоровье и функции жизненно важных систем, но и психологически крайне неблагоприятно влияя на больного. Поэтому для практических целей герпес–вирусные инфекции классифицируют с учетом одновременно локализации процесса, рецидивирования и этиологии (табл. 2).
Причины рецидивирующего течения герпес-вирусных инфекций многообразны. Одна из них заключается в том, что трансформация острого герпес-вирусного процесса в хронический происходит при явном «попустительстве» иммунной системы. Если приобретенный иммунодефицит в результате химиотерапии или ВИЧ-инфекции легко объясним, то все попытки выяснить, чем обусловлен основной дефект иммунного ответа у иммунологически полноценных людей с рецидивирующим течением герпес-вирусной инфекции, оказались безуспешными. Другая причина заключается, по-видимому, в количественной и качественной особенности персистенции и латенции конкретного штамма герпес-вируса в организме больного.
Диагностика герпетической инфекции
Все методы индикации и идентификации вирусов основаны на следующих принципах:
- выявление вируса per se (электронная микроскопия);
- выявление и идентификация вирусов посредством взаимодействующих с ними клеток (накопление вирусов в чувствительных к ним клетках);
- выявление и идентификация вирусов с помощью антител (МФА, ИФА, РАЛ, ИБ, РН, РСК);
- выявление и идентификация нуклеиновых кислот (ПЦР, МГ).
Электронная микроскопия: быстрая диагностика позволяет обнаружить ГВ или их компоненты непосредственно в пробах, взятых от больного, и дать быстрый ответ через несколько часов. Возбудитель выявляют с помощью электронной микроскопии клинического материала при негативном контрастировании.
Серологические методы уступают по информативности и чувствительности другим способам лабораторной диагностики и не позволяют с достаточной степенью достоверности установить этиологию той или иной формы заболевания. Нарастание титров антител происходит
в поздние сроки (через несколько недель) после заражения или реактивации вируса, и в то же время оно может и не наблюдаться у иммунодефицитных лиц. Для установления 4-кратного нарастания титра антител к герпес-вирусной инфекции (показатель первичной инфекции) необходимо исследование парных сывороток. Серологические реакции (РСК, РН) обладают высокой специфичностью, но относительно низкой чувствительностью, а кроме того, сложны в постановке.
Широкое практическое применение получили иммунофлюоресцентный метод, ИФА, РАЛ, ИБ.
Наиболее точным методом диагностики герпес-вирусной инфекции является выделение вируса из различных клеточных культур.
Для обнаружения вируса герпеса используют молекулярно-биологические методы: полимеразную цепную реакцию и реакцию молекулярной гибридизации, которые позволяют выявить наличие вирусной нуклеиновой кислоты в исследуемом материале. ПЦР может считаться самой чувствительной и быстрой реакцией. Чувствительность метода дает возможность определить одну молекулу искомой ДНК в образцах, содержащих 10 клеток.
Лечение герпетической инфекции
Лечение герпетической инфекции до настоящего времени остается сложной задачей. Хроническое течение процесса приводит к иммунной перестройке организма: развитию вторичной иммунной недостаточности, угнетению реакции клеточного иммунитета, снижению неспецифической защиты организма. Несмотря на разнообразие лекарственных препаратов, использующихся для лечения герпетической инфекции, лекарственных средств, обеспечивающих полное излечение от герпеса, не существует. Герпес-вирусная инфекция относится к трудно контролируемым заболеваниям. Это связано, в первую очередь, с разнообразием клинических поражений, развитием резистентности вируса к лекарственным средствам, наличием у герпес-вирусов молекулярной мимикрии. Поэтому для успешного лечения герпетической инфекции необходимо правильно подобрать противовирусный препарат, его дозу и длительность лечения, использовать комбинацию различных лекарств. В схемы терапии для повышения эффективности лечения необходимо также включать иммунобиологические препараты, способствующие коррекции иммунного статуса, а также патогенетические средства, облегчающие состояние пациента.
В настоящее время все антигерпетические средства подразделяются на 3 основные группы антивирусных препаратов (табл. 3).
Механизм действия химиопрепаратов (аномальных нуклеозидов: валтрекса, вектавира, фамвира, цимевена) связан с угнетением синтеза вирусной ДНК и репликации вирусов путем конкурентного ингибирования вирусной ДНК-полимеразы.
В препаратах-иммуномодуляторах (алпизарин, имунофан, ликопид, полиоксидоний) активно действующие вещества обладают иммуностимулирующими свойствами в отношении клеточного и гуморального иммунитетов, окислительно-восстановительных процессов, синтеза цитокинов.
Препараты-индукторы ИФН (амиксин, неовир, циклоферон) сочетают этиотропный и иммуномодулирующий эффекты действия. Препараты индуцируют образование эндогенных ИФН (α, β, γ) Т- и В-лимфоцитами, энтероцитами, гепатоцитами.
Особое место среди средств антигерпес-вирусной терапии занимает герпетическая вакцина для активации клеточного иммунитета, его иммунокоррекции в фазе ремиссии. Вакцинация преследует 2 цели: предупреждение первичной инфекции и возникновения состояния латентности, а также предупреждение или облегчение течения заболевания.
Однако, несмотря на наличие обширного списка антигерпетических препаратов, герпес остается до сих пор плохо контролируемой инфекцией. Это обусловлено и генотипическими особенностями возбудителя, и длительной персистенцией вируса в организме, и формированием штаммов, устойчивых к антивирусным препаратам. Максимальный клинический эффект может быть получен только при рациональной комплексной терапии лекарственных средств с различным механизмом действия.
Санкт-Петербургской группой ученых вирусологов и инфекционистов во главе с В. А. Исаковым предложена программа лечения и профилактики герпетической инфекции (табл. 4).
Преимущества комплексной терапии ГИ.
- Сочетанное применение противогерпетических химиопрепаратов и иммунобиологических средств обеспечивает синергидный эффект.
- Благодаря снижению дозы противовирусного ХПП уменьшается вероятность развития побочных эффектов, сокращается токсическое воздействие на организм больного.
- Снижается вероятность возникновения устойчивых штаммов герпес-вирусов к данному препарату.
- Достигается иммунокорригирующий эффект.
- Сокращается продолжительность острого периода болезни и сроков лечения.
Таким образом, терапия ГИ является сложной и многокомпонентной задачей.
По вопросам литературы обращайтесь в редакцию.
Т. К. Кускова, кандидат медицинских наук
Е. Г. Белова, кандидат медицинских наук
МГМСУ, Москва
На основании собственных многолетних данных произведен ретроспективный анализ особенностей динамики активной репликации персистирующих инфекций у детей. В статье описано, как изменяются показатели активной репликации геномов облигатных внутриклеточных пар
Based on our own multi-year data, a retrospective analysis of the dynamics of active replication of persistent infections in children was made. The article describes how the indicators of active replication genomes of obligate intracellular parasites and herpesviruses vary with age and seasonal changes.
Персистирующие инфекции могут являться причиной целого ряда заболеваний. Некоторые из них характеризуются тяжелым клиническим течением, особенно в раннем возрасте. В России, к сожалению, сохраняется высокий уровень детской инфекционной заболеваемости [1]. Известно, что в основном передача инфекции осуществляется в первые годы жизни человека, иногда — внутриутробно. Так, заражение герпес-вирусами человека 1–2, а также 4–6 типов в большинстве случаев реализуется в возрасте до двух лет. Источником инфекции чаще всего является ближайшее окружение ребенка, которое в первые два года его жизни представлено членами семьи и/или обслуживающим персоналом (няни, воспитатели и пр.). За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [2]. При этом, по данным литературы, у детей маркеры активной персистирующей инфекции выявляют чаще, чем у взрослых [3]. Одним из факторов, обусловливающих высокий уровень репликации инфекционных агентов, является незрелость иммунной системы в раннем возрасте [4]. Несмотря на обилие научных работ, посвященных проблеме персистирующих инфекций, вопрос особенностей динамики их активности остается открытым.
Объект и материалы исследования
Предметом анализа явились данные, полученные при обследовании детей и подростков, находившихся на стационарном лечении в клинике Московского НИИ педиатрии и детской хирургии (в последние годы — Обособленное структурное подразделение Научно-исследовательский клинический институт педиатрии им. акад. Ю. Е. Вельтищева ФГБОУ ВО РНИМУ им. Н. И. Пирогова) Минздрава РФ, и их родителей.
Проанализированы результаты обследования 1079 пациентов, из которых 1064 (98,6%) составили дети и подростки в возрасте от 2 месяцев до 17 лет и 15 (1,4%) взрослых в возрасте от 23 до 52 лет.
У каждого пациента одновременно исследовали от одного до трех образцов различных биологических материалов, всего 2051 образец. Из них осадков мочи — 877 (42,8%); буккальных соскобов — 104 (5,1%); объединенного материала, включающего осадок мочи и буккальный соскоб, — 901 (43,9%); крови — 169 (8,2%) (табл. 1).
Методы исследования
ДНК персистирующих инфекций в исследованных материалах выявляли посредством полимеразной цепной реакции, при постановке которой использовали полные наборы реактивов (kits) для лабораторной диагностики in vitro производства «ВСМ», «Диасан» и «Гентех», г. Москва, Россия. Использовали моноспецифические наборы, укомплектованные нелиофилизированными супермиксами, готовыми к употреблению, замороженными и хранившимися при температуре от –25 до –28 °С. По нашим данным, использование именно таких наборов позволяет достичь наиболее качественных результатов.
Оценивали активность репликации следующих микроорганизмов: Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, цитомегаловирус, вирус Эпштейна–Барр, вирус простого герпеса 1–2 типов.
Среди пациентов девочки и женщины составили 56,7% от числа обследованных, мальчики и мужчины — 43,3%.
Возрастная характеристика пациентов отражена в табл. 2: возраст большинства пациентов составил от двух до 16 лет.
При определении периодов активной репликации персистирующих инфекций в зависимости от возраста фрагмент исследования включал данные, полученные при обследовании 876 пациентов.
Основным критерием отбора явилось одновременное исследование в материале не менее 3 инфекций (герпес-вирусов 4–6 типов и/или облигатных внутриклеточных паразитов). У каждого больного, соответственно, исследовали 3 или 6 инфекций. Такой подход позволил снизить избирательность выборки по той или иной инфекции.
Результаты исследования и их обсуждение
Выявлены следующие закономерности (рис. 1):
Отчетливая закономерность показана для цитомегаловируса: частота выявления ДНК в образцах стабильно снижается до 0 у обследованных взрослых, что можно рассматривать как доказательство зависимости активной репликации цитомегаловируса именно от зрелости иммунной системы (рис. 2).
Аналогичные, хотя и не столь четко выраженные изменения частоты активной репликации в зависимости от возраста можно проследить и для вирусов Эпштейна–Барр и вируса простого герпеса 1–2 типов.
Для ответа на вопрос, существуют ли сезонные изменения активности персистирующих инфекций, мы проанализировали частоту положительных проб в течение двух полных лет; был обследован 871 пациент.
Диаграмма отражает закономерности изменения количества положительных проб Chlamydia trachomatis, Mycoplasma hominis и Ureaplasma urealyticum в течение года (рис. 3).
Вопреки ожиданиям, наибольшая активность Chlamydia trachomatis приходится на период с апреля по июнь. Отмечаются существенные колебания показателя в первом полугодии с максимумом в июне и минимумом в марте и стабильно низкие показатели во втором полугодии.
Частота выявления ДНК Ureaplasma urealyticum крайне нестабильна с декабря по июнь, а в июле резко уменьшается и сохраняется на относительно низком уровне до ноября. В декабре значение показателя возрастает, достигая максимума. Таким образом, общим для исследованных внутриклеточных паразитов является нестабильность и более высокие значения показателя в первом полугодии (для Ureaplasma urealyticum — с декабря по июнь) и, напротив, относительно низкое и стабильное число положительных проб во втором полугодии. Не исключено, что снижение и стабилизация показателя в период с июля по декабрь вызвана улучшением метаболизма, а значит, и адаптивного иммунитета во второй половине лета и осенью.
Для персистирующих герпес-вирусов какой-либо четкой сезонной закономерности не выявлено, однако частота выявления ДНК вируса простого герпеса 1–2 типов стабильно повышается, в мае достигая максимума, а затем снижается к концу года до минимального значения (рис. 4).
Выводы
Проведенное нами исследование позволило сделать следующие выводы:
При исследовании сезонной активности всех облигатных внутриклеточных паразитов выявлена ее существенная вариативность в первом полугодии с максимумом в июне и относительное снижение и стабилизация во втором полугодии.
Литература
- Мазанкова Л. Н., Захарова И. Н. // Рос. вест. перинат. и педиатрии. 2010. № 5. С. 8–11.
- Лобзин Ю. В. Проблемы детских инфекций на современном этапе // Инфекционные болезни. 2009. № 2. С. 7–12.
- Учайкин В. Ф., Нисевич Н. И., Шамшева О. В. Инфекционные болезни и вакцинопрофилактика у детей. М.: ГЭОТАР-медиа. 2006. 688 с.
- Щеплягина Л. А., Круглова И. В. Возрастные особенности иммунитета у детей // РМЖ. № 23, 2009, с. 1564.
Е. И. Шабельникова 1 , кандидат медицинских наук
В. С. Сухоруков, доктор медицинских наук, профессор
Е. А. Ружицкая, кандидат медицинских наук
А. В. Семенов, кандидат медицинских наук
М. В. Кушнарева, доктор медицинских наук, профессор
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Герпес: причины появления, симптомы, диагностика и способы лечения.
Определение
Герпесом, или герпетической инфекцией, называют несколько заболеваний, вызываемых вирусами отряда Herpesvirales семейства Herpesviridae.
Все они характеризуются поражением кожи, слизистых оболочек с локализацией либо в области глаз, носа и губ, гениталий, а также нервных волокон.
У лиц с иммунодефицитом могут наблюдаться генерализованные формы инфекции с вовлечением в процесс других органов и тканей.

Среди известных науке восьми типов герпеса самым распространенным является вирус герпеса простого типа (Herpes simplex virus).
Простой вирус герпеса достаточно неустойчив во внешней среде. В условиях комнатной температуры сохраняется до 24 часов, на металле — до 2 часов. Под действием температуры выше 50°C погибает за 30 минут, под действием спирта и хлорсодержащих веществ - в течение нескольких минут, при замораживании сохраняется до пяти суток.
Причины герпетической инфекции
Источником инфицирования всегда служит человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Возбудитель может передаваться воздушно-капельным, контактно-бытовым или половым путем, а также от матери плоду через плаценту, во время родов или грудного вскармливания.
К вирусу восприимчивы все люди, хотя у многих отмечаются бессимптомные формы заболевания. Попадая через слизистую рта, половых органов или дыхательные пути в организм человека, герпесная инфекция остается в нем навсегда. Вирус, скрытый внутри клетки-хозяина, не доступен для иммунных клеток, уничтожающих возбудителей. Вирус активизируется при ослаблении иммунитета в результате переохлаждения, перегрева, простудного заболевания, недостатка витаминов, переутомления, стресса, нехватки сна. Рецидив инфекции могут вызвать травмы, оперативные вмешательства, а также половой контакт при условии повреждения слизистой оболочки. Использование лекарственных и косметических средств, содержащих стероидные гормоны, также способствует манифестации вируса герпеса.
Классификация герпеса
В МКБ-10 (Международной классификации болезней) выделяют две группы заболеваний, связанных с вирусом простого герпеса:
- Инфекционные герпетические заболевания:
- герпетическая экзема (экзема Капоши);
- герпетический везикулярный дерматит;
- герпетический гингивостоматит и фаринготонзиллит;
- герпетический менингит;
- герпетический энцефалит;
- офтальмогерпес;
- диссеминированная герпетическая болезнь (герпетический сепсис);
- другие формы герпетических инфекций;
- неуточненная герпетическая инфекция.
- Генитальные герпетические инфекции:
- герпетические инфекции перианальных кожных покровов и прямой кишки;
- неуточненная аногенитальная герпетическая инфекция.
По клинической картине и локализации высыпаний:
- Типичные формы:
- герпес кожи — с поражением губ, крыльев носа, лица, рук, ягодиц и других частей тела;
- герпес глаз — иридоциклит, кератит, конъюнктивит, неврит зрительного нерва;
- герпес слизистых оболочек желудочно-кишечного тракта — стоматит, гингивит, фарингит, эзофагит;
- герпес половых органов — поражение слизистой оболочки полового члена, влагалища, вульвы, цервикального канала;
- герпес внутренних органов — гепатит, пневмония, панкреатит, трахеобронхит;
- герпес нервной системы — неврит, менингит, менингоэнцефалит, поражения бульбарных нервов, энцефалит;
- генерализованный простой герпес — висцеральная форма (пневмония, гепатит, эзофагит) и диссеминированная форма (сепсис).
- Атипичные формы:
- герпетиформная экзема Капоши — обширные сливающиеся высыпания по всему телу;
- абортивный герпес — почти незаметные папулы на грубой коже или дискомфорт без высыпаний;
- язвенно-некротический герпес — с развитием некроза тканей;
- эрозивно-язвенный герпес — с образованием язв и эрозий;
- геморрагический герпес — с кровянистым пропитыванием высыпаний и тканей;
- отечный герпес — с отеком тканей и болью в области губ и век;
- зостериформный простой герпес — с локализацией по ходу нервного ствола;
- диссеминированный герпес — с тенденцией перехода в генерализованную форму при ВИЧ;
- рупиоидный герпес — возникает на лице с присоединением вторичной бактериальной флоры;
- мигрирующий герпес — с тенденцией к изменению локализации высыпаний.
- латентная стадия — носительство с отсутствием симптомов;
- локализованная стадия — наличие одного очага поражения;
- распространенная стадия — наличие не менее двух очагов поражения;
- генерализованная стадия — висцеральная, диссеминированная.
При заражении герпесом детей в возрасте от 6 месяцев до 3 лет чаще всего развивается герпетический стоматит, для которого характерно острое начало с симптомами интоксикации и подъемом температуры.
На слизистой оболочке полости рта появляются сгруппированные пузырьки с прозрачным содержимым, на месте которых после вскрытия образуются болезненные эрозии. У детей старшего возраста первичный герпес характеризуется появлением зудящих пузырьков на красной кайме губ и коже носогубного треугольника. После их вскрытия остаются неглубокие язвочки, которые покрываются корочками. Корочки, отпадая, не оставляют следов на коже.
При первичном заражении взрослых вирусом простого герпеса симптомы более выражены, чем при дальнейших рецидивах. Больной испытывает озноб, головные боли, повышенную утомляемость, у него отсутствует аппетит, может наблюдаться расстройство сна. Покраснение, а затем характерные пузырьки появляются на губах, возле крыльев носа. В некоторых случаях увеличиваются подчелюстные лимфоузлы.
Герпетические нейроинфекции сопровождаются наиболее тяжелым течением, особенно если вирус поражает оболочки или ткань головного мозга.
В этих случаях симптомы включают головные боли, подъем температуры тела, напряжение затылочных мышц, психомоторное возбуждение (болезненное состояние, при котором наблюдается беспокойство и двигательная активность различной степени выраженности, вплоть до судорог). При несвоевременной диагностике заболевания существует риск летального исхода.
Офтальмогерпес сопровождается покраснением глаза, развитием блефаро- или кератоконъюнктивита, эрозиями роговицы.
Диагностика герпеса
Типичные случаи герпетической инфекции выявляются на основании клинической картины и анамнеза заболевания. Характерно его волнообразное течение со сменой периодов обострения и ремиссии.
Косвенным признаком служит склонность к простудным заболеваниям, чувствительность к переохлаждению, периодически возникающие состояния, сопровождаемые подъемом температуры, усталостью, депрессией.

При атипичных формах герпетической инфекции необходимы дополнительные обследования: клинический анализ крови, биохимический анализ крови (общий белок, белковые фракции, С-реактивный белок, АЛТ, АСТ, ЛДГ, креатинин, электролиты: калий, натрий, хлор, кальций) и клинический анализ мочи - для выявления поражения внутренних органов и предупреждения осложнений.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
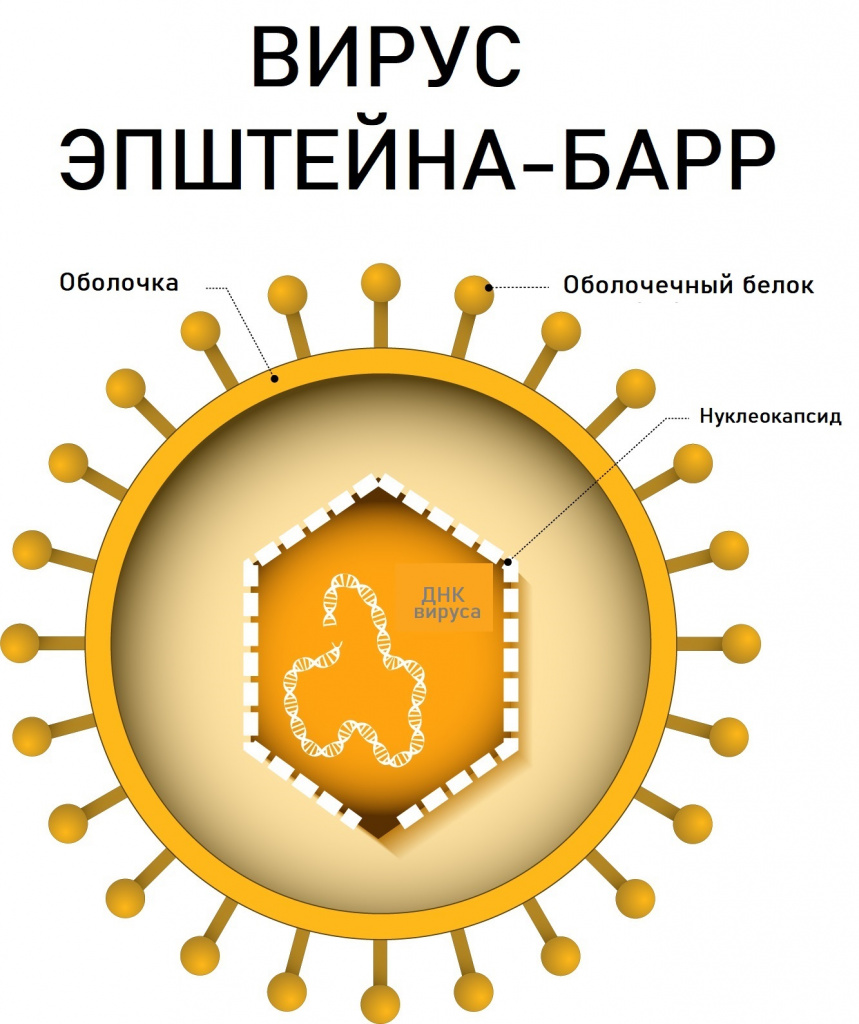
Причины появления заболеваний, вызванных вирусом Эпштейна-Барр
Вирус может распространяться от человека к человеку через биологические жидкости (воздушно-капельный путь передачи). Вот почему инфекционный мононуклеоз, одно из самых известных заболеваний, вызываемых ВЭБ, называют «болезнью поцелуев».
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Определение ДНК вируса Эпштейна-Барр в крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени». Вирус Эпштейна - Барр (ВЭБ) является причиной инфекционного мононуклеоза. С вирусом Эпштейна-Барр связывают также этиологию некоторых онкологических.
Читайте также:

