Что такое перфузия кожи
Обновлено: 02.05.2024
АНО «Научно-исследовательский институт микрохирургии»
АНО «Научно-исследовательский институт микрохирургии»
Реперфузионный синдром: сосудистые проявления в кожно-фасциальных лоскутах
Журнал: Пластическая хирургия и эстетическая медицина. 2021;(2): 40‑47
АНО «Научно-исследовательский институт микрохирургии»
Синдром ишемии/реперфузии наиболее ярко проявляет себя в свободных мышечных, кожно-мышечных и кожно-мышечно-костных лоскутах, а также в крупных реплантатах конечностей. В первую очередь это происходит в энергонеустойчивых скелетных мышцах. Несомненно, определенного рода проявления данного синдрома возможны и в кожно-фасциальных лоскутах.
ЦЕЛЬ РАБОТЫ
Сравнительное изучение реакции сосудов в кожно-фасциальных лоскутах после полной хирургической денервации и периода первичной ишемии.
МАТЕРИАЛ И МЕТОДЫ
Было выполнено 3 серии экспериментальных исследований (белые крысы, n=53): 1) изучение анатомии сосудов кожи в пределах разметки эпигастрального кожно-фасциального лоскута (n=3); 2) операция транспозиции осевого эпигастрального кожно-фасциального лоскута после его полной хирургической денервации (периадвентициальной симпатэктомии сосудистой ножки на протяжении 0,5—0,7 см) и изоляции лоскута от окружающих тканей (n=25); 3) операция реплантации свободного эпигастрального лоскута у крыс по P.G. van der Sloot (2002) (n=25). Реакцию сосудистого русла кожи эпигастральной области крыс исследовали путем инъекции в сосудистое русло синей массы Героты.
РЕЗУЛЬТАТЫ
Впервые были описаны сосудистые реакции в ответ на реперфузию свободного кожно-фасциального эпигастрального лоскута (реплантата). Они характеризуются значительной дилатацией и извитостью как артериальных, так и венозных сосудов на фоне трехдневного постреперфузионного тканевого отека. Дилатация и извитость кожных сосудов уменьшалась к 14-м суткам, но полностью не исчезала. На 10-е сутки на фоне гемодинамических расстройств и поврежденного механизма ауторегуляции микроциркуляции происходило приживление кожно-фасциального лоскута с формированием нормотрофического кожного рубца. Артериально-венозные сосудистые реакции в реперфузируемом кожно-фасциальном лоскуте, сохраняющиеся в течение 14 сут, можно интерпретировать как комплекс реперфузионного и нейрогенного повреждения мышечной оболочки кожных сосудов. При этом кожа и фасция, обладающие высокой толерантностью к аноксии, остаются вне этого реперфузионного воздействия.
АНО «Научно-исследовательский институт микрохирургии»
АНО «Научно-исследовательский институт микрохирургии»
Дата принятия в печать:
Цель исследования — сравнительное изучение реакции сосудов в кожно-фасциальных лоскутах после полной хирургической денервации и периода первичной ишемии.
1. Изучить анатомию сосудов кожи в пределах разметки эпигастрального лоскута (без его подъема).
2. Оценить состояние сосудов кожи несвободного эпигастрального лоскута после его полной хирургической денервации, а также приживление денервированного лоскута на фоне сосудистых расстройств.
3. Оценить состояние сосудов кожи и приживление реперфузируемого свободного эпигастрального лоскута после 60—90-минутной ишемии.
Материал и методы
Выбор экспериментальной модели основан на ее универсальности в плане моделирования разнообразных вариантов пересадки лоскутов у экспериментальных животных.
Выполнено три серии экспериментальных исследований (n=53):
1. Изучение анатомии сосудов кожи в пределах разметки эпигастрального кожно-фасциального лоскута (n=3).
2. Операция транспозиции осевого эпигастрального кожно-фасциального лоскута после его полной хирургической денервации (периадвентициальной симпатэктомии сосудистой ножки на протяжении 0,5—0,7 см) и изоляции лоскута от окружающих тканей (n=25).
3. Операция реплантации свободного эпигастрального лоскута у крыс по P.G. van der Sloot (2002) (n=25) [9].
С целью изучения реакции сосудистого русла кожи эпигастральной области крыс использовали способ инъекции в сосудистое русло синей массы Героты. Далее выполняли просветление полученных препаратов по способу В. Шпальтегольца (1921) в модификации Д.А. Жданова (1943), после чего производили препаровку и изготовление микроанатомических препаратов. Реакцию сосудистого русла эпигастральных лоскутов исследовали под микроскопом Carl Zeiss Opmi Pro (ув. ×32). Подсчет численной плотности артериальных и венозных сосудов выполняли по препаратам, взятым от двух животных для каждой контрольной точки. Подсчет проводился в 5 полях зрения каждого препарата с пересчетом количества сосудов на 1 мм 2 . При морфометрии сосудов артериального и венозного русла лоскута измеряли диаметр просвета сосуда (см).
Функциональное состояние периферического сосудистого русла лоскутов оценивали в динамике по цвету кожи лоскута, симптому исчезающего пятна (капиллярный ответ) и контактному кровотечению. Состояние волосяного покрова лоскута в динамике и тип формирующегося кожного рубца (нормотрофический, гипертрофический, атрофический) характеризовали его кровоснабжение и процесс приживления в реципиентном ложе.
Статистическую обработку полученных результатов проводили с помощью программ Statistica 7.0 for Windows и SPSS Statistics 17.0 (коэффициент корреляции Спирмена). Достоверность различий качественных признаков определяли с помощью точного критерия Фишера [10].
Результаты
Наше обращение к эпигастральному лоскуту обусловлено тем, что этот лоскут на поверхностных эпигастральных сосудах — единственный известный нам лоскут, в котором аксиальную артерию сопровождает только одна, а не две бесклапанные аксиальные вены. В качестве контроля мы использовали морфометрические данные сосудов кожи в области разметки этого лоскута. Численная плотность артериальных сосудов в коже в пределах разметки эпигастрального лоскута составила 4,48 [4,48; 5,19] на 1 мм 2 . Венозные аксиальные сосуды и их ветви имели слегка извитой ход. Преобладало дихотомическое деление сосудов (рис. 1 и 2). Показатели численной плотности венозных сосудов в коже области разметки эпигастрального лоскута составили 18,06 [16,56; 20,53] на 1 мм 2 . При этом микроциркуляторное русло равномерно прокрашивается. Диаметр аксиальных сосудов: а=39,5 [28,3; 43,1] мкм; v=67,7 [57,4; 70,1] мкм.

Рис. 1. Артериальное русло кожи в пределах разметки эпигастрального лоскута.
Инъекция синей массы Героты. Ув. ×16.

Рис. 2. Венозное русло кожи в пределах разметки эпигастрального лоскута.
Инъекция синей массы Героты. Ув. ×16.
Во второй (опытной) группе животных выделенные из структуры ангиосома эпигастральные лоскуты были не только лишены связи с окружающими тканями на уровне кожи, подкожной клетчатки и собственной фасции, но и хирургически денервированы на уровне сосудистой ножки: периартериальная + перивенозная симпатэктомия. Денервация сосудистой ножки прерывает чувствительную спинномозговую и сосудодвигательную иннервацию сосудистого русла несвободного лоскута. В данной экспериментальной группе у 10 (40%) из 25 животных наступил некроз лоскута, связанный с ранним венозным тромбозом аксиальных сосудов, т.е. на 3-и сутки после операции. Неосложненное послеоперационное течение было у 15 (60%) животных.
Особенность реакции сосудистого русла в полностью денервированном несвободном эпигастральном лоскуте состояла в том, что основные изменения происходили в артериальных сосудах. С первых суток они проявлялись дилатацией и извитостью артерий на фоне немного дилатированных, но прямолинейно расположенных вен (рис. 3а, 3б).

Рис. 3. Сосудистое русло кожи центральной части несвободного эпигастрального лоскута после полной хирургической денервации, 3-и сутки после операции.
Инъекция синей массы Героты. Ув. ×16. а — артериальное русло: видны расширенные и извитые кожные артерии; б — венозное русло: дилатированные, прямолинейно расположенные вены.
Динамика изменения диаметра сосудов кожи эпигастральных лоскутов после полной хирургической денервации характеризовалась двухфазной реакцией: уменьшением диаметра артерий и вен в течение первых 3 сут после операции, затем статистически значимым увеличением их диаметра на 7-е сутки (p<0,05). Явления вазодилатации сохранялись почти в неизменном состоянии до 14-х суток (табл. 1).
Таблица 1. Диаметр осевых артерий и вен (мкм) эпигастрального лоскута после периадвентициальной симпатэктомии сосудистой ножки, Me [Q25; Q75]
Периферическое кровоснабжение в денервированном несвободном лоскуте и приживление в реципиентном ложе
При неосложненном течении послеоперационного периода сразу после денервации сосудистой ножки и транспозиции выделенного эпигастрального лоскута цвет кожи лоскута бледно-розовый; симптом исчезающего пятна — 2 с; умеренная отечность лоскута; контактное кровотечение (игла G25) — кровь красного цвета. Повязка умеренно промокала геморрагическим отделяемым, кожные швы спокойные, состоятельные. На 3-и сутки: цвет кожи лоскута розовый; симптом исчезающего пятна — 2 с; сохраняется умеренный отек лоскута; контактное кровотечение (игла G25) — кровь красного цвета. Полное приживление лоскута происходило к 10-м суткам: цвет кожи розовый, симптом исчезающего пятна — 3 с; сохраняется умеренный отек лоскута; контактное кровотечение (игла G25) — кровь красного цвета. Мелкое, ячеистое шелушение кожных покровов. К 14-м суткам кожные покровы лоскута в проекции рубца не выступали над поверхностью реципиентного ложа; множественные мелкие волоски. Рубец широкий, атрофический (рис. 4).

Рис. 4. Несвободный эпигастральный лоскут после его транспозиции с хирургической денервацией (неосложненное течение).
Широкий атрофический кожный рубец, 14-е сутки после операции.
В третьей (опытной) группе животных — реплантация полностью денервированного свободного эпигастрального лоскута по P.G. van der Sloot (2002); в отличие от полностью хирургически денервированного несвободного лоскута ситуация усугублялась пролонгированной первичной ишемией. Несмотря на 60—90-минутную первичную ишемию и синдром ишемии/реперфузии (компенсированный), в 91% случаев послеоперационное течение было неосложненным. Осложненное течение с гибелью лоскутов на 3-и сутки было в 9% случаев. Причина — тромбоз бедренной вены.
Микроанатомия сосудистого русла в полностью денервированном свободном эпигастральном лоскуте отличалась от микроанатомии сосудов в полностью денервированном несвободном эпигастральном лоскуте. Если после реперфузии полностью денервированного свободного лоскута (реплантата) сосудистые реакции касались в равной степени артериального и венозного звеньев, то после транспозиции полностью денервированного несвободного эпигастрального лоскута основные сосудистые реакции касались в основном артериального звена (рис. 5 и 6, табл. 2).

Рис. 5. Артериальное русло реплантированного эпигастрального лоскута, 3-и сутки после операции.
В центре — дилатированная аксиальная артерия. Инъекция синей массы Героты. Ув. ×16.

Рис. 6. Венозное русло реплантированного эпигастрального лоскута, 3-и сутки после операции.
В центре — резко расширенная аксиальная вена. Инъекция синей массы Героты. Ув. ×16.
Таблица 2. Диаметр осевых артерий и вен (мкм) свободного эпигастрального лоскута после его реперфузии, Me [Q25; Q75]
Примечательно, что в свободном реперфузируемом эпигастральном лоскуте (реплантате) значительная дилатация и извитость артериальных и венозных сосудов была весьма продолжительной, уменьшалась она только к 14-м суткам. Эти сосудистые реакции отличаются от тех, которые наступают после полной хирургической денервации лоскута. Они могут исчезнуть только после полной реиннервации паравазальных сосудодвигательных нервов, которая, по нашим данным, наступает через 30 сут после хирургического восстановления целостности пересеченных нервов [11]. Поэтому сосудистые реакции в реперфузируемом кожно-фасциальном (эпигастральном) лоскуте, выявляемые до 14-х суток после операции, можно интерпретировать как реперфузионное повреждение мышечной оболочки артериальных и венозных сосудов.
Периферическое кровообращение в денервированном свободном лоскуте и приживление в реципиентном ложе
В течение первых 2 ч после реперфузии лоскут был бледным. Умеренное пропитывание повязки кровью и серозным отделяемым по ходу раны; симптом исчезающего пятна — 2 с; контактное кровотечение (игла G25) — кровь красного цвета. На 3-и сутки после операции окраска реплантата соответствовала таковой окружающих тканей; симптом исчезающего пятна — 2 с; умеренная отечность лоскута; контактное кровотечение (игла G25) — кровь красного цвета (рис. 7).

Рис. 7. Свободный эпигастральный лоскут после его пересадки (неосложненное течение), 3-и сутки после операции.
Цвет кожи лоскута соответствует окраске кожных покровов окружающих тканей.
К 5-м суткам в области краев раны — участки шелушения эпидермиса; воспалительный процесс отсутствовал; капиллярный ответ (симптом исчезающего бледного пятна) был положительным. При надавливании зажимом лоскут бледнел, а через 2 с после прекращения давления восстанавливалась естественная окраска лоскута. Рана заживала первичным натяжением к 10—14-м суткам (рис. 8).

Рис. 8. Свободный эпигастральный лоскут на 14-е сутки после его пересадки (неосложненное течение).
Нормотрофический кожный рубец.
Заключение
Особенность реакции сосудистого русла в полностью денервированном несвободном эпигастральном лоскуте, изолированного от окружающих тканей (кожи, подкожной клетчатки, поверхностной фасции) с десимпатизированными сосудами, — это двухфазные изменения микроанатомии кожных артериальных сосудов с частичной блокадой микроциркуляции (с гипоперфузией). С первых суток (до трех) они проявлялись сужением просвета артерий (первая фаза), а затем их дилатацией (вторая фаза) и извитостью на фоне немного дилатированных и прямолинейно расположенных вен. Эта реакция (вторая фаза) была весьма продолжительной; она оставалась неизменной и на 14-е сутки, когда завершался процесс приживления лоскута в реципиентном ложе с формированием патологического атрофического кожного рубца. Вторая фаза может завершиться, предположительно, после полной реиннервации паравазальных сосудодвигательных нервов. В свободном реперфузируемом эпигастральном лоскуте (реплантате) сосудистые реакции в коже характеризовались значительной дилатацией и извитостью как артериальных, так и венозных сосудов на фоне трехдневного тканевого отека после реперфузии. Дилатация и извитость сосудов уменьшалась к 14-м суткам, но полностью не исчезала. И тем не менее на 10-е сутки после успешной реперфузии на фоне поврежденного механизма ауторегуляции микроциркуляции в коже происходило приживление кожно-фасциального лоскута с формированием нормотрофического кожного рубца.
Таким образом, артериально-венозные сосудистые реакции в успешно реперфузируемом кожно-фасциальном (эпигастральном) лоскуте до 14-х суток можно интерпретировать как комплекс реперфузионного и нейрогенного повреждения мышечной оболочки кожных сосудов. При этом кожа и фасция, обладающие высокой толерантностью к аноксии, остаются вне этого реперфузионного воздействия.
Кровоснабжение кожи. Интенсивность кровотока в сосудах кожи. Миогенная, гуморальная регуляция кровотока в коже.
Кожа в большей степени, чем другие органы, подвержена прямому действию высоких и низких температур, ультрафиолетовых лучей, механических факторов и т. д. Кровоток по ее сосудам значительно превышает собственные нутритивные потребности. Это объясняется тем, что выполнение важнейшей функции кожи человека — участие в терморегуляции — определяется не активностью метаболических процессов в ней, а теплопереносящей функцией кровотока.
В покое при нейтральной температуре внешней среды кожа получает от 5 до 10 % сердечного выброса. Суммарный кожный кровоток взрослого человека при этом составляет 200—500 мл/мин. В различных частях поверхности тела кожный кровоток значительно отличается. Например, в коже спины он составляет 9,5 мл/100 г/мин, на передней поверхности тела 15,5 мл/100 г/мин. Наиболее интенсивный кровоток отмечается в коже пальцев рук и ног, где находится большое количество артериовенозных анастомозов.
Диапазон возможного возрастания кровотока в коже велик: отношение объемной скорости кровотока в покое к максимальной его величине составляет 1:8. Максимальной величины кожный кровоток у человека достигает при тепловом стрессе. В условиях высокой внешней температуры он может возрастать с 200—500 мл/мин до 2,5—3 л/мин, а при продолжительном нагревании организма человека (температура кожи 42 °С) увеличивается до 8 л/мин, составляя 50—70 % сердечного выброса.
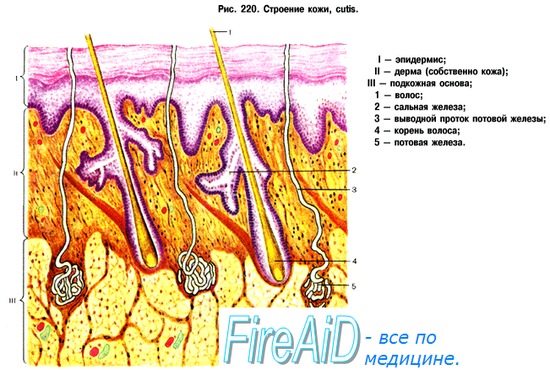
Нервная регуляция кровоснабжения кожи обеспечивается широко представленной иннервацией ее сосудов (особенно артериовенозных анастомозов) симпатическими адренергическими сосудосуживающими волокнами. Повышение их активности обусловливает сужение кожных сосудов, а торможение — приводит к вазодилатации.
Главным фактором в регуляции кожного кровотока является температура тела, снижение которой приводит к рефлекторному сужению как артериальных, так и венозных сосудов кожи, что способствует перемещению крови в глубокие вены и сохранению тепла. При общем охлаждении снижается кровоток как через артериовенозные анастомозы, так и через капилляры кожи. Эта реакция опосредована через гипоталамус, а эффектор-ными ее путями являются адренергические нервные волокна. При общем воздействии на организм высоких температур происходит увеличение кожного кровотока за счет, главным образом, раскрытия артериовенозных анастомозов, кровоток через которые увеличивается в 3—3,5 раза. Раскрытие анастомозов является следствием угнетения сосудосуживающей им-пульсации к кожным сосудам по симпатическим адренергическим волокнам, обусловливающим стимуляцию В-адренорецепторов. Медиаторами активной кожной вазодилатации являются гистамин и допамин.
Гуморальная регуляция. В коже имеется большое количество тучных клеток — источника вазоактивных веществ. Дегрануляция тучных клеток и выделение вазоактивных веществ (гистамина, серотонина и др.) происходит при непосредственном воздействии на кожу ультрафиолетового облучения, механических и других факторов. В сосудах кожи имеются Н,-и Н2-гистаминовые рецепторы, опосредующие вазодилататорное действие эндогенного и экзогенного гистамина. Расширение сосудов кожи вызывает субстанция Р, оказывая при этом как прямое влияние на гладкую мышцу сосудов, так и опосредованное — через гистамин, выделяющийся из тучных клеток. В коже происходит биосинтез простагландинов. Внутрикожное введение простагландинов Е2 и Н2 вызывает расширение кожных сосудов, а простагландина F2a — сужение их.
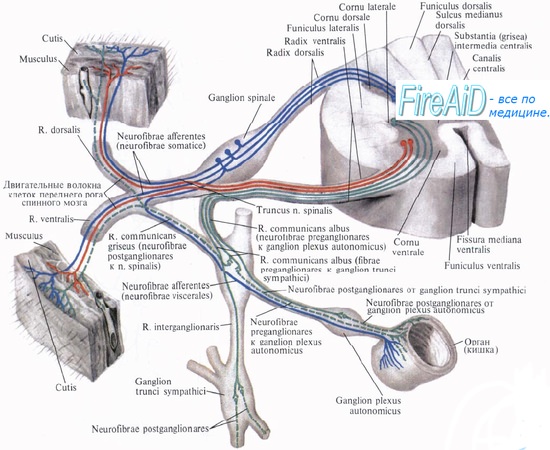
Температура самой крови является фактором, играющим важную роль в локально действующих механизмах контроля сосудистых функций в коже. При локальном нагревании кожи имеет место увеличение капиллярного кровотока без существенных изменений кровотока через артериовенозные анастомозы. В механизме вазодилатации при локальном нагревании кожи большую роль играет освобождение вазоактивных веществ (АТФ, субстанция Р, гистамин) и накопление метаболитов. Однако большее значение в развитии гиперемии в этом случае имеет прямое действие тепла на гладко-мышечные элементы кожных сосудов. При повышении температуры крови снижается миогенный тонус и уменьшаются реакции гладких мышц сосудов кожи на симпатическую импульсацию и вазоконстрикторные вещества, в частности на норадреналин. Снижение адренореактивности гладких мышц кожных сосудов под влиянием гипертермии связано с уменьшением чувствительности их альфа-адренорецепторов.
При локальном действии на кожу низких температур имеют место вазоконстрикции и снижение кожного кровотока, что обусловлено как повышением сосудистого тонуса, так и увеличением вязкости крови.
Советы мониторингу и пульс-оксиметрии у пациентов в хирургии
1. Принцип работы пульс-оксиметра?
В крови взрослых людей циркулируют 4 типа гемоглобина, которые обладают различным спектром свегопоглощеиия:
• Восстановленный гемоглобин (RHb)
• Оксигемоглобин (HbО2)
• Метгемоглобин (Met Hb)
• Карбоксигемоглобин (СО Hb)
Современные пульс-оксиметры излучают свет 2 длин волн: красные (длина волны 680 нм) и инфракрасные (длина волны 940 нм). Эти волны позволяют наиболее точно дифференцировать HbО2 и RHb. В принципе работы пульс-оксиметра лежит оптическая плетизмография, что позволяет измерять насыщение гемоглобина кислородом только во время пульсации артерии.
2. Какова точность пульс-оксиметрии?
Метод высокоточен, если гемоглобин составляет 70-95%.
3. Насколько точно можно определить "на глаз", что артериальная кровь недостаточно оксигенирована?
Не очень точно. Пульс-оксиметрию следовало бы считать пятым по значимости параметром жизнедеятельности.
4. Как пульс-оксиметр реагирует на патологические формы гемоглобина?
При отравлении угарным газом или цианидами нульс-оксиметр воспринимает патологические соединения гемоглобина как комбинацию HbО2 и RHb. Это приводит к завышению показателей насыщения кислородом. При метгемоглобинемии пульс-оксиметр занижает показатели насыщения гемоглобина кислородом в артериальной крови.
5. Могут ли еще какие-нибудь внешние факторы или клинические состояния приводить к неточным показаниям пульс-оксиметра?
Достоверность пульсовой оксиметрии зависит от наполнения пульса и качества светопередачи. Поэтому неточность показателей наблюдается при гипотензии (имеется в виду артериальное давление ниже 50 мм рт. ст.), гипотермии (ниже 35°С), сосудистых заболеваниях (плохая периферическая перфузия) и вазопрессорной терапии (вазоконстрикция). Кроме того, ошибки в передаче сигнала вызывают яркие лампочки, внутривенные контрастные вещества, лак на ногтях и активные движения.
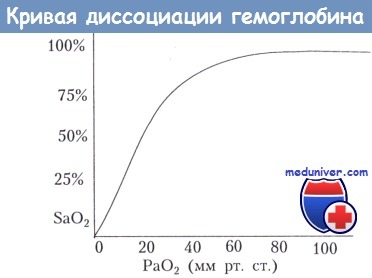
6. Какова взаимосвязь между насыщением оксигемоглобина кислородом (SaО2) и парциальным давлением кислорода (РаО2)?
Для правильного использования пульс-оксиметрии необходимо вспомнить кривую диссоциации оксигемоглобина. Отклонение кривой в правую сторону (понижение сродства Hb к О2) способствует более быстрому отсоединению кислорода па уровне тканей. Повышение температуры, повышение РаСО2, повышение 2,3-ДФГ (дифосфорглицерат) и повышение концентрации ионов водорода (все “повышаются”) вызывают отклонение кривой вправо. Однако, когда РаО2 превышает 100 мм рт. ст., кривая практически становится прямой. Следовательно, значительное снижение РаО2 может произойти без видимых изменений SaО2.
7. Каковы показания к непрерывной пульс-оксиметрии?
В палатах интенсивной терапии пульс-оксиметрия должна быть включена в стандартный мониторинг. Пульс-оксиметрия является уникально ценным методом наблюдения за больным во время транспортировки, при отключении от респиратора и существенных изменениях параметров вентиляции. Кроме того, непрерывная пульс-оксиметрия используется для мониторинга за тяжелыми больными, находящимися вне БИТ (приемное отделение, рентгеновский кабинет).
8. Как проводится непрерывная оксиметрия смешанной венозной крови?
В основе оксиметрии смешанной венозной крови лежит отраженная спектрофотометрия. Узкий спектр света посылается через фиброоптический пучок на верхушку катетера к потоку крови и отражается другим фиброоптическим пучком па фотодетектор. Последний определяет относительное поглощение света. Затем микропроцессор рассчитывает насыщение гемоглобина кислородом в смешанной венозной крови (SvО2).
9. Назовите нормальные значения насыщения О2 смешанной венозной крови?
Нормальное парциальное давление О2 в смешанной венозной крови (PvО2) составляет 40 мм рт. ст. В стандартных условиях этот показатель соответствует 75% SvО2, то есть крутому подъему кривой диссоциации гемоглобина. Таким образом, 3/4 О2, поступающего из аорты (DО2), возвращается в правые отделы сердца.
10. Как с помощью катетеризации легочной артерии определить количество поступающего к тканям и поглощаемого кислорода?
Уравнение Фика выражает отношение между общей доставкой кислорода (ДО2) и объемом кислорода, потребленного тканями (ПО2):
ПО2 = СО х (СаО2 - CvО2),
где СаО2 — концентрация кислорода в артериальной крови; CvО2 — концентрация кислорода в смешанной венозной крови и СО — сердечный выброс. Доставленный кислород определяется следующим уравнением:
ДО2 = СаО2 х СО,
где СаО2 = (1,36 х [концентрация гемоглобина] х [сатурация кислорода в артериальной крови] + РаО2 х 0, 003), a CvО2 = (1,36 х [концентрация гемоглобина] х [сатурация кислорода в венозной крови] + РаО2 х 0,003).
11. Опишите 4 главные причины внезапного падения SvО2?
Стабильно нормальные показатели SvО2 придают уверенности в сбалансированности процессов доставки и поглощения кислорода. В то же время внезапное падение SvО2 предупреждает о (1) низком сердечном выбросе; (2) ненасыщенности кислородом артериальной крови; (3) снижении гемоглобина или (4) повышенном поглощении кислорода тканями.
12. Почему SvО2 повышается в условиях общей анестезии и при септическом шоке?
Общая анестезия снижает метаболические потребности организма. Поэтому поглощение кислорода тканями сокращается, a SvО2 повышается. При сепсисе наблюдается значительное шунтирование крови на периферии, высокий сердечный выброс и слабое поглощение кислорода тканями. Все это способствует повышению SvО2.
13. Каковы преимущества непрерывного мониторинга сатурации кислорода в венозной крови?
SvО2 является быстрым показателем обратной связи между проводимым лечением и динамикой заболевания. Однако мониторинг динамики SvО2 имеет более важное значение по сравнению с абсолютными значениями SvО2. Верхушка катетера может покрываться тканевыми белками, и катетер нужно калибровать каждые 12-24 часа.
14. Имеются ли недостатки у компьютерного мониторинга гемодинамики?
Да. Даже в тех случаях, когда компьютер выдает ошибочные значения, мы склонны доверять ему. Показатели гемодинамики представляют собой целое созвездие параметров: сердечный выброс, PaО2, SvО2, диурез, концентрацию лактата в крови и температуру большого пальца стоны.
15. Что такое двойная оксиметрия?
Двойная оксиметрия заключается в одновременном мониторинге насыщения гемоглобина кислородом в артериальной (SaО2) и венозной (SvО2) крови. Это позволяет непрерывно получать текущую информацию о функционировании легких, транспортировке и поглощении кислорода. Двойная оксиметрия особенно важна для подбора оптимальной величины положительного давления в конце выдоха.
16. Что такое чрескожный мониторинг оксигенации?
Чрескожный мониторинг оксигенации — это метод непрерывной регистрации РО2 в коже (РчкО2), которое не всегда равно РО2 в артерии. В 1975 году Ban Дюзи обнаружил, что жировой компонент рогового слоя кожи при повышении температуры плавится, и диффузия газов увеличивается в 1000 раз. Следовательно, электрод РчкО2 должен нагреть кожу до 44-45°С. При повышении температуры поток крови через кожу также усиливается, и капиллярная кровь “артериализируется”. Тем не менее результаты пульс-оксиметрии и чрескожного мониторинга оксигенации интерпретируются одинаково.
17. Если кожа под датчиком артериализирована, почему РачкО2 не равно РаО2?
Четыре фактора способствуют различию РчкО2 и РаО2 (1) сдвиг вправо кривой диссоциации оксигемоглобина при нагревании; (2) различная проницаемость кожи для кислорода; (3) потребление кислорода самой кожей; и (4) поток крови через кожу. Поскольку факторы 1 и 3 противоположно направлены, взаимосвязь между РчкО2 и РаО2 является линейной и зависит только от проницаемости кожи для кислорода и от тока крови через кожу.
18. Что такое кислородная задолженность?
Кислородная задолженность — это совокупная разница между потреблением кислорода в стандартных условиях и при любом патологическом процессе. Другими словами, кислородная задолженность — это количество кислорода, необходимого клеткам для компенсации разницы между доставкой кислорода к тканям и потребностях в нем.
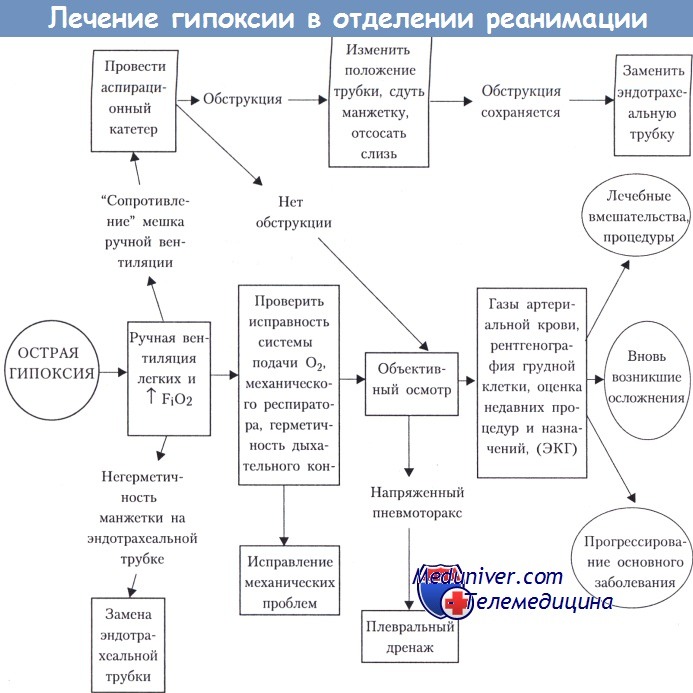
19. Как лечить гипоксию?
При выявлении гипоксии больному немедленно подается дополнительный кислород. Все интубироваиные больные сразу переводятся на ручную вентиляцию легких мешком Амбу. Порванная манжетка эндотрахеальной трубки говорит сама за себя, в то время как ощущение “сопротивления” мешка при ручной вентиляции может возникать по многим причинам: механическая обструкция дыхательных путей, бронхоспазм или напряженный пневмоторакс. Об обструкции эндотрахеальной трубки свидетельствует невозможность проведения через нее аспирационного катетера. Если обструкция не устраняется после изменения положения головы или после сдутия манжетки, эндотрахеальную трубку нужно немедленно заменить. Если при вентиляции мешком Амбу возникают затруднения, по данные за механическую обструкцию воздушных путей отсутствуют, необходимо провести срочное исследование грудной клетки для исключения напряженного пневмоторакса. Необходимо проверить исправность механического респиратора и герметичность дыхательного контура. Для подтверждения факта гипоксии и исключения возможной гиповентиляции определяются газы артериальной крови.
Вторым этапом проводится рентгенографическое исследование грудной клетки передвижным аппаратом, анализ последних назначений лекарственных препаратов и проведенных лечебных процедур (например, санация воздушных путей, изменение положения тела, медсестринские процедуры), а также изменений в клиническом состоянии. В большинстве своем острая гипоксия в палатах интенсивной терапии случается по механическим причинам, которые легко обнаружить и устранить. Например, отсоединение от системы подачи кислорода или скопление слизи, которую необходимо отсосать.
20. Больной был доставлен в больницу после автомобильной аварии. Через 4 часа после диагностической лапаратомии медицинская сестра сообщила, что параметры жизнедеятельности (пульс, температура, частота дыхания, артериальное давление), диурез и показатели транспорта кислорода у него в норме. Существует ли по-прежнему опасность для жизни больного?
Программа реанимации при тяжелой травме (ATLSP) определяет шок как нарушение кровообращения, которое приводит к неадекватной перфузии внутренних органов и недостаточной оксигенации тканей. Это определение абсолютно понятно для декомпенсированного шока. Однако после тяжелых травматических повреждений больные редко переходят из декомпенсированного шока в нормальное физиологическое состояние без признаков продолжающегося субоптимального снижения перфузии тканей. Такие признаки наблюдаются у 85% больных с нормальными АД, ЧСС и диурезом. Оценка эффективности кровоснабжения жизненно важных органов, основанная на нормальных показателях транспорта кислорода, бесполезна, так как не говорит ничего о перераспределении крови к жизненно важным органам и адекватном потреблении О2 клетками. Чтобы полностью компенсировать задолженность по кислороду у больных в группе высокого риска, изменчивые показатели транспорта кислорода должны быть подкреплены одновременным мониторингом косвенных показателей перфузии: концентрация лактата, дефицита оснований и PH слизистой желудка.
21. Являются ли повышенные показатели транспорта кислорода (ДО2, ПО2, сердечный индекс) критериями успешной реанимации?
Да, но этот вопрос не закрыт. Показателями повышенного транспорта кислорода считаются: сердечный индекс = 4,5 л/мип/м2, индекс доставки кислорода > 600 мл/мин/м2 и индекс потребления кислорода > 170 мл/мин/м2. На основании клинического опыта, большинство молодых (а значит, здоровых) пациентов достигают этих показателей при небольшой дополнительной помощи. С другой стороны, у пожилых людей с сердечно-сосудистыми заболеваниями, находящихся в группе повышенного риска, усиление транспорта кислорода может привести к увеличению летальности. Целью основных реанимационных мероприятий является возврат накопленного "кислородного долга". Хотя окончательное воздействие форсированного транспорта кислорода неизвестно, в целом задача ясна. Больного нужно согреть, выбрать оптимальные параметры искусственной вентиляции легких, обеспечить адекватную седацию, обезболить и поддерживать адекватный объем циркулирующей крови.
22. Существуют ли специфические показатели адекватного кровообращения?
Электрокардиография и диурез позволяют оцепить перфузию сердца и почек, соответственно. Кровоснабжение головного мозга можно считать адекватным, если больной говорит вам: “. я помню, сколько придурков набросились на меня. ”. Желудочная тонометрия — это метод оценки кровообращения в органах брюшной полости (висцеральной перфузии). Висцеральная гиперперфузия развивается уже на начальных стадиях шока и может предшествовать изменению общих гемодинамических показателей, показателей транспорта кислорода и кислотно-щелочного состояния.
23. Как выполняется желудочная тонометрия?
Желудочная топометрия осуществляется при помощи назогастральпого зонда, к концу которого прикреплен баллон, проницаемый для СО2. Через некоторое время РСО2 слизистой желудка уравновешивается с РСО2 физиологического раствора в баллоне. Спустя 60 минут после установки баллона определяют РСО2 наполняющего его физраствора; полученное значение принимают за РСО2 слизистой желудка. Для определения концентрации бикарбоната | НСО3-] исследуются газы артериальной крови. Затем pH слизистой желудка рассчитывается по формуле Гендерсона-Гассельбаха:
pHi = 6,1 + Ig ([НСО3-] в артерии/(РСО2 физиологического раствора x 0,03)).
В норме pHi приблизительно составляет 7,38 (7,35 — 7,41). Доказано, что если у тяжелых больных удается предупредить отклонения pHi и удержать его значения на цифрах выше 7,32 в первые 24 часов от начала заболевания, то это улучшает прогноз выживаемости.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Регуляция кровотока в головном мозге. Перфузия мозга
В норме скорость мозгового кровотока (перфузии мозга) составляет 700-850 мл/мин (каждые 100 г мозгового вещества в минуту получают 55 мл крови), что составляет 20 % общего сердечного выброса. В головном мозге существуют механизмы саморегуляции объема мозгового кровотока, при помощи которых ткани мозга способны самостоятельно регулировать величину собственной перфузии.
Миогенный механизм — самый чувствительный, обеспечивает саморегуляцию мозгового кровотока при изменении давления внутри артериол посредством сокращения или расслабления мышц сосудистой стенки. В экспериментальных условиях при исследованиях на животных показано, что миогенный механизм способен поддерживать постоянный уровень перфузии мозга в условиях колебания системного артериального давления в диапазоне 80-180 мм рт. ст. (11-24 кПа).
Кроме того, саморегуляция кровотока происходит за счет реакции гладкой мускулатуры артериол паренхимы мозга на изменение концентрации ионов Н + в межклеточной тканевой жидкости, окружающей сосуды. При гиперкапнии (повышении концентрации СО2 в плазме крови) происходит расширение артериол, а при гипокапнии — сужение.
Увеличение локального кровотока происходит в отделах коры головного мозга и подкорковых ядрах, обеспечивающих выполнение двигательных, чувствительных и когнитивных функций. Локальное расслабление артериол происходит в результате увеличения концентрации ионов К + при распространении потенциала действия, а также ионов Н + в результате клеточного метаболизма.
Резюме. Саморегуляция. Гиперкапния вызывает компенсаторное расширение артериол, а гипокапния—сужение. Повышение давления в просвете артериол приводит к активации миоген-ного механизма саморегуляции.
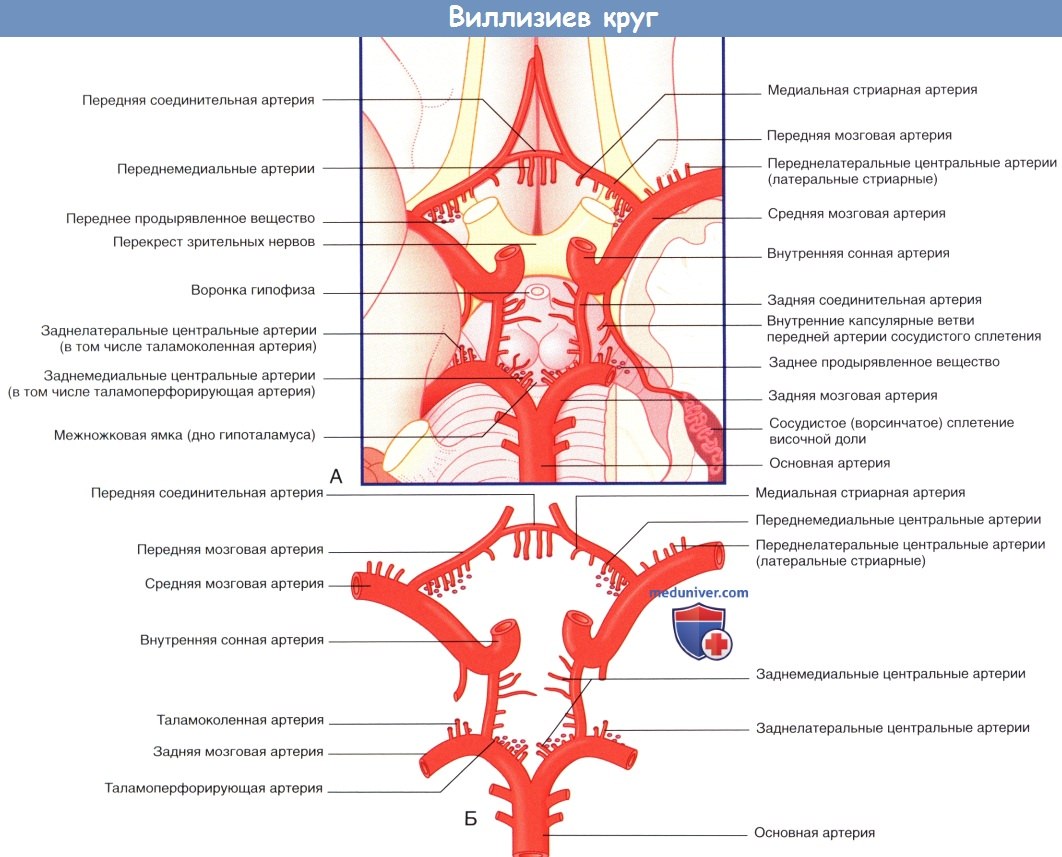
(А) Мозг и структуры виллизиева круга (вид снизу). Левая височная доля частично удалена (в правой части изображения), чтобы показать сосудистое сплетение, расположенное в нижнем роге бокового желудочка.
(Б) Артерии, образующие виллизиев круг. Продемонстрированы четыре группы центральных ветвей. Таламоперфорирующие артерии относят к заднемедиальной группе, таламоколенчатые артерии — к заднелатеральной группе.
Опасные патологические образования в конечностях (например, неоперабельные опухоли) – одна из классических причин ампутации. Изолированная перфузия избавляет от такой перспективы. В данной методике объединены эндоваскулярная хирургия, регионарная химиотерапия, гипертермия и другие инновационные виды лечения. Хорошие результаты дает изолированная перфузия конечностей при лечении неоперабельной саркомы или меланомы, расположенной в руке или ноге.
В международной клинической практике нередко встречается английское название этой процедуры: isolated limb perfusion, или ILP. В клиниках Германии применяется название: isolierte Extremitätenperfusion, либо более полный вариант: isolierte hypertherme Extremitätenperfusion.
Extremitäten – это конечности, Perfusion значит, в широком смысле, протекание жидкости, а в данном случае – кровообращение.
Смысл процедуры состоит в том, что в конечности, пораженной опухолью, на время устанавливается собственный круг кровообращения, изолированный от организма. Для чего это нужно? В кровь, циркулирующую в конечности, добавляют высокодозированные химиопрепараты (цитостатики), разрушающие опухоль. Концентрация этих препаратов была бы губительной для организма. Но в данном случае она губительна только для опухоли.
К тому же кровь, пропускаемую по изолированному кругу, значительно нагревают против нормальных физиологических значений, что также убивает опухоль. Эндоваскулярная хирургия выступает в данном случае как один из элементов онкологического лечения.
После проведения изолированной перфузии возможна полная ремиссия опухоли. Впрочем, основная задача, которую ставят врачи (и она практически во всех случаях достижима!), – ремиссия опухоли до операбельного масштаба. Добившись значительного уменьшения опухоли, ее удаляют обычным хирургическим методом.
Следует, впрочем, отметить, что процедуры изолированной перфузии, требующие сложного оборудование и особой квалификации врачей, проводятся лишь в немногих клиниках в мире. В том числе в Германии. Мировой центр такого лечения – клиника Medias в Бургхаузене, которую возглавляет один из создателей метода изолированной перфузии, известнейший немецкий хирург, гематолог и онколог профессор Карл Райнхард Айгнер.
Как проходит процедура
Она длится около 90 минут, под полным наркозом. Перед ее началом выявляют основную артерию, питающую зону опухоли. Сюда будут введены высокодозированные цитостатики для жесткого подавления опухоли. Нередко цитостатики комбинируют с препаратами из группы факторов некроза опухоли (TNF-альфа). В результате опухоль вместе с кровью получает сильные подавляющие вещества.
Они были бы высокотоксичны и для организма. Но организм пациента оказывается на время процедуры изолированным от «промывания» опухоли цитостатиками.
Для того, чтобы изолировать кровообращение, в главную артерию пораженной конечности и в главную вену вводят баллонные катетеры. Баллоны раздуваются и блокируют кровоток. Кровообращение в изолированной конечности поддерживают через внешнюю систему (аппарат искусственного кровообращения). Это ядовитая кровь, к тому же нагретая до губительной для опухоли температуры. Полтора часа она протекает через опухоль – но не поступает в организм. В нем циркулирует чистая кровь нормальной температуры, свободная от цитостатиков. Эта кровь не поступает в изолированную конечность.
Гарантии безопасности
Чтобы не допустить смешивания «внешней» крови с кровью в конечности, на всем протяжении процедуры ведется так называемый «мониторинг протечек» (Leckagemonitoring). Направления внешнего и изолированного кровотока отображают на особом экране эритроциты пациента, которые накануне были помечены радиоактивными изотопами. Если происходит даже незначительное смешивание наружных и изолированных эритроцитов, экран покажет «протечку». В этом случае процедура будет остановлена. Но при корректном блокировании сосудов такого не случается.
К тому же вместе с наркозом пациент получает гормональную добавку из катехоламинов, которые вызывают сужение сосудов. Баллонное блокирование суженных сосудов получается особо плотным, «протечка» исключена.
По завершении процедуры производят очистку крови из изолированной конечности. Для этого ее прогоняют аппаратом искусственного кровообращения через фильтры. Затем, спустив блокирующие баллоны, выводят их из сосудов, восстанавливая общее кровообращение.
Расчет стоимости процедуры изолированной перфузии конечностей
Стоимость процедуры, разумеется, отнюдь не низкая. Но и, что называется, не поражающая воображение. Она не превышает затрат на полный курс системного лечения или на проведение операции по удалению опухоли. К тому же не будем забывать: альтернативной операцией в данном случае была бы ампутация пораженной конечности. Изолированная перфузия проводится при высокостадийной опухоли, когда спасти конечность (да и жизнь пациента!) иными способами невозможно.
Разумные затраты – этим вообще отличается эндоваскулярная хирургия. За проведение одного цикла изолированной перфузии в клиниках Германии взимают плату около трех тысяч евро. Следует, впрочем, знать, что для достижения результата циклы должны повторяться (не менее трех раз через три-четыре недели). Кроме того взимается плата и за сопутствующие процедуры, а также за пребывание в стационаре (примерно неделя при каждом цикле).
Читайте также:

