Что такое папилломатоз кожи готтрона
Обновлено: 25.04.2024
Папилломатоз — общее название для патологического процесса, характеризующегося образованием множественных папиллом на участке кожи или слизистых оболочек различных органов. Папиллома являет собой доброкачественное новообразование, развивающееся из плоского или переходного эпителия, возвышающееся над ним и имеющее форму сосочка.
Причины развития папилломатоза
В большинстве случаев папилломы имеют вирусную этиологию. Возбудитель заболевания — ДНК-содержащий вирус папилломы человека (ВПЧ) семейства паповавирусов. К настоящему времени определено около 100 типов этого вируса, многие из которых обладают различным по степени риска потенциалом к онкогенности.
Вирус может передаваться от человека к человеку контактным (в том числе половым) путём; установлено, что один из путей заражения вирусом — передача от матери плоду в течение беременности или во время родов, что обуславливает появление папилломатоза и у детей младшего возраста.
Чаще всего инфицирование ВПЧ приводит к бессимптомному носительству, но в ситуациях, когда иммунитет снижается (после длительной болезни, в стрессовых ситуациях, при авитаминозе, при беременности, в случае приёма определенных лекарств, например, глюкокортикостероидов), возникает непосредственное клиническое проявление в виде папиллом.
Помимо вирусной причины, папилломатоз может быть следствием хронических воспалительных процессов. Интересно отметить, что в отдельных ситуациях при выявлении папилломатоза не выявляется признаков вирусного инфицирования, что побуждает к поиску иных причин развития данного заболевания.
Отдельные виды папилломатоза
Папилломы могут поражать кожу и слизистую оболочку практически любого внутреннего органа. Ниже приведены описания отдельных видов папилломатоза в зависимости от того, какая часть тела поражена.
Папилломатоз гортани
Вызывается преимущественно ВПЧ 6 и 11 типов, менее распространены типы 16, 18. Частота встречаемости паппиломатоза гортани в популяции — 2 на 100 000 среди взрослых и 4 на 100 000 среди детей.
Характерными симптомами являются охриплость голоса и нарушения дыхания. Несмотря на то, что папилломатоз гортани является доброкачественным заболеванием, возможны такие серьезные осложнения, как стеноз гортани, распространение папиллом на трахею и бронхи с последующим развитием лёгочной недостаточности, а также перерождение в злокачественную опухоль, особенно если папилломатоз вызван вирусом ВПЧ 16 или 18 типа, у которых высокий уровень потенциальной онкогенности.
Кроме того, папилломатоз гортани может рецидивировать; выделяют «агрессивный» и «неагрессивный» типы рецидивирования. К агрессивному типу относится папилломатоз, по поводу которого проведено 10 и более операций, или более трех операций за год, или при распространении процесса на подголосовой отдел гортани.
Вестибулярный папилломатоз
Этот термин применяется для обозначения мелких паппиломовидных образований преддверия влагалища. Встречается довольно часто у женщин в возрасте до 30 лет и становится показанием к обследованию слизистых влагалища и шейки матки, в том числе и на предмет наличия вируса папилломы человека, так как может сочетаться с поражением шайки матки, хотя сам по себе вестибулярный папилломатоз может и не иметь вирусной природы.
Вестибулярный папилломатоз часто может развиваться без клинических симптомов и обнаруживается при осмотре у гинеколога с профилактической целью или по поводу иных жалоб, но может и проявляться белями, болями и жжением в области вульвы, явлениями диспареунии, сочетаться с локальным воспалительным процессом.
Вестибулярный папилломатоз, в отличие от поражений шейки матки, склонен к рецидивированию — по данным литературы, частота рецидивов составляет до 17%. Обычно рецидивы характерны при инфицировании папилломавирусном низкого онкогенного риска.
Папилломатоз кожи
Папилломатозом кожи называют разрастания многочисленных кожных новообразований на ограниченном участке. Папиллома образуется при разрастании верхнего слоя кожи — эпидермиса. Обычно кожные папилломы имеют размер 5–7 миллиметров, реже до 2 сантиметров. Форма варьирует от точечного или немного свисающего выроста кожи до горошины. Цвет папилломы чаще неотличим от цвета окружающего кожного покрова, но может быть и белого или коричневого цвета. Обыкновенные папилломы чаще всего локализуются на коже спины, ладоней и пальцев рук, подошв и стоп, нитевидные папилломы — в местах с тонкой кожей (веки, шея, подмышечные и паховые области).
Обычно имеет бессимптомное течение и являет собой преимущественно косметический дефект, однако папилломы кожи могут часто травмироваться, что может привести к развитию воспаления или быть фактором риска их озлокачествления.
Особого внимания заслуживает карциноидный папилломатоз кожи Готтрона — редкое предраковое заболевание, характеризующееся специфическими разрастаниями эпидермиса. Основным фактором его возникновения является предрасположенность к развитию множественного поражения кожи папилломами; среди прочих факторов риска следует упомянуть регулярную травматизацию кожных покровов, хронические заболевания кожи, нарушения кровообращения. При данном заболевании очаги расположены симметрично на голенях, чаще на передней поверхности, на фоне длительно существовавшего поражения кожи, имеют вид выступающих над поверхностью на 1–1,5 см папилломатозных бородавчатых разрастаний и вегетаций в виде бляшек значительного размера. Бороздки между очагами заполнены желтовато-белыми липкими массами с неприятным запахом, на некоторых участках они ссыхаются в желтовато-серые корки. Иногда возникают эрозии, поверхностные язвы, легко кровоточащие грануляции. В силу высокого риска озлокачествления (стоит отметить, что ряд авторов приравнивает карциноидный папилломатоз к высокодифференцированному плоскоклеточному раку кожи) данное заболевание требует консультации и лечения у онколога.
Папилломатоз пищевода
Является редкой патологией — согласно данным литературы, его частота составляет всего 4,5%. Папилломы имеют вид полиповидного или листовидного образования белесоватого цвета, размером обычно до 1 см. Характерна локализация поражений в дистальных отделах пищевода. Хотя основной причиной развития данной патологии считается наличие папилломовирусной инфекции, по данным ряда авторов, папилломатоз пищевода встречается и при отсутствии вирусной контаминации. Кроме того, отмечается связь между развитием папилломатоза и гастроэзофагеальным рефлюксом, который в силу длительного воздействия соляной кислоты, содержащейся в желудочном соке, приводит к повреждению и хроническому воспалению слизистой пищевода.
Папилломы пищевода могут долгое время не проявлять себя никакой симптоматикой, но по мере их роста могут появляться следующие жалобы: затрудненное глотание, легкая или умеренная боль за грудиной, отрыжка, тошнота.
В настоящее время считается, что папилломы пищевода являются предраковым заболеванием, и именно папилломатоз в силу распространённости поражения слизистой оболочки пищевода обладает наибольшим риском малигнизации, поэтому выявление папиллом пищевода — это показание к хирургическому лечению.
Внутрипротоковый папилломатоз
Под данным термином понимают папилломы, расположенные в млечных протоках молочной железы. Папилломы могут возникать как в периферических протоках любого квадранта молочной железы, так и в протоках, расположенных сразу за соском. Периферический папилломатоз представлен обычно мелкими, до 1 см, образованиями. В отдельных случаях внутрипротоковые папилломы могут иметь гигантский (более 5 см) размер, в этом случае они значительно деформируют молочную железу. По мере роста папилломы в просвете возникает механическое расширение протока, что может являться причиной развития болевого синдрома.
Внутрипротоковые папилломы могут развиваться в любом возрасте, но чаще возникают в возрасте 35–55 лет. Факторами риска их образования считаются приём оральных контрацептивов и препаратов заместительной гормональной терапии, семейный анамнез, эндокринологические нарушения, наличие хронических воспалительных процессов придатков. Наиболее частым симптомом является появление выделений из соска, не связанных с лактацией, янтарного цвета или с примесью крови. Кроме того, в связи с ростом папиллом может появиться болезненность, становится возможным пропальпировать уплотнения в молочной железе.
Внутрипротоковый папилломатоз требует хирургического лечения в объёме резекции поражённого квадранта или же, в случае значительной распространённости процесса, радикальной мастэктомии, так как обладает значительным потенциалом к перерождению в протоковый рак.
Диагностика папилломатоза
Установить диагноз «папилломатоз» возможно даже при первичном осмотре поражённой области из-за типичного вида новообразований. Папилломы представляют собой мягкую плотную опухоль на ножке (реже на широком основании) размером около одного-двух сантиметров с неровной внешней поверхностью, цвет варьируется от белого до коричневого. В некоторых случаях папиллома может разрастаться и приобретать вид, напоминающий цветную капусту.
Применяемые инструментальные методы диагностики зависят от локализации папилломатоза. Так, при папилломатозе гортани показано проведение ларингоскопии, при поражении пищевода — ЭГДС, при локализации папиллом в протоках молочной железы — дуктография.
Для подтверждения вирусной природы папиллом и определения конкретного типа вируса используются лабораторные методики, позволяющие идентифицировать ДНК вируса — полимеразная цепная реакция (ПЦР), гибридизационные методы.
Наконец, в рамках комплексного лечения целесообразно оценить иммунный статус пациента с целью назначения медикаментозной терапии для профилактики рецидивирования папилломатоза.
Лечение папилломатоза
Основной метод лечения – хирургический. При всей эффективности традиционного хирургического иссечения папиллом существует риск рубцевания слизистой оболочки, поэтому в настоящее время широкое распространение получили не менее эффективные, но более щадящие методы лечения папилломатоза:
- Лазерное удаление
- Ультразвуковая дезинтеграция
- Радиочастотная холодная аблация
- Фотодинамическая терапия
- Электродеструкция
- Криодеструкция
- Диатермокоагуляция
- Удаление химическими агентами (солкодерм, подофиллин)
К сожалению, ни одна из вышеуказанных методик даже при условии полного и тщательного удаления папилломатоза не гарантирует отсутствия рецидива.
Поэтому при наличии факторов риска развития рецидива в послеоперационном периоде может быть назначена адъювантная лекарственная терапия, в рамках которой могут быть назначены следующие препараты:
- Препараты α-интерферона,
- Противовирусные препараты (ацикловир, рибавирин, цидофовир)
- Иммуностимуляторы (ликопид, галавит, циклоферон)
Также в настоящее время проводятся клинические исследования вакцины против вирусов папилломы человека в качестве противорецидивного средства.
Несмотря на обнадеживающие результаты, на данный момент применение вакцины для профилактики рецидивов у больных с уже выявленным папилломатозом стандартом лечения не является.
Профилактика
До недавнего времени наиболее эффективной профилактикой папилломатоза считалось предотвращение заражения папилломавирусной инфекцией, а также лечение сопутствующих хронических инфекционных заболеваний и скрининг, направленный на раннее выявление болезни. Сейчас возможно выполнение профилактической вакцинации. Вакцина направлена против четырех типов папилломавируса, которые имеют наибольшее клиническое значение и наибольший онкогенный риск. Вакцинация возможна как у детей для профилактики заражения этими типами вируса, так и у взрослых. Перед вакцинацией обследование на наличие вирусов папилломы не требуется, так как даже если человек уже заражен один из тех типов, на которые направлена вакцина, иммунопрофилактика убережет его от заражения остальными тремя.
Если папилломатоз уже диагностирован и подвергнут лечению, пациенты подлежат динамическому контролю. Так, больные папилломатозом гортани подлежат обязательной диспансеризации в зависимости от частоты рецидивирования заболевания, но не менее чем раз в три месяца. В случае вестибулярного папилломатоза, даже если доказано отсутствие связи его возникновения с папилломавирусной инфекцией, также требуется активное динамическое наблюдение.
Существует мнение, что практически все живущие ныне люди заражены минимум одним из типов вируса папилломы человека. Большинство являются здоровыми носителями, но проявления инфекции в виде папилломатоза может развиться у любого человека, неся с собой проблемы — от безобидного косметического дефекта до грозного риска развития злокачественной опухоли. Своевременное обращение к врачам «Евроонко» гарантирует решение этих проблем и предотвращение их дальнейшего усугубления.
Акрогерия семейная – это крайне редкое наследственное заболевание, которое относится к группе атрофических дерматозов. Симптомами заболевания является истончение и атрофия кожных покровов на дистальных участках конечностей, в некоторых случаях могут поражаться предплечье и лицо. Диагностика производится на основании исследования состояния кожи у больных семейной акрогерией, гистологического изучения материала биопсии, составления наследственного анамнеза. Эффективное лечение на сегодняшний момент не разработано, с переменным успехом используют витаминные препараты и биогенные стимуляторы.
МКБ-10
Общие сведения
Акрогерия семейная (синдром Готтрона) – редкая форма атрофического дерматоза кожи, поражающая преимущественно кожные покровы кистей, стоп, предплечий, иногда лица (особенно в области носа). Была впервые описана в 1941 году немецким врачом-дерматологом Х. Готтроном. Ему же принадлежит теория, что семейная акрогерия представляет собой ослабленную или абортивную форму прогерии (синдром Гетчинсона-Гилфорда). В настоящий момент в научных кругах других популярных теорий развития этого заболевания не существует. Встречаемость семейной акрогерии по причине значительной редкости заболевания не определена. Дерматоз преимущественно поражает женщин, однако причины этого явления также неясны. В пользу теории Готтрона говорит также наличие наследования семейной акрогерии, появление на ее фоне иных симптомов и пороков развития, характерных для прогерии.

Причины
О непосредственных причинах наследственного атрофического дерматоза практически ничего неизвестно – путем изучения наследственного анамнеза больных было высказано предположение, что он передается по аутосомно-рецессивному типу. Патогенез практически не изучен, разными учеными выдвигаются теории, что при семейной акрогерии имеет место нарушение функций фибробластов определенных участков кожи, дефекты структуры и образование коллагена, недостаточность гипофиза. Кожная атрофия при этом имеет аналогичные с прогерией изменения, которые, однако, располагаются только на определенных участках тела. Тогда как другие характерные проявления синдрома Гетчинсона-Гилфорда (нанизм, тонкость волос и ранняя алопеция, гипоплазия половых органов) при семейной акрогерии никогда не регистрируются.
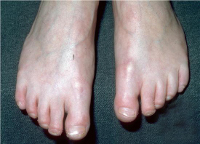
Симптомы семейной акрогерии
Проявления синдрома Готтрона преимущество обнаруживаются у девочек, возможно их выявление сразу после рождения или в первые годы жизни ребенка. Кожа на кистях и стопах истончается, приобретает желтоватый, «пергаментный» вид, очень сильно похожий на старческие изменения кожных покровов. Через истончившуюся кожу хорошо видны кровеносные сосуды.
Возможны дерматологические изменения не только на конечностях, но и на лице – например, на лице нередко имеется яркая эритема. Кроме того, атрофия кожных покровов при семейной акрогерии может развиваться и на лице, особенно на кончике носа. При этом придатки кожи на пораженных участках сохраняются, активность процессов потоотделения остается без изменений.
Помимо кожных симптомов, при семейной акрогерии нередко имеют место и другие проявления. Самым частым из них является акромикрия – уменьшение относительных размеров кистей, пальцы истончены, иногда имеют конусовидную форму. Может регистрироваться микрогнатия, нарушение формирования зубного ряда – помимо искривлений и дефектов наблюдается задержка смены молочных зубов на коренные. Частым спутником семейной акрогерии является склеродермия, ломкость и тонкость кровеносных сосудов. Из-за этого на коже больных легко образуются кровоподтеки даже при незначительном воздействии. У взрослых со временем также обнаруживаются симптомы атрофического гастрита из-за ранней инволюции слизистой оболочки желудка.
Диагностика
В клинической дерматологии диагностика семейной акрогерии зачастую не представляет проблемы из-за характерных проявлений заболевания. Однако значительная редкость этого состояния все-таки может приводить к тому, что оно будет распознано не сразу. Помимо осмотра, для диагностики применяют гистологические исследования биоптата кожи, рентгенологические методики, расспрос больного по поводу наличия или отсутствия подобных изменений у его родственников.
Гистологическая картина пораженных кожных покровов при семейной акрогерии довольно типична для атрофических дерматозов – выраженная атрофия дермы, дегенеративные и беспорядочно расположенные коллагеновые и эластиновые волокна. При этом подкожная клетчатка может сохранять вполне обычный и здоровый вид, такая же ситуация и с эпидермисом – патологические изменения затрагивают только дерму. Также в биоптате наблюдаются дистрофические изменения фибробластов – они увеличены в размерах, имеют многочисленные включения в виде вакуолей.
При семейной акрогерии изменения затрагивают и структуру костей, особенно дистальных отделов конечностей. На рентгенограммах наблюдается уплотнение компактного слоя, костный инфантилизм, иногда обнаруживаются процессы склерозирования. Путем расспроса больного можно составить его наследственный анамнез – во многих случаях проявления семейной акрогерии наблюдались у его родственников, что говорит о генетической природе патологии. Рекомендуется консультация генетика.
Дифференциальная диагностика
Дифференциальную диагностику следует проводить с приобретенными формами геродермии, атрофическим хроническим акродерматитом и другими дегенеративными кожными патологиями.
Лечение семейной акрогерии
Этиотропного лечения акрогерии семейной на сегодняшний день не существует, так как до сих пор не определены ни этиология, ни патогенез заболевания. Рекомендуется применять общие и местные средства, улучшающие питание тканей – на основе витаминов (токоферол, ретинол), гемодеривата крови телят, а также ангиопротекторы. Эффективность этих средств неодинакова у разных больных.
Прогноз и профилактика
Прогноз в отношении жизни пациента благоприятный, но в плане выздоровления – неопределенный или неблагоприятный. Больным следует избегать значительных механических воздействий на пораженные участки кожи, так как это может приводить к развитию кровоподтеков и шрамов, а также ускорять процессы атрофии.
1. Карциноидный папилломатоз кожи Готтрона (клиническое наблюдение)/ Кубанов А.А. и др.// Трудный пациент. - 2018.
2. Клинико-морфологические аспекты карциноидного папилломатоза кожи Готтрона/ Тлиш М.М., Кузнецова Т.Г., Сычева Н.Л.// Медицинский вестник Юга России. - 2014.
Карциноидный папилломатоз кожи Готтрона – редкое дерматологическое заболевание с неясной этиологией, имеющее длительное хроническое течение и достаточно трудно поддающееся лечению. При его развитии на поверхности кожных покровов, преимущественно нижних конечностей, возникают обширные, величиной с ладонь, возвышающиеся бляшки. Диагностика карциноидного папилломатоза кожи Готтрона производится путем осмотра больного, изучения его анамнеза и гистологического исследования тканей в очаге поражения. Этиотропного лечения не разработано, проводится симптоматическая и поддерживающая терапия с использованием антибиотиков, витаминных препаратов, антисептических и цитостатических средств.
Общие сведения

Причины карциноидного папилломатоза кожи Готтрона
Этиология и патогенез этого заболевания до сих пор остаются неясными. Удалось выяснить, что кожные проявления в виде бляшек возникают на месте длительно протекающих дерматологических патологий – псориаза, красного плоского лишая, экземы, ихтиоза, некоторых форм туберкулеза кожи. Предположения о генетической или наследственной природе этого состояния не нашли своего подтверждения. Некоторыми специалистами поддерживается мнение, что это заболевание обусловлено особенностями реактивности организма и его склонностью к папилломатозным разрастаниям. При этом на длительное постоянное травмирование или раздражение кожных покровов (что и происходит при вышеуказанных заболеваниях) ткани реагируют развитием бляшек, характерных для карциноидного папилломатоза кожи Готтрона. Присоединение к этому сапрофитной микрофлоры и вторичной инфекции усугубляет патологический процесс.
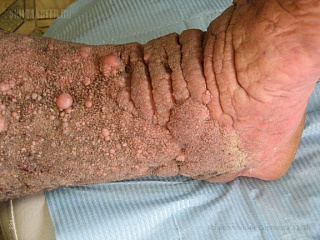
Симптомы карциноидного папилломатоза кожи Готтрона
Самым выраженным и практически единственным проявлением карциноидного папилломатоза кожи Готтрона является образование значительных по размеру (до 10-15 сантиметров) бляшек, приподнятых над окружающей поверхностью на 1-1,5 сантиметра. Преимущественной их локализацией являются нижние конечности на участках, которые подвергались иным дерматологическим заболеваниям. Расположение бляшек, как правило, симметричное, их поверхность покрыта опухолевидными образованиями и многочисленными вегетациями. Они имеют тестообразную консистенцию и отделяемое с неприятным запахом, обусловленное жизнедеятельностью сапрофитной микрофлоры. Грязно-желтый вязкий секрет покрывает всю поверхность бляшки и пространства между вегетациями; засыхая, он образует плотно прилегающие к поверхности образования корки. Опухолевидные образования при карциноидном папилломатозе кожи Готтрона легко подвергаются мацерации, в таком случае на их месте образуются эрозивные очаги.
Диагностика карциноидного папилломатоза кожи Готтрона
Диагностика заболевания осуществляется на основании результатов осмотра дерматолога, изучения анамнеза пациента, гистологических исследований. Осмотр выявляет бляшки с поверхностью, напоминающей из-за опухолевидных узелков и вегетаций цветную капусту и покрытой грязно-желтым секретом и корками с неприятным запахом. Очаги поражения при карциноидном папилломатозе кожи Готтрона расположены симметрично, в случае длительного течения заболевания на их поверхности можно обнаружить эрозии и язвы на месте подвергшихся мацерации вегетаций. При опросе выясняется, что у пациента длительное время до развития настоящего состояния на пораженных участках кожных покровов имелись различные воспалительные заболевания. Аналогичные данные можно получить, изучая историю болезни человека или его амбулаторную карту.
При проведении биопсии кожи и последующего гистологического исследования тканей выявляется выраженный акантоз с образованием тяжей, которые в виде тонких отростков проникают глубоко в дерму. Некоторые из них затем теряют связь с эпидермисом, формируя в дерме эпителиальные «островки» и скопления. Также выявляется выраженная псевдокарциноматозная гиперплазия эпидермиса, в клетках не обнаруживают атипии, характерной для злокачественных новообразований. Часть акантозных тяжей и эпителиальных островков подвергаются ороговению. Также в тканях патологического очага при карциноидном папилломатозе кожи Готтрона выявляется выраженная лимфоцитарная и гистиоцитарная инфильтрация. Дифференциальную диагностику заболевания следует проводить с хронической язвенно-вегетирующей пиодермией, плоскоклеточным раком кожи, хромомикозом.
Лечение карциноидного папилломатоза кожи Готтрона
Этиотропного лечения данной патологии в дерматологии не разработано, для облегчения симптомов используют цитостатические препараты, антибиотики широкого спектра действия, витаминные средства. Из цитостатиков при карциноидном папилломатозе кожи Готтрона наиболее широко применяют проспидин. Второстепенным препаратом для лечения данного состояния являются ксантинола никотинат – средство, обладающее способностью улучшать микроциркуляцию и трофику тканей. Витаминные средства необходимы для нормализации обмена веществ и улучшения регенерационных свойств организма, антибиотики позволяют избежать вторичной инфекции и, по некоторым данным, тоже способствуют уменьшению выраженности симптомов.
Местно при карциноидном папилломатозе кожи Готтрона используют разнообразные антисептические растворы – фурацилина, перманганата калия и др. Регулярные примочки такими препаратами позволяют несколько уменьшить скорость образования корок, снизить количество отделяемого секрета и убрать неприятный запах. Также, по некоторым данным, местные внутрикожные инъекции кортикостероидов, производимые вокруг бляшек, способствуют выздоровлению. Однако в целом данное дерматологическое состояние является трудноизлечимым и не всегда реагирует на предпринимаемые терапевтические меры.
Прогноз и профилактика карциноидного папилломатоза кожи Готтрона
Несмотря на выраженность симптомов и тяжесть проявлений, это состояние редко создает угрозу для жизни больного – карциноидный папилломатоз кожи Готтрона не перерождается в злокачественное новообразование, единственной угрозой является риск вторичной инфекции. Она может спровоцировать тяжелое гнойное воспаление и обусловленные им токсический шок или сепсис. Но прогноз относительно выздоровления неблагоприятный – развитие вегетаций и бляшек может длиться на протяжении многих лет, то затихая, то активизируясь. Кроме того, неприятный запах и неприглядный внешний вид кожных проявлений могут стать причинами психологических проблем у больного. Для профилактики карциноидного папилломатоза кожи Готтрона необходимо своевременно и в полном объеме производить лечение дерматологических патологий, которые могут стать основой для развития этого состояния.
ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ Московской области «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ Московской области «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»;
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
Журнал: Архив патологии. 2020;82(6): 59‑62
ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
В статье представлено наблюдение редкого в Российской Федерации имплантационного микоза — хромобластомикоза. Приводятся данные о распространенности заболевания, этиологии, клинической картине, возможностях диагностики. Подчеркивается ведущая роль патоморфологического исследования в диагностике хромобластомикоза на территории неэндемичных стран, в том числе в России. Дано подробное описание клинической и патоморфологической картины. Обнаружение при гистологическом исследовании пигментированных сферических или полигональных клеток размером 5—12 мкм, которые являются элементами гриба, в цитоплазме макрофагов и внеклеточно позволяет диагностировать хромобластомикоз. Отказ от патоморфологического исследования приводит к диагностическим ошибкам и нерациональной лечебной тактике.
ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ Московской области «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»
ГБУЗ Московской области «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского»;
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
Дата принятия в печать:
Болеют хромобластомикозом преимущественно мужчины в возрасте 41—70 лет [8, 9]. Заболевание начинается после внедрения инфекционного агента в местах микротравм кожи [6, 10]. Чаще поражаются стопы, голени, колени и кисти рук, также сообщается о локализации процесса на коже туловища, носа, век, ушных раковин, плеч и ягодиц [5, 6]. Инкубационный период может варьировать от нескольких недель до нескольких месяцев, причем ряд пациентов не могут вспомнить момент заражения. Первоначально на коже появляется небольшое пятно розового цвета, постепенно трансформирующееся в папулу. Со временем формируются папулосквамозные бляшки, разрастающиеся по периферии, могут появляться сателлитные очаги. Спустя годы очаги приобретают опухолевидную форму, за счет аутоинокуляции процесс распространяется, занимая все более обширные участки. Выделяют несколько клинических форм хромобластомикоза: узловую, опухолевую, веррукозную, рубцующуюся, бляшечную и смешанную, а также 3 степени тяжести (легкую, среднюю, тяжелую) [5]. В результате расчесывания и переноса инфекции на другие участки кожи могут появиться отдаленные от первичного процесса очаги. Описано несколько случаев лимфогенного распространения инфекции от основного очага [11].
Процесс, как правило, развивается достаточно медленно. На начальных этапах и при легких формах заболевание имеет незначительную симптоматику, вследствие чего пациенты практически не обращаются за медицинской помощью. Без лечения процесс продолжает прогрессировать, со временем могут развиваться фиброзные изменения тканей и лимфостаз с образованием лимфедемы. На этом фоне нередко присоединяется вторичная инфекция. В тяжелых случаях у пациентов могут наблюдаться хроническая лимфедема и анкилозы [12]. В случае длительно существующих язвенных или веррукозных поражений, не отвечающих на противогрибковую терапию, возможно развитие плоскоклеточного рака с метастазированием, приводящее к летальному исходу [13].
Для диагностики хромобластомикоза требуется лабораторное подтверждение. В эндемичных странах, где клиницисты хорошо знакомы с данной патологией, обычно проводят микроскопию чешуек для выявления округлых коричневых клеток (так называемых муриформных), которые являются элементами гриба. Поскольку необходимость видовой принадлежности грибов для назначения лечения отсутствует, культуральное исследование проводят редко. В странах, где случаи заболевания единичны, как правило, клиницисты проводят дифференциальный диагноз между несколькими патологиями, для чего берут биоптат кожи. На основании гистологического исследования в этих случаях обычно ставят диагноз «хромобластомикоз». При гистологическом исследовании выявляется выраженная гиперплазия эпидермиса, иногда псевдокарциноматозная, с наличием интраэпителиальных абсцессов из нейтрофилов; в дерме — фиброз, воспалительная инфильтрация из нейтрофилов, эозинофилов, гистиоцитов, лимфоцитов и плазматических клеток, определяются абсцессы с очагами некроза, окруженные зоной гранулематозного воспаления микотические гранулемы. Морфологическая картина хромобластомикоза сходна с другими глубокими микозами, критерием постановки диагноза является обнаружение в цитоплазме макрофагов и внеклеточно склеротических телец — пигментированных сферических или полигональных клеток грибковых микроорганизмов размером 5—12 мкм [14].
Приводим собственное наблюдение хромобластомикоза у мужчины, потупившего в отделение дерматовенерологии.
Больной П., 67 лет, рабочий, житель Московской области, жалобы на множественные образования на коже правого бедра. Считает себя больным в течение 15 лет. После травматизации кожи нижней трети правого бедра металлическим предметом, загрязненным землей, заметил появление пятна красного цвета. Постепенно пятно стало увеличиваться в размере и покрываться сухими корками. Обращался к дерматологу, который рекомендовал использование кортикостероидных мазей. Два года назад рост очагов стал более интенсивным. Одни очаги регрессировали с образованием рубца, рост других продолжался. При обращении дерматолог на основании клинического осмотра диагностировал гипертрофическую форму красного плоского лишая и назначил прижигания раствором Суперчистотела. После использования Суперчистотела пациент отметил интенсивный рост элементов по периферии очагов, обработанных раствором. При удалении гиперкератотических масс в отдельных очагах заметил появление кровотечения. Во время прохождения диспансеризации по месту работы был направлен для установления диагноза и лечения в отделение дерматовенерологии.
При поступлении процесс локализовался на коже правого бедра. Поражение имело размер 25×20 см и представляло возвыщающиеся опухолевидные очаги, покрытые преимущественно сухими гиперкератотическими массами, а также очаги рубцовой атрофии (рис. 1). Субъективных ощущений нет. Сопутствующие заболевания: гипертоническая болезнь IA стадии.

Рис. 1. Поражение бедра у пациента П., 67 лет.
Fig. 1. Hip injury in Patient P., aged 67 years.
На основании клинической картины больному проводился дифференциальный диагноз между карциноидным папилломатозом кожи Готтрона, плоскоклеточным раком и глубоким микозом. Для уточнения диагноза была выполнена биопсия кожи с последующим гистологическим исследованием, при котором в эпидермисе выявлены акантоз, папилломатоз, признаки псевдоэпителиоматозной гиперплазии эпидермиса, интраэпителиальные микроабсцессы из нейтрофилов (рис. 2, а). В дерме — фиброз, гранулематозное воспаление с наличием в цитоплазме отдельных многоядерных гигантских клеток сферических телец коричневого цвета (рис. 2, б, в). Заключение: гистологические изменения соответствуют хромобластомикозу.
На основании клинической и морфологической картины установлен диагноз: хромобластомикоз смешанного варианта (сочетание веррукозного и рубцующегося), тяжелая степень течения. Назначены прием итраконазола в дозе 300 мг/сут и внутривенное ведение 50 мг амфотерицина В. Рекомендовано лечение в течение 8—12 мес с дальнейшим выполнением хирургической эксцизии.

Рис. 2. Пациент П., гистологическое исследование.
а — акантоз, папилломатоз, признаки псевдоэпителиоматозной гиперплазии эпидермиса, внутриэпидермальные микроабсцессы из нейтрофилов, ×200; б — в дерме фиброз, гранулематозное воспаление, ×100; в — в цитоплазме многоядерных гигантских клеток сферические тельца коричневого цвета, ×400; а — в — окраска гематоксилином и эозином.
Fig. 2. Patient P., histological examination.
a — acanthosis; papillomatosis; signs of pseudoepitheliomatous hyperplasia; intraepidermal neutrophilic microabscesses, ×200; b — fibrosis of the dermis; granulomatous inflammation, ×100; c — spherical brown bodies in the cytoplasm of multinucleated giant cells, ×400; a — c — H&E.
Хромобластомикоз редко встречается в РФ, поскольку благоприятной средой обитания для димациевых грибов является тропический и субтропический климат. Кроме того, заболевание в нашей стране диагностируется редко, поскольку врачи, в том числе дерматологи, недостаточно знакомы с данной патологией. За последние 10 лет (2010—2019 гг.) в отечественной литературе мы встретили 2 случая хромобластомикоза, причем один также был диагностирован сотрудниками нашей клиники [13, 15]. В обоих случаях диагноз «хромобластомикоз» был гистологической находкой. Важно подчеркнуть, что в сложных диагностических ситуациях необходимо проводить гистологическое исследование, которое помогает верифицировать диагноз. Как показывает история нашего пациента, неправильная диагностика, основанная только на клинической картине заболевания, и назначенное лечение привели к бурному прогрессированию процесса. Поскольку хромобластомикоз может осложняться развитием плоскоклеточной карциномы, гистологическое исследование при данном заболевании особо актуально.
Папилломатоз гортани остается одной из неразрешимых проблем современной оториноларингологии. В статье отражается историческая последовательность изучения заболевания, приводятся варианты лечения и ре- зультаты собственного исследования, в ходе которого сравнивались 2 способа лечения больных папилломатозом гортани.
Для цитирования: Свистушкин В.М., Волкова К.Б. Современное состояние проблемы респираторного папилломатоза гортани. РМЖ. 2015;23:1377-1380.
В статье приведено современное состояние проблемы респираторного папилломатоза гортани
Для цитирования. Свистушкин В.М., Волкова К.Б. Современное состояние проблемы респираторного папилломатоза гортани // РМЖ. 2015. No 23. С. 1377 –1380.
Резюме: папилломатоз гортани остается одной из неразрешимых проблем современной оториноларингологии. В статье отражается историческая последовательность изучения заболевания, приводятся варианты лечения и результаты собственного исследования, в ходе которого сравнивались 2 способа лечения больных папилломатозом гортани.
Ключевые слова: папилломатоз гортани, вирус папилломы человека, противовирусная терапия.
1. Ашуров З.М., Зенгер В.Г. Респираторный папилломатоз у детей. М.: Медиа-сфера, 2004.
2. Солдатский Ю.Л., Киселев В.И., Онуфриева Е.К., Стеклов А.М., Шепин Н.В., Стрыгина Ю.В., Гаспарян С.Ф., Погосова И.Е. Анализ эффективности противорецидивной терапии ювенильного респираторного папилломатоза при помощи индинола // Вестник оториноларингологии. 2006. № 1. С. 46–48.
3. Best S.R., Friedman A.D., Landau-Zemer T., Barbu A.M., Burns J.A., Freeman M.W., Halvorsen Y.D., Hillman R.E., Zeitels S.M. Safety and dosing of bevacizumab (avastin) for the treatment of recurrent respiratory papillomatosis // Ann Otol Rhinol Laryngol. 2012 Sep. Vol. 121 (9). Р. 587–593.
4. Кучерова Л.Р. Клинико-иммунологическое обоснование местного применения рекомбинантного интерферона-альфа2 в терапии рецидивирующего респираторного папилломатоза: Дисс. … канд. мед. наук. М., 2011.
5. Carvalho C.M., Huot L., Charlois A.L., Khalfallah S.A., Chapuis F. Prognostic factors of recurrent respiratory papillomatosis from a registry of 72 patients // Acta Otolaryngol. 2009 Apr. Vol. 129 (4). Р. 462–470.
6. Свистушкин В.М., Мустафаев Д.М. Папилломатоз гортани: современное состояние проблемы // Вестник оториноларингологии. 2013. № 2. С. 79–85.
7. Derkay C.S., Volsky P.G., Rosen C.A., Pransky S.M., McMurray J.S., Chadha N.K., Froehlich P. Current use of intralesional cidofovir for recurrent respiratory papillomatosis // Laryngoscope. 2013 Mar. Vol. 123 (3). Р. 705–712. DOI: 10.1002/lary.23673. Epub 2012 Oct 15.
8. Abramson A.L., Levy A.S., Hirschfield L.S. The pathologic and thermal effects of gold vapour laser photodynamic therapy on the larynx. Experimental study // Arch. Otolaryngol. Head Neck Surg. 1990, Jun. Vol. 116. N 6. P. 687–691.
9. Bell R., Hong W.K., Itri L.M., McDonald G., Strong M.S. The use of cis-retinoic acid in recurrent respiratory papillomatosis of the larynx: a randomized pilot study // Am J Otolaryngol. 1988 Jul-Aug. Vol. 9 (4). Р. 161–164.
10. Hartnick C.J., Boseley M.E., Franco R.A. Jr, Cunningham M.J., Pransky S. Efficacy of treating children with anterior commissure and true vocal fold respiratory papilloma with the 585-nm pulsed-dye laser // Arch Otolaryngol Head Neck Surg. 2007 Feb. Vol.133 (2). Р. 127–130.
11. Bishai D., Haskins K. Keerti Shah The Cost of Juvenile-Onset Recurrent Respiratory Papillomatosis // Arch Otolaryngol Head Neck Surg. 2000. Vol. 126 (8). Р. 935–939.
12. Carney A.S., Evans A.S., Mirza S., Psaltis A. Radiofrequency coblation for treatment of advanced laryngotracheal recurrent respiratory papillomatosis // Journal of Laryngology and Otology. 2010. Vol. 124 (5). Р. 510–514.
13. Donne A.J., Hampsonb L. Homer J.J., Hampsonb I.N. The role of HPV type in Recurrent Respiratory Papillomatosis // International Journal of Pediatric Otolaryngology. 2010. Vol. 74 (1). Р. 7–14.
14. Kashima H., Mounts P., Leventhal B., Hruban R.H. Sites of predilection in recurrent respiratory papillomatosis // Ann Otol Rhinol Laryngol. 1993 Aug. Vol. 102 (8 Pt 1). Р. 580–583
15. Kashima H.K., Kessis T., Mounts P., Shah K. Polymerase chain reaction identification of human papillomavirus DNA in CO2 laser plume from recurrent respiratory papillomatosis // Otolaryngol Head Neck Surg. 1991 Feb. Vol. 104 (2). Р. 191–195.
16. Carvalho C.M., Huot L., Charlois A.L., Khalfallah S.A., Chapuis F. Prognostic factors of recurrent respiratory papillomatosis from a registry of 72 patients // Acta Otolaryngol. 2009 Apr. Vol. 129 (4). Р. 462–470.
17. Chadha N.K., James A. Adjuvant antiviral therapy for recurrent respiratory papillomatosis // Cochrane Database Syst Rev. 2012 Dec 12. Vol. 12. CD005053.
18. Derkay C.S., Hester R.P., Burke B., Carron J., Lawson L. Analysis of a staging assessment system for prediction of surgical interval in recurrent respiratory papillomatosis // Int J Pediatr Otorhinolaryngol. 2004 Dec. Vol. 68 (12). Р. 1493–1498.
19. Derkay C.S., Volsky P.G., Rosen C.A., Pransky S.M., McMurray J.S., Chadha N.K., Froehlich P. Current use of intralesional cidofovir for recurrent respiratory papillomatosis // Laryngoscope. 2013 Mar. Vol. 123 (3). Р. 705–712. DOI: 10.1002/lary.23673. Epub 2012 Oct 15.
20. Derkay C.S. Recurrent respiratory papillomatosis // Laryngoscope. 2001. Vol. 111 (1). Р. 57–69.
21. Derkay C.S., Wiatrak B. Recurrent respiratory papillomatosis: a review // Laryngoscope. 2008 Jul. Vol. 118 (7). Р. 1236–1247.
21. Mahnke C.G., Fröhlich O., Lippert B.M.,Werner J.A. Recurrent laryngeal papillomatosis. Retrospective analysis of 95 patients and review of the literature // Otolaryngol P. 1996. Vol. 50 (6). Р. 567–578.
22. Förster G., Boltze C., Seidel J., Pawlita M., Müller A. Juvenile laryngeal papillomatosis--immunisation with the polyvalent vaccine gardasil // Laryngorhinootologie. 2008. Vol. 87 (11). Р. 796–769.
23. Hallmo P., Naess O. Laryngeal papillomatosis with human papillomavirus DNA contracted by a laser surgeon // Eur Arch Otorhinolaryngol. 1991. Vol. 248 (7). Р. 425–427.
24. Hermann J.S., Pontes P., Weckx L.L., Fujita R., Avelino M., Pignatari S.S. Laryngeal sequelae of recurrent respiratory papillomatosis surgery in children // Rev Assoc Med Bras. 2012. Vol. 58 (2). Р. 204–208.
25. El-Bitar M.A.,Zalzal G.H. Powered instrumentation in the treatment of recurrent respiratory papillomatosis: an alternative to the carbon dioxide laser // Arch Otolaryngol Head Neck Surg. 2002 Apr. Vol. 128 (4). Р. 425–428.
26. Hester R.P., Derkay C.S., Burke B.L., Lawson M.L Reliability of a staging assessment system for recurrent respiratory papillomatosis // Int J Pediatr Otorhinolaryngol. 2003 May. Vol. 67 (5). Р. 505–509.
27. Larson D.A., Derkay C.S. Epidemiology of recurrent respiratory papillomatosis // APMIS. 2010 Jun. Vol. 118 (6-7). Р. 450–454.
28. McMurray J.S., Connor N., Ford C.N. Cidofovir efficacy in recurrent respiratory papillomatosis: a randomized, double-blind, placebo-controlled study // Ann Otol Rhinol Laryngol. 2008 Jul. Vol.117 (7). Р. 477–483.
29. Shikowitz M.J. Comparison of pulsed and continuous wave light in photodynamic therapy of papillomas: an experimental study // Laryngoscope. 1992 Mar. Vol. 102 (3). Р. 300–310.
30. Zeitels S.M., Akst L.M, Burns J.A., Hillman R.E., Broadhurst M.S., Anderson R.R. Office-based 532-nm pulsed KTP laser treatment of glottal papillomatosis and dysplasia // Ann Otol Rhinol Laryngol. 2006 Sep. Vol. 115 (9). Р. 679–685.
31. Lee R.G., Vecchiotti M.A., Heaphy J., Panneerselvam A., Schluchter M.D., Oleinick N.L., Lavertu P., Alagramam K.N., Arnold J.E., Sprecher R..C. Photodynamic therapy of cottontail rabbit papillomavirus-induced papillomas in a severe combined immunodeficient mouse xenograft system // Laryngoscope. 2010 Mar. Vol. 120 (3). Р. 618–624.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:

