Что такое оппортунистические микозы
Обновлено: 26.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Онихомикоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Онихомикоз – это грибковое поражение ногтя, при котором наблюдается изменение его цвета, толщины и отделение от ногтевого ложа. Онихомикоз - часто встречающееся заболевание ногтевого аппарата (не менее 50% всех заболеваний ногтей), которым болеет около 5,5% людей во всем мире. Взрослые болеют чаще, чем дети, поскольку распространенность онихомикозов увеличивается с возрастом (поражение ногтевых пластинок грибком встречается почти у 50% лиц старше 70 лет).
Причины возникновения онихомикоза
Онихомикоз могут вызывать грибы-дерматофиты, дрожжевые грибы и плесневые грибы-недерматофиты.
Дерматофиты становятся причиной заболевания в 60-70% случаев, при этом до 50% приходится на Тrichophyton rubrum. Плесневые грибы-недерматофиты вызывают около 20% всех онихомикозов, а дрожжевые грибы, в том числе Candida spp., - 10-20%.
Достаточно часто обнаруживается ассоциированное поражение грибами и бактериями, а также одновременное инфицирование ногтевой пластинки двумя и более грибами.
Развитию онихомикоза способствуют травмы опорно-двигательного аппарата, нарушение кровоснабжения конечностей (например, вследствие сердечной недостаточности, облитерирующего эндартериита или варикозного расширения вен), сахарный диабет, ожирение, плоскостопие, деформация стоп, курение, псориаз, иммунодефициты. К другим предрасполагающим факторам относят ношение тесной обуви, повышенную потливость, травмы ногтей. Высокий риск приобрести грибок есть у тех, кто участвует в спортивных мероприятиях, посещает общественные бани и бассейны, проживает с родственниками, у которых диагностирован грибок, или у тех, кто уже болел онихомикозом ранее.
Ногти на ногах поражаются чаще, чем на руках, что, вероятно, связано с их более медленным ростом, худшим кровоснабжением и с тем, что ношение тесной обуви создает среду, благоприятную для размножения грибка.
Заражение патогенными грибками может происходить при непосредственном контакте с больным онихомикозом, а также через обувь, одежду, предметы обихода (коврики в ванной, мочалки, маникюрные принадлежности и др.). В условиях повышенной влажности (в бассейнах, банях, душевых) грибы длительное время сохраняются и размножаются, особенно на неокрашенных деревянных поверхностях.
При заражении возбудитель проникает в ногтевую пластинку, ложе, матрикс и проксимальный валик ногтя. Ноготь не обладает эффективным клеточным иммунитетом, поэтому очень восприимчив к инфекции. Грибы производят ферменты, разрушающие ногтевую пластину, что облегчает их проникновение вглубь.
Частые очаги онихомикоза - подошвы и межпальцевые промежутки. Обычно грибы поражают ногтевую пластинку, начиная со свободного края, таким образом основные патологические процессы протекают не в самой пластинке, а под ней - в ложе ногтя.
Классификация онихомикоза
Различают нормотрофический, гипертрофический и онихолитический (атрофический) онихомикоз.
При нормотрофической форме пораженный ноготь сохраняет свою толщину и блеск, но меняет цвет.
При гипертрофической форме помимо изменения цвета наблюдается нарастающий подногтевой гиперкератоз. Ноготь теряет блеск, становится тусклым, утолщается и деформируется вплоть до образования онихогрифоза (утолщения и искривления ногтя наподобие когтя мифической птицы грифона), частично разрушается, особенно с боков, нередко пациенты испытывают боль при ходьбе.
Для онихолитической формы характерна тусклая буровато-серая окраска пораженной части ногтя, ее атрофия и отторжение от ложа - обнаженный участок покрыт рыхлыми гиперкератотическими наслоениями; в то же время проксимальная часть ногтя долго остается без существенных изменений.
Кроме того, применяют классификацию, основанную на локализации поражения ногтя: выделяют дистальный онихомикоз (с поражением ногтя у свободного края), латеральный (с поражением боковых сторон), проксимальный (с поражением заднего валика) и тотальный (с поражением всего ногтя).
Симптомы онихомикоза
Основное проявление онихомикоза – изменение цвета ногтевой пластинки: она белеет или становится желто-коричневой, может приобретать фиолетовый, зеленоватый или черный цвет. К другим клиническим проявлениям относят утолщение и зуд кожи в области ногтевых валиков (подногтевой гиперкератоз), отслоение ногтя от ногтевого ложа (онихолизис) и утолщение ногтевой пластинки (онихауксис). Для грибкового поражения ногтя характерен такой признак как дерматофитома - продольная полоса желтовато-белого или коричневатого цвета, локализующаяся в глубине ногтевой пластинки.
Ногти пальцев ног поражаются в 7-10 раз чаще, чем рук, причем чаще всего поражаются большие пальцы. Как правило, грибок одновременно присутствует на нескольких ногтях, нередко у больных онихомикозом выявляется также микоз стоп.
Диагностика онихомикоза
Диагностика онихомикоза основывается на данных клинической картины и результатах лабораторных исследований.
-
Проведение микроскопического исследования пораженных ногтевых пластинок.
Исследование используется в диагностике грибковых заболеваний кожи и ногтей. Особенности инфекции. Грибковые заболевания (микозы) кожи и ногтей – заразные заболевания, передающиеся от человека к человеку. Передача инфекции может произойти при непосредственном контакте с активным о.
Оппортунистические микозы - группа микозов, которые вызываются условнопатогенными грибами из родов Absidia, Aspergillus, Candida, Mucor, Penicillium и др. у иммунодефицитных лиц.
Среди инфекционных болезней оппортунистические микозы, которые вызываются условнопатогенными грибками, занимают особое место.
Патогенез (что происходит?) во время Оппортунистических микозов:
В отличие от большинства инфекционных болезней, где внешние этиологические факторы явно доминируют во взаимодействии над внутренними факторами, при оппортунистических микозах роль внутренних факторов (иммунодефицитные состояния различного характера и другие проявления недостаточности) при взаимодействии часто превалирует над внешними этиологическими факторами.
Условно-патогенная флора, к которой относятся возбудители оппортунистических микозов, в одиночку неспособна в просвете полостей и трубчатых структур, куда она попадает извне, быть достаточной для того, чтобы ее представителей можно было бы расценивать истинными паразитами. Чаще она пребывает в состоянии паразитоносительства, мнимого (ложного) паразитизма. Однако, когда возникают ассоциации вирусов, патогенных бактерий, грибов, зоопаразитов и прочих микроорганизмов и они совместно обитают в просвете полостей и трубчатых систем конкретного хозяина и оказывают друг на друга существенное влияние, то создаются условия их интеграции - паразитоценоза, поэтому следует учитывать, что обретение условнопатогенными грибками агрессивных свойств связано не только с угнетением защитных сил организма, но и явлениями возникающего паразитоценоза.
Каждый из участников этой интеграции (гриб, бактерия, вирус) в отдельности недостаточен для возникновения болезни, но необходим в совокупности для того, чтобы она стала достаточной и смогла стать причиной заболевания, которое является многокомпонентным. Обязательным условием достаточности для возникновения заболевания является интеграция необходимых причин, долевое участие которых может быть различно по своей значимости и времени воздействия.
Патоморфогенез оппортунистических микозов следует изучать с его начальных звеньев, когда транзиторное носительство трансформируется в начальную форму в виде микст-микоценоза и локализуется в просвете и на поверхности слизистой оболочки. В условиях нарушения неспецифической резистенции, связанной с угнетением системы нейтрофилов, значительного ослабления иммунной защиты в многоуровневых барьерах слизистой оболочки, просветочная микопатия переходит в инвазивную форму. Переход этот может носить узко локальный характер и, потому, он крайне трудно определим при гистологическом исследовании. Поэтому так часто имеет место отрицательный ответ о наличии инвазии. Он может принимать и манифестированную форму, что наблюдается при повреждении или отсутствии эпителиальной выстилки и выраженном иммунодефиците у резко ослабленных больных.
Трансформация просветочной микопатии в инвазивную форму отмечается при различного рода проявлениях иммунодефицита, связанных не только с каким-либо предшествующим заболеванием, но и обусловленных ятрогенными факторами, в том числе лечением антибиотиками, гормонами, цитостатиками. В этих условиях развиваются своеобразные терминальные инвазивные оппортунистические микозы на фоне выраженного иммунодефицита, трудно поддающиеся лечению. Иногда подобные инвазивные висцеральные формы могут развиваться, когда условнопатогенные грибки у ослабленных больных попадают в обход защитных барьеров в кровь при внутривенных вливаниях, операциях на органах кровообращения, в условиях трансплантационной хирургии.
Висцеральные инвазивные формы оппортунистических микозов, которые чаще возникают в терминальный период, по своей патогенетической сущности следует расценивать как вторую индуцированную болезнь, или болезнь конца какого-либо предшествующего страдания.
Симптомы Оппортунистических микозов:
Оппортунистические микозы вызывают сапрофитические виды, проникающие из внешней среды либо входящие в состав микробных сообществ организма человека. Патогенность возбудителей очень низкая, и они обычно не вызывают поражений у здоровых лиц (что, собственно, и отражает общее название заболеваний).
Оппортунистические микозы обычны для лиц с различными нарушениями иммунобиологической резистентности. Инфекции, вызываемые Кандидами и другими дрожжеподобными грибами, обычно развиваются как эндогенные заболевания. Плесневые грибы (аспергиллы и др.), конидии которых постоянно выделяют из воздуха, вызывают экзогенные поражения.
Как правило, большинство оппортунистических микозов протекает как моноинфекция, но при глубоких иммунодефицитах наблюдают смешанные инфекции, вызванные несколькими видами грибов.
Диагностика Оппортунистических микозов:
Дифференцированная диагностика миконосительства и различных форм поражений слизистых оболочек, выстланных многослойным плоскими цилиндрическим эпителием, различается при поражении слизистых оболочек, выстланных многослойным плоским эпителием.
Выделяют поверхностную (интраэпителиальную) и инвазивную (с нарушением целостности эпителия и базальной мембраны) формы.
Наибольшие трудности возникают при определении микотических поражений слизистых, выстланных цилиндрическим эпителием, особенно в пищеварительном тракте, где содержится громадное количество микроорганизмов, отделенных от «стерильных» тканей всего лишь одним слоем эпителиальных клеток слизистой оболочки. «Держать в узде» огромное количество потенциальных врагов (различного рода микроорганизмов), находящихся в просветах, призвано и позволяет значительное количество нейтрофилов, которые участвуют в контроле за соответствующей микробиотой. Наличие нейтрофилов в местах скопления ассоциаций условнопатогенных грибков с различными возбудителями связано, по-видимому, с поддержанием в просветах и на поверхности слизистых оболочек надлежащего количественного или качественного состава микробиоты.
Лечение Оппортунистических микозов:
Лечение всех системных оппортунистических микозов требует комплексного этиопатогенетического подхода и включает:
- общеукрепляющую витаминотерапию, направленную на активизацию иммунозащитных свойств организма (комплекс витаминов с микро- и макроэлементами, средства, стимулирующие гемопоэз - Кокарбоксилаза, Левамизол и т.д.);
- симптоматическую терапию (сердечно-сосудистые, гипотензивные, седативные препараты, при болях в суставах и мышцах - противовоспалительные нестероидные средства), в отдельных случаях применение бронхолитиков, отхаркивающих средств и гормонов по показаниям, особенно - при бронхиальной астме;
- назначение ферментных препаратов (Панкреатин, Фестал, Панзинорм форте), регуляторов кишечной микро флоры (Бактисубтил, Хилак), желчегонных средств, гепа топротекторов (Липостабил, Карсил, Эссенциале);
- назначение эуобиотиков, антиоксидантов, иммуно корректоров, вагинальных антисептиков при поражении генитальной сферы;
- специфическая этиотропная терапия заключается в назначении антимикотиков с учетом вида возбудителя, локализации поражения, характера течения и тяжести заболевания, а также веса и возраста больного.
К каким докторам следует обращаться если у Вас Оппортунистические микозы:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Оппортунистических микозов, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Оппортунистические инфекции – это большая группа инфекционных заболеваний, которые развиваются у пациентов с различными типами иммунодефицитов и нехарактерны для людей с нормальным иммунным статусом. Патологии поражают любую систему органов и вызывают соответствующую симптоматику. К общим клиническим проявлениям относят длительный субфебрилитет, лимфаденопатию, астенический синдром. Диагностика оппортунистических инфекций включает серологические, молекулярно-генетические, бактериологические и другие методы детекции патогенных возбудителей. Программы лечения сочетают длительную этиотропную терапию с методами иммунокоррекции.
МКБ-10


Общие сведения
Проблема оппортунистических инфекций (ОПИ) становится все более актуальной, что вызвано ростом числа ВИЧ-инфицированных людей, разработкой эффективных, однако агрессивных методов лечения онкопатологии. При этом многие люди являются бессимптомными носителями возбудителей ОПИ: 60% инфицированы цитомегаловирусом, 90% – герпесвирусами 1 и 2 типов, около 30% – токсоплазмой. Учитывая клинический полиморфизм и отсутствие специфических симптомов, диагностика и лечение оппортунистических болезней представляет серьезную мультидисциплинарную проблему.

Причины
Для манифестации оппортунистических инфекций необходимо заражение патогенным микроорганизмом: вирусом, бактерией, грибком или простейшим. Известно более 20 типичных возбудителей ОПИ, в современной инфектологии этот перечень постоянно дополняется. Болезнь возникает при активации латентного очага, реже выступает следствием текущего заражения. Первостепенную важность играет нарушение иммунного статуса вследствие следующих патологий:
- ВИЧ-инфекция. Самая частая причина, поскольку на определенном этапе снижения числа CD4-клеток ОПИ развиваются у каждого больного. Инфекционные болезни используются для диагностики заражения ВИЧ и определения стадии заболевания, поэтому в данном контексте они называются СПИД-ассоциируемыми или СПИД-индикаторными патологиями.
- Злокачественные новообразования. Патофизиология любого опухолевого процесса предполагает угнетение собственной иммунной системы пациента и снижение ее ответа на чужеродные агенты. При этом уменьшается число Т-клеток, угнетаются процессы фагоцитоза. Проблема наиболее выражена при гемобластозах – лейкозах и лимфомах.
- Хроническая соматическая патология. Угнетение активности клеточного и гуморального иммунитета происходит при эндокринных заболеваниях (сахарный диабет, гипотиреоз), почечной недостаточности, тяжелых воспалительных патологиях ЖКТ.
- Ятрогенные факторы. Применение цитостатиков и других видов иммуносупрессоров является важным предиктором развития оппортунистических инфекций. Подобная ситуация наблюдается в группе пациентов после лучевой терапии, трансплантации органов и костного мозга.
- Первичные иммунодефициты. В эту группу относят все виды иммунной недостаточности, которые имеют генетический характер или возникают внутриутробно под влиянием тератогенов. Они манифестируют в раннем детском возрасте, проявляются затяжными оппортунистическими болезнями, которые с трудом подаются терапии.
Патогенез
Хотя возбудители оппортунистических инфекций таксономически неоднородны, в развитии заболеваний большую роль имеют общие особенности их патогенности и вирулентности. К свойствам микроорганизмов, вызывающих ОПИ, относят возможность длительного и даже пожизненного персистирования в организме человека, внутриклеточное паразитирование, склонность к поражению клеток моноцитарно-макрофагальной системы.
Инфекции активизируются при иммунодефицитах любой этиологии и склонны к хроническому течению с периодическими обострениями, поражением жизненно важных органов. Для оппортунистических болезней характерна лимфогенная и гематогенная диссеминация микроорганизмов, образование эктопических очагов. Собственный иммунитет пациента не способен оказать должное сопротивление инфекционному агенту, лекарственные средства не всегда эффективны.
Сложность и опасность оппортунистических инфекций заключается еще и в том, что они способны подавлять естественный иммунитет. В последние годы говорят о возможности пожизненной иммуносупрессии при персистировании герпесвирусов. Таким образом, формируется порочный круг, когда иммунодефицит провоцирует активацию возбудителей ОПИ, которые усугубляют явления иммунной недостаточности и потенциируют дальнейшие полиорганные нарушения.

Классификация
Единой систематизации оппортунистических инфекций на сегодня не существует. Условно возбудителей объединяют в 3 группы: патогены, которые поражают лиц с нарушениями иммунитета и здоровых людей; микробы, встречающиеся только при иммунодефицитах; вакцинные штаммы микроорганизмов. Общепринятой является классификация ОПИ согласно типу возбудителя:
Симптомы оппортунистических инфекций
В инфектологии выделяют общую группу клинических признаков, которая встречается при любом варианте ОПИ. Наиболее типичным симптомом признан длительный субфебрилитет, которые возникает без видимой причины и беспокоит пациента больше 1 месяца. Нередко повышение температуры возникает после перенесенного ОРВИ или кишечной инфекции, которые выступают пусковым фактором активации оппортунистического заболевания.
Вторым настораживающим симптомом считается лимфаденопатия – увеличение лимфатических улов. Чаще всего в процесс вовлекается лимфоидная ткань шейно-подчелюстной, подмышечной и паховой зоны. Лимфоузлы достигают диаметра около 1 см, имеют плотноэластическую консистенцию, не спаяны с окружающими тканями и безболезненны при ощупывании.
Третью группу общей симптоматики оппортунистических инфекций составляет астенический синдром. Он включает слабость, повышенную утомляемость, снижение переносимости умственных и физических нагрузок. Зачастую пациенты жалуются на ночную потливость, головокружения и головные боли, нарушения сна. При длительном существовании таких признаков наблюдается когнитивная дисфункция, эмоциональная подавленность, стойкое снижение работоспособности.
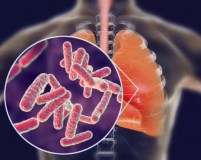
Пациента с иммуносупрессией должен насторожить кашель и одышка – типичные признаки туберкулеза и пневмоцистной пневмонии (ПЦП), снижение остроты зрения – возможное проявление цитомегаловирусного ретинита, длительно сохраняющаяся диарея – признак криптоспоридиоза, микроспоридиоза. Жжение и сухость полости рта в комбинации с эрозиями и белыми налетами на слизистых указывают на орофарингеальный кандидоз.
Оппортунистические болезни не имеют четко выраженного тропизма. Один и тот же вид возбудителя может вызывать миокардит, плеврит, артрит, менингит и другие нозологические формы. Зачастую они имитируют симптомы хронических соматических заболеваний, с которыми пациенты длительно и безрезультатно посещают врачей разных специальностей. Исключение составляет пневмоцистоз, который в основном поражает легкие с развитием ПЦП.
Осложнения
Оппортунистические инфекции – тяжелые и потенциально смертельные заболевания. Среди пациентов с терминальными стадиями ВИЧ-инфекции ОПИ составляют 90% в структуре летальности, оставшиеся 10% приходятся на саркому Капоши, лимфомы и прочие неинфекционные последствия СПИДа. Смертность при церебральном токсоплазмозе составляет около 33%, при криптококковом менингите – 20-30%, при пневмоцистной пневмонии – 10-20%.
Особую тревогу вызывает сочетание нескольких видов оппортунистических заболеваний у одного пациента. Микробные ассоциации более характерны для позднего периода и хронического течения основной патологии, вызвавшей иммунодефицит. Сочетанное инфицирование типично для иммунокомпрометированных пациентов, пребывающих на стационарном лечении: у 40-50% больных в послеоперационном периоде, у 70-80% при перитонитах и плевритах.
Распространение оппортунистических инфекций негативно сказывается на репродуктивном здоровье населения. Они обуславливают многие случаи самопроизвольного прерывания беременности, эмбриопатий и фетопатий, задержки внутриутробного развития. Дети, рожденные от матерей с ОПИ, находятся в группе риска развития заболеваний новорожденных, перинатальных энцефалопатий.

Диагностика
Обследование пациентов проводится мультидисциплинарной командой врачей, в которую входят врач-инфекционист, иммунолог, онколог и другие узкопрофильные специалисты. Большое клиническое значение имеет выяснения времени и условий появления симптоматики, характера течения заболевания, наличия факторов риска иммунодефицитных состояний. Для подтверждения оппортунистических инфекций проводятся следующие методы диагностики:
- Инструментальная визуализация. С учетом ведущей клинической симптоматики выполняется рентгенография органов грудной клетки и живота, УЗИ брюшной полости, КТ или МРТ головного мозга. При необходимости назначается бронхоскопия, ЭФГДС и колоноскопия, люмбальная пункция. По возможности у больных с иммуносупрессией избегают инвазивных методов диагностики.
- Серологическое тестирование. Клинически значимым для острого процесса или обострения латентной инфекции является нарастание титров антител в 4 и более раза при РСК. Для определения давности заражения, особенно для ЦМВ и других герпесвирусов, определяют авидность антител. Также проводится ИФА на антитела IgM.
- ПЦР-диагностика. Молекулярно-генетический метод остается «золотым стандартом» определения большинства инфекций. Для его проведения используют разные типы биоматериала. Благодаря высокой чувствительности ПЦР обнаруживает даже единичные копии оппортунистических возбудителей в образце.
- Микробиологические посевы. Для выращивания микроорганизмов применяются специальные культуральные среды с учетом предполагаемого возбудителя. При получении колоний патогенов их тестируют на чувствительность к противомикробным препаратам, чтобы правильно подобрать лечение.
- Иммунограмма. Для диагностики клеточного иммунодефицита важную роль играет количество разных типов Т-лимфоцитов, соотношение CD4/CD8 клеток – иммунорегуляторный индекс. Гуморальное звено иммунитета оценивается по уровню CD19 (маркера В-лимфоцитов), концентрации разных классов иммуноглобулинов.
Лечение оппортунистических инфекций
В процессе лечения практикующие инфекционисты сталкиваются с такими нюансами, как множественная лекарственная устойчивость патогенов, гетерогенность популяции возбудителей, низкая активность естественных иммунных факторов. Основу терапии составляет прием этиотропных противомикробных препаратов: антибиотиков, антимикотиков, противопротозойных и противовирусных. Лечение ОПИ имеет ряд особенностей:
- в основном назначаются комбинации из 2-3 препаратов для повышения их эффективности;
- продолжительность противомикробной терапии повышается в 1,5-2 раза и более в сравнении с лечением инфекционных болезней у иммунокомпетентных лиц;
- при подборе терапии ориентируются не только на клиническую картину болезни, но и на текущий иммунный статус пациента;
- при вирусных инфекциях обязательно назначаются этиотропные препараты, тогда как у людей без иммуносупрессии противовирусные средства используют только по показаниям.
Для успешного лечения ОПИ требуется максимально возможное восстановление иммунной функции. В группе пациентов с ВИЧ-инфекцией назначаются протоколы антиретровирусной терапии (ВААРТ), чтобы повысить число CD4-клеток и улучшить отдаленные прогнозы. При ведении онкологических больных используются персональные схемы иммуномодуляторов, экспериментальные направления иммунотерапии и регенеративной медицины с применением стволовых клеток.
Прогноз и профилактика
Течение любой инфекции на фоне иммуносупрессии является сложным и непредсказуемым, однако усовершенствованные протоколы лечения позволяют достичь стойкой ремиссии или даже полного излечения. К прогностически неблагоприятным факторам относят пожилой и старческий возраст, неправильно подобранную терапию, невозможность проведения иммунокоррекции основного заболевания.
При иммунодефицитах показана первичная медикаментозная профилактика оппортунистических инфекций. Применяют сульфаниламиды, макролиды‑азалиды, противогрибковые средства. При положительной пробе Манту или недавнем контакте с больным туберкулезом назначается химиопрофилактика сроком на 6 месяцев. Также пациентам рекомендовано строго соблюдать противоэпидемические меры, в периоде резкой иммуносупрессии необходимо пребывание в стерильных боксах.
3. Клинические особенности сочетанных оппортунистических инфекций (обзор)/ В.В. Шкарин, Н.В. Саперкин// Медицинский альманах. – 2017. – №4.
4. Оппортунистические инфекции: проблемы и перспективы/ Под общ. ред. проф. Ю.В. Редькина, О.А. Мирошника, В.В. Лобова. – 2002.
Оппортунистические микозы. Кандидоз. Возбудитель кандидоза.
Оппортунистические микозы вызывают сапрофитические виды, проникающие из внешней среды либо входящие в состав микробных сообществ организма человека. Патогенность возбудителей очень низкая, и они обычно не вызывают поражений у здоровых лиц (что, собственно, и отражает общее название заболеваний). Оппортунистические микозы обычны для лиц с различными нарушениями иммунобиологической резистентности. Инфекции, вызываемые Кандидами и другими дрожже подобны ми грибами, обычно развиваются как эндогенные заболевания. Плесневые грибы (аспергиллы и др.), конидии которых постоянно выделяют из воздуха, вызывают экзогенные поражения.
Как правило, большинство оппортунистических микозов протекает как моноинфекция, но при глубоких иммунодефицитах наблюдают смешанные инфекции, вызванные несколькими видами грибов.
Кандидоз. Возбудитель кандидоза.
Кандидоз — антропонозный микоз, характеризующийся поражением слизистых оболочек и кожи. Возможны тяжёлые висцеральные формы, чаще с вовлечением лёгких и органов пищеварения. Кандидоз обычно возникает эндогенно как следствие дисметаболических расстройств и дисфункций иммунной системы.
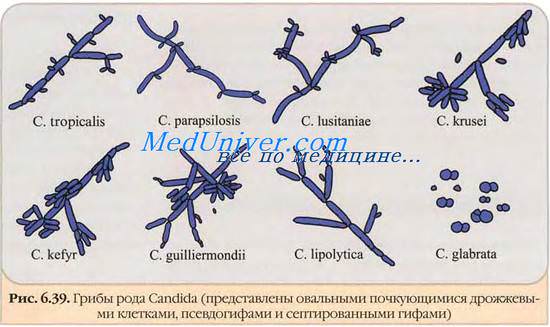
Возбудители кандидоза — дрожжеподобные грибы рода Candida. Кандиды не относят к истинным диморфным грибам, так как в тканях можно выявлять как дрожжевые клетки, так и гифы. Переход в мицелиальную фазу можно наблюдать при культивировании при более низкой температуре (22-25 С) или при истощении питательной среды. In vivo переход дрожжевой фазы в мицелиальную (плесневую) можно наблюдать при прорастании в ткани организма. Дрожжевая фаза представлена овальными или круглыми клетками-бластоспорами (4-8 мкм), размножающимися многополюсным почкованием. Клеточная стенка содержит 5-7 слоев.
Оптимальная температура для роста кандид составляет 25—28 С. Мицелиальная фаза кандидоза представлена цепочками удлинённых клеток с трёхслойной клеточной стенкой, образующими псевдомицелий. На нём беспорядочно располагаются дрожжеподобные бластоспоры (рис. 35, см. цветную вклейку). Некоторые виды, включая С. albicans, формируют терминальные хламидиоспоры.
Поражения у человека вызывают С. albicans (более 90% поражений), С. tropicalis, С. krusei, С. lusitaniae, С. parapsilosis, С. kefyr, С. guilliermondii и др. В начале XX в. кандидозы наблюдали сравнительно редко, но заболеваемость значительно возросла с началом применения антибиотиков и растёт в настоящее время. На сегодняшний день кандиды — наиболее распространённые возбудители оппортунистических микозов.
С. albicans — нормальный комменсал полости рта, ЖКТ, влагалища и иногда кожи. Любые нарушения резистентности организма либо изменения нормального микробного ценоза могут приводить к развитию заболевания. Возможность передачи возбудителя при бытовых контактах не определена, однако первичная колонизация детей кандидами происходит при прохождении через родовые пути матери или при кормлении грудью. Мочеполовой кандидоз передаётся половым путём.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России, лаборатория микробиологической диагностики и лечения инфекций в онкологии, Москва, Россия
Место Aureobasidium pullulans среди возбудителей оппортунистических инфекций человека (обзор литературы)
Журнал: Лабораторная служба. 2018;7(2): 12‑18
ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России, лаборатория микробиологической диагностики и лечения инфекций в онкологии, Москва, Россия
Aureobasidium pullulans — сапрофитный гриб, который широко распространен в окружающей среде и активно используется в различных промышленных технологиях. Как и многие сапрофитные грибы, при определенных условиях A. pullulans может вызывать оппортунистические микозы у человека. Глубокий микоз, обусловленный A. pullulans, зачастую трудно поддается лечению, стандартная терапия отсутствует. Тактика ведения таких пациентов основана на данных in vitro в экспериментах на животных, на клиническом опыте, полученном, в основном, при экспертной оценке описанных клинических случаев.
ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России, лаборатория микробиологической диагностики и лечения инфекций в онкологии, Москва, Россия
Факторы риска. Развитию микромицетов в зданиях способствуют аварийные протечки, места с наличием образования капельно-жидких конденсатов влаги, нарушенной гидроизоляцией фундаментов и стен, теплоизоляцией, вентиляцией и т. д. при реконструкции и модернизации зданий, в частности с использованием оконных конструкций из пластика, алюминия и деревоалюминия. Неправильный их подбор и некачественный монтаж приводит к появлению конденсата по периметру оконных коробок, что создает условия для развития микромицетов. Подобное явление отмечается при декорировании фасадов с применением декоративного бетона и плохой заделке швов. Вероятнее всего, на материалах, в составе которых содержатся вещества естественного происхождения, например целлюлоза, минералы строительных и отделочных смесей и т. д., может развиваться в первую очередь комплекс видов, тем или иным образом связанных в природе с этими субстратами. Конденсационная влага и капиллярное смачивание приводит к повышению влажности отделочных материалов и способствует развитию микромицетов на внутренней стороне, например обоев, штукатурки. Наличие влаги, особенно капельно-жидкой, выводит споры микромицетов из состояния анабиоза. В закрытых помещениях основной перенос спор грибов, часто адсорбированных на частицах пыли, осуществляют конвенционные потоки воздуха. Анализ мест наибольшего накопления и адсорбции пылевых частиц со спорами микромицетов показал, что это происходит в вентиляционных системах и даже в помещениях при ламинарном и кондиционированном воздухообмене. Вероятно, элементы конструкций кондиционеров так же, как и радио-, и телеаппаратуры, и компьютеров, могут служить источником концентрации спор микромицетов из-за статического заряда на деталях и направленного потока воздуха от вентиляторов [8].

Особенности роста A. pullulans. A. pullulans растет в температурном диапазоне (+)2—35 °C с оптимальным ростом при (+)25—30 °C и отличается своей фенотипической пластичностью. На морфологию колонии влияет ряд факторов, например источник углерода, возраст колонии, температура, свет и субстрат. Колонии могут быть и гомогенными, и гетерогенными, и дрожжеподобными, и с мицелиальным ростом, величина колоний варьирует от маленьких до больших размеров [6, 7]. A. pullulans созревает быстро, в течение 7 дней после инкубации при комнатной температуре. На картофельно-декстрозном агаре колонии имеют диаметр 1—3 см после инкубации при 25 °C в течение 7 дней. На агаре с солодовым экстрактом при 24 °C колонии достигают диаметра 4 см за 7 дней. Колонии меняют окраску в процессе роста: цвет варьирует от белого до кремового или бледно-розового. Позднее, вследствие образования хламидоспор колонии становятся частично коричневыми или черными, часто секторами. У некоторых штаммов обратная сторона может быть белой, светло-оранжевой или абрикосовой (рис. 1). Рис. 1. Колонии A. pullulans на агаре Сабуро, 12 сут (из архива Н.С. Багировой).
A. pullulans относится к быстро растущим видам. Молодые колонии можно наблюдать в микроскоп: влажные дрожжевые клетки (бластоконидии). По мере взросления колоний становятся видны септированные гифы (диаметром 2—16 мкм). Первичные конидии гиалиновые*, гладкие, эллипсоидные, одноклеточные, различной формы и размера. В старых культурах могут образовываться темно-бурые, толстостенные гифы. Конидиеносцы недифференцированные, расположены интеркалярно или терминально, или выглядят короткими боковыми ветвями. Эндоконидии образуются интеркалярно и высвобождаются в соседнюю пустую клетку. Гифы гиалиновые, гладкие, тонкостенные, с поперечными перегородками (рис. 2, 3). Рис. 2. Микроскопия по Граму мазков-отпечатков из очагов некроза селезенки (иммерсия, ×1000) (из архива Н.С. Багировой). Рис. 3. Мазок по Граму, чистая 12-суточная культура A. pullulans (иммерсия, ×1000) (из архива Н.С. Багировой).
Идентификация. В большинстве опубликованных биологических исследованиях описана идентификация A. pullulans, основанная на морфологии клеток или колоний, что приводит к сложностям в распознавании A. pullulans как самостоятельного возбудителя.
Причины частых ошибок в идентификации этих грибов можно объяснить их небольшими размерами, отсутствием специфических морфологических характеристик. Диагноз основывается на гистологической экспертизе клинических образцов и культуральном методе исследования. Кроме того, рекомендуется мультилокусное секвенирование для точной идентификации видов, особенно для необычных или недавно описанных патогенных микроорганизмов. Молекулярная характеристика микромицетов — это надежный метод молекулярной систематики с мультилокусными наборами данных, обширной выборкой таксона и строгими нормированными аналитическими методами [9]. Однако использование данного метода в клинической лаборатории в основном ограничивается эпидемиологическими исследованиями и выявлением необычных и редко встречающихся видов или трудно идентифицируемых штаммов. Молекулярная идентификация большинства видов основана на секвенировании рибосомных генов и сравнении с опубликованными базами данных, особенно в GenBank. Однако более 10% этих находок могут быть ошибочными [10]. Следует заметить, что в настоящее время в отношении A. pullulans отсутствует межлабораторная стандартизация методов секвенирования. Несколько международных обществ по микологии человека и животных (ISHAM), а также институт по клиническим и лабораторным стандартам США (CLSI) работают над стандартизацией метода секвенирования грибов. Молекулярная характеристика всегда должна оцениваться в свете фенотипических особенностей микроорганизмов, поскольку молекулярные диагностические методы пока недостаточно надежны для встречающихся разнородных видов микозов [6, 7, 11].
Связь A. pullulans с аллергическими реакциями. В некоторых странах нозокомиальные грибы сгруппированы в 3 класса опасности, основанные на связанном с ними риске для здоровья. A. pullulan относится к классу опасности В: грибы, продукты метаболитов которых могут вызывать аллергические реакции у обитателей, если они присутствуют в помещении в течение длительного периода времени. В настоящее время более 80 грибковых родов ассоциируются с аллергией. Наиболее часто в связи с этим сообщается о Cladosporium spp., Penicillium spp., Aspergillus spp., Alternaria spp. и Aureobasidium spp. [13]. Специфические аллергенные компоненты A. pullulans не изучены. Хроническое воздействие A. pullulan на человека через увлажнители или кондиционеры может привести к гиперчувствительности, пневмониту (иначе называемому аллергическим альвеолитом). Это состояние характеризуется острым началом: одышкой, кашлем, лихорадкой, инфильтратами в грудной клетке и острой воспалительной реакцией. Состояние также может быть хроническим и опосредованным лимфоцитами. Хроническое состояние рентгенографически характеризуется ретикулонодулярными инфильтратами в легких [14—16].
Частота микозов человека, обусловленных A. pullulans. A. pullulans по санитарно-эпидемиологическим правилам СП 1.3.2322−08 в рубрике «Опасные для человека грибы-возбудители заболеваний» относится к IV группе. На сегодняшний день в пределах рода Aureobasidium разновидность A. pullulans var. pullulans наиболее часто является возбудителем микозов, особенно у иммунокомпрометированных пациентов [17]. A. pullulans редко вызывают инфекционные осложнения у людей (возбудитель феогифомикоза, в том числе легочных форм). Но в последние годы демациевые грибы все чаще признают возбудителями самых разнообразных форм микозов человека. Следует заметить, что для установления диагноза требуется высокая клиническая настороженность. Первый случай висцерального микоза, вызванного A. pullulans, был описан в зарубежной литературе в 1986 г. [18]. К настоящему времени сообщается о немногим более 30 подобных случаев у человека [19].
Широкое распространение разнообразных видов грибов в природе, их постоянное присутствие в ближайшем окружении и среде обитания человека обусловливают особое значение исследований о возможности присутствия и развития в микробиоте искусственных медицинских материалов и технике токсиногенных и оппортунистических форм грибов. Процессы биоповреждения и биоразрушения инициируют развитие микробных очагов потенциальных инфекций. Полимерные материалы, пораженные микробами, могут быть источниками подобных осложнений, что повышает актуальность разработки новых, биоустойчивых материалов [20]. A. pullulans имеет сродство к синтетическим материалам и хирургическим имплантированным устройствам, так как гриб был выделен из стационарных перитонеальных диализных катетеров и центральных венозных катетеров. У иммунокомпрометированных пациентов описаны тяжелые инфекции, при которых A. pullulans был выделен из крови, бронхоальвеолярного лаважа, лимфатических узлов, абсцесса селезенки или цереброспинальной жидкости. Инфекции развивались главным образом вследствие повреждения кожи или глаз, а также интратекального введения цитотоксических препаратов [11].
Современные методы лечения онкологических больных нередко основаны на применении высоких доз цитостатических препаратов, что позволяет значительно увеличить частоту достижения полной ремиссии, но при этом развивается глубокая аплазия костного мозга, которая часто осложняется присоединением инфекции, в том числе грибковой. Известно, что препараты для лечения злокачественных новообразований крови способны подавлять выработку провоспалительных цитокинов, активацию и пролиферацию Т-лимфоцитов [21—23]. Ведущая роль в защите от оппортунистических грибковых инфекций принадлежит Т-хелперам 1-го типа и провоспалительным цитокинам, которые активируют нейтрофилы и макрофаги, непосредственно отвечающие за уничтожение клеток грибов [24]. Баланс между ключевыми цитокинами, обеспечивающими противогрибковую защиту (ИФН-γ, ФНО-α, ИЛ-6, ИЛ-8), и противовоспалительными цитокинами (ИЛ-4 и ИЛ-10), определяет исход инфекционного процесса [25].
Терапия. Глубокий микоз, обусловленный A. pullulans, зачастую трудно поддается лечению. Стандартная терапия отсутствует. Тактика ведения таких пациентов основана на данных in vitro в экспериментах на животных, клиническом опыте, полученном в основном при экспертной оценке описанных клинических случаев. Нередко тактика ведения таких больных требует хирургического вмешательства и продолжительной антимикотической терапии. Комбинированная противогрибковая терапия может обеспечить лучшие результаты, чем традиционные подходы к лечению. По данным зарубежной литературы [6, 7], хорошая противогрибковая активность в отношении A. pullulans in vitro отмечается у вориконазола и итраконазола. До недавнего времени не было систематических данных о чувствительности A. pullulans к антимикотикам. В исследовании M. Javad Najafzadeh и соавт. [19] изучена чувствительность 104 штаммов A. pullulans (51 штамм из клинического материала) после идентификации на молекулярно-генетическом уровне. Амфотерицин В, итраконазол и позаконазол были признаны препаратами с наилучшей активностью против A. pullulans. Это первое всестороннее исследование активности противогрибковых препаратов в отношении большого количества клинически значимых штаммов A. pullulans. Результаты данного исследования не противоречат терапевтическим рекомендациям, опубликованным Европейским обществом клинической микробиологии и инфекционных заболеваний/Европейской конфедерацией медицинской микологии (ESCMID/ECMM) [11]. Длительная терапия при инфекциях, вызванных подобными микромицетами, обычно колеблется от нескольких недель до месяцев или дольше. Положение осложняется тем, что нет специальных диагностических тестов. Необходимы дальнейшие исследования, направленные на диагностику подобных инфекций и выработку стратегии ведения больных редкими микозами [6, 7, 11].
Заключение
Последние десятилетия большое внимание медицинского сообщества привлекает проблема микозов, вызываемых оппортунистическими (потенциально патогенными) грибами. Спектр видов оппортунистических грибов, способных вызывать микозы человека, постоянно расширяется. Вероятность развития микотических осложнений во многом определяется состоянием человека и в первую очередь связана с его иммунным статусом. Каковы должны быть природные свойства микромицетов, которые могут стать опасными для человека, а также условия заражения, к сожалению, изучено недостаточно. Для решения этой проблемы важно знание оптимальных экологических условий развития потенциально патогенных грибов, особенностей их накопления в окружающей среде, путей проникновения в среду обитания человека. Важнейшими для развития микромицетов экологическими факторами являются: содержание органических веществ, влажность, температура, рН среды их обитания. Значение других экологических свойств в оценке развития потенциально патогенных грибов исследовано в значительно меньшей степени. Анализ распространения видов потенциально патогенных грибов в разных климатических зонах России показал, что наибольший уровень присутствия таких видов в окружающей среде, как правило, выявляется именно в южных регионах, а наиболее «чистыми» являются северные и горные районы. Существует гипотеза, что современные тенденции изменения климата (возможное потепление) способны приводить к отбору видов, имеющих более высокие температурные оптимумы роста. Оптимальные температурные условия могут влиять на распространение микозов, особенно обусловленных редкими видами. Для формирования опасных микологических свойств в городской среде большое значение имеет возможность развития микромицетов в помещениях при стабильных и повышенных температурах [26].
Автор заявляет об отсутствии конфликта интересов.
*Гиалиновые конидии: бесцветная бесполая репродуктивная единица, сформированная любым способом, который не включает цитоплазматическое расщепление и действует как орган распространения.
Читайте также:

