Что такое метаплазия эпителия пищевода
Обновлено: 25.04.2024
Пищевод Барретта - это предраковое состояние, которое протекает бессимптомно и обнаруживается случайно при гастроскопическом исследовании.
Впервые цилиндрический эпителий в пищеводе описал в 1950 году N. Barrett, ошибочно истолковав эту ситуацию, как врожденный укороченный пищевод. Далее в 1953 году, P. Allison и A. Johnstone установили, что описанные изменения относятся непосредственно к слизистой оболочке пищевода, и являются следствием замещения плоского эпителия в цилиндрическим. Затем в 1970 году C. Bremner в научных работах на животных продемонстрировал возникновение цилиндроклеточной метаплазии пищеводного эпителия при гастроэзофагеальном рефлюксе, вызванном экспериментально, доказав приобретенный характер подобных изменений и связь с ГПОД или ГЭРБ.
Актуальность этой проблемы состоит в том, что вероятность возникновения железистого рака у пациентов с цилиндроклеточной (кишечной) метаплазией составляет 0,5-0,8% в год или 5-8% в течение жизни.
Распространенность метаплазии пищевода у жителей Европы, по разным данным, колеблется от 2% до 5%. В тоже время, при наличии гастроэзофагеальной рефлюксной болезни (ГЭРБ) с ГПОД или без нее, цилиндроклеточная метаплазия слизистой оболочки пищевода диагностируется у 10-15% пациентов. Аденогенный рак пищевода, развившийся на фоне метаплазии, впервые был описан в 1952 году B. Morson и J. Belcher, а в 1975 году, A. Naef теоретически обосновал развитие аденокарциномы из метаплазированного эпителия пищевода. Аденокарцинома пищевода – смертельное заболевание с пятилетней выживаемостью менее 20%, диагностируемое в России на поздних стадиях. Среди больных пищеводом Барретта риск опухолевого поражения выше в 30-120 раз.
В 1983 году, D. Skinner на обширном клиническом материале доказал наличие патогенетической цепочки: гастроэзофагеальный рефлюкс - цилиндроклеточная метаплазия - аденогенный рак пищевода.
Выше описанные соображения заставляют рассматривать цилиндроклеточную метаплазию слизистой оболочки пищевода как важную хирургическую проблему, требующую вдумчивого подхода к ее решению.
Использование правильного и современного алгоритма в лечении гастроэзофагеальной рефлюксной болезни, протекающей с развитием цилиндроклеточной метаплазии пищевода, позволяет при использовании хирургических эндоскопических технологий не только добиться значительного улучшения качества жизни пациентов, но профилактировать развитие аденокарциномы пищевода.
Диагностика пищевода Барретта

Способ оценки барьерной функции клапанов полых органов в абдоминальной хирургии
Пищевод Барретта диагностируется при эндоскопическом исследовании пищевода и желудка. Исследование проводится на видеоэзофагогастроскопе с NBI или хромоскопией с взятием биопсии, не менее, чем из 4 участков. Препараты подвергаются гистологическому или иммуногистохимическому исследованию. При этом визуально в нижней трети пищевода определяются изменения слизистой с яркой красной окраской как «языки пламени».
Высота изменений слизистой (протяженность пищевода Барретта) может быть трех типов: короткая – когда длина пораженного участка менее 3 см, средняя – 3-5 см и длинная – более 5 см. Очень важно понимать степень и вид диспластических изменений в измененной слизистой (классификация Р.Х. Риддела (1983)).
Стоит заострить внимание, что для осмотра такой деликатной зоны как нижняя треть пищевода и кардиальный отдел желудка, оценки состояния области гастроэзофагеального перехода и функции нижнего пищеводного сфинктера необходимо спокойное состояние пациента и отсутствие антиперистальтических сокращений из-за рвотного рефлекса. Как говорят многие авторы, необходим полный «внутрипросветный штиль на палубе корабля, когда в океане шторм». Поэтому использование короткой внутривенной седации облегчает пациенту перенос процедуры и дает врачу более точно выставить диагноз. В условиях нашей клиники мы предлагаем пациентам видеофиброскопию с использованием амбулаторных анестетиков производства США.
В последние годы гистологи стали отмечать, что материал, взятый из одного участка пищевода Барретта, может соответствовать различным видам дисплазии: кишечная метаплазия, желудочная метаплазия или кардиальный тип метаплазии. Таким образом, в одном участке пищевода может встречаться два или три типа эпителия. Это происходит в результате патологического рефлюкса агрессивного содержимого желудка в пищевод (желчи или кислоты) и последовательной перестройки пищеводного эпителия сначала в кардиальный, а потом в кишечный. Причем такая ситуация отмечается у 30% пациентов. С практической точки зрения важно понимать, это основывается на больших группах исследований, что вид дисплазии не влияет на частоту перерождения в рак. В связи с этим показания для комплексного хирургического лечения должны выставляться при наличии доказанного пищевода Барретта, вне зависимости от вида и стадии дисплазии.
Стоит отметить, что пищевод Барретта в 70% развивается на фоне грыжи пищеводного отверстия диафрагмы (ГПОД) и гастроэзофагеальной рефлюксной болезни (ГЭРБ) без ГПОД. Поэтому для постановки точного диагноза и главное понимания причин развития этого состояния мы должны иметь максимум информации о состоянии верхних отделов желудочно-кишечного тракта. С этой цельно необходимо выполнить эзофагогастроскопию, при которой оценить состояние слизистой пищевода и желудка, взять из нескольких точек биопсию (зона выраженных изменений) и определить протяженность изменой слизистой пищевода в сантиметрах, а также обнаружить наличие желчи в желудке и оценить состояние привратника. Далее необходимо выполнить суточную рН метрию пищевода и желудка, для четкого понимания вида патологического рефлюкса: кислый или щелочной. Затем провести рентгенологическое исследование пищевода и желудка, во время которого удается поставить или отвергнуть диагноз ГПОД, а также проанализировать эвакуацию из желудка и обнаружить явления и степень дуоденостаза.
Эта информация ложиться в основу выбора алгоритма индивидуального лечения конкретного пациента.
Лечение пищевода Барретта с использованием малоинвазивных технологий: лапароскопия и эндоскопия.
Мой опыт лечения пациентов с ГПОД и рефлюкс-эзофагитом различной степени выраженности, составляет 24 года. За это время мне удалось успешно лапароскопически прооперировать и вылечить более 2000 пациентов. У 10% из них был выявлен пищевод Барретта, с которым в 97% мы успешно справились, использую наш комплексный подход малоинвазивного лечения.
Стоит отметить, что только в результате четкого и полного обследования мы можем получить достаточного много информации о пациенте. При обнаружении пищевода Барретта на эндоскопическом исследовании и подтвержденном гистологическими анализами ставится вопрос об обязательном его лечении, так риск перерождения в рак очень велик.

Пучков К.В., Филимонов В.Б. Грыжи пищеводного отверстия диафрагмы: монография. - М.: МЕДПРАКТИКА - М., 2003. - 172с.
На этом этапе для точного выбора метода хирургического лечения помогают результаты цитологического и гистологического исследований. Мы уже говорили, что пищевод Барретта характеризуется гиперкератическими, метапластическими и диспластическими изменениями слизистой оболочки пищевода. Следовательно, при обнаружении гиперкератоза, желудочной, тонкокишечной и толстокишечной метаплазии, дисплазии лёгкой и средней тяжести, мы говорим только о доброкачественном процессе. В случае дисплазии тяжёлой степени или при обнаружении плоскоклеточного неороговевающего рака, выставляется диагноз онкологического заболевания. Это позволяет нам четко разграничить два вида лечения – в первом случае органосохраняющий и во втором случае – органоуносящий (операция Льюиса).
Иммуногистохимическое исследование, наряду с гистологическим исследованием биоптатов, позволяет выявить ранние формы аденокарциномы пищевода. Рак пищевода характеризуется увеличением площади экспрессии маркера Ki-67 и антиапоптозного фактора bcl-2 по сравнению со значениями при гастроэзофагеальной рефлюксной болезни и пищеводе Барретта. Таким образом, дифференциальная диагностика пищевода Барретта и аденокарциномы пищевода может быть дополнительно достигнута благодаря изучению результатов иммуногистохимического исследования клеток пищевода, продуцирующих синтазу оксида азота и эндотелин-1.
Если в результате проведенного эндоскопического исследования, гистологических и иммуногистохимических исследований не выявлена дисплазия тяжелой степени и аденокарцинома пищевода, мы должны вести речь только об органосохраняющем лечении пищевода Барретта. Этапы этого алгоритма, будут описаны мной ниже.
В случае отсутствия ГПОД, особенно у молодых пациентов, мы используем радиочастотную абляцию (РЧА) пищевода Барретта. В послеоперационном периоде на 6-8 недель назначается терапия блокаторами протонной помпы (подавление желудочной секреции) и мотилиум (улучшение моторики желудка). В течение нескольких месяцев проводится динамическое наблюдение - гастроскопия. При возникновении рецидива заболевания эту процедуру можно проводить повторно, так как воздействие оказывается только в пределах слизистой оболочки, не вызывая повреждения всей толщи стенки пищевода.
При наличии грыжи пищеводного отверстия диафрагмы, на первом этапе необходимо выполнение хирургического вмешательства - лапароскопической фундопликации по Тоупе (двухсторонняя фундопликация на 270 градусов) и крурорафии. Это вмешательство ликвидирует грыжу и прекращает патологический заброс агрессивного содержимого желудка в пищевод. Без этого этапа, дальнейшее лечение пищевода Барретта, как правило, не приносит положительного результата. В послеоперационном периоде, на 3-4 месяца, назначается терапия блокаторами протонной помпы.
Этот этап позволяет в 90 % случаев прекратить патологический рефлюкс в пищевод и тем самым прекратить патологическую трансформацию слизистой оболочки и перестройку обратное пищеводный эпителий.
После операции через 2-3 месяца необходимо выполнить радиочастотную абляцию ( РЧА) пораженной слизистой, а затем проводить контрольные осмотры пищевода (ФГС) через 3 и 6 месяцев. В случае положительной динамики, проводится дальнейшее наблюдение 1-2 раза в год.
У ряда пациентов при большой длине изменений в слизистой (длинный сегмент пищевода Барретта), необходимо дополнительно 1-2 сеанса РЧА.
Если при повторной оценке состояние слизистой пищевода, по данным ФГС, поражение слизистой уменьшается, то проводим дальнейшее динамическое наблюдение, выполняя ФГС с интервалом 6 месяцев. Через 1 год проводится заключительная оценка наличия или отсутствия пищевода Барретта. У большинства пациентов проявления пищевода Барретта подвергались обратному развитию (особенно у пациентов с ГПОД и кислотым рефлюксом). Если морфологически, при биопсии, мы видим сохранение изменений слизистой (метаплазии), то переходим к следующему этапу – эндоскопической (РЧА) или аргоноплазменной коагуляции слизистой пищевода в зоне пищевода Барретта.
Радиочастотная абляция и аргоноплазменная коагуляция проводятся под эндоскопическим контролем, как правило, под общим обезболиванием (кратковременная внутривенная седация). При сегменте поражения до 3 см, как правило, хватает одного сеанса. При поражении более 3 см может возникнуть необходимость в повторной процедуре. После радиочастотной абляции поврежденная ткань замещается плоским эпителием и заживает без рубцов. В своей практике мы предпочитаем использовать РЧА, который по своему принципу является улучшенной версией методики аргононоплазменной коагуляции, так как обладает меньшими побочными эффектами.
Стоит отметить, что если в зоне метаплазии выявлялись участки неоплазии высокой степени, при которой вероятность инвазивного роста существенно возрастает, также может быть выполнена радиочастотная абляция. При глубоких поражениях выполняется эндоскопическое радикальное удаление участка слизистой оболочки пищевода. При площади изменений до 2 см2, как правило проводится эндоскопическая резекция слизистой оболочки пищевода (EMR-C), а при площади изменений более 2 см2 – диссекция новообразования в подслизистом слое (ESD).
Далее обязательно проводится пожизненное диспансерное наблюдение – в течение первого года через 3 месяца, далее один раз в год выполнение ФГС с возможной биопсией слизистой подозрительных участков.
Крайне редко после такого комплексного и этапного лечения возникают рецидивы пищевода Барретта (мене 5%), как правило, это возникает при рецидиве ГПОД и остатках измененной слизистой после РЧА.
Ряд авторов проводят хирургическое лечение в обратной последовательности – в начале РЧА, а затем лапароскопическую фундопликацию. Здесь стоит отметить, что оптимальным сроком выполнения лапароскопической операции на пищеводе является 3-4 месяца после первого этапа. Так, как по данным УЗИ пищевода, очень длительно сохраняется отек его стенки (на фоне РЧА) и выполненная фундопликация в более ранние сроки может привести к развитию стеноза в области пищеводно-желудочного перехода. Естественно, что и заживление слизистой в пищеводе будет проходить гораздо дольше, так как рефлюкс агрессивного содержимого из желудка остается не корректированным. Именно поэтому, мы в своей работе используем разумную последовательность. В первую очередь патогенетический этап по прекращению рефлюкса и только после этого - радиочастотная абляция измененной слизистой. Как я писал уже ранее, у части больных второй этап не требуется, так как слизистая приходит в норму благодаря собственным репаративным процессам.
Таким образом, проведение лапароскопической фундопликации на первом этапе лечения позволяет уменьшить размеры пораженного сегмента пищевода, что в дальнейшем может потребовать всего 1-2 сеанса РЧА и соответственно меньшим риском развития стриктуры пищевода, а у ряда больных полностью избежать второго этапа.
Ответы на вопросы пациентов с пищеводом Баррета
Излечим ли пищевод Барретта?
Пищевод Барретта - это предраковое состояние, если пациент с таким диагнозом прошел необходимый курс лечения, регулярно посещает врача для контроля ситуации, выполняет все его рекомендации, то вероятность излечения очень высокая. Данное заболевание, особенно на ранних стадиях, хорошо поддается лечению при условии, что оно назначается индивидуально компетентным специалистом и проводится комплексно. Комплекс должен включать в себя все необходимые методы – медикаментозные, диетические, эндоскопические и хирургические. Таким образом, для полного излечения пищевода Барретта необходимы совместные усилия лечащего врача и пациента.
Как лечить пищевод Барретта?
В лечении пищевода Барретта важнейшим фактором является своевременность выявления патологии. Если пациент проходит регулярные осмотры, то врач сможет обнаружить болезнь на ранней стадии. После эффективного лечения риск возможного злокачественного перерождения клеток будет практически исключен.
Лечение проводится комплексно и, в зависимости от конкретной ситуации, включает как оперативные, так и консервативные методы. Терапевтическая программа составляется индивидуально для каждого пациента с учетом особенностей его организма и клинической картины. В результате снимается риск дальнейшего развития патологии и осложнений, опасных для жизни пациента, улучшается его самочувствие, повышается качество жизни.
Если ситуация позволяет назначить только консервативное лечение, пациент должен быть готов тщательно следовать назначенной схеме приема медицинских препаратов в течение длительного времени (от 3-х месяцев до 2 лет). Помимо этого для успеха лечения потребуется определенная коррекция диеты и образа жизни пациента – укрепляющие иммунитет процедуры, разумное дозирование труда и отдыха, снижение веса тела, отказ от вредных привычек (алкоголь, курение, шоколад, газировка, чай, кофе).
Многие пациенты, по рекомендации врача, проходят сразу сеанс радиочастотной абляции ( РЧА) слизистой пищевода, во время которой при гастроскопии проводят дозированную деструкцию измененной слизистой. В результате этой процедуры, происходит замещение метаплазированого эпителия в нормальную слизистую. Срок консервативного медикаментозного лечения укорачивается в несколько раз.
Если заболевание развилось на фоне ГПОД и уже вошло в стадию, требующую использования хирургических методов лечения, в нашей клинике применяются лапароскопические методы, которые не только результативны, но наносят минимум травм, поэтому достаточно легко переносятся пациентом.
Целью комплекса оперативных и консервативных методов является минимизация риска развития рака и восстановление слизистой оболочки пищевода. Также оперативное лечение назначается, если консервативное не принесло ожидаемых результатов.
Сколько живут с пищеводом Барретта?
Если лечение увенчалось успехом, что происходит в большинстве случаев, то пациенты, которым был поставлен диагноз «пищевод Барретта», живут нормальной жизнью.
Вот почему важно выявить болезнь на ранней стадии и выполнять все рекомендации лечащего врача. Опасность для жизни представляет не синдром как таковой, а его осложнения. К сожалению, с каждым годом число больных раком пищевода увеличивается. Лечение рака пищевода только хирургическое и сопровождается длительным и очень объемным оперативным вмешательством с удалением всего пищевода и пластикой его желудком.
Как часто пищевод Барретта переходит в рак?
Пищевод Барретта от обычных хронических заболеваний отличается тем, что перерождение клеток в любой момент может стать злокачественным. На первый взгляд спокойно протекающая болезнь может внезапно обернуться раком пищевода. Причем онкологический процесс отличается быстрым развитием.
В настоящее время мировая медицина отмечает значительное увеличение количества пациентов, страдающих от рака пищевода, который является следствием запущенного пищевода Барретта. Вероятность, что этот синдром перейдет в рак, по данным Всемирной организации здравоохранения в разных странах составляет различный процент, от 0,5% до 10%. Учитывая, что в нашей стране люди склонны уделять своему здоровью недостаточно внимания, списывают тревожные симптомы на недомогание, вероятность, что заболевание будет диагностировано на поздних стадиях и процесс перерождения клеток примет злокачественный характер, склоняется в сторону больших цифр.

Локализация пищевода Барретта в желудочно-пищеводном переходе

Визуальная картинка при эндоскопии, варианты слизистой при пищеводе Барретта
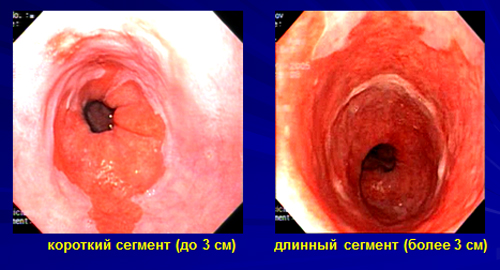
Визуальная картинка при эндоскопии, длина поражения слизистой при пищеводе Барретта
Пищевод Барретта (ПБ, синдром Барретта) — это изменение слизистой нижнего отдела пищевода по цилиндрическому типу любой длины, так называемая метаплазия. Эти изменения могут быть распознаны при эндоскопическом исследовании, после взятия биопсии из измененных участков и гистологического подтверждения.
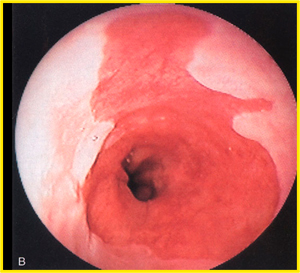 | 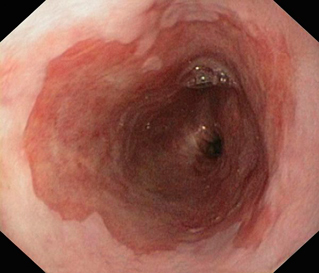 |
Причины и симптомы заболевания
Пищевод Барретта — это заболевание которое возникает в течении жизни, зачастую по причине следующих факторов:
- недостаточность нижнего пищеводного сфинктера, из-за чего содержимое желудка (кислая среда) попадает в пищевод;
- двойной рефлюкс — когда развиваются одновременно гастроэзофагеальная рефлюксная болезнь (ГЭРБ) и дуоденогастральная рефлюксная болезнь (ДГР);
- ослаблена сократительная функция пищевода;
- повышена секреция соляной кислоты;
- экзогенные факторы — курение, погрешности в питании, избыточный вес, злоупотребление алкоголем, комбинированная химиотерапия.
Наиболее частые формы патологических изменений слизистой оболочки пищевода, которые могут привести к ПБ:
- Дисплазия — нарушение нормального строения слизистой, при котором происходит старение клеток и увеличивается склонность к их бесконтрольному делению. Это состояние называют предраком, так как риск перерождения в онкологию есть, хоть и небольшой.Выделяют умеренную и тяжелую степень дисплазии, при тяжелой риск развития ПБ выше. При исключении провоцирующих факторов, заболевание не прогрессирует.
- Метаплазия — при этом состоянии происходит замещение нормальной слизистой пищевода клетками несвойственными этой зоне, чаще всего желудочными или кишечными. Состояние стойкое, оно не исчезает даже если исключить факторы риска. Есть данные, что при длине метаплазии 3 см и более высока вероятность развития злокачественной опухоли — аденокарциномы пищевода.
- Эрозивная форма — наличие эрозий и эрозивно-язвенных дефектов (как острых, так и эпителизирующихся) на слизистой пищевода в нижней трети (чаще в проекции перехода пищевода в желудок).
Основные жалобы пациентов и признаки пищевода Барретта
- боль во время глотания пищи по всему пищеводу, за грудиной или в эпигастрии;
- отрыжка кислым содержимым, особенно после еды, изжога;
- першение в горле возникающее после еды, усиливающееся при наклоне туловища, осиплость голоса;
- дисфагия, когда пациент жалуется, что ему трудно или больно глотать пищу, особенно твердую;
- тошнота и срыгивание после еды, особенно при натуживании или с отрыжкой;
- истончение эмали зубов.
Не следует игнорировать перечисленные симптомы и откладывать поход к врачу, лучше профилактировать заболевание и начать лечение на ранних этапах, ведь процессы, происходящие на клеточном уровне не обратимы.
Диагностика пищевода Барретта
Основной и наиболее эффективный метод диагностики синдрома Барретта — эндоскопический. Его цель — получение биопсийного материала. При этом морфологическое исследование направлено на:
- подтверждение метаплазии слизистой оболочки пищевода;
- выявление дисплазии;
- выявление злокачественных клеток, чаще аденокарциномы.
Для определения более точных границ измененной слизистой во время эндоскопического исследования используют хромоскопию, это окраска слизистой. Обычно используют раствор Люголя, при аллергии на йод — метиленовый синий, уксусную кислоту.
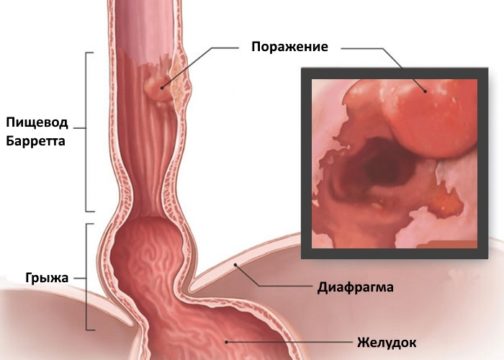
Лечение пищевода Барретта
Применяют следующие методы лечения пищевода Барретта:
- Медикаментозное. Проводится гастроэнтерологами. Зачастую назначают антацидные средства, которые снижают кислотность, прокинетики, которые стимулируют моторику и продвижение пищи по ЖКТ и ингибиторы протонной помпы.
- Эндоскопическое. И тут выбор у врача эндоскописта большой, все зависит от объема поражения, выраженности дисплазии, глубины инвазии (проникновения) и других факторов.
- аргонноплазменная коагуляция;
- эндоскопическая резекция (диссекция) слизистой оболочки;
- эндоскопическая абляция эпителия пищевода биполярным электродом;
- фотодинамическая терапия;
- криодеструкция;
- лазерная абляция.
- Хирургическое.
Для профилактики развития пищевода Барретта проводят фундопликацию по Ниссену. Суть операции в том, что вокруг пищевода из дна желудка делается манжетка, которая должна препятствовать забросу содержимого желудка в пищевод.
Еще один применяемый и весьма радикальный метод — удаление нижней части пищевода.

Профилактика
Не существует специфической профилактики синдрома Барретта.
Предупредить его развитие помогает своевременная диагностика и лечение гастроэзофагеальной рефлюксной болезни, регулярные и своевременные посещения гастроэнтеролога, обследования и стойкое динамическое наблюдение.
- При дисплазии слизистой оболочки пищевода – необходим ФГДС-контроль с биопсией 1 раз в 6 мес.
- При метаплазии – ФГДС-контроль 1 раз в год.
После эффективного консервативного и хирургического лечения пищевода Барретта всем пациентам необходимо проходить ежегодное эндоскопическое обследование с биопсией эпителия.

Авторская публикация:
ВИНЦКОВСКАЯ АЛЕКСАНДРА ИГОРЕВНА
онколог, эндоскопист
НМИЦ онкологии им Н.Н. Петрова
Рак пищевода представляет собой опухоль злокачественного характера, происходящую из эпителиальных клеток пищевода. Заболевание берет начало с внутреннего слоя, то есть слизистой оболочки, а затем распространяется наружу, преодолевая подслизистый и мышечный слои.
Существует два основных вида такого заболевания:
- Плоскоклеточный рак. Он возникает из клеток, составляющих слизистую оболочку пищевода. Чаще всего встречается в зоне шеи, а также двух верхних третей грудной клетки.
- Аденокарцинома, другими словами – железистый рак. Чаще всего диагностируется в нижней трети пищевода. Вначале происходит замещение железистого эпителия плоскоклеточным (при пищеводе Барретта).
Статистика
Чаще всего (до 80% случаев) новообразование находится в нижне- и среднегрудном отделах пищевода. С частотой 10-15% случаев диагностируется рак шейного отдела пищевода.
Факторы риска
Основные факторы риска возникновения и развития такой болезни:
- мужской пол, потому что мужчины чаще подвержены вредным привычкам – курению и употреблению спиртного в больших количествах;
- возраст – чем он больше, тем выше риск, лишь 15% пациентов были младше 55-ти лет;
- избыточная масса тела;
- курение и злоупотребление спиртным;
- употребление очень горячих напитков и еды;
- пищевод Барретта (когда в нижней части пищевода возникает клеточное перерождение, вызываемое кислотным повреждением хронической формы);
- рефлюкс;
- ахалазия (когда нарушена запирательная функция отверстия между желудком и пищеводом);
- рубцы в пищеводе, приведшие к его сужению;
- синдром Пламмера-Винсона (для такого синдрома характерна триада, то есть три вида нарушений одновременно: нарушенная глотательная функция, суженный пищевод, железодефицитная анемия);
- контакт с химикатами.
Примерно у 1/3 заболевших диагностирован ВПЧ (вирус папилломы человека).
Риск заболеть этим видом рака можно снизить, если разнообразно питаться, не пить крепкий алкоголь, а при наличии синдрома Барретта отслеживать изменения в слизистой оболочке.
Скрининг этого заболевания не проводится. Однако при повышенном риске появления рака пищевода рекомендуется проходить эндоскопическое исследование, при необходимости с биопсией подозрительной зоны.
Симптомы
Обычно рак пищевода обнаруживается на поздних стадиях, когда терапия уже осложнена, или случайно.
Наиболее частая симптоматика включает следующее:
- Дисфагия. Этот симптом представляет собой нарушенную функцию глотания. Пациенты описывают свое состояние как ощущение «комка в горле». Заболевшие начинают уменьшать порции пищи, избегают твердой еды. На поздних стадиях возможно употребление только жидкой пищи.
- Повышенное слюноотделение. Больше слюны в ротовой полости начинает вырабатываться для того, чтобы помочь продвинуться пищевому комку через суженный просвет пищевода.
- Дискомфорт и боль в грудине. Эти симптомы не всегда относятся к раку пищевода, они могут вызываться межреберной невралгией, стенокардией, гастроэзофагеальным рефлюксом. Поэтому не являются специфическими.
- Снижение массы тела. При затрудненном глотании и общей слабости заболевший человек начинает отказываться от еды, поэтому похудение часто сопровождает рак пищевода.
Есть и более редкие симптомы:
- кашель;
- икота;
- хриплый голос;
- рвота;
- костные боли (при наличии метастазов);
- пищеводное кровотечение (после того как кровь проходит по ЖКТ, стул окрашивается в черный цвет);
- как следствие кровотечения – анемия (человек становится бледным, слабым, быстро утомляется, испытывает постоянную сонливость).
Важно! Наличие подобных симптомов еще не означает рак. Однако нужно обязательно обратиться к врачу и обследоваться.
Классификация рака пищевода
По области возникновения:
- внутригрудной отдел пищевода;
- шейный отдел (от нижней границы перстневидного хряща до входа в грудную полость);
- верхняя грудная зона (от входа в грудную полость до области бифуркации трахеи);
- средняя грудная область (проксимальная часть пищевода распространяется от зоны бифуркации трахеи до соединения пищевода с желудком);
- нижняя грудная область (дистальная часть пищевода примерно 10 см в длине, включая абдоминальную часть пищевода, распространяется от зоны бифуркации трахеи до соединения пищевода и желудка).
По характеру роста опухоли:
- в просвет пищевода (экзофитный);
- язвенный (эндофитный);
- круговая форма (инфильтративный склерозирующий).
По степени дифференцировки новообразования:
- степень не определена – Gx;
- высокодифференцированное образование – G1;
- умеренно дифференцированное – G2;
- малодифференцированное – G3;
- недифференцируемое – G4.

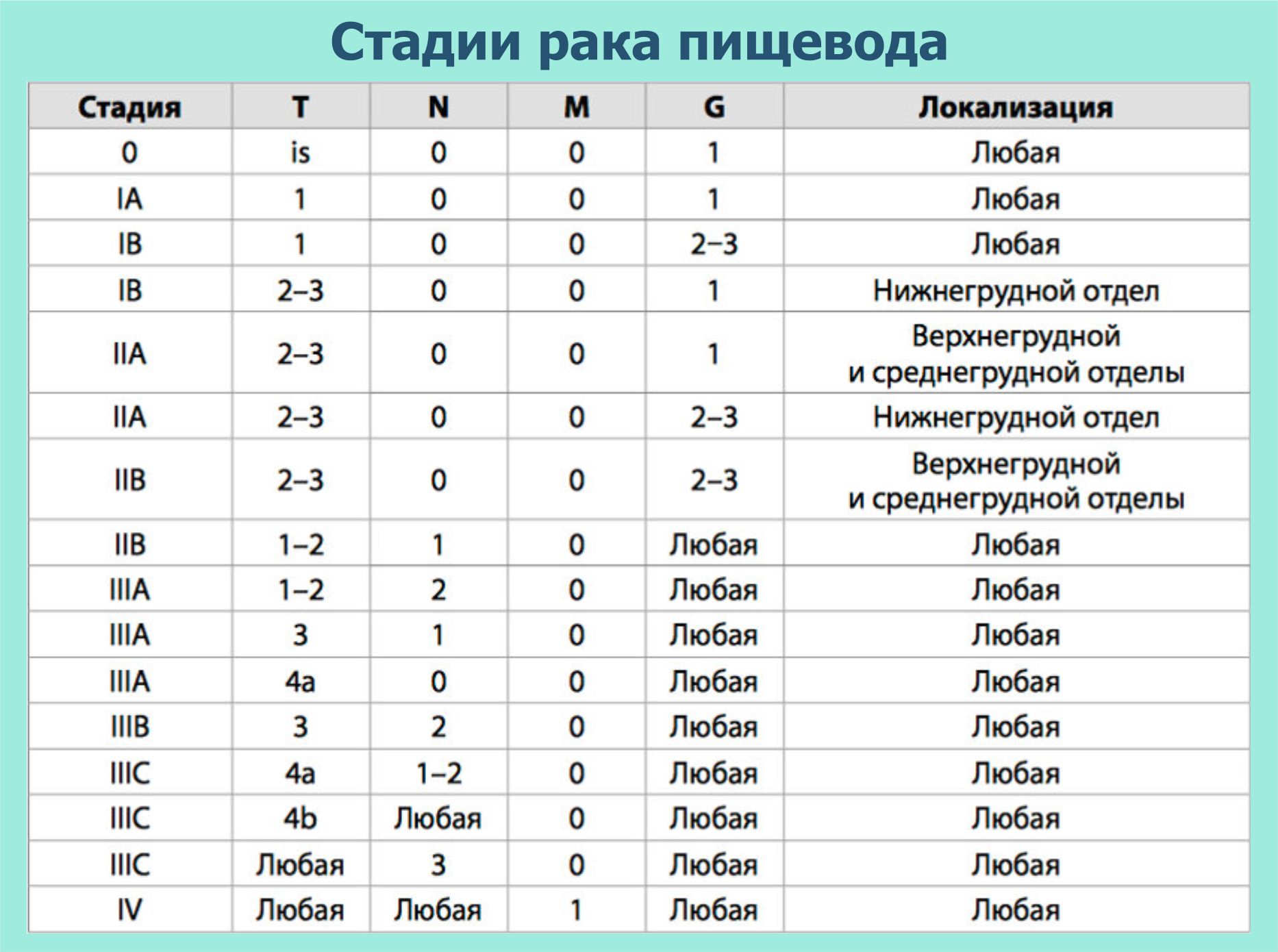
Стадии рака пищевода
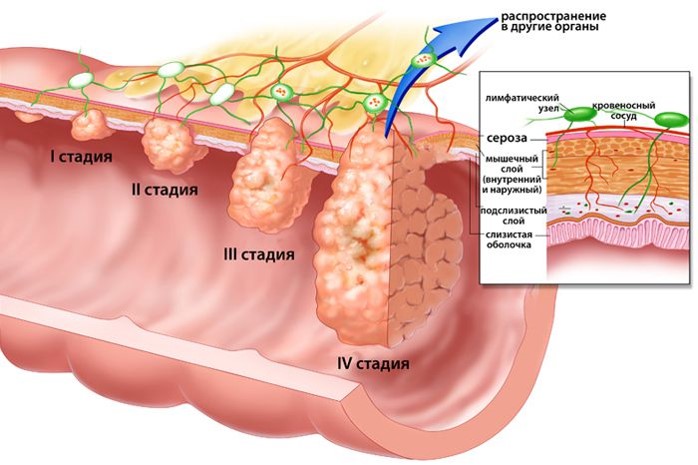
Предлагаем ознакомиться с таблицей стадирования заболевания:
Диагностика
Диагностирование осуществляется инструментальными и лабораторными методами.
-
Рентгенография с бариевым контрастом. Пациент принимает внутрь сульфат бария, который обволакивает стенки пищевода. Это позволяет увидеть на снимке рельеф стенок и обнаружить сужение просвета. На ранней стадии рак может иметь вид небольших круглых выпуклостей, то есть бляшек. На поздней стадии развития новообразование принимает вид большой опухоли неправильной формы, которая может вызывать сильное сужение пищевода. Рентгенография также позволяет диагностировать трахеопищеводную фистулу, то есть когда из-за разрушения новообразованием стенки пищевода на всю толщину пищевод начинает сообщаться с трахеей.
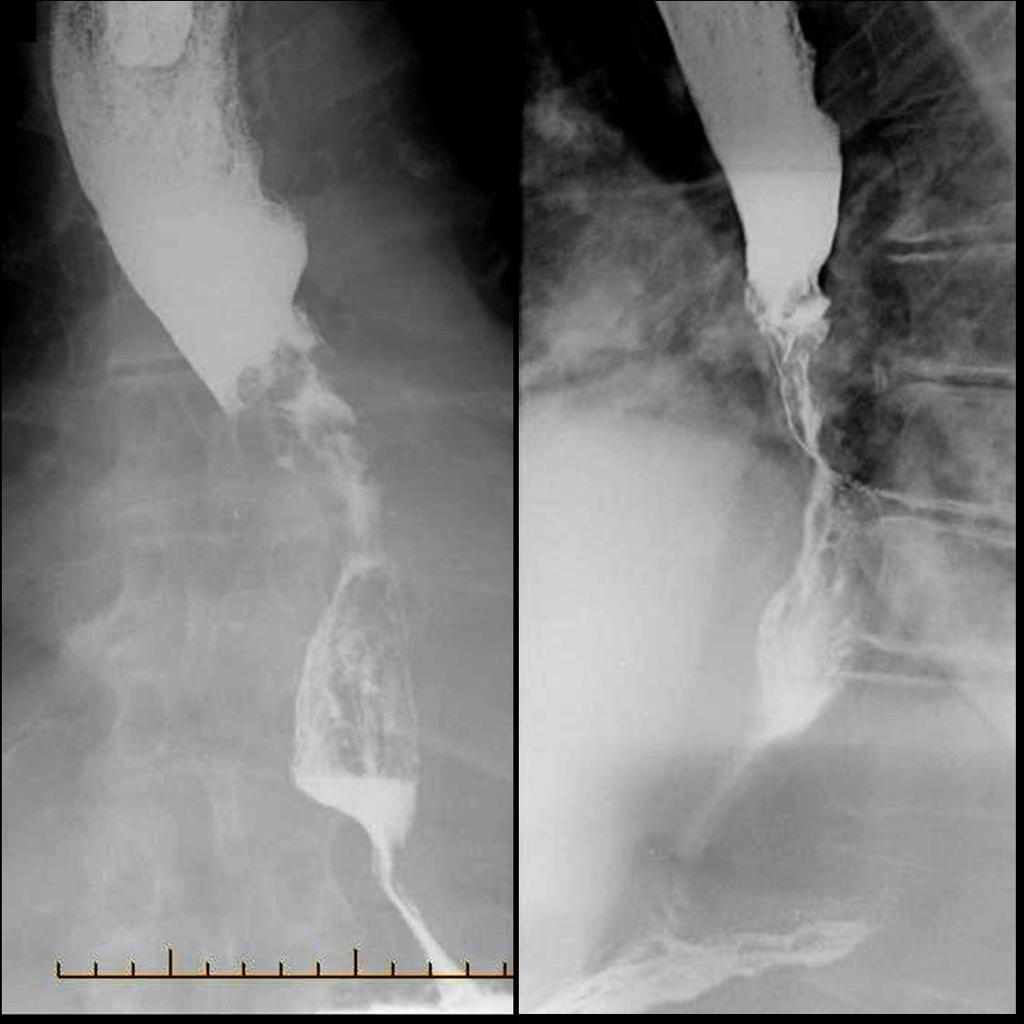
Рентгенодиагностика рака пищевода
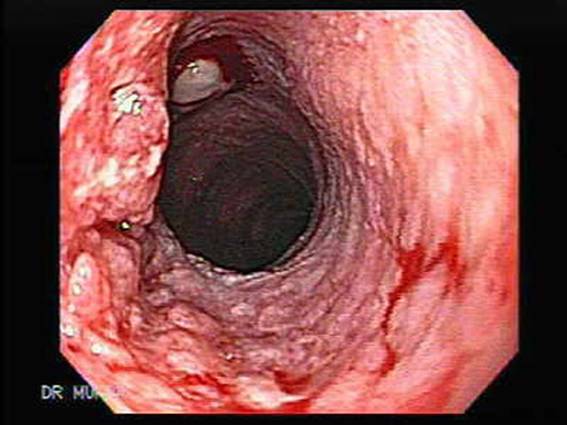
Эндоскопическая картина аденокарциномы
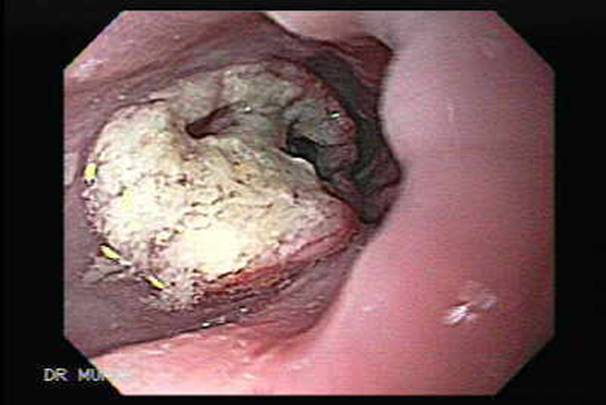
Эндоскопическая картина плоскоклеточного рака
Лабораторные исследования
- Клинический анализ крови. Позволяет выявить анемию, которая возникает из-за кровотечения или скудного рациона.
- Биохимический анализ крови. Он показывает состояние внутренних органов, а именно почек, печени и др.
- Анализ на онкомаркеры СА 19-9, РЭА.
- Исследование биоматериала, взятого во время биопсии. В нем определяют рецепторы белка HER2. При их наличии против новообразования можно использовать таргетную терапию.
Лечение
Основной метод лечения – хирургическая операция, однако комплексный подход позволяет улучшить результаты. Поэтому различные методики комбинируются.
Хирургическое лечение
В ходе операции удаляют пищевод целиком или его часть, все зависит от распространенности и локализации патологического процесса.
Когда опухоль находится в шейном отделе, удаляют большую часть пищевода. После этого желудок поднимают и подшивают к оставшейся части пищевода. Кроме того, вместо удаленной части методом пластической операции может быть использована часть толстой или тонкой кишки. При возможности выполнения резекции шейного отдела пищевода может быть выполнена пластика кишкой с микрососудистым анастомозом сосудов на шее.
При локализации опухоли в шейном отделе пищевода с большим распространением приходится выполнять операцию в объеме: удаления фаринголарингоэктомии с одномоментной пластикой пищевода желудочным трансплантатом, с пришиванием его к корню языка.
Хирургическое вмешательство по удалению части пищевода с последующим замещением трансплантатом может быть проведено открытым способом или методом торакоскопии и лапароскопии.
При любом типе вмешательства удаляют регионарные лимфоузлы, которые потом исследуют в лаборатории методом гистологии. Если в них обнаруживаются раковые клетки, то после операции пациенту прописывают лучевое лечение или химиотерапию в комбинации с ЛТ.
Также существуют паллиативные операции. Их проводят для того, чтобы пациент мог питаться, если из-за опухоли он не может глотать. Этот тип вмешательства называется гастростома, то есть введение через переднюю брюшную стенку в желудок специальной трубки для питания.
Лучевая терапия
Применяется ионизирующее излучение с целью уничтожения клеток новообразования. Такая терапия может проводиться:
- Тем пациентам, которым по состоянию здоровья нельзя делать операцию. В этом случае облучение, обычно вместе с химиотерапией, представляет собой основную методику лечения.
- При локализации опухоли в области шейного отдела пищевода химиолучевая терапия является первым этапом комбинированного метода лечения.
- Перед операцией вместе с химиотерапией. Это нужно, чтобы уменьшить опухоль и обеспечить ее лучшее удаление (называется «неоадъювантная терапия»).
- После хирургического вмешательства вместе с химиотерапией. Таким образом воздействуют на остаточную опухоль, которую нельзя было увидеть во время операции (носит название «адъювантная терапия»).
- Для облегчения симптоматики при распространенном раке пищевода. Позволяет снизить интенсивность болевого синдрома, устранить кровотечение и трудности с глотанием. В данном случае это паллиативная терапия.
Разновидности лучевого лечения:
- Наружное (дистанционное). Источник ионизирующего излучения находится на расстоянии от пациента.
- Контактное (называется «брахитерапия»). Источник излучения эндоскопическим методом размещается как можно ближе к новообразованию. Ионизирующие лучи проходят малое расстояние, поэтому достигают опухоли, но мало затрагивают расположенные рядом ткани. Лечение позволяет уменьшить новообразование и восстановить проходимость.

Дозное распределение, получаемое при дистанционной конформной лучевой терапии и внутрипросветной брахитерапии
Химиотерапия
Данная методика представляет собой введение в организм препаратов, затормаживающих жизнедеятельность опухолевых клеток или уничтожающих их. Лекарственные средства принимаются внутрь или вводятся в вену, после чего попадают в кровоток и достигают почти всех областей организма.
Химиотерапия осуществляется циклами. Это связано с тем, что действие препарата направлено на те клетки, которые постоянно делятся. Введение повторяется через определенное число дней, что связано с клеточным циклом. Циклы химиотерапии, как правило, имеют продолжительность 2-4 недели, больным обычно показано несколько циклов.
Как и облучение, химиотерапия показана в адъювантном и неоадъвантном режимах. Также она применяется, чтобы облегчить симптоматику тем больным, у которых рак распространен и не поддается хирургическому лечению.
- «Цисплатин» и «5-фторурацил» («5-FU»);
- «Паклитаксел» и «Карбоплатин»;
- «Цисплатин» совместно с «Капецитабином»;
- схема ECF: «Эпирубицин», «Цисплатин» и «5-FU»;
- схема DCF: «Доцетаксел», «Цисплатин» и «5-FU»;
- «Оксалиплатин» совместно либо с «Капецитабином», либо с «5-FU»;
- «Иринотекан».
Таргетная терапия
Направлена на блокировку роста новообразования путем воздействия на определенные мишени, то есть на те молекулы, которыми определяются деление и рост опухоли. Если в биоматериале, взятом методом биопсии, находят такие белковые молекулы, то может быть эффективна именно таргетная терапия.
Паллиативные методы
При проведении паллиативной терапии применяют следующие методики:
- Бужирование, то есть расширение пищевода.
- Установку стентов эндоскопическим методом. Стенты – это полые цилиндры, которые устанавливаются в просвет пищевода, чтобы обеспечить проходимость пищи.
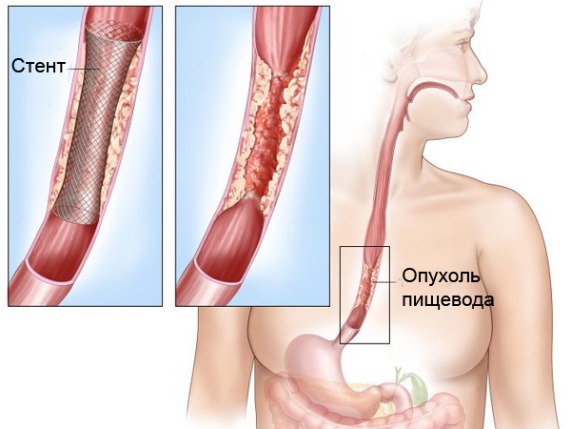
Стентирование рака пищевода
Лечение рака пищевода изменяется в зависимости от стадии
0 стадия
Опухоль на этой стадии – это не истинный рак. В ней содержатся аномальные клетки. Такое состояние называют «дисплазией», это разновидность предраковых заболеваний. Аномальные клетки имеют вид раковых, но встречаются только во внутренней оболочке пищевода (эпителии), они не растут в глубокие слои пищевода.
Обычно применяются эндоскопические методики лечения:
- PDT, или фотодинамическая терапия;
- RFA, то есть радиочастотная абляция;
- EMR, эндоскопическое удаление опухоли слизистой оболочки (после этого обеспечивается длительное наблюдение с применением эндоскопии, чтобы вовремя заметить рецидив, если он возникнет).
I стадия
Новообразование затрагивает мышечную или собственную пластинку слизистой, но не поражает другие органы и лимфоузлы.
- Рак T1. Заболевание на ранней стадии, когда оно находится только в небольшой зоне слизистой и не достигло подслизистой основы (новообразования Т1а), может быть удалено путем эндоскопической резекции в рамках слизистой или подслизистого слоя. Иногда медики рекомендуют хирургически удалить часть пищевода, а затем провести облучение и химиотерапию.
- Рак Т2. Опухоль затрагивает мышечную пластинку слизистой. Таким пациентам перед операцией проводятся химиотерапия и облучение. Исключительно хирургическое удаление рекомендовано, только когда новообразование менее 2 см в размере.
Когда рак локализуется в зоне шеи, вместо операции в качестве основного метода лечения могут быть рекомендованы облучение и химиотерапия.
II и III стадии
На второй стадии опухоль распространяется на главный мышечный слой пищевода либо его наружную оболочку. Также новообразование поражает 1 или 2 расположенных рядом лимфоузла.
При третьей стадии новообразование прорастает на наружную оболочку пищевода, может распространяться на соседние органы, им поражены регионарные лимфоузлы. Рекомендовано комбинированное лечение, которое включает операцию и предваряющие ее химиотерапию либо химиотерапию в сочетании с облучением. Если по состоянию здоровья для пациента есть риск не пережить операцию, то химиотерапия в сочетании с облучением становится основным методом лечения.
IV стадия
Рак затрагивает отдаленные лимфоузлы, есть метастазы в отдаленных органах (легких, печени). На такой стадии основная цель лечения – как можно более долгий контроль над распространением и размером новообразования. Пациентам проводится симптоматическое лечение для облегчения боли, восстановления возможности питаться и др. Применяется лучевая терапия и химиотерапия.
Профилактика
Чтобы предупредить такое заболевание, нужно исключить алкоголь и курение, контролировать массу тела. Если у человека присутствует повышенный риск развития этого типа рака (это такие патологии, как пищевод Барретта, ахалазия кардии, стриктуры пищевода, хронические эзофагит), то он должен регулярно обследоваться с обязательным применением эндоскопии.
Важно! Если рано диагностировать рак пищевода, то его можно вылечить с вероятностью от 85% до 100%.
Когда лечение рака завершено, нужно регулярно проходить контрольные обследования:
- После радикального лечения, сочетающего хирургию, химиотерапию и лучевую терапию: в первые 2 года – каждые 3-6 месяцев, в следующие 3-5 лет – каждые 6-12 месяцев, затем – каждый год.
- Тем, у кого был обнаружен ранний рак и кто подвергся эндоскопическому удалению слизистой: в первый год – каждые 3 месяца эндоскопическое обследование, во 2-й и 3-й годы – каждые полгода, затем – каждый год.


Авторская публикация:
Бекяшева Зоя Салаватовна
Ординатор хирургического отделения опухолей головы и шеи
НМИЦ онкологии им Н.Н. Петрова

Под научной редакцией:
Раджабова Замира Ахмедовна
Заведующий отделением опухолей головы и шеи, врач-онколог, научный сотрудник, доцент, кандидат наук
НМИЦ онкологии им. Н.Н. Петрова
Наиболее серьезным осложнением ГЭРБ является пищевод Баррета (метаплазия Баррета), заболевание, являющееся фактором риска развития рака пищевода (аденокарциномы). Перерождение клеток слизистой оболочки при пищеводе Баррета происходит по типу так называемой кишечной метаплазии, когда обычные клетки слизистой оболочки пищевода замещаются клетками, характерными для слизистой оболочки кишечника.
Кроме собственно рефлюксной болезни независимым фактором риска развития аденокарциномы пищевода является ожирение. При наличии обоих факторов риск развития аденокарциномы значительно повышается. Однако абсолютный риск аденокарциномы остается достаточно низким даже у людей с выраженными симптомами рефлюкса.
В зависимости от участка пищевода, где развивается метаплазия Баррета (и затем, возможно, аденокарцинома), специалисты разделяют это заболевание на три типа: метаплазия в области длинного сегмента пищевода, метаплазия в области короткого сегмента пищевода (в 3 см и менее от места перехода пищевода в желудок) и метаплазия в области кардиальной части желудка (часть желудка, расположенная сразу после перехода пищевода в желудок).
Распространенность метаплазии Баррета в области длинного сегмента пищевода по данным эндоскопических исследований составляет около 1%. Этот процент возрастает с увеличением тяжести ГЭРБ. Этот тип метаплазии чаще встречается в возрасте 55-65 лет, значительно чаще у мужчин (соотношение мужчин и женщин 10:1).
Метаплазия Баррета в области короткого сегмента встречается чаще, однако, распространенность этого заболевания оценить сложно, так как этот тип метаплазии при эндоскопическом исследовании сложно отличить от метаплазии в кардиальном отделе желудка. При этом злокачественная опухоль при метаплазии в области короткого сегмента пищевода и кардиальной части желудка развивается реже, чем при метаплазии в области длинного сегмента пищевода.
Хотя совершенно очевидно, что метаплазия Баррета в пищеводе возникает на фоне ГЭРБ и иногда приводит к развитию рака пищевода, остается не совсем ясно, почему происходит перерождение клеток по типу кишечной метаплазии в области кардиальной части желудка. Этот тип метаплазии встречается как при ГЭРБ, так и при гастрите при наличии инфекции Helicobacter pylori. Причем согласно данным исследований, метаплазия Баррета с области кардиальной части желудка, скорее всего, развивается на фоне гастрита даже чаще, чем на фоне ГЭРБ. Однако кишечная метаплазия и воспаление в этой области могут появиться и в отсутствии Helicobacter pylori, и в этом случае являться следствием хронического рефлюкса. Распространенность этого типа метаплазии составляет 1,4%.
Хотя непосредственная причина метаплазии Баррета остается неясной, тем не менее, очевидным является тот факт, что метаплазия развивается на фоне ГЭРБ и связана с чрезмерным патологическим воздействием кислоты на слизистую оболочку пищевода. Исследования с использованием рН-мониторирования показали, что у пациентов с метаплазией Баррета значительно увеличена частота рефлюксов и продолжительность пищеводного клиренса. Это может быть связано с выраженным нарушением сократительной функции мышц пищевода, развивающимся вследствие тяжелого эзофагита. Кроме того, у большинства пациентов с тяжелым эзофагитом имеется грыжа пищеводного отверстия диафрагмы.
Кроме того, манометрические измерения в области длинного сегмента пищевода при метаплазии Баррета показали, что при этом имеется снижение тонуса нижнего пищеводного сфинктера и нарушение перистальтики, сходные с таковыми при тяжелом эзофагите. Остается неясным, почему у одних пациентов с выраженным эзофагитом развивается метаплазия Баррета, а у других – нет. Существует предположение, что определенное значение имеет генетическая предрасположенность.
Пищевод Баррета - Наблюдение и лечение
В терапии больных с пищеводом Баррета основное внимание уделяется двум моментам: лечению ГЭРБ, на фоне которой развилась метаплазия, и предотвращение развития аденокарциномы пищевода. Принципы лечения имеющегося эзофагита и метаплазии Баррета остаются такими же, как и при обычной ГЭРБ, с учетом того, что поскольку имеется более выраженное воздействие кислоты на слизистую оболочку пищевода, терапия должна быть более интенсивной. Обычно бывает достаточно назначения ингибиторов протонной помпы, однако, может потребоваться и хирургическое вмешательство в случае неэффективности медикаментозного лечения.
Некоторые специалисты, основываясь на данных исследований, которые показали, что клеточные изменения происходят именно за счет патологического воздействия кислоты на слизистую оболочку желудка, предлагают использовать для лечения пищевода Баррета препараты, подавляющие секрецию соляной кислоты в желудке. Однако клинически не доказано, что применение антисекреторных препаратов или антирефлюксная операция могут предотвратить развитие аденокарциномы пищевода или привести к обратному развитию кишечной метаплазии. Таким образом, основной целью лечения является терапия эзофагита..
Поскольку в настоящее время не известны пути предотвращения развития метаплазии Баррета, действия врача должны быть направлены на уменьшение риска развития рака пищевода. С этой целью пациенты с пищеводом Баррета периодически проходят эндоскопическое обследование с обязательной биопсией на предмет степени перерождения клеток слизистой оболочки пищевода (метаплазия или дисплазия; насколько выраженная).
Сроки обследования устанавливаются в зависимости от тяжести имеющихся изменений слизистой оболочки пищевода. Так пациенты, у которых имеется только метаплазия Баррета без дисплазии, проходят обследование один раз в 2-3 года.
Если обнаружена дисплазия, проводится более тщательное обследование для определения степени дисплазии, так как при дисплазии высокой степени рак может развиться в течение 4 лет.
Пациентам с низкой степенью дисплазии назначается 12-недельный курс ингибиторов протонной помпы в высоких дозах, затем проводится повторное обследование с биопсией. Если обследование подтверждает наличие дисплазии низкой степени выраженности, то в последующем эндоскопия проводится через 6 месяцев, а затем ежегодно, если не отмечено развития дисплазии высокой степени.
Хирургическое лечение пищевода Баррета
Хирургическое лечение пищевода Баррета направлено на снижение количества эпизодов рефлюкса.
Хотя рефлюксная болезнь является фактором риска развития аденокарциномы пищевода, до конца не ясно, само ли существование пищевода Баррета предрасполагает к развитию рака или какие-то другие причины способствуют злокачественно перерождению клеток при наличии пищевода Баррета.
Уменьшению симптомов заболевания способствует как медикаментозное, так и хирургическое лечение пищевода Баррета. Однако по данным исследований даже прием ингибиторов протонной помпы в больших дозах не способствует уменьшению частоты рефлюкса. Поэтому, несмотря на улучшение состояния пациентов вследствие приема лекарств, хирургическое лечение пищевода Баррета имеет большое значение. Кроме того, данные некоторых исследований показывают, что после лапароскопической фундопликации риск развития рака пищевода значительно снижается, по сравнению с медикаментозной терапией. Хотя после хирургической операции повышается риск смертности, что связано с необъяснимым увеличением частоты заболеваний сердца у таких пациентов. В связи с этим решение об операции принимается врачом после тщательного взвешивания всех аргументов за и против хирургического лечения. Если операция проводится опытным хирургом, то ее результат может быть очень хорошим, хотя и не гарантирует полностью исчезновение симптомов заболевания, что иногда требует послеоперационного приема препаратов.
Данные исследований показывают, что медикаментозная терапия, в отличие от хирургического лечения, оказывает меньший эффект на частоту возникновения рефлюкса во время сна. В этой ситуации достаточно эффективными оказываются как лапароскопическая, так и открытая операция.
Кроме того, по некоторым данным, основанным на продолжительных наблюдениях, после фундопликации риск развития дисплазии и рака пищевода ниже, чем после лекарственной терапии.
Хирургическое лечение рекомендуется также пациентам, с пищеводом Баррета в сочетании с наличием грыжи пищеводного отверстия диафрагмы.
Эндоскопическая абляция
Этот метод хирургического лечения пищевода Баррета сопряжен с меньшим риском развития осложнений, чем большая хирургическая операция. Теоретически, данный метод является относительно безопасным.
Методика операции состоит в удалении пораженной части слизистой оболочки пищевода. На этом месте в дальнейшем происходит восстановление нормальной слизистой оболочки, что снижает риск развития рака пищевода. Пораженная часть слизистой оболочки удаляется с помощью воздействия лазерного или другого высокоэнергетического излучения. При этом пациенту назначается дополнительный прием ингибиторов протонной помпы в высоких дозах для улучшения восстановления нормальной слизистой оболочки пищевода.
Операция проводится либо без подготовки, либо после приема специальных препаратов, воздействующих на клетки измененной части пищевода и подготавливающих к лазерному воздействию для улучшения результата операции.
Хирургическое лечение при наличии высокой степени дисплазии
При дисплазии высокой степени риск развития аденокарциномы также становится высоким. Дисплазия может быть обнаружена только на одном участке слизистой оболочки пищевода (фокальная), а может развиться сразу в нескольких местах (мультифокальная), и такая дисплазия сочетается со значительным риском развития аденокарциномы (27% в течение 3 лет).
У пациентов с пищеводом Баррета с высокой степенью дисплазии не всегда целесообразно проведение эндоскопической абляции слизистой оболочки пищевода. Это связано с тем, что при таком подходе достаточно трудно полностью удалить пораженную ткань, а при высокой степени дисплазии риск развития рака пищевода также является высоким, даже при наличии небольшого участка пораженной ткани. Поэтому для проведения эндоскопической операции должны быть строгие показания. Должен быть тщательно оценен риск операции.
Эндоскопическая абляция проводится у тех пациентов, которым не рекомендуется проведение эзофагэктомии (большая операция, при которой удаляется часть пищевода или весь пищевод). В остальных случаях предпочтительным методом хирургического лечения пищевода Баррета с высокой степенью дисплазии остается эзофагэктомия.
Эзофагэктомия является эффективным методом лечения у молодых и в остальном здоровых пациентов, однако сопряжена с относительно высоким риском смертности (3-10%). В связи с этим некоторые специалисты рекомендуют вместо немедленной операции при дисплазии высокой степени у пациентов с пищеводом Баррета поводить постоянное (с высокой периодичностью) эндоскопическое наблюдение.
Поскольку операция удаления пищевода сопряжена с высоким риском, в качестве альтернативного метода хирургического лечения пищевода Баррета с высокой степенью дисплазии применяется эндоскопическая абляция. Эта операция может проводиться термическим, химическим или механическим способом. В любом случае операция состоит в удалении метаплазированного или дисплазированного эпителия в сочетании с интенсивной антисекреторной терапией, что в последующем обуславливает восстановление нормального эпителия слизистой оболочки пищевода.
Эндоскопическая резекция слизистой оболочки пищевода
Это еще один метод хирургического лечения пищевода Баррета. Методика операции состоит в хирургическом иссечении пораженной части слизистой оболочки с помощью специальных эндоскопических инструментов, в том числе электрокоагулятора (который используется, например, при эндоскопическом удалении полипов).
Успех данной операции достаточно высок, однако часто уже в течение первого года после операции может развиться рецидив заболевания.
Термическая абляция производится с помощью электрокоагулятора, аргонового плазменного коагулятора или лазерного облучения. Одним из осложнений данной операции является перфорация пищевода. Другой способ абляции – фотодинамическое облучение с помощью специального прибора. Как и термическая абляция, данный метод может вызвать некоторые побочные эффекты: боль в груди, тошноту и развитие стриктур пищевода. Кроме того, следует предупредить пациентов о том, что после операции необходимо избегать длительного пребывания на солнце, так как возможно развитие реакции повышенной чувствительности к ультрафиолетовому облучению со стороны кожи. Данная процедура является весьма эффективной и приводит к обратному развитию дисплазии у 90% пациентов. Остаточные явления метаплазии Баррета наблюдаются в течение 2-62 месяцев у 58% пациентов, прошедших процедуру фотодинамической абляции.
Механическая абляция заключается в механическом удалении измененной части слизистой оболочки пищевода с помощью специальных эндоскопических инструментов. Эта процедура рекомендуется тем пациентам, у которых наблюдается ранняя стадия развития рака пищевода и которым по тем или иным причинам не может быть проведена большая хирургическая операция (удаление пищевода).
Читайте также:

