Что такое лизис кожи
Обновлено: 25.04.2024
Синдром быстрого лизиса опухоли у гематологических больных - диагностика, лечение
Синдром быстрого лизиса опухоли - одно из самых драматичных осложнений специфического лечения злокачественных опухолей обусловлено быстрой гибелью большой клеточной массы под действием цитостатической терапии. Тяжелые метаболические расстройства возникают из-за стремительного разрушения клеточной мембраны опухолевых клеток и выброса в циркуляцию внутриклеточных электролитов и продуктов обмена (калий, фосфаты, продукты пуринового обмена).
Синдром быстрого лизиса опухоли (tumor lysis syndrome, ТЛС) обусловлен крайней степенью выраженности таких метаболических расстройств, выходящих за рамки функциональных возможностей систем естественной детоксикации. Наиболее выражен ТЛС у больных с развитием «порочного круга», при котором происходит повреждение почек продуктами распада тканей, что в свою очередь снижает почечный клиренс этих продуктов.
Чаще всего наблюдается после назначения цитостатиков больным с массивными проявлениями опухоли, чувствительной к цитостатической терапии: при остром и хроническом лимфобластном лейкозе и лимфомах (лимфома Беркитта) и т. д. Крайне редко ТЛС развивается еще до начала лечения опухоли (лимфома Беркитта).
Симптомы синдрома быстрого лизиса опухоли варьируют от незначительных тонических судорог и сонливости (гиперфосфатемия, гипокальциемия), «субклинических» аритмий до острой почечной недостаточности (ОПН, обычно в форме фосфатной и уратной нефропатии), тяжелой дыхательной недостаточности и остановки сердечной деятельности (обычно вследствие гиперкалиемии).
Риск развития ОПН повышен у больных с предшествующим нарушением функции почек (нефротоксичная химиотерапия, хроническая почечная недостаточность любой этиологии) и/или некорригированными до начала химиотерапии метаболическим ацидозом и дегидратацией.

Профилактика синдрома быстрого лизиса опухоли необходима у пациентов с большой массой опухолевой ткани и прогнозируемым быстрым цитолизом. Цель профилактических мероприятий — активация системы естественной детоксикации (увеличение почечной фильтрации) и предупреждение почечной недостаточности (уменьшение продукции мочевой кислоты, непочечное связывание фосфатов).
Гидратация изотоническим раствором хлорида натрия или гипотоническими жидкостями (раствор Рингера, 5 % раствор глюкозы, 0,45 % раствор хлорида натрия) в суточном объеме 3000 мл/м 2 (200—250 мл/ч) необходима для поддержания высокого водного диуреза и должна начинаться за несколько часов до введения цитостатиков. Одновременно нужно оценить водовыделительную функцию почек: в норме в ответ на водно-солевую нагрузку диурез увеличивается, и через 2—4 ч темп диуреза становится равен темпу инфузии.
При выраженной задержке жидкости применяют петлевые диуретики или ацетазоламид (диакарб) в дозе 5 мг/кг в сутки.

Показанием к проведению экстренного гемодиализа являются неподдающиеся консервативному лечению гиперурикемия (уровень мочевой кислоты выше 100 мг/л), гиперкалиемия (калий сыворотки выше 6,5 ммоль/л или появление характерных изменений ЭКГ), гиперфосфатемия, развитие тяжелой почечной недостаточности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Синдром лизиса опухоли - причины, лечение, профилактика
Острое метаболическое расстройство может происходить в результате быстрого разложения опухоли, следующего за химиотерапией. Это наиболее вероятно появляется у детей с лимфомой Беркитта или острой лимфобластической лейкемией и неходжкинской лимфомой у детей, подростков и молодых людей. Синдром появляется, когда опухоль высокочувствительна к лечению, и практически не встречается у взрослых людей с нелимфоидными неоплазмами. Масса опухоли может исчезать очень быстро, и ее умершие клетки высвобождают продукты метаболизма азота, особенно мочевину, мочевую кислоту и большие количества фосфата.
Быстрое уменьшение в массе опухоли вызывает гиперурикемию, гиперфосфатемию, гиперкалиемию и уремию.
Гиперурикемия может приводить к острому осаждению мочевой кислоты в почечных канальцах (уратная нефропатия), что ведет к острой почечной недостаточности, или, менее кардинально, к уменьшению скорости гломерулярной фильтрации, которая обостряет гиперурикемию. Иногда синдром достаточно серьезен, вызывает острую или продолжительную уремию. Гипефосфатемия приводит к снижению уровня кальция в плазме и даже к тетании.
Синдром чаще наблюдается у детей с лимфомой Беркитта, у которых была экстенсивная болезнь, особенно при наличии интра-абдоминальных масс, с ухудшенной почечной функцией из-за опухолевой инфильтрации почек или постренальной обструкцией из-за увеличения лимфоидных узлов.
Синдром редко встречается у взрослых, так как у них опухоли менее чувствительны к действию химиотерапии, и их растворение происходит менее быстро. Это может, однако, случиться, если имеется соответствующая почечная недостаточность, вызванная какой-либо другой причиной, мочевая обструкция или инфильтрация почек опухолью.

Синдром лизиса опухоли можно предотвратить. Перед началом химиотерапии пациенту с высоким риском рекомендуется давать аллопуринол (обычно через рот) в общей дозе (50-100 мг каждые 8 ч для детей, дважды в день ту же дозу для взрослых) в течение 24 ч. Этот ингибитор ксантин-оксидазы частично предотвратит формирование мочевой кислоты. Предшественники, ксантин и гипоксантин, таким образом, присутствуют в большом избытке, но они более растворимы, чем мочевая кислота и не вызывают нефропатию.
Прием аллопуринола рекомендуется продолжать принимать в первые несколько дней лечения и прекратить, когда уровень мочевой кислоты в плазме будет на нормальном уровне. Если при этом давать 6-меркаптопурин, то доза должна быть уменьшена, так как аллопуринол ингибирует его метаболизм. В то же время пациент должен употреблять достаточное количество жидкостей, обычно в форме внутривенного солевого раствора, для того чтобы обеспечить хороший диурез. Эти меры должны предотвратить и гиперурикемию, и гиперфосфатемию.
При лимфоме Беркитта введение химиотерапии иногда дается в уменьшенных дозах до тех пор, пока уменьшение опухоли не будет значительным, затем принимается полная доза. Аллопуринол рекомендовано давать взрослым с начальным лечением высокодифференцированной лимфомы с интенсивной химиотерапией; его использование должно быть рассмотрено в остальных случаях, если существует некоторая возможность ухудшения работы почек.
Развившиеся гиперурикемию и острую почечную недостаточность обычно лечат приостановлением химиотерапии, осмотрительным применением внутривенных жидкостей с подщелачиванием мочи для обеспечения выведения мочевой кислоты и аллопуринолом. Если уровень мочевины в крови и уровень мочевой кислоты в плазме продолжают расти, понадобится перитонеальный диализ для того, чтобы преодолеть острую почечную недостаточность пациента. Если приняты меры профилактики, это редко бывает необходимо.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Дегенеративно-дистрофическая деструкция кости. Деструкция кости от вытеснения и остеолиз
Дегенеративно-дистрофическая деструкция. При ней замещающим субстратом является фиброзная, неполноценная остеоидная ткань с участками кровоизлияний и некроза, окрашенными в темно-коричневый цвет (бурая опухоль). К этой группе деструкции относятся: киста, гиганто-клеточная опухоль (остеобластокластома) и множественные кисты при болезни Реклингаузена. Рентгенологическая картина при этих процессах проявляется наличием деструктивного симптомокомплекса.
При солитарной кисте выявляется единичный круглый очаг или фокус деструкции округлой формы, окаймленный со всех сторон склеротизированной костной каемкой, иногда имеющей крупноячеистый рисунок из-за наличия внутренних перекладин.
Отличие болезни Реклингаузена от солитарной кисты только в том, что первая имеет множественность поражений и в деструктивных очагах чаще не бывает перекладин, т. е. полости большей частью с однородным рисунком.
При гигантоклеточной опухоли (остеобластокластоме) будет выявляться одиночный крупный фокус деструкции в метаэпифизарном отделе кости с множественными крупными ячейками (в виде мыльных пузырей) — ячеистая форма; или в виде краевого деструктивного дефекта с четко ограниченными контурами — литическая форма остеобластокластом.
Деструкция от вытеснения. При ксантоматозе, главным образом в плоских костях, особено в черепе, будут выявляться множественные очаги деструкции в виде сплошных дефектов с изъязвленными контурами различной формы и величины без признаков периостальной реакции.

Остеолиз - лизирование костной ткани без ее разрушения и вытеснения. В этом отличие остеолиза от деструкции.
Остеолиз возникает при заболеваниях центральной нервной системы (табес, сирингомиелия), при повреждениях периферических нервов, при отморожениях, эндартериите и т. д.
Рентгенологическая картина остеолиза такая же, как и при деструкции, она проявляется просветлениями различной формы и величины. Характерная особенность остеолиза в его локализации, т. к. остеолизу подвергаются самые периферические и свободные участки скелета: ногтевые отростки, суставные концы костей, а деструкция располагается в любом отделе кости. При остеолизе рассасывается вся кость: корковый слой, губчатая кость и субхондральная пластина.
Патоморфологической основой остеонекроза является гибель костных клеток при сохранении плотного промежуточного вещества, в связи с чем плотные элементы в некротическом участке преобладают, и на единицу веса мертвой кости минерального остатка приходится больше, чем живой. Некроз участка кости наступает в результате недостаточного или полного прекращения кровоснабжения, а живая костная ткань, окружающая омертвевший участок, обычно гиперемирована и процессы всасывания в ней усилены по сравнению с нормой.
Различают септический и асептический остеонекрозы. Асептические некрозы наблюдаются при остеохондропатиях или деформирующих артрозах, при тромбозах и эмболиях, возникающих у работников определенных профессий (кессонщиков, водолазов, высотников).
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.

Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
При некоторых злокачественных болезнях крови или лимфатической ткани на фоне химиотерапии тоже возникает распад, но без формирования зоны некроза, при этом массово погибающие раковые клетки выбрасывают в кровь свое содержимое, которое не успевает утилизироваться фагоцитами, «забивает» почки и заносится в сосуды других органов.
Массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.
С течением времени центральная часть злокачественного новообразования любой морфологической принадлежности начинает испытывать трудности с доставкой питательных веществ. Происходит это из-за того, что раковые клетки размножаются быстрее, чем формируется «кормящая» их сосудистая сеть. Голодающие клеточные пласты погибают, что проявляется распадом с образованием зоны некроза, отграниченной от живой опухолевой ткани, с постепенным формированием полости, в которой протекают процессы медленного гниения.

Если некротическая полость находится близко к коже, то может прорваться наружу в виде распадающегося «гнойника» и образованием незаживающей язвы, к примеру, молочной железы. В легком при рентгене внутри ракового узла с распадом будет видна тёмная «дырка» с отдельно расположенным внутри островковым кусочком некротической ткани — секвестром.
Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.
Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
Для эффективного лечения распадающегося опухолевого конгломерата необходимо восстановление внутриопухолевого питания посредством быстрого формирования новой сосудистой сети, что совершенно невозможно. Поэтому при спонтанном распаде прибегают к симптоматической терапии, в том числе паллиативным хирургическим — «санитарным» вмешательствам.
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Что такое эксфолиативный кератолиз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Похлебкиной Алевтины Алексеевны, педиатра со стажем в 6 лет.
Над статьей доктора Похлебкиной Алевтины Алексеевны работали литературный редактор Вера Васина , научный редактор Владимир Горский и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
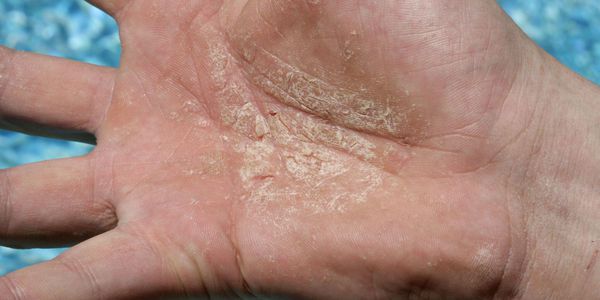
Эксфолиативный кератолиз — это очаговое симметричное шелушение кожи на ладонях, поверхности пальцев и, реже, на подошвах. Заболевание характеризуется сухостью кожи и поверхностными пузырями, заполненных воздухом.
Также эксфолиативный кератолиз называют рецидивирующей фокальной ладонной десквамацией, сухим пластинчатым дисгидрозом и рецидивирующей ладонной десквамацией.
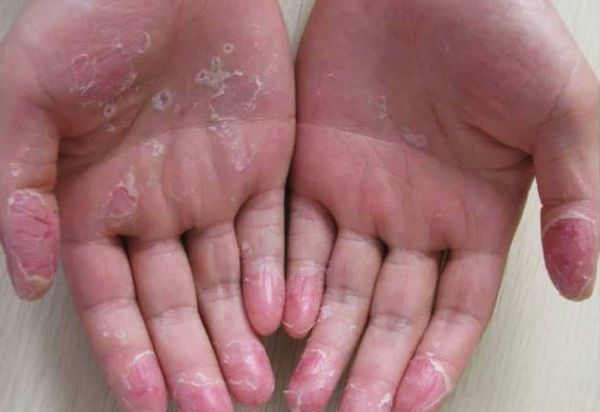
Заболевание широко распространено и часто носит хронический, но доброкачественный характер. Эксфолиативный кератолиз чаще встречается у детей и подростков, реже у взрослых. Нередко его ошибочно принимают за псориаз, экзему или хронический контактный дерматит. У людей с повышенной потливостью рук состояние ухудшается в тёплую погоду и может быть связано с гипергидрозом — усиленным потоотделением [1] .
Ранее эксфолиативный кератолиз называли дисгидротической экземой , и считалось, что заболевание вызвано нарушением работы потовых желёз. Эта связь уже опровергнута, но термин "дисгидротическая экзема" всё ещё используется [2] .
Дисгидротическая экзема, также называемая помфоликсом, может предшествовать эксфолиативному кератолизу. При этом состоянии на пальцах рук, ног, ладонях и подошвах образуются волдыри, наполненные жидкостью, и возникает сильный зуд [2] . Причина дисгидротической экземы неизвестна, но, вероятно, на развитие заболевания влияет множество факторов. В большинстве случаев причину и предрасполагающий фактор выделить невозможно [17] .
Причины эксфолиативного кератолиза
Предполагалось, что экфолиативный кератолиз может быть вызван грибковым поражением, но в дальнейших исследованиях эта гипотеза не подтвердилась.
Возможные провоцирующие факторы эксфолиативного кератолиза:
- трение и контакт с водой[3][6];
- мыло, моющие средства и растворители: химические вещества, содержащиеся в них, могут привести к появлению трещин и пузырей на руках;
- аллергия: продукты питания, загрязнение воздуха и другие вещества могут спровоцировать появление аллергии на коже;
- стресс: может не только вызвать, но и усугубить течение болезни;
- жаркий климат: при тёплой погоде потоотделение усиливается, что может привести к шелушению кожи;
- воздействие солёной воды;
- сухость кожи.
Эксфолиативный кератолиз не связан с дефицитом какого-либо витамина . Встречаются семейные случаи заболевания, однако генетическая роль в развитии эксфолиативного кератолиза изучена недостаточно [14] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы эксфолиативного кератолиза
Эксфолиативный кератолиз часто протекает без выраженных симптомов и проявляется незначительным поражением кожи ладонно-подошвенной области [5] . Отшелушиванию кожи предшествует появление наполненных воздухом пузырей, которые никогда не бывают заполнены жидкостью [3] . В некоторых случаях заболевание начинается только с очагового шелушения кожи, без образования пузырей.
После вскрытия пузырей остаются широкие сетчатые, круглые или овальные очаги. Они шелушатся, распространяются по периферии и образуют большие округлые участки, напоминающие кружева.
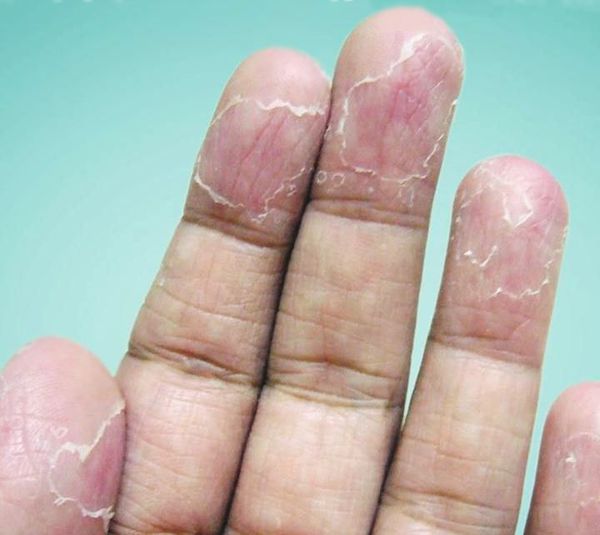
Участки слущенного эпителия теряют защитную функцию, становятся красными, сухими и покрываются трещинками. Шелушению может предшествовать небольшой зуд или жжение, в некоторых случаях область слущенного эпителия становится болезненной [3] .
Высыпания всегда симметричные. Иногда на кончиках пальцев образуются глубокие трещины, кожа становится жёсткой и немеет — в таком случае для полного заживления потребуется 1—3 недели. Эксфолиативный кератолиз может повториться через несколько недель после того, как на месте отшелушивания образовалась новая кожа.
Патогенез эксфолиативного кератолиза
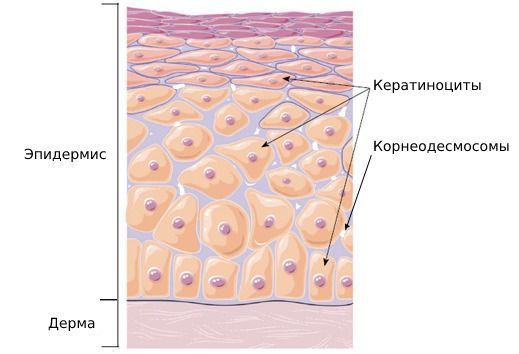
Эпидермис — верхний наружный слой кожи, состоящий из кератиноцитов. Эти клетки содержат белок кератин, необходимый для прочности и эластичности кожи. Когда кератин разрушается, прочность кожи снижается, из-за чего она начинает шелушиться.
Также в эпидермисе содержатся корнеодесмосомы — белковые структуры, которые соединяют кератиноциты в сеть. В верхнем роговом слое кожи количество таких структур обычно уменьшается. Это нормальный физиологический процесс. Он называется десквамацией. Благодаря нему клетки кожи отшелушиваются, при этом поддерживается постоянная толщина рогового слоя [8] .
Исследование 24 пациентов с эксфолиативным кератолизом показало, что заболевание может возникать из-за дисбаланса активности ферментов, участвующих в процессе десквамации, особенно на коже ладоней [3] .
Точный механизм развития эксфолиативного кератолиза неизвестен. Прояснить возможные генетические или приобретённые причины заболевания помогут дальнейшие исследования десквамационных ферментов и ингибиторов — веществ, подавляющих или задерживающих течение ферментативных процессов. К таким веществам относятся ингибитор секреторной лейкоцитарной протеазы (SLPI), альфа-2 макроглобулин-1 (A2ML1), сульфат холестерина и ион цинка.
Классификация и стадии развития эксфолиативного кератолиза
По МКБ-10 (Международной классификации болезней) дерматологи часто кодируют эксфолиативный кератолиз как L26, относя заболевание к "другим эксфолиативным состояниям".
Классификации и стадийности эксфолиативный кератолиз не имеет. Заболевание иногда может приобретать хроническое течение с периодами ремиссии и обострения.
Осложнения эксфолиативного кератолиза
Эксфолиативный кератолиз не вызывает системных проявлений или осложнений. При заболевании может повреждаться кожа, в результате чего присоединяется бактериальная инфекция. Её признак — красные пятна, которые превращаются в гнойнички и пузырьки. Пузырьки безболезненные и легко вскрываются, образуются желтоватые чешуйки, так называемые "медовые корочки". При этом может возникать зуд.
Диагностика эксфолиативного кератолиза
Диагноз "эксфолиативный кератолиз" ставится на основании данных клинического обследования и сбора анамнеза [15] . Некоторые пациенты отмечают, что состояние усугубляется после воздействия химических или физических раздражителей, таких как вода, мыло и моющие средства. Другие ассоциируют шелушение кожи с повышенным потоотделением.
Эксфолиативный кератолиз, вероятно, распространён, но часто протекает бессимптомно, поэтому врачи его наблюдают редко.
При осмотре отмечаются симметричные округлые участки шелушения на ладонях и, реже, на стопах. При этом воспаление на коже отсутствует.
Обычно дополнительное диагностическое тестирование не требуется. Однако в более сложных случаях, при подозрении на грибковое поражение, может потребоваться исследование с гидроксидом калия (KOH).
Биопсия кожи при кератолизе показывает расщепление и частично разрушенные корнеодесмосомы в роговом слое.
Патч-тесты , оценивающие потенциальную контактную аллергию , при эксфолиативном кератолизе отрицательны.
Дифференциальную диагностику проводят со следующими заболеваниями:
- различные формы дерматита рук, включая контактный дерматит, — для него характерен зуд, воздействие провоцирующих факторов в анамнезе, положительный ответ на гормональные мази;
- дисгидроз — сопровождается зудом, появлением трещин и везикул, наполненных жидкостью; — бляшки с чёткими границами бордово-красного цвета, выступающие над поверхностью кожи;
- дерматофития рук — изменение ногтей на руках и ногах, положительный ответ на противогрибковые препараты, не всегда симметричное поражение;
- простой буллёзный эпидермолиз — пузыри на разных участках кожи младенцев, возникающие после трения;
- ограниченный ладонный гипокератоз — редкое состояние, характеризуется центральной розовой областью с тонкой кожей на ладонях или подошвах стопы, по краям резкий переход к нормальной коже;
- пальмоплантарная кератодерма — возникает на коже стоп и кистей, характеризуется выраженным утолщением кожи [11] ;
- синдром акрального шелушения кожи — генетическое заболевание с пожизненным отслаиванием кожи.
Лечение эксфолиативного кератолиза
Причин возникновения эксфолиативного кератолиза может быть несколько, и не всегда они очевидны. Поэтому лечение болезни направлено на устранение симптомов и усугубляющих факторов. Это достигается защитой рук от физических или химических раздражителей ношением перчаток, когда это возможно.
Активное увлажнение кожи — важный, безопасный и эффективный метод лечения [10] . Наиболее подходящим способом для большинства пациентов являются кератолитические кремы, содержащие мочевину, молочную кислоту, лактат аммония или салициловую кислоту. Кремы с мочевиной увлажняют кожу и предотвращают её сухость. Кремы могут содержать мочевину 20 % или 40 %, 12 % лактата аммония, 6 % салициловой кислоты и 12 % молочной кислоты. Любой из них применяют до двух раз в день.

Приём наружных гормональных препаратов (стероидов) не требуется, так как воспаление отсутствует.
В некоторых исследованиях упоминается использование фотохимиотерапии с псораленом и ультрафиолетовым светом (PUVA), но только при тяжёлых случаях, так как риски этой терапии превышают пользу [9] .
PUVA-терапия заключается в приёме пациентом фотоактивного материала псоралена с последующим воздействием на кожу UVA лучей. Данных, подтверждающих пользу фототерапии при эксфолиативном кератолизе, на сегодняшний день недостаточно.
Возможные побочные эффекты PUVA-терапии: покраснение кожи вплоть образования пузырей, зуд; к редкими побочными эффектам относятся головная боль, головокружение, учащённое сердцебиение и слабость [4] .
Также в литературе встречаются данные о лечении эксфолиативного кератолиза ацитретином [7] [14] . Но для рутинного применения ацитретина в качестве лечения кератолиза информации пока недостаточно. Ацитретин — это производное витамина А, которым лечат псориаз.
Прогноз. Профилактика
Прогноз благоприятный. Обычно симптомы эксфолиативного кератолиза проходят самостоятельно или после прекращения контакта с провоцирующим фактором. Спустя несколько недель или месяцев формируется здоровая кожа. Однако через несколько недель может возникнуть рецидив.
Иногда кератолиз приобретает хронический характер и длится много лет подряд. В таком случае заболевание трудно поддаётся лечению. С возрастом эксфолиативный кератолиз возникает реже [2] .
Меры профилактики:
- избегать веществ, которые способствуют шелушению, например растворителей, антибактериального мыла и некоторых тканей;
- соблюдать гигиену рук и ног с частой стрижкой ногтей — это поможет избежать вторичного инфицирования;
- использовать перчатки при контакте с химическими веществами;
- наносить увлажняющие кремы для рук, особенно полезны кремы, содержащие мочевину, молочную кислоту или силикон.

Роль продуктов питания в развитии эксфолиативного кератолиза не доказана, поэтому соблюдать диету не нужно.
Читайте также:

