Что такое лечение рака печени уколами под кожу
Обновлено: 01.05.2024
Выбор метода лечения обусловлен размерами и локализацией первичной опухоли, наличием метастазов в печени и других органах, состоянием ткани печени и самого пациента. Поэтому терапия подразделяется на две линии: при наличии цирроза печени и при отсутствии цирроза.
Профилактической терапии, способной снизить риск рецидива печёночно-клеточного рака и продлить жизнь, к сожалению, не существует.
Хирургическое лечение рака печени
Даже при современном развитии медицины без хирургического воздействия невозможно вылечить злокачественную опухоль, и рак печени не исключение.
Операцию делают невозможной:
- метастазы в печень;
- метастазы в другие органы и ткани;
- низкие функциональные возможности печени и почек;
- тромбоз воротной вены.
Объём вмешательства зависим от распространения поражения печени. Без сопутствующего цирроза при раннем раке – небольшой опухоли до 5 см – методом выбора считается резекция печени.
При вовлечении в опухоль участков обеих долей печени на стороне максимального поражения выполняется гемигепатэктомия, в доле с меньшим повреждением предпочтительно локальное воздействие: экономная резекция, радиочастотная аблация или криодеструкция.
Большой объём опухоли на фоне цирроза поставит вопрос о трансплантации печени. При ожидании трансплантации возможно локальное воздействие на опухоль, в том числе аблация, эмболизация и парциальная резекция печени.

При единственной опухоли или единичных узлах опухоли не более 3 см, не подлежащих оперативному лечению, выполняют локальную деструкцию: радиочастотную или микроволновую аблацию, криодеструкцию.
Радиочастотная аблация печени (РЧА)
Предпочтительным и наиболее часто используемым методом считается радиочастотная аблация. Этот вариант термической деструкции применяется при:
- раннем гепатоцеллюлярном раке до 3 см;
- рецидиве опухоли;
- с паллиативной целью при узле до 5 см;
- единичных опухолевых узлах, числом не более 5.
Противопоказания почти такие же, как и для хирургического вмешательства, но менее жёсткие: отдалённые метастазы, декомпенсированный цирроз печени, не купируемый асцит, энцефалопатия, наличие кардиостимулятора, выраженные нарушение свёртываемости крови и активное желудочное кровотечение, и конечно, прилежание опухоли к другим органам и крупным желчным протокам.
Наилучший результат достигается при небольших опухолях, особенно, при возможности термического воздействия на окружающую ткань, хорошем доступе к узлу во время РЧА. Лечение эффективно, когда удаётся добиться 100% некроза опухоли. Пятилетняя выживаемость пациентов с компенсированным циррозом и ГЦР менее 5 см в диаметре достигает 60%.
Вероятность осложнений есть, но она менее 10%, главное – они не фатальны для больного и устранимы. Нередко РЧА комбинируют с другими методами локального воздействия, в частности, с трансартериальной химиоэмболизацией.
Выполняется также микроволновая аблация – манипуляция аналогична РЧА, но с другой частотой волны. Показания и противопоказания схожи.
Криодеструкция опухоли
Криодеструкция – прямое воздействие жидкого азота, охлаждающего ткани до температуры минус 180°С. Непосредственное охлаждение опухоли с помощью специального устройства вызывает гибель клеток, а в окружении опухоли формируются микрососудистые тромбы, которые усугубляют повреждение за счёт дополнительного нарушения её питания.
Во время манипуляции, которую могут выполнять через кожу или во время операции, к опухоли подводится специальный аппликатор, охлаждаемый до минус 180°С. Криодеструкция позволяет лечить опухоли больших размеров.

О комплексном подходе в лечении рака печени рассказывают врачи «Евроонко».
Трансартериальная химиоэмболизация (ТАХЭ)
Химиоэмболизация – ведущий метод локорегиональной терапии ГЦР, применяемый в первой линии паллиативной терапии не подлежащего операции опухолевого процесса без признаков вовлечения сосудов и внепечёночных проявлений заболевания – метастазов.
По установленному в процессе ангиографии катетеру в питающую опухоль артерию вводится рентген-контрастное вещество с химиопрепаратом, жировой эмульсией или микросферами. Из химиопрепаратов чаще всего используют доксорубицин и митомицин, нередко их комбинацию, обязательно с жировой эмульсией липиодол. Это называется «масляная» химиоэмболизация. Если к этой смеси добавить микросферы ПВА, то ТАХЭ уже станет «комбинированной».
Самая современная доставка химиопрепарата осуществляется биосовместимыми нерезорбируемыми полимерными микросферами, элиминирующими цитостатик или проще DEB. Эти микросферы состоят из поливинилового спирта, который способен не только связываться с доксорубицином, но и «отпускать» его в опухоли для лечения. Из акриламида созданы суперабсорбирующие полимерные микросферы, тоже хорошо взаимодействующие с доксорубицином.
Наилучший эффект ТАХЭ достигается при невыраженном циррозе и сохранной функцией печени, но при тромбозе воротной вены и выраженном циррозе эмболизация не выполняется.
Микросферы блокируют кровоток в питающих опухоль сосудах, не вовлекая крупных ветвей печёночной артерии, поэтому оказывают максимальный терапевтический эффект при минимизации нежелательных последствий эмболии.
Трансартериальная радиоэмболизация (ТАРЭ)
Почти аналогичная ТАХЭ манипуляция, но на поверхности микросфер располагается радиоактивный изотоп иттрия-90. При ТАРЭ эмболизирующее действие микросфер сочетается с локальным облучением опухоли печени.
Лучевая терапия рака печени в клинической практике, вне научных исследований, почти не применяется
Химиотерапия при раке печени
Современные возможности лекарственной терапии рака печени ограничены, поскольку опухоль устойчива к цитостатикам. Как правило, химиотерапия печени используется при противопоказаниях к локальным методам воздействия, метастазах внепечёночной локализации и при прогрессировании после локального воздействия.
Основная цель лечения – увеличение продолжительности жизни, а достоверно её увеличивает только сорафениб. Иные химиопрепараты и их комбинации демонстрируют эффективность в 20% случаев, но не влияют на длительность жизни больных.
При циррозе печени переносимость химиотерапии ухудшается, что ограничивает возможности активного лечения. При хроническом гепатите В или носительстве вируса к химиотерапии присоединяют противовирусные препараты. Но при хроническом гепатите С нет нужды в противовирусной терапии, зато вероятность гепатотоксичности и развития лекарственного гепатита очень высоки, поэтому проводят их профилактику. В рекомендациях отмечена неэффективность эссенциальных фосфолипидов – широко распространённого в России Эссенциале.
В научной литературе не доказали, что применение аналогов соматостатина увеличивает продолжительности жизни, но на нём могут регистрировать уменьшение опухоли. Интерферон-2α в стандартных дозах бесполезен, но оказывает небольшой эффект в сочетании с химиотерапией.
При наличии противопоказаний к химиотерапии при раке печени мы проводим симптоматическую терапию, направленная на повышение качества жизни и улучшение самочувствия пациента.
Лечение рака печени, несмотря на видимую простоту доступа для диагностики и радикального лечения (хирургии либо воздействия ионизирующим излучением) - сложная задача, требующая применения самых современных методик и оборудования. О том, как обеспечить эффективное и безопасное лечение рака печени на уровне мировых стандартов, как минимум, 2018 года, рассказывает сайт МИБС.
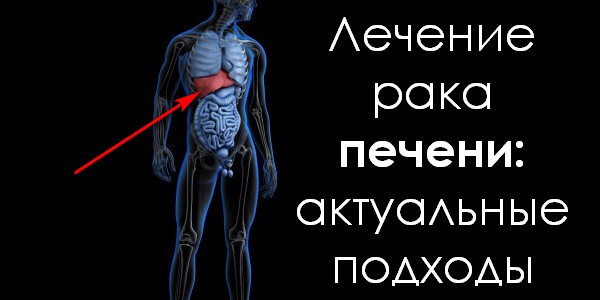
Для понимания важности, которую имеет лечение рака печени в масштабе человечества, следует привести статистику. По данным 2017 года, в мире чаще всего диагностируются такие виды рака:
- рак легких - 11,6%
- рак груди - 11,6%
- колоректальный рак - 10,2%
- рак простаты - 7,1%
- рак желудка - 5,7%
- рак печени - 4,7%
Таким образом на рак печени приходится почти каждый двадцатый случай рака на земле. Но еще более важен показатель смертности.
Наибольшее количество смертей вызвано такими видами рака:
- рак легких - 18,4%
- колоректальный рак - 9,2%
- рак желудка - 8,2%
- рак печени - 8,2%
- рак молочной железы - 6,6%
Статистика показывает, что рак печени делит с раком желудка третье место в списке самых смертельных онкологических заболеваний. И лишь немного (не более одного процента!) уступает колоректальному раку, идущему вторым в этой печальной таблице “рекордов”.
При этом рак желудка, который принято считать одним из самых сложных в лечении видов онкологических заболеваний, встречается чаще. А значит лечение рака печени, демонстрирующего большую агрессивность, - задача не менее ответственная.
Что такое рак печени?
Рак печени - это первичная опухоль, растущая из малигнизированных (трансформировавшихся в злокачественные) клеток органа. Растущая из гепатоцитов гепатоцеллюлярная карцинома - самая распространенная первичная злокачественная опухоль печени. На ее долю приходится 4 из 5 всех случаев рака печени. Второй по частоте тип злокачественных новообразований печени, холангиокарцинома (рак желчного протока или опухоль Клацкина), в разы уступает по частоте выявления. Остальные злокачественные опухоли, растущие в печени из различных типов клеток, присутствующих в органе - опухоли сосудистого происхождения (ангиопластическая саркома печени или ангиосаркома, гемангиосаркома), а также гепатобластома (опухоль из эмбриональных клеток) - диагностируются еще реже.
С точки зрения биологии, только гепатоцеллюлярная карцинома является раком печени. Но, с точки зрения лечения опухолей печени, любые новообразования, растущие в пределах органа, можно рассматривать в качестве рака печени. Это упрощает пониманием пациентом тактики предстоящей терапии.
Первичные раки печени чаще всего возникают из-за паразитарных, инфекционных и химических поражений. Лидирующие позиции среди причин первичного рака печени принадлежат Гепатиту Б и С, а также папилломавирусу человека - до 86% всех случаев гепатоцеллюлярной карциномы. Исследования доказали связь этих вирусных заболеваний с повышенным риском риск развития рака печени и рака шейки матки.
Метастатический рак печени (метастазы в печень)
Диагностика рака печени
Как и в случае любого онкологического заболевания, лечение рака печени более эффективно на ранних стадиях. Поэтому ранняя диагностика - не менее важная задача, чем комплексная терапия.
Осложняет задачу то, что симптомы рака печени не отличаются уникальностью. Утомляемость, тошнота, тяжесть в правом подреберье, даже механическая желтуха (пожелтение склер и кожных покровов вследствие сдавливания желчных путей растущей опухолью или нарушения функций печени) - такая симптоматика присуща практически всем нарушениям работы органа. Тем более у пациентов с хроническим гепатитом или циррозом печени.
Тем не менее, при своевременном обращении выявить рак печени несложно. Как и при любых нарушениях работы органа базовый метод диагностики – недорогое и доступное в большинстве лечебных учреждений ультразвуковое исследование (УЗИ), которое с высокой степенью достоверности определит наличие, положение и размеры новообразования в печени, вызывающее симптомы, с которыми пациент обратился к врачу.
Подтвердить диагноз поможет биопсия новообразование. Морфологическая диагностика взятого образца покажет тип клеток, из которых состоит опухоль. Это позволит определить, является ли новообразование первичным раком, или речь идет о метастатическом поражении и пациенту предстоит лечение распространенного процесса. А иммуногистохимия даст ответ о возможности проведения таргетной терапии, основанной на специфической уязвимости конкретной опухоли к одному из таргетных препаратов, или иммунотерапии.
Но почему тогда рак печени демонстрирует настолько высокую смертность? Ответ прост: схема “симптомы - первичное обращение - диагностика - установление диагноза” описывает большинство клинических случаев. Но проявление симптоматики означает значительный размер новообразования. Соответственно, лечение рака печени будет более сложным, кроме того высока вероятность метастазирования.
Специальные скрининговые исследования на предмет выявления рака печени не проводятся. Однако обычное внимание к своему здоровью, заключающееся в регулярном (1-2 раза в год) прохождении профилактических исследований, в состав которых входит УЗИ органов брюшной полости и анализ крови для определения “работоспособности" печени (так называемые, “печеночные пробы") позволит выявить возможный опухолевый процесс на тех стадиях, когда лечение рака печени будет эффективным.
У пациентов с циррозом печени, гепатитом В или С вероятность развития злокачественной опухоли печени во много раз выше. Им рекомендовано включать в состав регулярного обследования анализ крови на уровень альфа-фетопротеина - уровень АФП значительно повышается при гепатоцеллюлярной карциноме, метастазах в печень, что дает возможность использовать альфа-фетопротеин, как онкомаркер рака печени.
Ранняя диагностика метастазов в печень может быть эффективной при соблюдении качества лечения первичной опухоли в части онконастороженности врача и пациента - наблюдению за возможными органами-мишенями. Например, лечение колоректального рака должно обязательно включать регулярный контроль состояния печени, в которую заболевание метастазирует в 20% случаев.
Лечение рака печени
Наибольший эффект позволяет достичь тактика, включающая хирургическое удаление первичной опухоли и химиотерапию. Такое сочетание наиболее востребовано, учитывая невысокую статистику раннего выявления рака печени
Ожидаемую эффективность определяет успешность хирургического вмешательства, которая значительно зависит от подготовки хирурга и технического обеспечения клиники, в частности, позволяющего проводить малоинвазивные лапароскопические резекции печени. Именно лапароскопическая хирургия – основа комплексного лечения рака печени в Онкологической клинике МИБС.
Химиотерапия призвана закрепить эффект, воздействуя на те опухолевые клетки, которые из-за высокого риска для жизни невозможно будет удалить во время хирургического вмешательства, а также возможные метастазы рака печени, которые невозможно выявить ввиду их малого размера.
Таргетное лечение рака печени
С развитием возможностей иммуногистохимии, выявляющей потенциальную генетическую уязвимость конкретной опухоли, воздействие на которую одним из препаратов позволяет остановить рост исключительно данного типа клеток, открывает новые возможности для лечения онкологических заболеваний в целом и рака печени в частности.
Иммуногистохимия опухолей пациентов Онкологической клиники МИБС проводится в собственной лаборатории, работающей по самым высоким международным стандартам.
В таргетной терапии злокачественных новообразований печени наибольших успехов наука достигла в лечении печеночноклеточного рака (гепатоцеллюлярной карциномы). Кроме того, таргетная терапия может быть успешной при метастатическом поражении печени, источник которого – рак легких, рак молочной железы и др. Это дает новые шансы пациентам на поздних стадиях рака.
Локальные методы лекарственного лечения рака печени
В отличие от химиотерапии и таргетного лечения, оказывающих системное воздействие на весь организм, при раке печени могут применяться малоинвазивные методы локального воздействия на опухоли, при которых используется доступ через крупные кровеносные сосуды, относящиеся к методам эндоваскулярной (внутрисосудистой) хирургии и интервенционной радиологии.
И химиоэмболизация, и радиоэмболизация в основе своей используют принцип закрытия просвета кровеносных сосудов, питающих крупные опухоли, специальным веществом, вводимым непосредственно в эти сосуды через катетер. Отличия лишь в свойствах “пломбирующего” препарата - при химиоэмболизации внутри опухоли остаются частицы препарата химиотерапии высокой дозы, при радиоэмболизации внутрь опухоли помещается радиоактивное вещество с коротким сроком активности. В каждом из случаев опухоль впитывает губительное для нее “лекарство”, попадание которого в общую систему кровообращения исключено.
Менее широкое распространение в мировой практике получило лечение рака печени другими радикальными методами (радиочастотная абляция, термическая абляция).
Несмотря на то, что трансплантация печени в открытых источниках упоминается, как возможный вариант при раке печени, на практике этот метод используется крайне редко. Как ввиду высокой дороговизны и сложности такой операции, так и ввиду низкого показатели раннего выявления опухолей печени (при значительном размере новообразования, особенно локализованного вблизи крупных кровеносных сосудов, трансплантация, учитывая высокую вероятность метастазирования, - бесперспективна).
Лучевое лечение рака печени
Клетки печени имеют слабую устойчивость к воздействию ионизирующего излучения. Но это касается не только малигнизированных клеток печени, но и всего органа, что делает применение лучевого лечения практически невозможным. Протонная терапия – исключение. В отличие от фотонной лучевой терапии, при которой пучки фотонов буквально пронизывают организм, облучая практически равной дозой ткани на траектории от входа до выхода из тела человека, фотоны действуют точнее. В основе лечения протонами лежит свойство этих элементарных частиц отдавать максимум энергии на коротком финальном участке своего пробега. Управляя энергией пучка протонов и его траекторией, врач получает возможность произвести буквально “укол радиации” в четко указанную точку, находящуюся в границах опухоли.
Наиболее совершенная на сегодня технология PBS (“pencil beam scanning” или “сканирование карандашным пучком”), доступная пациентам Центра протонной терапии МИБС, позволяет последовательно подать множество пучков на разную глубину и в разные точки организма, буквально “заштриховывая” опухоль высокой дозой радиации.
Лечение метастатического рака печени
Как правило, еще более тяжелая задача, чем лечение первичного рака печени. При выборе метода терапии следует учесть ранее полученное или назначенное лечение первичной опухоли, а также проводимое или ожидаемое системное воздействие при химиотерапии или таргетном лечении. Учитывая, что метастазы в печени - прогнозируемое явление при ряде онкозаболеваний, дополнительный шанс получают высокоточные лучевые методы лечения. При единичных некрупных новообразованиях хорошего эффекта можно достичь, применяя радиохирургию с тщательным распределением пучков для защиты здоровых тканей печени. Инвазивность радиохирургии - минимальна, что позволяет провести лечение у пациентов в тяжелом общем состоянии.
Паллиативное лечение рака печени
В тех случаях, когда рак выявлен на поздней стадии, прогноз, как правило, неблагоприятный. И перед врачом уже предстоит задача не победить опухоль, а продлить жизнь пациента с раком печени, обеспечив максимально возможное сохранение ее уровня. В качестве паллиативного лечения при раке печени широко используется шунтирование или стентирование желчных путей (особенно при холангиокарциноме), восстанавливающее их проходимость. В некоторых случаях эффект будет от проведения лучевой терапии, также применяется химиотерапия.
В заключение хочется отметить: несмотря на уникальность каждого клинического случая, лечение рака печени - крайне вариативно. Поэтому, для максимального эффекта от лечения, важно обращаться в медицинские центры, которые имеют в своем арсенале возможности для подбора методов диагностики и терапии согласно потребностям пациента, а не техническому обеспечению клиники. Лишь в таком случае можно говорить о более высоких шансах на победу над опухолью либо на максимально возможное продление жизни.
Именно так действует МИБС. Онкологическая клиника МИБС – это комплексная помощь при любом виде опухолей. Все этапы лечения в МИБС – от первичной диагностики до регулярного контроля после лечения, от хирургии до протонной терапии, – проводятся в соответствии с высокими международными стандартами. Звоните сейчас!

Михайлов Алексей Валерьевич
Кандидат медицинских наук, врач-радиотерапевт, заведующий отделением лучевой терапии
Рак печени подразделяется на первичный и вторичный (метастатический). Первичный, о котором пойдет речь в данной статье, представляет собой сравнительно редкое заболевание. К нему относятся по разным данным от 0,2% до 3% случаев диагностированного рака. Ежегодно в мире раком печени заболевают не менее 250 тысяч человек, большая часть которых проживает в развивающихся странах Африки и Юго-Восточной Азии. В России первичный рак печени ежегодно диагностируется примерно у 7 тысяч пациентов. Но количество выявленных заболевших быстро растет. За три последних десятилетия, с середины 1980-х годов, заболеваемость раком печени в России выросла втрое - с 1,6 до 4,6 случаев на 100 тыс. населения.
Что такое рак печени?
Печень является самым большим органом в теле человека, имеет пирамидальную форму и располагается в правом подреберье. Она разделена на два отдела, называемые долями. В отличие от большинства органов, имеет два источника кровоснабжения: печеночная артерия несет кровь, богатую кислородом, а воротная вена снабжает печень кровью, насыщенную питательными веществами из кишечника.
Печень - жизненно важный орган, без которого организм не может функционировать. Она расщепляет и хранит питательные вещества, поступающие из кишечника; производит желчь, необходимую для правильного пищеварения; играет важную роль в обеспечении свертываемости крови; помогает выводить отработанные вещества.
От 60% до 80% массы печени человека составляют гепатоциты – клетки, участвующие в синтезе и хранении белков, холестерина, играющие важную роль в трансформации углеводов, желчеобразовании, а также – в детоксикации и выводе из организма образующихся в нем субстанций.
Виды рака печени
Основными типами первичного рака являются:
Гепатоклеточная карцинома - результат злокачественного перерождения гепатоцитов. Наиболее часто встречающийся вид первичного рака печени: по разным данным, к ней относятся от 70% до 90% выявленных онкологических заболеваний данного органа. Карциномы образуются либо как одна опухоль, либо сразу в нескольких местах. Второй случай является превалирующим, он наиболее часто диагностируется у людей с повреждениями печени, такими как цирроз.
Фиброламеллярная карцинома – редкий подтип гепатоклеточной карциномы, который имеет более высокие шансы на успешное лечение, чем другие типы рака печени. Данная опухоль встречается редко, в основном - у детей и лиц моложе 35 лет. Она поражает небольшие участки ткани, не распространяясь на весь орган.
Рак желчевыводящих путей (внутрипеченочная холангиокарцинома). Один или два из каждых десяти диагностированных случаев рака печени начинаются в желчевыводящих путях, которые представляют собой тонкие трубки, переносящие желчь к желчному пузырю.
Гепатохолангиоцеллюлярная карцинома - тип первичного рака, совмещающий признаки как гепатокарциномы, так и холангиокарциномы. У некоторых больных могут одновременно развиться оба типа рака.
Цистаденокарцинома - редкая опухоль, которая диагностируется у взрослых, преимущественно у женщин, вследствие малигнизации доброкачественной цистаденомы или даже врожденной кисты. Имеет большие размеры, поликистозное строение, чаще локализуется в правой доле печени, содержит окрашенную желчью слизь.
Ангиосаркомы и гемангиомы начинаются в кровеносных сосудах в печени. Эти быстрорастущие опухоли обычно диагностируются на поздних стадиях.
Гепатобластома - очень редкий тип рака печени. Наиболее часто встречается у детей младше 4 лет. Крайне редко диагностируется у детей более старшего возраста и у взрослых пациентов. При ранней диагностике процент выживаемости составляет более 90%.
Причины и группы риска
Статистически достоверно доказано, что развитию рака печени способствуют следующие факторы:
Хронические заболевания. В первую очередь - вирусный гепатит В. Риск возникновения печеночноклеточного рака у носителей вируса возрастает в 200 раз.
К другим болезням, приводящим к раку данного органа, относятся цирроз печени,
гемохроматоз (избыточное содержание в организме железа), желчнокаменная болезнь, сахарный диабет, паразитарное заражение, а также сифилис и алкоголизм.
Воздействие вредных веществ. Работа на производствах, связанных с использованием мышьяка, ртути, хлорид винила может пагубно сказаться на состоянии печени. Развитие новообразований в этом органе связывают также с использованием некоторых промышленных продуктов, к примеру, хлорированных углеводородных растворителей. Небезобидны для печени некоторые пищевые продукты, такие, как арахис, соевые бобы, кукуруза, порой содержащие афлатоксины. Бездумное употребление некоторых витаминов, БАДов, оральных контрацептивов, анаболических стероидов также могут спровоцировать появление недоброкачественных новообразований в данном органе.
Наследственность. Наличие среди кровных родственников двух и более человек, заболевших раком печени, автоматически включает человека в группу риска.
Пол. Мужчины гораздо в большей степени рискуют заболеть раком печени, чем женщины. Возможно, причина в большей приверженности вредным привычкам – употреблению спиртного и курению, а также в потреблении стероидов.
Симптомы
На ранних стадиях первичного рака печени симптомы отсутствуют. А если они и есть, то варьируются от человека к человеку. С ростом опухоли могут появиться:
- потеря веса;
- боль в правом боку верхнего отдела брюшной полости или под правой лопаткой
- потеря аппетита;
- вздутие брюшной полости;
- твердое уплотнение под ребрами с правой стороны;
- усталость или слабость;
- тошнота или рвота;
- жар;
- желтизна кожи и глаз, а также потемнение мочи;
- чувство переедания после приема небольшого количества пищи;
- зуд;
- вспухшие вены на животе;
- ухудшение состояния при хроническом гепатите или циррозе.
Некоторые типы рака печени производят гормоны, которые могут вызывать:
- высокий уровень кальция в крови, провоцирующий запоры, тошноту или дезориентацию;
- низкий уровень сахара в крови, который может вызывать усталость или обморочные состояния;
- увеличение груди или уменьшение размера яичек у мужчин;
- высокое количество красных кровяных телец, которые становится причиной покраснения лица.
Стадии заболевания
Рак печени подразделяется на стадии в зависимости от размера и локализации опухоли.
I стадия. Единичная опухоль, которая не распространилась на близлежащие кровяные сосуды.
II стадия. К этой стадии относят один из двух вариантов проявления болезни:
- одна опухоль, которая распространилась на близлежащие кровяные сосуды;
- более одной опухоли, не превышающих 5 см в большем измерении каждая.
Стадия III А. К этой стадии относят один из двух вариантов проявления болезни:
- более одной опухоли размером больше 5 сантиметров;
- одна опухоль, которая распространилась на одну из основных ветвей кровяных сосудов рядом с печенью.
Стадия IIIB. В наличии одна или более опухолей любого размера, которые:
- распространились на близлежащие органы, за исключением желчного пузыря;
- прошла через оболочку брюшной полости.
Стадия IIIC. Рак распространился на близлежащие лимфатические узлы.
Стадия IV. Рак печени распространился за пределы органа на другие части тела, такие как кости или легкие. Опухоли любого размера также могут быть распространены на близлежащие кровяные сосуды и/или лимфатические узлы.
Диагностика
Рак печени трудно диагностировать. На ранних стадиях он обычно не имеет симптомов и опухоли не прощупываются. Если у врача возникает подозрение на рак печени, то диагностика проводится в следующем порядке:
Физический осмотр. Врач прощупывает живот пациента для проверки печени, селезенки и близлежащих органов; проверяет живот на асциты – аномальное скопление жидкости; обследует кожу и глаза, выявляя признаки желтухи.
Лабораторные исследования. Обычный анализ крови обнаруживает альфа-фетопротеин, который может являться признаком рака печени. Другие анализы крови могут измерить, насколько хорошо работает ваша печень.
Ультразвуковое исследование. Современные аппараты УЗИ позволяют выявить рак печени на ранних стадиях.
Магнитно-резонансная томография (МРТ). Благодаря высокой разрешающей способности высокопольных (1,5Т) и сверхвысокопольных (3Т) магнитно-резонансных томографов, дополнительным уникальным программам с очень тонкими срезами в ходе исследования можно увидеть изменения структуры печени размером до нескольких миллиметров, выявить патологические процессы на их начальной стадии, а также провести дифференциальную диагностику патологических образований. При наличии объемных опухолей врач может назначить МРТ с контрастным болюсным усилением. Контрастное усиление - методика которая заключается во внутривенном введении контрастного вещества в зависимости от веса пациента. Она позволяет оценить степень кровоснабжения опухоли и судить о доброкачественном или злокачественном характере.
Если в ходе основного МР исследования органов брюшной полости и забрюшинного пространства выявлено наличие объемных образований в печени, то проводится динамическое контрастирование – методика, которая позволяет оценить степень кровоснабжения опухоли и судить о доброкачественном или злокачественном ее характере.
Компьютерная томография (КТ). Рентгеновское послойное исследование органов брюшной полости и забрюшинного пространства. Выполняется как без контраста, так и с болюсным контрастированием, то есть - с внутривенным введением рентгеноконтрастного препарата при помощи специального автоматического шприца. Стандартное КТ исследование позволяет выявить патологические изменения в печени. КТ с контрастным усилением применяется для исключения врастания опухолей в сосуды; при стадировании опухолевой патологии; для выявления показаний и противопоказаний к хирургическим вмешательствам или лучевой терапии.
Ангиограмма. Врач вводит краситель в артерию, что позволяет видеть кровяные сосуды в печени в рентгеновских лучах.
Лапароскопия. Делается небольшой надрез на животе и затем вводится тонкая трубка с подсветкой (лапароскоп) для осмотра опухоли.
Биопсия печени. Биопсия и тонкоигольная аспирационная биопсия используются тогда, когда визуальные исследования не могут определить характер новообразования. В орган вводится длинная игла для забора крошечного образца ткани, который изучают под микроскопом.
Фьюжен биопсия. Современное направление в методике забора материала для гистологического анализа, сочетающее возможности магнитно-резонансной или компьютерной томографии и ультразвуковой диагностики. Перед проколом выполняется исследование на аппаратах КТ или МРТ. Основываясь на его результатах, врач планирует место прокола, рассчитывает ход биопсийной иглы и глубину проникновения. Сама биопсия проводится под контролем УЗИ. Метод обеспечивает максимальную точность попадания в пораженный участок.
Лечение
Хирургическая операция. Хирургия является основным способом лечения рака печени. Так как печень играет важную роль в свертывании крови, кровотечение после вмешательства является частым побочным эффектом. Основными типами хирургических операций при раке печени являются:
- пересадка печени. Пораженная заболеванием печень полностью удаляется и заменяется здоровым органом от донора. При циррозе печени или больших размерах опухоли является наиболее вероятным методом лечения. Однако имеется риск серьезной инфекции и других проблем со здоровьем;
- частичная гепатэктомия. Часть печени с раковыми клетками удаляется хирургическим путем. Операция требует особой виртуозности от хирурга: он должен тщательно удалить все поврежденные ткани, чтобы вылечить рак, и в тоже время - оставить достаточный объем печени для ее нормальной работы.
Абляция опухоли. Местное лечение, при котором тепло (радиочастотная абляция) или сверхнизкий холод (криохирургия или криотерапия) используются для заморозки или выжигания рака печени. Абляция показана в тех случаях, когда удаление опухоли хирургическим путем невозможно.
Эмболизация. Мельчайшие частицы из пластика или другого материала вводятся в артерии, которые несут кровь к опухоли. Они блокируют поток крови, что сдерживает рост рака печени.
Химиотерапия. Обычно не используется для лечения рака печени из-за малой эффективности.
Химиоэмболизация. Игла вводится в артерию в паху, а затем тонкая трубка ввинчивается в артерию, ведущую к печени. После этого к раковым клеткам подается высокая доза лекарства. Затем артерия блокируется, чтобы предотвратить снабжение печени кровью и дальнейшее развитие рака.
Лучевая терапия. Так как радиация вместе с раковыми клетками может разрушить и здоровые ткани печени, она применяется только в малых дозах. Лучевая терапия не излечивает рак печени, но она способна уменьшить опухоль и облегчить боль.
Помимо облучения на обычных линейных ускорителях, лечение на которых может занять 2-3 месяца, в Центре онкологии, радиохирургии и радиотерапии МИБС применяют так называемую конформную лучевую терапию. При этом современном подходе конфигурация облучающего пучка и интенсивность излучения скрупулезно рассчитываются с помощью специальных программ. Это позволяет добиться точного соответствия распределения дозы радиации форме новообразования, подать на мишень – в центр опухоли – максимально высокую дозу облучения, одновременно щадя периферийные нормальные ткани.
Лечение на аппарате Кибер-нож. Ткань печени обладает высокой чувствительностью к лучевому воздействию, что ограничивает применение стандартной лучевой терапии. Роботизированная радиохирургическая система Кибер-нож способна сфокусировать максимальную дозу облучения непосредственно на опухоли, в то же время сохраняя здоровую ткань печени.
Система Кибер-нож может применяться как при лечении первичного рака печени, так и в терапии очагов метастатического поражения (если химиотерапия неэффективна или если очаг слишком велик для иных методов локального воздействия, например, радиочастотной абляции). Возможно одномоментное облучение нескольких очагов поражения.
Протонная терапия. Пучок протонов доставляет высокие дозы радиации с большой точностью прямо в область локализации рака печени. Этот современный метод лучевой терапии уничтожает раковые клетки, минимально задевая нормальную ткань за пределами опухоли.
Решение о выборе тактики лечения конкретного пациента в МИБС принимается коллегиально врачами клинических и диагностических специальностей. На каждом этапе составляется индивидуальный план дальнейшего наблюдения и контроля эффекта, включающий все самые информативные диагностические методы, применяющиеся сегодня в ведущих онкологических центрах Европы и США.
Химиотерапия — один из основных методов лечения (два других — хирургия и лучевая терапия) онкологических заболеваний. Химиопрепараты повреждают раковые клетки таким образом, что те больше не могут размножаться и погибают.
Разные опухоли отвечают на химиотерапию по-разному. Одни поддаются лечению хорошо, другие практически не реагируют на него. Рак печени относится ко второй категории. Для системной химиотерапии (такой, когда препарат вводят внутривенно или принимают в виде таблеток) можно использовать лишь немногие химиопрепараты: цисплатин, 5-фторурацил, адриамицин (доксорубицин), но и они эффективны далеко не у всех пациентов, опухоли печени быстро вырабатывают по отношению к ним устойчивость.
Однако, при раке печени могут быть эффективны некоторые методы местной химиотерапии.
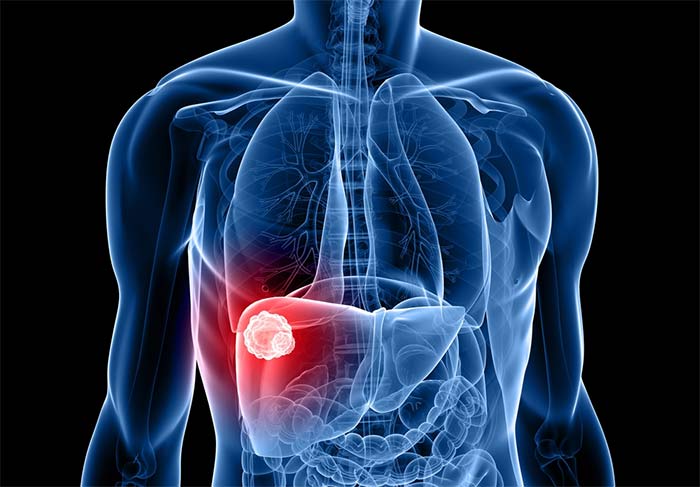
Местная химиотерапия при раке печени
Местной называют такую химиотерапию, при которой препарат вводят непосредственно в опухолевую ткань, в общий кровоток он практически не попадает. Для этого прибегают к специальным процедурам. При раке печени применяют интраартериальную химиотерапию и химиоэмболизацию.
Интраартериальная химиотерапия
Одна из функций печени состоит в том, что она разрушает токсичные вещества. С этим связана главная проблема химиотерапии при раке печени. Химиопрепараты не успевают достичь опухолевой ткани и оказать свои эффекты, так как их захватывают и разрушают печеночные клетки — гепатоциты. Решением могло бы стать увеличение дозировок, но при системной химиотерапии это приводит к тяжелым побочным эффектам.
При интраартериальной химиотерапии препарат вводят непосредственно в печеночную артерию. Он попадает только в печеночную ткань и не разносится по всему организму. Благодаря этому можно сильно увеличить дозу, не боясь нежелательных эффектов.
Чаще всего для интраартериальной химиотерапии при раке печени применяют такие препараты, как доксорубицин, митомицин С, цисплатин, флоксуридин.
Данный вид местной химиотерапии показывает достаточно высокую эффективность, но и он применим не у всех пациентов. Для того чтобы ввести химиопрепарат в печеночную артерию, в нее нужно вставить катетер, а для этого требуется хирургическое вмешательство. Не все больные в состоянии перенести операцию.
Химиоэмболизация
Печень — орган, который получает двойное кровоснабжение. Гепатоциты кровоснабжаются из воротной вены. Она собирает кровь от кишечника и несет в печень вещества, которые всасываются в пищеварительном тракте. Раковые клетки кровоснабжаются из печеночной артерии. Логична идея каким-либо образом заблокировать кровоток в печеночной артерии. Благодаря этому раковые клетки перестали бы получать кровь, кислород и питательные вещества. При этом гепатоциты продолжили бы кровоснабжаться, как прежде.
И такой метод существует. Называется он эмболизацией. В печеночную артерию вводят через катетер специальный эмболизирующий препарат, который содержит микросферы. Они перекрывают просвет сосудов. Модификация метода — химиоэмболизация, когда микросферы несут химиопрепарат. Таким образом, опухолевые клетки получают двойной удар.
Химиоэмболизацию проводят с помощью специального катетера, который вводят в бедренную артерию через надрез в паху. В сосуды вводят рентгеноконтрастный раствор, катетер под контролем рентгена проводят в печеночную артерию, и как только его кончик оказывается в нужном месте, вводят препарат.
Однако, и здесь не все так просто. Если заблокировать кровоток в печеночной артерии, часть здоровой ткани печени все же лишится притока крови. Из-за этого процедура может быть проведена не у всех пациентов.

Таргетная терапия при раке печени
Нормальные клетки становятся раковыми из-за изменений в их генах. Генетические нарушения приводят к тому, что некоторые молекулы начинают работать неправильно, они помогают опухолевым клеткам становиться бессмертными и бесконтрольно размножаться. С развитием молекулярной биологии и молекулярной генетики ученые смогли идентифицировать многие из этих веществ и понять, как их можно заблокировать. Это привело к созданию нового класса лекарств — таргетных препаратов.
При раке печени применяют следующие таргетные препараты:
- Сорафениб блокирует рост новых сосудов, которые опухоль «выращивает», чтобы обеспечить себя кислородом и питательными веществами. Также он блокирует белки-рецепторы на поверхности раковых клеток, которые активируют их размножение. Препарат принимают в виде таблеток 2 раза в день.
- Регорафениб работает похожим образом. Обычно его назначают, если неэффективен сорафениб. Препарат принимают в таблетках 1 раз в день в течение 3 недель, после чего делают перерыв.
За счет прицельного воздействия на опухолевые клетки, таргетные препараты вызывают меньше побочных эффектов по сравнению с химиопрепаратами.
Иммунотерапия при раке печени
Несколько десятилетий назад ученые выдвинули концепцию, согласно которой в ДНК клеток организма регулярно возникают поломки, и некоторые из них могут превратить клетку в раковую, поэтому должны работать естественные механизмы защиты. Основным из них был назван иммунитет.
Иммунная система устроена очень сложно. В ней постоянно присутствует тонкое равновесие: иммунитет должен эффективно реагировать на чужеродные агенты, включая антигены раковых клеток, но не должен быть агрессивен настолько, чтобы повреждать здоровые ткани. Для сдерживания чрезмерной иммунной агрессии предназначены особые вещества — контрольные точки. Однако, злокачественные опухоли используют их для того, чтобы избежать иммунной атаки.
Контрольные точки можно заблокировать искусственно. Для этого учеными созданы специальные иммунопрепараты — они называются ингибиторами контрольных точек.
При раке печени применяется препарат ниволумаб (коммерческое название — Опдиво). Он блокирует белок PD1 на поверхности T-лимфоцитов, который мешает их активации. В итоге иммунные клетки снова начинают атаковать опухолевую ткань. Вводят препарат внутривенно, обычно раз в две недели. Ниволумаб нередко назначают пациентам с раком печени, которые ранее получали лечение таргетными препаратами.
Злокачественные новообразования печени могут быть первичными и вторичными. Вторичные опухоли – это метастазы, которые возникают при распространении злокачественного процесса на IV стадии. Чаще всего в печень метастазирует колоректальный рак. Первичный рак печени развивается непосредственно из ткани органа, и здесь выделяют две разновидности новообразований:
-
. Она происходит непосредственно из печеночных клеток.
- Холангиокарцинома — ее субстратом являются клетки, выстилающие печеночные протоки, выводящие желчь.
По сути, это две совершенно разные опухоли, и объединяет их только то, что они обе изначально локализуются в печени. Далее в этой статье мы будем говорить о гепатоцеллюлярном раке, поскольку это новообразование встречается намного чаще, чем холангиокарцинома.
Симптомы рака печени
Рак печени может долгое время протекать бессимптомно. У многих пациентов его обнаруживают при проведении контрольных обследований или случайно, при обследовании по поводу другой патологии. Описаны случаи, когда у пациента была опухоль размером 15 см, а никаких клинических признаков при этом не было.
Уже на распространенных стадиях присоединяются следующие симптомы:
- Тяжесть и тупая боль в правом боку.
- Нарастающая слабость, быстрая утомляемость.
- Нарушение аппетита, тошнота, рвота.
- Увеличение объема живота из-за скапливающейся в брюшной полости жидкости (асцита).
- Расширение вен в области стенки живота.
- Пожелтение кожи и склер.
- Боль. Боль тем сильнее, чем больше растянута капсула печени. В ряде случаев она может отсутствовать.
Из клинических признаков присутствуют следующие:
- Увеличение размеров печени.
- Увеличение уровня билирубина. Он может быть повышен и на фоне цирроза.
- Увеличение размеров селезенки.
- Лихорадка, устойчивая к действию антибиотиков и противовоспалительной терапии.
- Желудочно-пищеводные кровотечения из варикозно-расширенных вен пищевода.
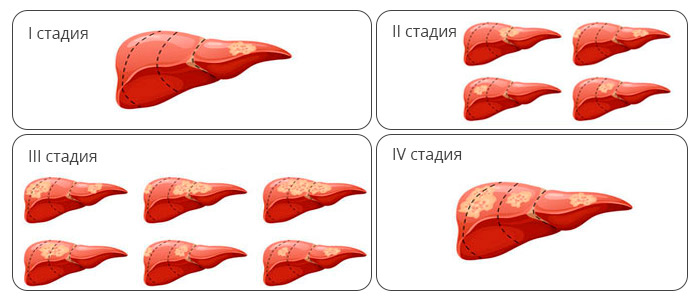
Стадии рака печени
Около 10-15% пациентов имеют признаки паранеопластического синдрома:
- Гипогликемия.
- Кожный зуд без желтухи.
- Остеопороз.
- Нарушение работы щитовидной и паращитовидной желез.
В ряде случаев первичные признаки со стороны печени отсутствуют, а симптомы появляются при развитии отдаленных метастазов, например, в легких, костях или головном мозге.
Диагностика рака печени
В рамках диагностики рака печени проводятся исследования, направленные на обнаружение новообразования, определение стадии распространенности опухолевого процесса, а также оценку функциональных резервов печени.

В рамках обнаружения рака проводят следующие исследования.
УЗИ печени. Метод прост, безопасен, доступен и обладает достаточной чувствительность и специфичностью. Также УЗИ позволяет определить инвазию рака в прилежащие к печени ткани, вовлеченность в процесс ворот печени, регионарные метастазы и наличие свободной жидкости в брюшной полости. Также аппараты экспертного класса позволяют оценивать степень фиброза печеночной ткани.
МРТ с контрастным усилением преобладает большей чувствительностью и специфичностью, по сравнению с УЗИ и позволяет обнаружить новообразования меньше 1 см на фоне цирроза.
Для верификации диагноза проводится биопсия опухолевого новообразования под контролем УЗИ.
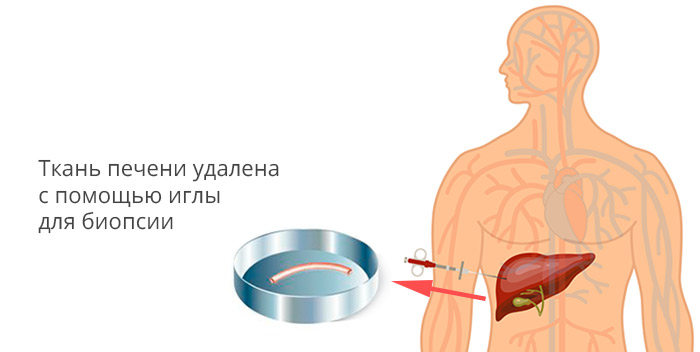
Пункционная биопсия печени
Для поиска метастазов рака печени проводится УЗИ брюшной полости, обзорная рентгенограмма органов грудной клетки или КТ ОГК. Также назначается КТ или МРТ головного мозга и сцинтиграфия костей.
Для определения функционального резерва печени при наличии цирроза проводится ряд тестов, которые учитывают наличие асцита, энцефалопатии, уровень альбумина и билирубина в сыворотке крови, а также МНО и протромбиновый индекс.
Лечение рака печени
При определении тактики лечения рака печени учитываются следующие факторы:
- Распространенность опухолевого процесса
- Функциональные резервы печени.
Возможные варианты лечения следующие:
- Хирургия — удаление пораженной части печени.
- Рентгенэндоваскулярные методы.
- Абляционные методы.
- Лучевая терапия.
- Медикаментозная терапия.
Хирургия
Если опухоль резектабельна, то предпочтение отдается резекции печени. Можно удалить до 75-80% печеночной ткани, и при этом сохранится ее функция, и пациент сможет жить. Но у больных с циррозом ввиду фибротических изменений, возможности хирургического лечения ограничены.
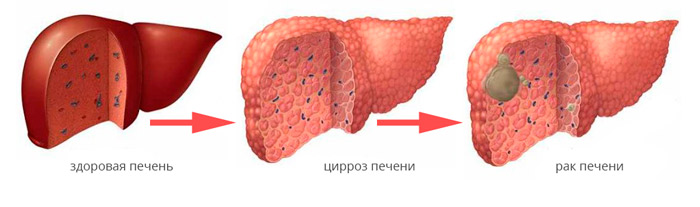
Развитие гепатоцеллюлярной карциномы на фоне цирроза печени
Трансплантация печени показана пациентам с циррозом, у которых соблюдаются следующие условия:
- Имеется одиночная опухоль размером менее 5 см.
- Наличие 2-3 очагов опухоли размером менее 3 см.
- Нет признаков прорастания рака в кровеносные сосуды.
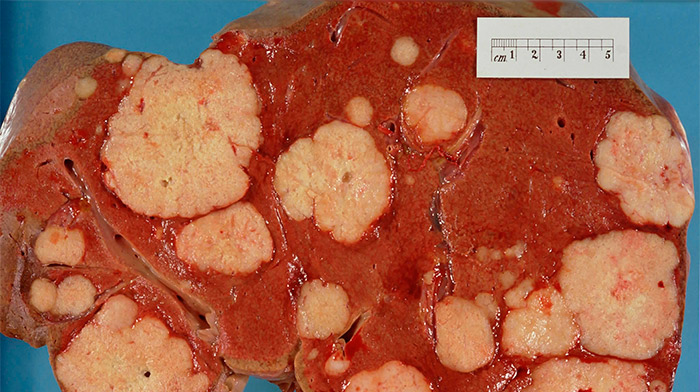
Удаленная печень со множественными злокачественными очагами
Абляция рака печени
В основе абляционных методов лечения лежит повреждение опухоли с помощью физических или химических агентов. Лечение проводится при единичных узлах. Применяются следующие методы:
- Лазер.
- Ультразвук.
- Радиочастотное воздействие.
- Микроволновое воздействие.
- Криоабляция — применение низких температур.
- Фотодинамическое воздействие.
- Введение в опухоль 96% этанола.
На практике чаще всего применяется радиочастотная или микроволновая абляция. Показанием к применению такого метода лечения являются единичные опухолевые узлы размером менее 5 см.

Рентгенэндоваскулярные методы
Применяются в рамках терапии первой линии при распространенной неоперабельной форме рака печени в комбинации с другими противоопухолевыми методами лечения при соблюдении следующих условий:
- Нет признаков прорастания рака в магистральные сосуды печени.
- Нет отдаленных метастазов.
- Нет признаков тромбоза магистральных сосудов печени.
Метод противопоказан в следующих случаях:
- Декомпенсированный цирроз.
- Коагулопатии с кровотечениями.
- Тромбоз или прорастание рака в магистральные сосуды печени.
- Внепеченочные очаги.
- Некупируемый асцит.
Суть лечения заключается во введении в опухоль химиопрепарата. Это возможно благодаря тому, что печень имеет двойное кровоснабжение. В нее входит воротная вена, которая приносит венозную кровь для фильтрации, и печеночная артерия, которая кровоснабжает саму печень и, соответственно, опухоль. Если блокировать артериальный кровоток в опухолевом узле, то это вызовет ее ишемию и, как следствие, уменьшение ее размеров. А если дополнительно в опухоль ввести химио-или радиопрепарат, то получается двойной эффект – от действия химиопрепарата и от ограничения кровотока.
Вначале вводится рентгеноконтрастный препарат, чтобы понять, какие ветви кровоснабжают опухоль. Затем в просвет сосуда доставляется масляный раствор с химиопрепаратом или специальные микросферы, насыщенные лекарственным средством. Таким образом, создается максимально высокая концентрацию препарата в опухоли плюс блокируется его кровоток.
Лучевая терапия рака печени
Лучевая терапия при лечении рака печени носит паллиативный характер и применяется у пациентов, имеющих противопоказания к вышеперечисленным методам лечения. У пациентов с единичными опухолевыми узлами возможно проведение стереотаксического облучения, которое позволяет подвести максимальную лучевую дозу непосредственно к опухолевому очагу, минимально затрагивая окружающие ткани.
Медикаментозная терапия гепатоцеллюлярного рака
Химиотерапия рака печени является малоэффективным методом лечения и помогает только 20% больных. Поэтому сейчас в рамках медикаментозной терапии применяется таргетная- и иммуно терапия, которая достоверно повышает продолжительность жизни таких пациентов. Терапией первой линии является сорафениб, либо комбинация таргетных и иммунопрепаратов: бевацизумаба и атезолизумаба. Также хорошие результаты показывает терапия регорафенибом.
Факторы риска рака печени
Основным фактором риска развития рака печени является цирроз самой разной этиологии. По сути цирроз является исходом хронического заболевания печени, которое в ряде случаев может длиться годами. Основными причинами развития цирроза являются:
- Хронические гепатиты В и С.
- Алкоголизм. При длительном и обильном употреблении алкоголя может развиться острый гепатит с трансформацией в хронический.
- Некоторые паразитарные инвазии.
- Гемохроматоз.
- Аутоиммунные гепатиты.
- Токсическое отравление афлотоксинами или винилхлоридом.
- Инсулинрезистентный сахарный диабет.
Только у 10% пациентов с раком печени опухоль развивается на фоне здоровой печеночной ткани.
Профилактика рака печени
Учитывая то, что рак печени в основном развивается на фоне цирроза, всем таким пациентам показано регулярное обследование. Проводится анализ на определение уровня онкомаркера альфа-фетопротеина и выполнение УЗИ печени.
Пациентам не из группы риска, т. е. у которых нет цирроза и сопутствующих заболеваний, можно предложить следующие мероприятия:
- Вакцинация против гепатита В.
- Регулярное обследование на определение маркеров вирусных гепатитов, и при постановке диагноза проведение своевременной антивирусной терапии.
- Отказ от употребления алкоголя.
- Соблюдение принципов рационального питания.
- Контроль веса и диабета.
- Контроль метаболического синдрома.
Популярные вопросы
Как можно предотвратить рак печени
В первую очередь, необходимо позаботиться о том, чтобы избежать хронических заболеваний печени, которые могут привести к циррозу. Если он уже есть, то необходимо раз в полгода сдавать анализы на альфа-фетопротеин и выполнять УЗИ брюшной полости.
Какие первые симптомы рака печени?
Первые симптомы могут развиться уже на распространенных стадиях, к тому же они могут маскироваться под признаки цирроза. Поэтому для ранней диагностики необходимо инструментальное обследование. Из симптомов чаще присутствует желтуха, нарушение аппетита, боль и тяжесть в правом подреберье.
Влияет ли цирроз на лечение рака печени?
Да, причем цирроз сам по себе может быть проблемой более серьезной, чем рак, поскольку при выраженной печеночной недостаточности происходит нарушение метаболизма различных соединений и синтеза многих белков, что само по себе приводит к развитию тяжелых состояний. Кроме того, цирроз может оказывать влияние на выбор тактики лечения онкологических пациентов.
Читайте также:

