Что такое кандидоз кожи стопы
Обновлено: 22.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Онихомикоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Онихомикоз – это грибковое поражение ногтя, при котором наблюдается изменение его цвета, толщины и отделение от ногтевого ложа. Онихомикоз - часто встречающееся заболевание ногтевого аппарата (не менее 50% всех заболеваний ногтей), которым болеет около 5,5% людей во всем мире. Взрослые болеют чаще, чем дети, поскольку распространенность онихомикозов увеличивается с возрастом (поражение ногтевых пластинок грибком встречается почти у 50% лиц старше 70 лет).
Причины возникновения онихомикоза
Онихомикоз могут вызывать грибы-дерматофиты, дрожжевые грибы и плесневые грибы-недерматофиты.
Дерматофиты становятся причиной заболевания в 60-70% случаев, при этом до 50% приходится на Тrichophyton rubrum. Плесневые грибы-недерматофиты вызывают около 20% всех онихомикозов, а дрожжевые грибы, в том числе Candida spp., - 10-20%.
Достаточно часто обнаруживается ассоциированное поражение грибами и бактериями, а также одновременное инфицирование ногтевой пластинки двумя и более грибами.
Развитию онихомикоза способствуют травмы опорно-двигательного аппарата, нарушение кровоснабжения конечностей (например, вследствие сердечной недостаточности, облитерирующего эндартериита или варикозного расширения вен), сахарный диабет, ожирение, плоскостопие, деформация стоп, курение, псориаз, иммунодефициты. К другим предрасполагающим факторам относят ношение тесной обуви, повышенную потливость, травмы ногтей. Высокий риск приобрести грибок есть у тех, кто участвует в спортивных мероприятиях, посещает общественные бани и бассейны, проживает с родственниками, у которых диагностирован грибок, или у тех, кто уже болел онихомикозом ранее.
Ногти на ногах поражаются чаще, чем на руках, что, вероятно, связано с их более медленным ростом, худшим кровоснабжением и с тем, что ношение тесной обуви создает среду, благоприятную для размножения грибка.
Заражение патогенными грибками может происходить при непосредственном контакте с больным онихомикозом, а также через обувь, одежду, предметы обихода (коврики в ванной, мочалки, маникюрные принадлежности и др.). В условиях повышенной влажности (в бассейнах, банях, душевых) грибы длительное время сохраняются и размножаются, особенно на неокрашенных деревянных поверхностях.
При заражении возбудитель проникает в ногтевую пластинку, ложе, матрикс и проксимальный валик ногтя. Ноготь не обладает эффективным клеточным иммунитетом, поэтому очень восприимчив к инфекции. Грибы производят ферменты, разрушающие ногтевую пластину, что облегчает их проникновение вглубь.
Частые очаги онихомикоза - подошвы и межпальцевые промежутки. Обычно грибы поражают ногтевую пластинку, начиная со свободного края, таким образом основные патологические процессы протекают не в самой пластинке, а под ней - в ложе ногтя.
Классификация онихомикоза
Различают нормотрофический, гипертрофический и онихолитический (атрофический) онихомикоз.
При нормотрофической форме пораженный ноготь сохраняет свою толщину и блеск, но меняет цвет.
При гипертрофической форме помимо изменения цвета наблюдается нарастающий подногтевой гиперкератоз. Ноготь теряет блеск, становится тусклым, утолщается и деформируется вплоть до образования онихогрифоза (утолщения и искривления ногтя наподобие когтя мифической птицы грифона), частично разрушается, особенно с боков, нередко пациенты испытывают боль при ходьбе.
Для онихолитической формы характерна тусклая буровато-серая окраска пораженной части ногтя, ее атрофия и отторжение от ложа - обнаженный участок покрыт рыхлыми гиперкератотическими наслоениями; в то же время проксимальная часть ногтя долго остается без существенных изменений.
Кроме того, применяют классификацию, основанную на локализации поражения ногтя: выделяют дистальный онихомикоз (с поражением ногтя у свободного края), латеральный (с поражением боковых сторон), проксимальный (с поражением заднего валика) и тотальный (с поражением всего ногтя).
Симптомы онихомикоза
Основное проявление онихомикоза – изменение цвета ногтевой пластинки: она белеет или становится желто-коричневой, может приобретать фиолетовый, зеленоватый или черный цвет. К другим клиническим проявлениям относят утолщение и зуд кожи в области ногтевых валиков (подногтевой гиперкератоз), отслоение ногтя от ногтевого ложа (онихолизис) и утолщение ногтевой пластинки (онихауксис). Для грибкового поражения ногтя характерен такой признак как дерматофитома - продольная полоса желтовато-белого или коричневатого цвета, локализующаяся в глубине ногтевой пластинки.
Ногти пальцев ног поражаются в 7-10 раз чаще, чем рук, причем чаще всего поражаются большие пальцы. Как правило, грибок одновременно присутствует на нескольких ногтях, нередко у больных онихомикозом выявляется также микоз стоп.
Диагностика онихомикоза
Диагностика онихомикоза основывается на данных клинической картины и результатах лабораторных исследований.
-
Проведение микроскопического исследования пораженных ногтевых пластинок.
Исследование используется в диагностике грибковых заболеваний кожи и ногтей. Особенности инфекции. Грибковые заболевания (микозы) кожи и ногтей – заразные заболевания, передающиеся от человека к человеку. Передача инфекции может произойти при непосредственном контакте с активным о.
Инвазивный кандидоз – это генерализованная грибковая инфекция, при которой наблюдается кандидемия и поражение внутренних органов грибами рода Кандида. До половины случаев заболевания вызвано возбудителем C. albicans, в тройке самых распространенных патогенов находятся C. parapsilosis и C. glabrata. Клинические проявления болезни определяются локализацией очага инфекции и степенью иммунного ответа. Для диагностики назначают серологические и культуральные исследования крови, инструментальные методы визуализации. Лечение требует индивидуального подбора противогрибковых препаратов.
МКБ-10


Общие сведения
Инвазивный кандидоз считается одной из самых распространенных инфекций среди госпитализированных пациентов. Ежегодно регистрируется более 250000 случаев, причем эксперты уверены, что истинная встречаемость инфекции намного выше. Заболевание чаще развивается у новорожденных и людей пожилого возраста. Высокая распространенность, неблагоприятный прогноз и сложности своевременной идентификации кандидоза заставляют специалистов искать новые пути диагностики и лечения болезни.

Причины
Возбудитель заболевания – грибы рода Candida, которые принадлежат к семейству Сахаромицеты, классу Аскомицеты. Известно более 20 патогенных для человека видов, однако до 90% случаев инвазивного кандидоза провоцируют только 5 из них: C. albicans, C. glabrata, C. tropicalis, C. parapsilosis и C. krusei. Лидирующее место в России продолжает занимать C. albicans (48%), часто встречаются возбудители C. parapsilosis (17%) и C. glabrata (14%).
Основным фактором риска инвазивного кандидоза является иммунная недостаточность, поскольку все звенья иммунитета участвуют в борьбе с грибковой инфекцией. Заболевание в основном встречается среди пациентов отделений интенсивной терапии, причем возраст больного до 1 года и старше 65 лет резко повышает вероятность грибковой инфекции. Выделяют и другие факторы риска:
- Пересадка внутренних органов. На долю кандидоза приходится более 53% всех инвазивных микозов, которые развиваются у пациентов после трансплантации. Наибольший риск имеет пересадка тонкого кишечника, поджелудочной железы и печени. Грибковая инфекция развивается у 3-4% больных с трансплантированным сердцем, почками, легкими.
- Постановка катетера. Центральный венозный катетер представляет собой оптимальные входные ворота для грибковых возбудителей. В его просвете формируются биопленки из грибов Кандида, которые вызывают катетер-ассоциированную кандидемию. Патология чаще встречается у новорожденных и вызвана видом C. parapsilosis.
- Антибиотикотерапия. Противомикробные препараты широкого спектра действия подавляют полезную микрофлору кишечника, повышают грибковую контаминацию ЖКТ. Наиболее опасными признаны цефалоспорины III поколения, которые в 2 раза увеличивают риск развития микозов.
- Онкопатология. Наибольшему риску подвергаются пациенты с гемобластозами, у которых отмечается выраженная нейтропения, нарушения выработки иммуноглобулинов и патологии системы комплемента. На поздних стадиях солидных опухолей также возрастает вероятность инвазивного кандидоза.
Патогенез
Большинство случаев связано с эндогенным путем передачи инфекции: проникновением грибов через слизистые оболочки желудочно-кишечного тракта либо через поврежденные полые органы брюшной полости. Заражению способствует увеличение грибковой нагрузки в кишечнике на фоне антибиотикотерапии. Реже наблюдается экзогенное инфицирование при инвазивных медицинских манипуляциях (постановка катетера, парентеральное питание, хирургическое вмешательство).
После проникновения грибов Кандида в кровеносную систему развивается кандидемия, обуславливающая гематогенное распространение возбудителя и формирование очагов во внутренних органах. Основным механизмом тканевой инвазии является способность к образованию псевдомицелия, который препятствует поглощению грибов макрофагами. К факторам патогенности относят ферменты (аспартилпротеиназы, фосфолипазы), фенотипическую нестабильность.

Симптомы инвазивного кандидоза
У трети пациентов наблюдается кандидемия без органических патологий внутренних органов, которая не имеет специфических признаков. Основным симптомом присоединения грибковой инвазии является резкий подъем температуры на фоне антибиотикотерапии. Лихорадка зачастую имеет волнообразное течение. При глубоком иммунодефиците проявления системного воспалительного процесса стерты или полностью отсутствуют.
При вовлечении в процесс внутренних органов клиническая картина разнообразна. Поражение органов брюшной полости проявляется классическими признаками перитонита: резкие боли по всему животу, напряжение мышц передней брюшной стенки, многократная тошнота и рвота. Инфицирование мочевых путей сопровождается кандидозным циститом и пиелонефритом. Частным признаком инфекции является пневмония, которая протекает без особенностей.
При установке ликворных шунтов и других инвазивных нейрохирургических манипуляциях возможно поражение ЦНС. Инвазия грибами Кандида чаще всего проявляется менингитом с подострым течением. При воспалении мозговых оболочек возникает сильная головная боль, длительная лихорадка, светобоязнь. Отличием грибкового менингита считается отсутствие ригидности затылочных мышц.
Поражение тканей сердца развивается у пациентов после установки искусственных клапанов. Клинические проявления манифестируют в течение 2 месяцев после операции. Больные страдают от лихорадки, одышки, болей в области сердца. Быстро присоединяются признаки сердечной недостаточности, гепатоспленомегалия, узелки Ослера. Есть риск вовлечения опорно-двигательного аппарата с развитием кандидозного артрита и остеомиелита.
Инвазивный кандидоз у новорожденных характеризуется классической картиной неонатального сепсиса. Возникает заторможенность, отказ от кормлений, одышка с эпизодами апноэ. Характерна сердечно-сосудистая нестабильность, затяжная желтуха. Фебрильная лихорадка наблюдается только в 50% случаев, при этом до 40% пациентов имеют физиологическую норму лейкоцитов крови.
Осложнения
Несмотря на достижения практической инфектологии, летальность при инвазивном кандидозе остается стабильно высокой. У взрослых уровень смертности составляет 40%, среди иммунокомпрометированных больных он может достигать 50-70%. Суммарная детская смертность при инвазивной форме кандидоза варьирует в пределах 37-44%, неонатальная – 43-54%. Прогностически неблагоприятным фактором является задержка идентификации возбудителя на 48 часов и более.
Жизнеугрожающие последствия инвазивного кандидоза в основном связаны с септическим шоком и полиорганной недостаточностью. Причинами смерти выступают критические поражения головного мозга, сердечно-легочной системы и почек. Большую опасность представляют коагулопатии, тромбоэмболии, синдром диссеминированного внутрисосудистого свертывания (ДВС).
Диагностика
Поскольку инвазивный кандидоз в основном развивается у госпитализированных больных, обследование проводит лечащий врач совместно с реаниматологом и инфекционистом. Большое значение уделяют сбору анамнеза, выяснению иммунного статуса, анализу текущей схемы фармакотерапии. При осмотре определяются признаки системного воспаления и полиорганной недостаточности. Для подтверждения диагноза назначаются такие методы:
- Определение поверхностного антигена Candida. Наличие в анализе маннана и антиманнановых антител специфично для кандидозной инфекции. Позитивные результаты на 5-6 дней опережают ответ при посеве гемокультуры, имеют важное значение для своевременного старта терапии. Чувствительность и специфичность метода составляют 80-85%.
- Исследование гемокультуры. Выявление грибов Кандида в образцах крови, взятых из трех разных вен, является достоверным признаком инвазивного кандидоза. Такой метод требует длительного времени и дает положительные результаты только у 75% пациентов, поэтому он не подходит для ранней диагностики.
- Инструментальная визуализация. Для обнаружения очагов кандидозной инфекции используют ультразвуковое исследование, чреспищеводную эхокардиографию, компьютерную и магнитно-резонансную томографию. Подтвердить грибковую этиологию воспалительных очагов удается путем анализа биоптатов.
- Прогностические шкалы. Поставить точный диагноз помогает шкала «Кандида» и прогностическое правило, представленное в Российских клинических рекомендациях. Для определения индивидуального риска используют индекс колонизации Candida.

Дифференциальная диагностика
Ввиду отсутствия патогномоничных проявлений, при постановке диагноза исключают бактериальный сепсис, генерализованную герпетическую инфекцию, аспирационную и вентилятор-ассоциированную пневмонию. Дифференциальную диагностику проводят с малярией, системной красной волчанкой, васкулитами. У новорожденных необходимо исключить респираторный дистресс-синдром.
Лечение инвазивного кандидоза
Основу лечения составляет длительное парентеральное введение противогрибковых препаратов. Лекарства назначают эмпирически до получения результатов посева крови, предварительно взяв биоматериал для микробиологической диагностики. При выборе препарата для лечения кандидоза обращают внимание на иммунный статус пациента, наличие и характер сопутствующих заболеваний, анамнестические данные о грибковых инфекциях.
Стандартные протоколы терапии включают препараты из группы полиеновых антибиотиков, азоловых антимикотиков, эхинокандинов. Клинический ответ на проводимое лечение развивается в течение 3 дней. При его отсутствии необходим пересмотр режима дозирования антимикотиков или их замена. Критерием завершения антимикотической терапии служат отрицательные посевы крови в течение 14 суток.
Фармакотерапия инвазивного кандидоза сочетается с лечением основного заболевания. Значимые усилия прикладывают для нормализации иммунного статуса, если это возможно. Для исключения повторного инфицирования грибками проводят замену катетеров. При тяжелом иммунодефиците, состоянии после трансплантации костного мозга или внутренних органов пациенты проходят лечение в стерильном боксе.
Прогноз и профилактика
У пациентов с сохранными функциями иммунной системы, которым вовремя начата терапия антимикотиками, удается достичь полного выздоровления. При иммунодефиците и тяжелом соматическом статусе прогноз остается сомнительным даже при ранней и комплексной медицинской помощи. Для профилактики инвазивного кандидоза пациентам из группы высокого риска рекомендован прием флуконазола в стандартной дозировке.
3. Инвазивный кандидоз: современные аспекты эпидемиологии, диагностики, терапии и профилактики у различных категорий пациентов (в вопросах и ответах)/ А.В. Веселов, Р.С. Козлов. – 2016.
4. Инвазивный кандидоз в отделениях реанимации и интенсивной терапии/ Н.А. Карпун, С.А. Бурова, Е.А. Евдокимов, Н.И. Чаус// Неотложная медицина. – 2014. – №2.
Кандидоз — инфекционное заболевание, обусловленное дрожжеподобными грибами рода Candida . Клинические проявления микоза широко варьируют от поверхностных, слабовыраженных поражений кожи и слизистых оболочек до тяжелых, угрожающих жизни инвазивных висцер
Кандидоз — инфекционное заболевание, обусловленное дрожжеподобными грибами рода Candida. Клинические проявления микоза широко варьируют от поверхностных, слабовыраженных поражений кожи и слизистых оболочек до тяжелых, угрожающих жизни инвазивных висцеральных форм. Диагностика и терапия кандидоза непроста и часто требует привлечения специалистов различного профиля [1, 4, 8].
Число больных поверхностными и глубокими формами кандидоза в последние десятилетия значительно возросло во всех странах мира. Этот факт связывают со снижением естественной иммунной реактивности организма значительной части населения из-за поражения СПИДом, ятрогенных иммунодефицитов, возникающих при химиотерапии онкологических больных, трансплантации органов, вследствие применения глюкокортикоидов, цитостатиков, антиметаболитов, антибиотиков широкого спектра действия, в том числе в отделениях реанимации и интенсивной терапии [4, 8].
Главным возбудителем кандидоза является Candida albicans, которая, как и другие виды грибов Candida, обнаруживается в норме на слизистых и кожных покровах большинства обследованных, но поражает лишь ослабленный организм. Именно в этом кроется сложность проблемы кандидоза.
Природа возбудителя, его взаимоотношения с макроорганизмом, многие аспекты защиты организма от кандидозной инфекции, генетические механизмы резистентности различных видов Candida spp. к основным антимикотикам, применяющимся в лечении кандидоза, подробно изучена. Установлено, что подавляющее большинство штаммов C. albicans, C. tropicalis, C. parapsilosis чувствительны к флуконазолу, однако у ВИЧ-инфицированных и других иммунокомпрометированных больных с инвазивным кандидозом возможна резистентность C. albicans к азольным соединениям. В то же время большинство штаммов C. krusei и часть штаммов C. Glabrata обнаруживают устойчивость к флуконазолу [8].
Известно, что грибы рода Candida сапрофитируют на коже и слизистых оболочках, не вызывая заболевания и лишь при повреждении наружных покровов, снижении местного иммунитета они могут проникнуть внутрь, пройдя стадии адгезии, колонизации и инвазии.
Адгезия грибов Candida обусловлена их способностью расщеплять секреторный иммуноглобулин А и α-антитрипсин и прикреплять жизнеспособный гриб к протеинам слизистых оболочек за счет гликопротеинадгезина клеточной мембраны гриба. Адгезия гриба к эпителию является основой его инвазии в организм, что происходит уже в первые минуты его взаимодействия со слизистой. Степень адгезии определяет уровень колонизации C. albicans, а степень инвазии — его вирулентность. Грибки продуцируют эндотоксины, гемолизины, дермотоксины, пирогены, протеолитические ферменты, облегчающие адгезию грибковых клеток к ороговевшему эпителию и слизистым оболочкам. Установлено, что у разных штаммов C. albicans способность к продукции этих «факторов агрессии», колонизации и инвазии выражена в различной степени, что должно учитываться при назначении лечения [5, 6]. В «Проекте рекомендаций по лечению кандидоза» указано на важность определения вида возбудителей и их чувствительности к противогрибковым препаратам, даются рекомендации по лечению различных форм инвазивного кандидоза, кандидемии и острого диссеминированного кандидоза — тяжелейших форм кандида-инфекции с высокой летальностью, перечисляются показания к проведению адекватного лечения амфотерицином В и флуконазолом [4]. Замена первого дорогостоящим липосомальным препаратом амбизомом позволяет избежать высокой нефротоксичности амфотерицина В и проводить лечение больных кандидозом с почечной недостаточностью, резистентной к антибиотикам фебрильной нейтропенией, при высоком риске развития острого диссеминированного кандидоза у больных без нейтропении, его органных форм (поражения сердца, сосудов, мочевыводящих путей, желудочно-кишечного тракта). В работе также приводятся рекомендации по лечению кандидоза кожи, ее придатков, хронического кандидоза кожи и слизистых оболочек, профилактике кандидоза у реципиентов трансплантатов органов.
Наиболее полное, систематизированное изложение проблемы кандидоза дано в вышедшей в 2000 году монографии «Кандидоз» [8].
Этиотропная терапия любого инфекционного заболевания, в том числе и кандидоза, ставит своей целью удаление (эрадикацию) возбудителя. Однако особенностью кандидоза является то, что грибы рода Candida входят в состав постоянной биоты — нормобиоты, бактериобиоты человека, и легко колонизируют слизистые оболочки, то есть сама эрадикация этого гриба почти никогда не бывает абсолютной и окончательной. Учитывая оппортунистическую природу кандида-инфекции, саму эрадикацию возбудителя связывают с патогенетическими факторами, определяющими клиническую форму и тяжесть инфекции. Это иммунодефициты, нейтропения и другие. Вот что определяет выбор антимикотика, его дозу и длительность терапии.
Лечение может быть направлено на предупреждение гиперколонизации организма грибами рода Candida (при назначении антимикотиков широкого спектра действия и иммуносупрессантов). Местные оральные антимикотики — полиены (нистатин, леворин, микогептин) нерастворимы и почти не всасываются из желудочно-кишечного тракта, поэтому редко могут обеспечить элиминацию Candida. Здесь необходимы пероральные препараты системного действия (флуконазол, итраконазол) или препараты для инъекций, такие как флюцитозин, амфотерицин В, амбизом. Если амфотерицин В вследствие его чрезвычайной нефротоксичности назначается при кандидозе в суточной дозе 0,5 мг/кг массы тела, амбизом в 10 раз и более превышает эту дозу и не имеет противопоказаний к назначению [1, 2, 3, 4, 9, 10]. При лечении кандидозов кожи и слизистых оболочек часто используются антимикотики для наружного применения: полиены (леворин, нистатин, натамицин), производные имидазола (кетоконазол, оксиконазол, эконазол, тиоконазол, клотримазол, миконазол, изоконазол, бифоназол, амиказол), триазолы (терконазол), аллиламины (нафтифин, тербинафин), морфолины (аморолфин), прочие препараты (производные унденциленовой кислоты, анилиновые красители и др.).
Одно только перечисление антикандидозных препаратов уже свидетельствует об их множестве и разной степени эффективности, связанной с химической структурой и особенностями фармакокинетики. В частности, наружные средства не всегда создают достаточную концентрацию в подслизистом слое половых путей, глубоких слоях кожи и ее придатках.
В последние годы в России и за рубежом в системной терапии кандидоза с успехом применяется медофлюкон (флуконазол) [2, 3].
Флуконазол (медофлюкон) — противогрибковый препарат из группы триазолов, эффективный при системных и локальных микозах. Флуконазол избирательно подавляет синтез эргостерина клеточной мембраны грибков на уровне образования диметил-эргостатриенола из ланостерина путем ингибирования зависимой от цитохрома Р-450 реакции С14-альфа-демитиляции. Этот путь биосинтеза стеролов характерен только для грибов. За счет более высокого сродства к ферментам, катализирующим синтез эргостерина у грибов, чем к ферментам, катализирующим образование холестерина у человека, селективность действия флуконазола на грибы рода Candida, дерматофиты и возбудители глубоких микозов в 10 000 раз выше, чем на клетки макроорганизма.
Спектр фунгистатического действия флуконазола: Candida albicans, некоторые штаммы Candida nonalbicans (C. guilliermondii, C. pseudotropicalis, C. torulopsis, C. kefyr, C. stellatoidea), Cryptococcus neoformans, Microsporum spp., Trichophyton spp., Blastomyces dermatitidis, Coccidioides immitis, Histoplasma capsulatum.
При пероральном и внутривенном применении фармакокинетика флуконазола сходная. При приеме внутрь биодоступность около 90%. Прием пищи не влияет на абсорбцию препарата. Максимальная концентрация достигается через 0,5 — 1,5 ч. После приема 150 мг она составляет 2,44 — 3,58 мкг/мл. Концентрация в крови прямо пропорциональна принятой дозе. Равновесная концентрация устанавливается к 4 — 5-му дню при приеме 1 раз в сутки. При использовании в первый день двойной дозы она достигается ко второму дню. Связь с белками плазмы 11 — 12%. Объем распределения приближается к общему объему воды в организме. Концентрации флуконазола в слюне, мокроте, суставной и перитонеальной жидкостях, вагинальном секрете, грудном молоке аналогичны таковым в плазме крови. Концентрация в ликворе составляет 50 — 90% (в среднем 70 — 80%) уровня в плазме крови, при менингите — до 93%. В роговом слое кожи, эпидермисе, дерме, потовой жидкости и моче концентрации достигают значений, в 10 раз превышающих концентрацию в плазме крови. Концентрация в роговом слое кожи после 12-дневного применения в дозе 50 мг 1 раз в сутки составляет 73 мкг/г. Концентрация в ногтях после 4-месячного применения в дозе 150 мг 1 раз в неделю составляет 4,05 мкг/г в здоровых и 1,8 мкг/г в пораженных ногтях. Препарат определяется в ногтях в течение 6 месяцев после завершения терапии. Т1/2 27 — 30 ч. Биотрансформации не подвергается. Экскретируется почками, на 80% — в неизмененном виде. Клиренс флуконазола пропорционален клиренсу креатинина. Концентрация флуконазола в плазме крови может быть уменьшена с помощью диализа (на 50% в течение 3 ч).
Медофлюкон применяется внутрь 1 раз в сутки (утром).
Дозы для взрослых:
- При кандидемии, диссеминированном кандидозе — 400 мг в первые сутки и 200 — 400 мг — в последующие дни. Продолжительность лечения 7 — 14 дней и более.
- При кандидозе кожи — 50 — 100 мг 1 раз в сутки или 150 мг 1 раз в неделю в течение 2 — 6 недель.
- При орофарингеальном кандидозе — 50 мг в сутки в течение 7 — 14 дней.
- При кандидозе другой локализации (кандидурии, кандидозном эзофагите и неинвазивном бронхолегочном кандидозе) — 50 — 150 мг в сутки в течение 14 — 30 дней.
- При онихомикозе — 50 мг 1 раз в сутки или 150 мг 1 раз в неделю в течение 3 — 6 месяцев при поражении ногтей пальцев рук и 6 — 12 месяцев — при поражении ногтей пальцев ног (до замещения инфицированного ногтя).
- При кандидозном баланопостите или вагинальном кандидозе — 150 мг однократно, при кандидозном вульвовагините — 50 мг в сутки в течение 7 дней или 150 мг двукратно, при хроническом рецидивирующем (3 — 4 раза в год или чаще) кандидозном вульвовагините 150 мг 3 — 4 раза в сутки с 3 — 7-дневными интервалами, иногда до 12 раз с месячными интервалами.
- При глубоких эндемических микозах — 200 — 400 мг в сутки ежедневно до 2 лет: 11 — 24 мес. при кокцидиомикозе, 2 — 17 мес — при паракокцидиомикозе, 1 — 16 мес. — при споротрихозе, 3 — 17 мес — при гистоплазмозе.
- При криптококковом менингите, криптококковых инфекциях другой локализации — 400 мг в первые сутки и 200 — 400 мг в последующие дни. Продолжительность лечения 7 — 14 дней, при криптококковом менингите — до 6 — 8 недель.
- Для профилактики грибковых инфекций — 50 — 400 мг в сутки на протяжении всего периода антибактериальной, глюкокортикоидной, цитостатической или лучевой терапии.
Специального подбора доз для пациентов пожилого возраста не требуется, если не угнетена функция почек (клиренс креатинина менее 40 — 50 мл/мин).
У больных с нарушениями функции почек доза должна быть снижена в соответствии со степенью почечной недостаточности.
Пациентам, находящимся на гемодиализе: однократно после каждого сеанса гемодиализа.
Российские авторы [3] приводят собственные данные о применении медофлюкона при различных поражениях, в том числе при висцеральных микозах, обусловленных грибами рода Candida. В частности, опубликованы данные об успешном лечении медофлюконом 9 больных кандидозом кишечника, 11 — полости рта, 3 — пищевода, 18 — вагинальным кандидозом при суточной дозе 50 — 200 мг и длительности курса 14 дней. Отечественные исследователи, оценив эффективность и безопасность препарата, уже в 1996 году назвали медофлюкон безусловным достижением в лечении кандидоза и рекомендовали его для лечения поверхностных и висцеральных форм микоза не только в стационаре, но и в амбулаторных условиях.
К такому же выводу пришли и авторы, проводившие исследования медофлюкона в Московском центре глубоких микозов [2]. По их данным, из 79 больных кандидозным бронхитом, получавших в течение 2 недель 100 — 400 мг медофлюкона в сутки, излечено 74,7%, улучшение наступило у 22,8%, при кандидозной пневмонии выздоровело 66,75%, улучшение отмечено у 33,3%, эрадикация возбудителя — в 97,5 — 100%.
В дерматовенерологии медофлюкон наиболее часто применяется при лечении урогенитальных кандидозов, кандидоза слизистой оболочки полости рта, онихомикозах [4, 6, 7, 8].
Данные, приведенные из литературы, и наш опыт применения медофлюкона при кандидозном вульвовагините и онихомикозе свидетельствуют о его высокой эффективности, хорошей переносимости и безопасности, что делает флуконазол препаратом выбора при лечении различных форм кандидоза слизистых оболочек, кожных покровов и внутренних органов.
В. М. Лещенко, доктор медицинских наук, профессор
Городской микологический центр, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кандидоз: причины появления, симптомы, диагностика и способы лечения.
Кандидоз – инфекционное заболевание, вызываемое дрожжеподобными грибками рода Candida. Оно обусловлено активным размножением грибка на слизистых оболочках полости рта, половых и внутренних органов и на коже.
Все представители рода Candida относятся к условно-патогенным микроорганизмам, то есть они постоянно присутствуют в составе нормальной микрофлоры. Но при снижении иммунитета, изменении гормонального фона и по ряду других причин эти грибки могут начать активно колонизировать слизистые оболочки и кожу.
Наиболее распространенные представители рода – Candida albicans и C. tropicalis. В 90-95% случаев урогенитального кандидоза именно C. albicans является доминирующим возбудителем.
![shutterstock_714362212 [преобразованный].jpg](https://www.invitro.ru/upload/medialibrary/d29/d29b49ccfe770f215bf7b01b406a2d2f.jpg)
Первый контакт с грибками рода Candida происходит во время прохождения ребенка по родовым путям. Однако в медицинской литературе описаны случаи обнаружения этих микроорганизмов в околоплодных водах, что свидетельствует о возможности вертикального (трансплацентарного) пути передачи. Также встречается передача грибка рода Candida при грудном вскармливании, кожном контакте ребенка с матерью, бытовым и пищевым путями.
Эти микроорганизмы вырабатывают эндотоксины и ферменты, вызывающие гибель клеток и некроз тканей, что способствует усилению адгезивной (прикрепление к клеткам слизистых оболочек или кожи) способности грибка и обеспечивает проникновение в ткани.
Гиперпродукция этих и ряда других веществ обуславливает патогенность представителей семейства Candida.
Причины возникновения кандидоза
- Экзогенные (внешние) факторы, способствующие проникновению грибков в организм:
- профессиональные вредности, приводящие к частым повреждениям кожи;
- длительное пребывание в теплой и влажной среде;
- нарушение целостности слизистых оболочек.
- Факторы, приводящие к снижению сопротивляемости организма:
- наличие хронических заболеваний;
- длительный прием препаратов, способствующих нарушению естественной микрофлоры;
- несбалансированное питание;
- частые стрессы, нарушения режима сна и отдыха.
- Нарушения обмена веществ (гиповитаминозы), заболевания иммунной системы (ВИЧ-инфекция), эндокринные патологии (сахарный диабет и пр.).
- Длительный прием некоторых препаратов: гормональных контрацептивов, системных глюкокортикостероидов, антибиотиков широкого спектра действия, цитостатиков.
- Длительное пребывание или проживание в местности с повышенной влажностью и температурой, комфортными для циркуляции спор грибков в окружающей среде.
По локализации процесса выделяют:
- Урогенитальный кандидоз.
- Кандидоз слизистой оболочки полости рта.
- Поверхностный кандидоз.
- Межпальцевый кандидоз.
- Кандидоз околоногтевых валиков и ногтей.
- Кандидоз желудочно-кишечного тракта.
Урогенитальный кандидоз (УГК) – широко распространенное заболевание: по данным медицинской статистики, около 75% женщин репродуктивного возраста хотя бы единожды регистрировали у себя симптомы УГК.
Выделяют острую и хроническую форму урогенитального кандидоза, кандидоз вульвы, вагины и других урогенитальных локализаций. В ряде случаев при диагностике используют уточнение: осложненный или неосложненный УГК, что отражает количество обострений в год и степень выраженности заболевания.
Симптомы женского урогенитального кандидоза
- Появление бело-желтых творожистых или сливкообразных выделений из половых путей. Интенсивность выделений может усиливаться перед менструацией, что связано с изменением гормонального фона.
- Неприятные ощущения, зуд в области гениталий, зачастую усиливающиеся при половом контакте или мочеиспускании.
- Покраснение и отечность слизистой вульвы и влагалища, наличие повреждений на коже половых органов (трещины, микротравмы).
- При хроническом течении УГК развивается сухость слизистых оболочек половых путей.
- Покраснение, отечность, неприятные ощущения в области половых органов.
- Беловатые выделения творожистой структуры из половых путей.
- Боль и жжение при половом контакте и при мочеиспускании.
Межпальцевый кандидоз локализуется в пространстве между пальцами. При этом отмечается покраснение участков кожи с последующим появлением пузырьков в прозрачным содержимым. Заболевание быстро распространяется в тесных коллективах (в детских садах, школах и т. д.).
Кандидоз слизистой оболочки полости рта (КСОПР)
Кандидоз полости рта вызывает неприятные ощущения, особенно при приеме пищи – жжение, боль, сухость. В зависимости от локализации процесса выделяют несколько форм кандидоза полости рта.
Часто КСОПР и желудочно-кишечного тракта сопровождает иммунодефицитные состояния: ВИЧ-инфекцию, синдром приобретенного иммунодефицита человека (СПИД) или врожденный иммунодефицит (например, при патологии Т-лимфоцитов). При наличии этих заболеваний кандидоз протекает с максимально выраженными симптомами, с трудом поддается лечению, носит агрессивный характер.
Самое частое проявление КСОПР – кандидозный стоматит, поражающий в основном грудных детей и взрослых с ослабленным иммунитетом.
При этой патологии слизистая оболочка полости рта краснеет, отекает, на ней появляются белесоватые пленки, имеющие творожистую консистенцию. На начальных стадиях болезни налет легко снимается. С течением заболевания пленки становятся плотнее, отделяются с трудом, при снятии обнажается кровоточащая слизистая оболочка.
При кандидозном стоматите возможно поражение языка, что проявляется покраснением спинки языка, появлением налета и слущиванием эпителия. Эти симптомы сопровождаются сильными болевыми ощущениями пораженной области при разговоре, приеме пищи и при пальпации (прощупывании) языка.
У курильщиков чаще других видов КСОПР развивается хронический гиперпластический кандидоз, сопровождаемый образованием белых, сливающихся между собой бляшек, которые возвышаются над поверхностью гиперемированной слизистой.
При этой патологии изменяется консистенция слюны: она становится вязкой и пенящейся; появляются неприятный запах изо рта, налет на слизистой серого или белого цвета. В 10-40% случаев эта клиническая форма кандидоза малигнизируется (т. е. приобретает злокачественный характер).
У пожилых людей чаще всего развивается хроническая атрофическая форма кандидоза полости рта. Слизистая оболочка при этом краснеет и отекает. Поражение часто локализуется под зубными протезами, что вызывает болевые ощущения.
Кандидозный хейлит и кандидоз углов рта в основном встречаются у детей и пожилых. Поражение обычно двустороннее, при этом образуются красные болезненные трещины в углах рта, покрытые легко снимающимся белым налетом или чешуйками. При длительном течении заболевания возможно присоединение бактериальной инфекции.
Диагностика кандидоза
Алгоритм диагностического поиска при кандидозе любой локализации включает в себя взятие материала с пораженной области с последующей его микроскопией, посевом для определения вида грибка и его чувствительности к антимикотическим (противогрибковым) препаратам.
В целях диагностики состояний, приведших к снижению иммунитета, используется общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Ежедневно к врачу дерматовенерологу обращается большое количество людей с изменениями ногтевых пластинок. Врач делит заболевания на 2 группы: грибкового и негрибкового характера. Здоровая ногтевая пластинка розового цвета с гладкой поверхностью с природным блеском. Любые изменения ногтевых пластинок-повод обратиться к врачу за консультацией и постановкой правильного диагноза. Зачастую, люди пытаются самостоятельно поставить себе диагноз и назначают самостоятельно лечение, что может привести к ухудшению состояния. Только врач, обладая необходимыми знаниями и опытом, используя дополнительные методы диагностики, может поставить правильный диагноз с назначением эффективного лечения.
Что относится к заболеваниям негрибкового характера:
I.Инфекционные заболевания — паронихия (воспаление околоногтевого валика по причине присоединения инфекции)
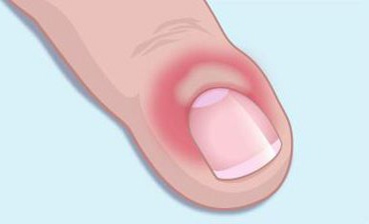
II. Неинфекционные – — дистрофия ногтей (ногти становятся плоскими или вогнутыми, появляются бороздки на поверхности. Чаще причина — эндокринные заболевания и несбалансированное питание.
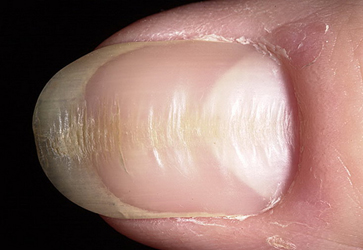
III. Другие- изменения ногтевых пластинок при недостаточности щитовидной железы (тонкость, ломкость, расcлоенность, ногти в виде ‘барабанных палочек’ при заболеваниях легких, cердечно — сосудистых изменениях, ВИЧ- инфекции, изменения ногтей при кожных заболеваниях таких как псориаз, красный плоский лишай.
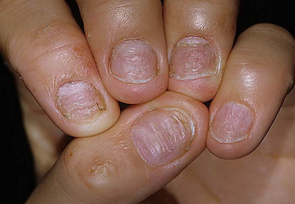
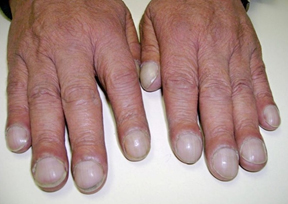
— онихолизис (отделение ногтевой пластинки от мягких тканей пальца)
— онихокриптоз (вросший ноготь) вследствие травмы, ношения тесной обуви, наследственности, неправильной обработки ногтей.
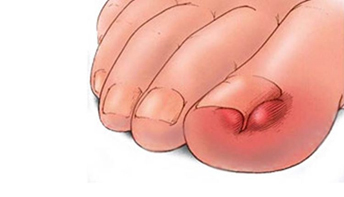
— онихошизм (поперечное расслоение ногтя) Ногтевая пластинка истончается и разделяется на несколько слоев. Причинами могут быть неправильное питание, травма, недостаток железа, и кальция в крови, сахарный диабет, использование некачественных лаков.
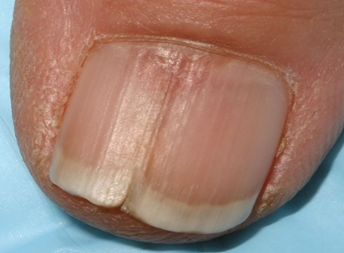
— меланонихия – почернения ногтя или образование полосы бурого цвета вследствие травмы, кровоизлияния в окружающие ткани.

Остановимся на таком серьезном изменении как меланонихия. Она заслуживает серьезного отношения , вследствие того, что является признаком такого серьезного заболевания как меланома ногтевой пластинки. Учитывая, что достаточно долгое время никаких серьезных признаков кроме как появление темных полос не вызывает, люди обращаются достаточно поздно.
Меланонихия начинается с появления бурых пятен или полос от коричневого до черного цвета. К меланонихии может привести:
- хроническая травматизация ногтя (например обувью, чаще 1,5 пальцы)
- поражение ногтей грибковой инфекцией ( некоторые виды грибов дают темный окрас)
- прием некоторых медикаментов, таких как линкомицин, химиотерапевтические препараты, противомалярийные.
- редко, но при такой патологии как амилоидоз, псориаз, ограниченная склеродермия.
- бактериальные инфекции
- Геморрагия в ногтевом ложе. Отличительной особенностью от меланомы является то, что гематома не достигает свободного края. НО! Наличие крови под ногтем не исключает злокачественности.
Лишь врач может провести дифференциальную диагностику с установкой правильного диагноза.
Следует не забывать, что существует ряд факторов, указывающих на наличие подногтевой меланомы:
- локализация на большом пальце руки или ноги
- локализация на одном краю
- возраст старше 60 лет, но не всегда
- внезапное появление на ранее нормальной ногтевой пластинке и быстро распространяющееся потемнение с нечеткими краями
- потемнение без предшествующей травмы
- появление без предшествующей травмы
- появление у людей с диспластическими невусами в анамнезе или семейном анамнезе
При любых изменениях ногтей следует немедленно обращаться к врачу.
10% меланом характеризуются нетипичной локализацией — на коже ладоней, подошв, коже пальцев и ногтевого ложа. Данный вид меланом называется акральная лентиго-меланома. Данный вид меланом опасен тем, что развивается медленно, и ее обнаруживают достаточно поздно.
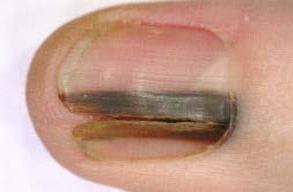
Чаще всего страдают люди более возрастной группы, но, в последнее время, наблюдается и у более молодой возрастной группы.
Инсоляция является одним из провоцирующих факторов возникновения, не менее важным является механическая травма.
Излюбленным местом патологии ногтевых пластинок являются ногти 1 и 5 пальцев, так как данные пальцы чаще других подвергаются травме. Первый признак данного вида меланом – это появление полоски или пятна от коричневого до черного цвета, начиная от ногтевого валика до свободного края ногтя, также пигментация на околоногтевом валике. В дальнейшем происходит утолщение ногтевой пластинки с последующим разрушением и изъязвлением ногтевого ложа.
На коже ладоней и подошв акральную лентиго-меланому часто расценивают как бородавку, костную мозоль, cтержневую мозоль. На ногтевой пластинке расценивают как грибковое поражение, подногтевую гематому, невус, вросший ноготь, кератоакантому. Поэтому людям с уже имеющимися родинками на стопах и ладонях следует бережно к ним относится и проходить ежегодный осмотр, а людям с вновь образованными родинками своевременно обращаться к врачу.
Читайте также:

