Что такое эпителия ацинусов
Обновлено: 03.05.2024
ГУЗ "Рязанский областной клинический онкологический диспансер"
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
Кафедра общей хирургии ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава РФ, Рязань, Россия
Ацинарная аденома поджелудочной железы
Журнал: Архив патологии. 2012;74(4): 46‑48
Виноградов И.Ю., Артемьева А.С., Виноградов И.И. Ацинарная аденома поджелудочной железы. Архив патологии. 2012;74(4):46‑48.
Vinogradov IIu, Artem'eva AS, Vinogradov II. Pancreatic acinar cell adenoma. Arkhiv Patologii. 2012;74(4):46‑48. (In Russ.).
ГУЗ "Рязанский областной клинический онкологический диспансер"
Представлены два случая редкой опухоли поджелудочной железы - ацинарной аденомы, диагностированные после оперативного вмешательства у женщин 70 и 58 лет. Приведены гистологическое описание опухоли и результаты иммуногистохимических реакций.
ГУЗ "Рязанский областной клинический онкологический диспансер"
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
Кафедра общей хирургии ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава РФ, Рязань, Россия
Доброкачественные опухоли поджелудочной железы развиваются крайне редко, частота их выявления на вскрытиях составляет 0,001—0,003%. Они могут быть представлены эпителиальными (аденомы, папилломы, цистаденомы), соединительнотканными (фибромы, липомы, миксомы), сосудистыми (гемангиомы, лимфангиомы) и другими редко встречающимися опухолями (миомы, невриномы, тератомы и др.).
В процессе эмбриогенеза поджелудочная железа формируется из первичной кишки, которая имеет выстилку из простого однослойного эпителия. По мере развития органа клетки первичного эпителия (стволовые клетки) дифференцируются в трех направлениях: на клетки протокового эпителия, ацинарные и эндокринные, имеющие различный иммуногистохимический профиль. Опухоли, развивающиеся из этих клеток, характеризуются соответствующим иммунофенотипом, в связи с чем современные представления о гистогенезе различных типов эпителиальных опухолей поджелудочной железы базируются не только на их клинико-морфологических характеристиках, но и на результатах иммуногистохимических (ИГХ) исследований.
Среди доброкачественных опухолей поджелудочной железы аденомы встречаются чаще всего. Различают следующие их варианты: ацинарная — по своему строению напоминает концевые отделы экзокринных желез, протоковая — из эпителия протоков и нейроэндокринные.
В целом клиническая картина зависит от размера, локализации и функциональной активности опухоли, чаще они бессимптомные, бывают случайными находками, в том числе операционными или аутопсийными. Зачастую подобные образования представлены цистаденомами, которые по мере увеличения размера могут достигать 20 см и более, прощупываются через переднюю брюшную стенку. Несмотря на значительный размер опухоли, общее состояние больного, как правило, длительное время остается удовлетворительным. Клинические проявления гормонально-активных опухолей обусловлены секрецией соответствующего гормона. По мере своего роста опухоль может сдавливать протоки поджелудочной железы и общий желчный проток, что приводит к развитию панкреатита, желтухи, холангита и других патологических состояний. Диагноз устанавливают на основании данных ультразвукового исследования (УЗИ) и компьютерной томографии (КТ) в сопоставлении с клинической картиной: минимальные клинические проявления имеют место даже при наличии опухоли большого размера без признаков роста при динамическом наблюдении. Окончательный диагноз устанавливается после гистологического исследования операционного материала.
Ацинарная аденома поджелудочной железы — это, как правило, кистозное эпителиальное образование, состоящее из клеток, по морфологии напоминающих ацинарные, с признаками продукции панкреатических ферментов. По данным литературы, это одно из самых редко встречающихся доброкачественных эпителиальных новообразований поджелудочной железы. Ацинарная аденома чаще локализуется в головке (63,8—87%), реже — в теле, еще реже — в хвосте железы. Величина данных опухолей варьирует от нескольких миллиметров до 10 см, растут они экспансивно, макроскопически имеют вид хорошо отграниченного узла мягкоэластической консистенции, розовато-белого цвета, могут иметь соединительнотканную капсулу. Ацинарная аденома состоит из кист различного размера и в разной степени расширенных пространств по типу ацинусов, выстланных базально ориентированными клетками с мономорфными ядрами, гранулярной цитоплазмой. Апикально цитоплазма клеток опухоли эозинофильна, в базальных отделах — базофильна, что напоминает неопухолевые ацинарные клетки. Просвет кист может содержать сгущенный эозинофильный ферментативный секрет. При ИГХ-исследовании клетки опухоли экспрессируют цитокератины, панкреатические ферменты (трипсин, химотрипсин, липазу), негативны к нейроэндокринным маркерам.
В Рязанском онкодиспансере в феврале 2011 г. последовательно были диагностированы два случая ацинарной аденомы поджелудочной железы. Оба случая проконсультированы в патологоанатомическом отделении МНИОИ им. П.А. Герцена.
1. Больная М., 71 год, поступила в онкодиспансер после планового УЗИ органов брюшной полости, при котором в головке поджелудочной железы было обнаружено образование 41 мм в диаметре. Пациентке выполнена операция в объеме панкреатодуоденальной резекции. Во время операции проведено срочное гистологическое исследование — образование признано доброкачественной эпителиальной опухолью.
Макроскопически операционный материал был представлен фрагментом тонкой кишки длиной 11 см с прилежащим фрагментом поджелудочной железы размером 7×4×3 см, в толще ткани железы обнаружен инкапсулированный опухолевый узел диаметром 4 см, на разрезе бледно-серого цвета, дольчатого вида. В прилежащей жировой клетчатке лимфатические узлы не определялись.

При микроскопии: опухоль представлена кистозными и железистыми структурами по типу ацинусов, выстланных кубическим и уплощенным эпителием, содержащих в просвете аморфные массы (рис. 1). Рисунок 1. Ацинарная аденома поджелудочной железы. Окраска гематоксилином и эозином. ×100. Эпителиальные клетки расположены на базальной мембране, сохраняют комплексность и полярность. Железистые структуры разделены волокнистой соединительной тканью, в которой расположены сосуды. Опухоль четко отграничена от ткани поджелудочной железы тонкой соединительнотканной капсулой.
Заключение: доброкачественная железистая опухоль головки поджелудочной железы, имеющая строение ацинарной аденомы; по краям резекции опухолевого роста не выявлено; признаки гиперплазии исследованных лимфатических узлов.
Для исключения нейроэндокринной природы опухоли было проведено ИГХ-исследование с антителами к ОЦК, СД-56, СД-99, синаптофизину, хромогранину А, NSE и Ki-67. Реакция с ОЦК положительная в клетках опухоли (рис. 2). Рисунок 2. Ацинарная аденома поджелудочной железы, экспрессия ОЦК клетками опухоли. ИГХ-реакция ДАБ. ×100. СД-56, СД-99, NSE, синаптофизин и хромогранин А опухолевые клетки не экспрессируют. Реакция с Ki-67 положительна менее чем в 1% клеток опухоли, что свидетельствует о низкой пролиферативной активности (рис. 3). Рисунок 3. Ацинарная аденома поджелудочной железы, экспрессия Ki67 в клетках опухоли. ИГХ-реакция ДАБ. ×200.
Заключение: иммунофенотип соответствует ацинарной аденоме.
2. Больная К., 58 лет, поступила в онкодиспансер после планового УЗИ органов брюшной полости, при которой в поджелудочной железе обнаружено образование. Пациентке выполнена резекция тела и хвоста поджелудочной железы со спленэктомией (в связи с повреждением капсулы селезенки).
Макропрепарат представлен фрагментом поджелудочной железы (тело и хвост) длиной 15 см с прилежащей клетчаткой и селезенкой размером 8×5×4 см с разрывом капсулы по нижнему полюсу. В теле железы локализуется опухоль размером 9×5×4 см, на разрезе серого цвета, плотная, дольчатого вида с четкой капсулой. В прилежащей жировой клетчатке лимфатические узлы не определяются.
При микроскопическом исследовании картина аналогична описанной выше (случай №1).
Заключение: ацинарная аденома тела поджелудочной железы.
Учитывая, что препараты поступили в отделение с интервалом в 2 нед, диагноз ацинарной аденомы во втором случае не вызвал сомнений и ИГХ-исследование не проводилось.
Оба представленных случая ацинарной аденомы поджелудочной железы явились диагностическими находками, протекали без существенных клинических проявлений. Окончательный диагноз был установлен после гистологического исследования операционного материала.
Респираторный отдел легких. Строение респираторного отдела легких.
Структурно-функциональной единицей респираторного отдела легких является ацинус. Этим термином обозначают систему, состоящую из респираторных бронхиол 1-3-го порядков, альвеолярных ходов и альвеолярных мешочков. Между воздухом внутри альвеол и кровью, находящейся в капиллярах, оплетающих альвеолярную стенку, происходит газообмен.
Ацинус начинается респираторной бронхиолой 1-го порядка, которая в свою очередь дихотомически делится на респираторные бронхиолы 2-го, а затем 3-го порядков. Последние разветвляются на альвеолярные ходы, заканчивающиеся двумя-тремя сферическими альвеолярными мешочками. Численность альвеол последовательно возрастает и, если в стенках репираторных бронхиол еще имеются участки, состоящие из однослойного кубического эпителия и тонкой прослойки коллагеновых волокон и гладких миоцитов, где не происходит газообмен, то альвеолярные мешочки имеют стенку, сплошь состоящую из альвеол. По форме ацинус напоминает пирамиду или конус, в вершину, которого входит респираторная бронхиола. 12-18 ацинусов образуют легочную дольку. Ацинусы отделены друг от друга соединительнотканными прослойками.
Важнейшим структурным элементом легочного ацинуса является альвеола. Средний диаметр альвеол у взрослого человека 260-290 мкм. Альвеолы тесно прилежат друг к другу. Между ними определяются тонкие межальвеолярные перегородки, по которым проходят кровеносные капилляры. Имеются также эластические и ретикулярные волокна, оплетающие альвеолы, и придающие им упругость. В перегородках между альвеолами обнаруживаются отверстия диаметром 10-15 мкм. Это так называемые альвеолярные поры Кона, создающие возможность проникновения воздуха из одной альвеолы в другую. Эластический каркас и гладкие мышечные клетки в легочных ацинусах участвуют в регуляции поступления воздуха в альвеолы.
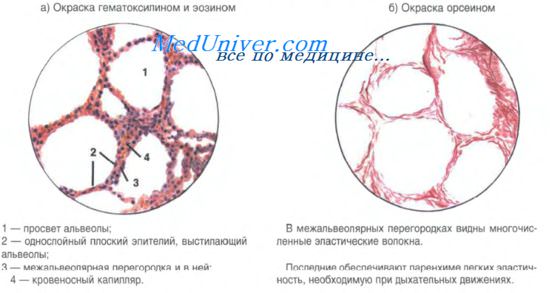
Изнутри альвеолы выстланы однослойным плоским эпителием. Альвеолярная выстилка включает несколько клеточных дифферонов. Респираторные плоские эпителиоциты (альвеолоциты 1-го типа) — это полигональной формы клетки. В них различают две части: более толстую ядросодержащую и тонкую безъядерную (пластинчатую). Околоядерная часть имеет толщину около 5 мкм. Толщина пластинчатой части не более 0,2 мкм. Органеллы располагаются около ядра. Через пластинчатую часть цитоплазмы происходит газообмен, и в ней много пиноцитозных пузырьков. Респираторные эпителиоциты лежат на тонкой базальной мембране. Своей пластинчатой частью они прилежат к базальным участкам эндотелиальных клеток кровеносных капилляров. В этих участках базальные мембраны альвеолярного эпителия и эндотелия могут сливаться, благодаря чему аэрогематический барьер (барьер "воздух-кровь") оказывается чрезвычайно тонким (около 0,5 мкм). Это благоприятствует газообмену. Обмен газов между альвеолярным воздухом и кровью происходит путем диффузии в связи с разницей парциального давления О2 и СО2 в альвеолярном воздухе и в крови. Респираторные эпителиоциты являются высокоспециализированными клетками, утратившими способность делиться митозом.
Аэрогематическим барьером называется комплекс элементов стенки альвеолы и кровеносного капилляра, который преодолевают газы (О2и СО2 в процессе внешнего дыхания. В его состав входят слой сурфактанта, цитоплазматические пластинчатые части респираторных эпителиоцитов, общая с эндотелиоцитами базальная мембрана, аблюминальная и люминальная поверхности эндотелиоцитов гемокапилляра, стенка эритроцита (если слияния базальных мембран нет, то структура барьера усложняется — между двумя базальными мембранами располагается тонкая соединительнотканная прослойка).
Большие эпителиоциты являются одновременно секретирующими и пролиферирующими клетками. Между респираторными и большими эпителиоцитами образуются межклеточные соединения типа плотных контактов. Кроме описанных выше клеток, в стенке альвеол и в гипофазе обнаруживаются альвеолярные макрофагоциты. Это производные моноцитов. Очищая вдыхаемый воздух, альвеолярные макрофаги выполняют функцию защиты.
Иннервация легких. К бронхиальному дереву подходят симпатические и парасимпатические нервы. Нервные импульсы, идущие по парасимпатическим нервным проводникам (ветви блуждающего нерва), вызывают сокращение гладких мышц бронхов, а раздражение симпатических волокон, напротив, вызывает расслабление мышц.
Возрастные изменения. В постнатальном периоде прогрессирующе увеличивается дыхательная поверхность легких. В пожилом возрасте происходит снижение газообменной функции в связи с постепенным разрастанием соединительнотканной стромы легких.
Регенерация легких связана в основном с явлениями компенсаторной гипертрофии клеток альвеолярной выстилки. Показано, что большие эпителиоциты 2-го типа могут делиться митозом. Регенерация легких связана также с пролиферацией и миграцией клеток бронхиального эпителия, который врастает в зону повреждения и участвует в формировании альвеолоподобных структур.
- Вернуться в оглавление раздела "гистология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эндокринная часть поджелудочной железы. Регенерация поджелудочной железы.
Островки состоят из эпителиальных клеток — панкреатических эндокриноцитов, или инсулоцитов. Величина островков, их форма и число входящих в состав клеток очень различны. Общее количество островков в поджелудочной железе достигает 1-2 млн. Средний размер островка 0,1-0,3 мм. Общий объем эндокринной части составляет около 3% всего объема железы. Островки пронизаны кровеносными капиллярами, окруженными перикапиллярным пространством. Эндотелий капилляров имеет фенестры, облегчающие поступление гормонов от инсулоцитов в кровь через перикапиллярное пространство.
В островковом эпителии различают 5 видов клеток: А-клетки, В-клетки, D-клетки, ВИП-клетки, РР-клетки.
А-клетки (альфа-клетки, или ацидофильные инсулоциты) — это крупные округлые клетки с бледным крупным ядром и цитоплазмой, содержащей ацидофильные гранулы. Гранулы обладают и аргирофилией. В состав этих гранул входит гормон глюкагон, расщепляющий гликоген и повышающий содержание сахара в крови.
А-клетки рассеяны по всему островку, образуя нередко небольшие скопления в центральной части. Они составляют около 20-25% от всех инсулоцитов.
В-клетки (бета-клетки, или базофильные инсулоциты) имеют кубическую или призматическую форму, крупное темное, богатое гетерохроматином ядро. Доля В-клеток достигает 70-75% от общего числа инсулоцитов. В цитоплазме В-клеток накапливаются осмиофильные гранулы, содержащие гормон инсулин. Инсулин регулирует синтез гликогена из глюкозы. При недостатке продукции инсулина глюкоза не превращается в гликоген, содержание ее в крови повышается и создаются условия для развития заболевания, называемого сахарным диабетом.
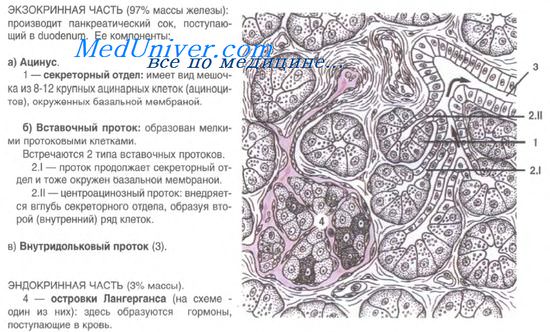
D-клетки (дельта-клетки, или дендритические инсулоциты) составляют 5-10% среди всех островковых клеток. Форма их иногда звездчатая с отростками. В цитоплазме определяются гранулы средних размеров и плотности. В гранулах накапливается гормон соматостатин. Он тормозит секрецию инсулина и глюкагона, снижает продукцию ряда гормонов желудочно-кишечного тракта — гастрина, секретина, энтероглюкагона, холецистокинина и др., подавляет секрецию соматотропного гормона в гипофизе.
ВИП-клетки (аргирофильные клетки) встречаются в островках в небольшом количестве. В цитоплазме выявляются плотные аргирофильные гранулы, содержащие вазоактиеный интестиналъный полипептид. Он обладает выраженным сосудорасширяющим дейтвием, снижает кровяное давление, угнетает секрецию соляной кислоты в желудке, стимулирует выделение глюкагона и инсулина.
РР-клетки — полигональной формы инсулоциты, расположенные преимущественно по периферии островка. Количество их — 2-5% от общего числа клеток островка. В цитоплазме РР-клеток выявляются мелкие гранулы, содержащие панкреатический полипептид. Основная роль панкреатического полипептида в организме — регуляция скорости и количества экзокринной секреции поджелудочной железы и желчи в печени. Таков клеточный состав островкового эпителия, представляющего собой мозаику дивергентно развивающихся клеточных дифферонов.
В дольках поджелудочной железы встречаются еще ацинозно-инсулярные клетки, в цитоплазме которых одновременно содержатся гранулы, характерные как для ацинозных, так и для островковых клеток.
Ткани поджелудочной железы иннервируют блуждающий и симпатический нервы. В интрамуральных вегетативных ганглиях находятся холинергические и пептидергические нейроны, волокна которых заканчиваются на клетках ацинусов и островков. Между нервными клетками ганглиев и островковыми клетками устанавливается тесная связь с образованием нейроинсулярных комплексов.
С возрастом в поджелудочной железе постепенно уменьшается количество островков. В островках наблюдаются закономерные возрастные изменения клеточных взаимоотношений, заключающиеся в быстрой смене после рождения преобладания А-клеток над В-клетками на преобладание В-клеток над А-клетками у взрослых. Затем происходит постепенное увеличение количества А-клеток, которое наряду с одновременным, хотя и незначительным, уменьшением числа В-клеток приводит нередко в пожилом и особенно старческом возрасте вновь к преобладанию А-клеток над В-клетками.
Регенерация поджелудочной железы. В эмбриогенезе островки растут благодаря пролиферации исходных клеток-предшественниц и их дивергентной дифференцировке в соответствующие клеточные диффероны. У взрослых физиологическая регенерация ацинозных и островковых клеток происходит в основном путем внутриклеточного обновления органелл. Митотическая активность клеток в связи с высокой специализацией низкая. После резекции части или повреждения органа наблюдается некоторое повышение уровня пролиферативной активности клеток ацинусов, протоков и островков, последующее образование новых ацинусов. Однако ведущей формой регенерации экзокринной части железы является регенерационная гипертрофия.
Восстановительные процессы в эндокринной части железы происходят за счет пролиферативной активности инсулоцитов и клеток эпителия протоков путем ацино-инсулярной трансформации.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Вторичные опухоли предстательной железы. Опухолеподобные процессы предстательной железы.
Вторичные опухолевые поражения предстательной железы чаще всего обусловлены непосредственным прорастанием в нее злокачественных опухолей (преимущественно рака) мочевого пузыря, намного реже—прямой кишки, семенных пузырьков, простатической части уретры. Метастазы в предстательную железу опухолей отдаленных органов возникают очень редко. Среди источников их наиболее часто оказываются лимфомы, рак легкого, меланома кожи. Иногда метастазы имитируют первичную опухоль предстательной железы.
Узловая гиперплазия (дисгармональная гиперпластическая простатопатия), часто именуемая практическими врачами также аденомой или гипертрофией предстательной железы, является одним из самых распространенных заболеваний мужчин пожилого возраста. В зависимости от преобладающего вида пролиферирующей ткани различают аденоматозную, фиброзную (или мышечно-фиброзную), мышечную несмешанную формы узловой гиперплазии. Чаще всего встречается аденоматоэная форма, при которой железистая ткань обычно представлена ацинарными структурами, окруженными фиброваскулярной стромой, часто с примесью гладких мышечных клеток.
Намного реже можно наблюдать выраженную папиллярную гиперплазию, внутриацинарную криброзную гиперплазию. Эпителий обычно высокий призматический, в кистозко расширенных железах—кубический, со светлой цитоплазмой, мономорфными округлыми базалько расположенными ядрами. Под ним можно видеть слой базальных клеток с более или менее уплощенными или овоидными ядрами. Во внутриацинарных папиллярных структурах эпителиальные клетки иногда имеют угловатые ядра.
Узлы (или узелки) из фиброзной, фиброваскулярной, мышечно-фиброзной или мышечной ткани могут залегать как в самой ткани предстательной железы, так и в ткани зоны аденоматозной гиперплазии. Чрезвычайно редко отмечается филлоидный тип гиперплазии, сходный с таковым в молочной железе. При наличии множественных узлов гиперплазии они могут иметь разное строение. Окружающая ткань предстательной железы оттесняется и сдавливается узлами гиперплазии с развитием атрофии паренхимы органа. При этом деформированные мелкие ацинусы с базофильным эпителием могут приобретать сходство с мелкоацинарной аденокарциномой.
Малигнизация железистой ткани узловой гиперплазии наблюдается редко, чаще отмечают врастание в нее рака из окружающей ткани самой предстательной железы.
Другие типы гиперплазии. Постатрофическую гиперплазию в виде разрастания мелких ацинусов с некоторым атипизмом эпителия рассматривают как проявление регенераторного процесса.
Фокальная интраацинарная гиперплазия эпителия в виде подушкообразных утолщений или папиллярных структур может возникать в кистозно расширенном ацинусе на фоне его уплощенной эпителиальной выстилки. Эти очаги рассматривают как выражение вторично возобновившейся гиперпластической активности эпителия после инволюции. Особое место занимает атипическая интраацинарная пролиферация эпителия с формированием папиллярных структур или полиморфных криброзных структур, не имеющих собственной стромы. Эти изменения чаще всего обнаруживаются поблизости с раковой опухолью и могут быть отнесены к тяжелой форме дисплаэии эпителия (предраковое изменение).
Гиперплазия базальных (резервных) клеток проявляется в виле интраацинарного и или интрадуктального их разрастания. Клетки с мономорфными гинерхромными овоидными ядрами и узким ободком цитоплазмы образуют многорядные пролифераты, суживая или даже обгурируя просветы ашгаусов и или протоков. Митозы встречаются редко.
Плоскоклеточная метаплазия ашшарного или протокового эпителия может быть выявлена по периферии инфарктов, очагов хронического продуктивного простатита, но чаще после эстрогенотерашга. Отличия этих изменений от плоскоклеточного рака указаны выше.
Другие опухолеподобные процессы. Кисты врожденного типа чаще всего связывают с пороками развития простатической маточки, парамезонефраль-ною протока. Эпителиальная выстилка чаще всего бывает представлена кубическим или уплощенным эпителием, реже переходным или многослойным плоским. Кисты приобретенные могут бьпь ретенционными или эхинококковыми.
Хронический простатит с преобладанием лимфоцитарной инфильтрации иногда приходится дифференцировать от злокачественной лимфомы или рака. В отличие от них при простатите инфильтраты часто множественные, с примесью плазматических клеток, лейкоцитов, скоплений пенистых макрофагов. Различные формы гранулематоэного простатита (полиморфно-клеточный с гигантскими клетками Пирогова Лат ханса, эозинофильный) чаще имитируют опухолевый рост клинически, но не микроскопически. Малакоплакия гистологически не отличается от соответствующего гранулематозною процесса в мочевом пузыре.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Аденоз молочной железы – форма фиброзно-кистозной мастопатии, сопровождающаяся разрастанием железистой ткани груди. Проявляется болями и нагрубанием груди, формированием в ней плотных участков, появлением выделений из соска. Диагностика аденоза основана на сборе жалоб и анамнеза, данных осмотра и пальпации груди, дополнительных методах исследования (УЗИ и рентгенография молочных желез, определение уровня гормонов, цитологическое исследование отделяемого из соска и биопсия). Лечение заболевания зависит от его формы и включает консервативную терапию (назначение гормонов) или оперативное вмешательство.
МКБ-10
Общие сведения
Аденоз относится к доброкачественным образованиям молочных желез гормонально-зависимого характера, что подтверждается возникновением симптомов во второй фазе цикла. Синонимами аденоза являются «фиброзирующий аденоз», «гиперплазия миоэпителия» или «лобулярный склероз».
Аденозом страдают женщины репродуктивного возраста – распространенность заболевания в возрастной группе 30–40 лет составляет 30–70%. У женщин с гинекологическими заболеваниями частота аденоза увеличивается до 100%. Данное состояние может развиваться у девочек в период установления менструаций и у женщин в первом триместре беременности, что считается физиологичным, так как все проявления аденоза исчезают самостоятельно через некоторое время, после стабилизации гормонального фона.

Причины аденоза молочной железы
Главной и единственной причиной патологии является гормональный дисбаланс – недостаток прогестерона и избыток эстрогенов. К этиологическим факторам, вызывающим гормональный сбой, относятся:
- Ожирение. Жировая ткань синтезирует эстрогены. При излишнем весе увеличивается продукция эстрогенов, что приводит к относительной гиперэстрогении (уровень прогестерона остается в норме).
- Самопроизвольные и искусственные аборты. Прерывание беременности, особенно на больших сроках (15–22 недели), провоцирует резкую гормональную перестройку и срыв компенсаторных механизмов. Уровень половых гормонов не сразу приходит в норму, что дает толчок к развитию эндокринных проблем, в частности, аденоза.
- Поздняя беременность. У женщин старше 35 лет функции яичников угасают. Наступившая беременность активизирует работу яичников, что вызывает послеродовый сбой в синтезе эстрогенов и прогестерона и гормональный срыв.
- Послеродовая агалактия. Агалактия свидетельствует о недостатке прогестерона, который отвечает за развитие и дифференцировку клеток паренхимы молочных желез, и избытке эстрогенов. При гиперэстрогении разрастается строма желез, недостаток прогестерона приводит к бесконтрольному росту железистого эпителия.
- Отказ от кормления грудью. Повышение концентрации пролактина на фоне отсутствия кормления грудью вызывает застой молока в протоках. Происходит их закупорка и расширение, что ведет к структурным изменениям - образованию кист.
- Бесконтрольный прием КОК. Прием гормональных таблеток без учета индивидуальных особенностей и соблюдения схемы вызывает гормональный дисбаланс и развитие диспластических процессов в груди.
Аденоз грудных желез чаще возникает у пациенток с гинекологической патологией (гиперплазией эндометрия, опухолями яичников, миомой матки, эндометриозом), которые также развиваются на фоне гиперэстрогении. Триггерами, запускающими гормональные нарушения, могут выступать соматические заболевания (артериальная гипертензия, болезни поджелудочной железы и печени), хронические стрессы, сексуальные расстройства, нарушенная экология, курение.
Патогенез
В грудных железах происходят циклические изменения, которые регулируются гормонами: гипоталамус-рилизинг-факторами, ФСГ и ЛГ, эстрогенами, пролактином, хорионическим гонадотропином, андрогенами, глюкокортикоидами, прогестероном, гормонами щитовидной и поджелудочной желез. Аденоз сопровождается абсолютной и относительной гиперэстрогенией, которая сочетается с дефицитом прогестерона. Эстрогены обеспечивают разрастание млечных ходов за счет избыточной пролиферации клеток и гиперплазию стромы путем активации фибробластов. К функциям прогестерона относится снижение числа эстрогеновых рецепторов на клеточных мембранах и уменьшение влияния эстрогенов на органы-мишени (грудь, матка).
При недостатке прогестерона снижается дифференцировка образовавшихся в значительном количестве клеток железистого эпителия и коллагена, тормозится блокировка пролиферативных процессов. В результате деление клеток становится бесконтрольным, нарушается процесс торможения пролиферации в тканях желез. Это приводит к структурным и морфологическим перестройкам: разрастанию и отеку внутридольковой соединительной ткани, активации пролиферации железистого эпителия в молочных ходах, что вызывает их закупорку, расширение и образование кист.
Классификация
В маммологии применяется единая классификация аденоза груди. Систематизация образований проводится по площади поражения тканей железы и гистологическому строению аденоза. По распространенности патологического образования выделяют 2 формы:
- Очаговую (локальную). В железе формируется подвижное крупное образование шаровидной или дискообразной формы. Узел имеет фиброзную капсулу и состоит из долек.
- Диффузную. В молочной железе возникает несколько участков уплотнений, форма и границы которых размыты. Образование разрастается неограниченно и располагается неравномерно.
По типу разросшихся клеток эпителия паренхимы железы различают:
- Склерозирующий аденоз. Сопровождается пролиферацией ацинусов (участки долек желез) с сохранением целостности их эпителиального и миоэпителиального слоев. Несмотря на сдавление ацинусов фиброзной тканью, их конфигурация сохраняется.
- Апокриновый аденоз. Характеризуется апокриновой метаплазией эпителия (переходом кубоидальных эпителиальных клеток в цилиндрические с появлением апокриновой секреции). По гистологическому строению апокриновый аденоз похож на инфильтрующий рак, но природа его доброкачественная.
- Протоковый аденоз. Отличается расширенными молочными протоками, которые ограничены клетками эпителия с цилиндрической метаплазией. Схож со склерозирующим аденозом.
- Микрогландулярный аденоз. Сопровождается диффузным и беспорядочным разрастанием мелких протоков. Склероз и сдавление тканей желез отсутствуют.
- Аденомиоэпителиальный аденоз. Данная форма встречается очень редко и сочетается с формированием аденоэпителиомы груди. Является очаговым аденозом.
Симптомы аденоза молочной железы
Симптоматика аденоза схожа с клинической картиной мастопатии. В зависимости от формы болезни различается выраженность тех или иных признаков. К общим симптомам аденоза относятся мастодиния (болезненность, нагрубание желез, их повышенная чувствительность), боли, усиливающиеся накануне менструации, появление отделяемого из сосков, болезненность груди при пальпации.
Локальная форма
При локальной форме патологии в железе прощупывается плотное, подвижное уплотнение с дольчатой структурой, не спаянное с окружающими тканями и имеющее четкие границы. Боль во время пальпации, истечение слизи/молока из соска, деформация кожи и увеличение подмышечных лимфоузлов не наблюдаются.
Диффузная форма
Для диффузной формы заболевания характерна разлитая болезненность железы (боль охватывает всю железу), грудь набухает перед менструацией, из соска появляется желтоватое или бесцветное отделяемое. Диффузный аденоз характеризуется образованием в железе нескольких узелков разного размера, которые не имеют четких границ и определенной формы. Рядом расположенные узелковые образования сливаются, что создает иллюзию опухоли значительных размеров. Пальпация груди болезненна, регионарные лимфоузлы не увеличены.
Осложнения
Поздние диагностика и терапия аденоза увеличивают риск появления осложнений (воспалительных заболеваний груди, деформации железы, образования кист в тканях груди и папиллом в млечных протоках). Согласно последним научным данным, доказана связь заболевания с раком молочной железы, вероятность которого возрастает при аденозе в 5 раз. Частота озлокачествления новообразования зависит от степени пролиферации эпителиальных клеток. Непролиферативные формы малигнизируются в 0,86%, в случае умеренной пролиферации рак груди развивается в 2,5%, аденоз с тяжелой степенью пролиферации клеток трансформируется в злокачественную опухоль в 32% случаев.
Диагностика
Для диагностики аденоза необходима консультация маммолога. Врач производит сбор анамнеза и жалоб, уточняет наличие сопутствующих соматических и гинекологических заболеваний, осуществляет физикальный осмотр и пальпацию груди. При необходимости к обследованию женщины привлекаются гинеколог, онколог и эндокринолог. При подозрении на аденоз назначаются инструментальные и лабораторные методы диагностики:
- Маммография. Позволяет определить локализацию процесса, его распространенность и границы. На рентгенограмме видны множественные, с размытыми границами и неправильными формами тени, соответствующие участкам разросшихся долек.
- УЗИ молочных желез. Помогает установить расположение пораженного участка железы, его границы, консистенцию и размеры. С помощью УЗИ выявляется повышенная плотность желез у молодых женщин, кисты небольших размеров (до 3 мм), образовавшиеся при закупорке протоков, оценивается состояние регионарных лимфатических узлов.
- Гормональные исследования. Определяется содержание половых гормонов, пролактина, ФСГ, ЛГ. По показаниям исследуется концентрация гормонов щитовидной железы и надпочечников.
- Гистологическое, цитологическое исследование. Выполняется цитограмма отделяемого из железы, пункционная биопсия подозрительного участка груди. В мазке определяется наличие/отсутствие атипичных клеток, в биопсийном материале оценивается степень пролиферации клеток образования.
Также назначаются клинические анализы крови и мочи, биохимия крови (сахар, печеночные ферменты и прочее) с целью выявления соматической патологии. Дифференциальную диагностику аденоза проводят с другими диспластическими процессами молочной железы (аденомой, фиброаденомой, кистой) и раком груди.
Лечение аденоза молочной железы
Тактика лечения аденоза (консервативная терапия или хирургическое вмешательство) определяется его формой и характером течения болезни.
При диффузной форме патологии назначается консервативное лечение, которое включает прием седативных средств, витаминов (А, Е, аскорбиновой кислоты, Р, группы В), минералов и гормональных препаратов. При легкой форме заболевания используются монофазные комбинированные оральные контрацептивы курсом на 6 месяцев. При выраженной симптоматике аденоза показан прием гестагенов на протяжении не менее 3-х месяцев.
Больным рекомендуется пересмотреть рацион питания: ограничить животные жиры, углеводы, увеличить потребление свежих овощей и фруктов. При малоподвижном образе жизни необходимо повысить физическую активность и нормализовать вес, по возможности избегать стрессовых ситуаций.
В случае очаговой формы аденоза выполняется секторальная резекция железы – иссечение образования в пределах здоровых тканей со срочным гистологическим исследованием узла. С косметической целью разрез груди выполняется вокруг ареолы соска, после заживления раны остается малозаметный рубец.
Прогноз и профилактика
При проведении ранней диагностики и своевременном начале лечения прогноз для жизни и заболевания благоприятный. Профилактика аденоза включает предупреждение абортов, грамотный подбор гормональных контрацептивов, лечение гинекологических и эндокринных заболеваний, сохранение первой беременности и лактации не менее 6 месяцев, отказ от вредных привычек и ведение здорового образа жизни. Также следует регулярно проводить самообследование груди, каждые полгода посещать гинеколога, придерживаться правильного питания, планировать первую беременность до 30 лет.
Читайте также:

