Что такое аутоиммунные заболевания коллагенозы
Обновлено: 19.04.2024
Лейкопения – это снижение уровня лейкоцитов в периферической крови ниже 4000 в 1 мкл. Причиной данного состояния могут быть инфекционные, воспалительные аутоиммунные заболевания, генетические дефекты иммунной системы и пр. Клинически лейкопения проявляется повышенной восприимчивостью организма к различным инфекциям, однако может протекать абсолютно бессимптомно. Уровень лейкоцитов измеряется при заборе венозной либо капиллярной крови утром натощак. Для коррекции данного лабораторного отклонения проводится лечение основного заболевания.
Классификация
Низкий уровень белых кровяных телец может встречаться у абсолютно здоровых лиц – конституциональная безвредная лейкопения отмечается примерно у 2-5% людей. По происхождению патологические лейкопении разделяют на:
- Наследственные (первичные). Низкое содержание лейкоцитов обусловлено генетически детерминированными нарушениями образования и созревания клеток в красном костном мозге. К ним относятся нейтропения Костмана, наследственная нейтропения аутосомно-доминантного типа и т.д.
- Приобретенные (вторичные). Более распространенный вариант. Лейкопения развивается вследствие действия ионизирующего излучения, неблагоприятного эффекта лекарственных препаратов, биологических агентов (бактерий, вирусов) или факторов иммунной аутоагрессии.
По патогенезу (механизму развития) различают лейкопении, возникшие вследствие:
- Нарушения поступления лейкоцитов в кровь из костного мозга. Развитие лейкопении обусловлено повреждением кроветворных клеток либо неэффективным лейкопоэзом из-за дефектов митоза, созревания лейкоцитов. Наблюдается при длительном приеме цитостатических лекарственных препаратов, действии ионизируюшей радиации, генетических заболеваниях, выраженном дефиците витамина В12, фолиевой кислоты.
- Перераспределения лейкоцитов. Происходит изменение соотношения между циркулирующим и пристеночным пулом белых клеток крови в результате их скопления в расширенных капиллярах органов-депо. Встречается при шоковых состояниях.
- Сокращения времени пребывания в крови. Время присутствия в крови лейкоцитов может уменьшаться из-за их деструкции антителами (при аутоиммунных патологиях), токсическими факторами (при тяжелых инфекциях), чрезмерно активированными макрофагами (при гиперспленизме). Усиленное выведение белых клеток крови может наблюдаться при гнойных процессах – холангите, эндометрите.
В зависимости от типа клеток лейкоцитарного ряда выделяют следующие разновидности лейкопении:
- Нейтропении. Снижение содержания нейтрофилов меньше 47% от общего числа лейкоцитов. Наиболее частый вариант лейкопении. Встречается при вирусных, бактериальных инфекциях, токсическом действии медикаментов. Также возможны наследственные формы нейтропении.
- Лимфопении. Уменьшение уровня лимфоцитов ниже 19%. Характерно для вирусных инфекций, коллагенозов, гранулематозных процессов.
- Эозинопении. Содержание эозинофилов меньше 1%. Наблюдается при избыточной продукции гормонов коры надпочечников (болезнь/синдром Иценко-Кушинга). Эозинопения является индикатором неблагоприятного прогноза при септических процессах.
- Моноцитопения. Показатели моноцитов в лейкоцитарной формуле опускаются ниже 2%. Встречается при острых инфекциях, длительном приеме глюкокортикоидов.
- Агранулоцитоз. Редкое тяжелое жизнеугрожающее состояние, характеризующееся полным или почти полным исчезновением нейтрофилов в крови (ниже 0,75х10^9/л). Наблюдается при приеме миелотоксичных лекарств (цитостатиков, тиреостатиков, некоторых НПВС), действии радиации.

Причины лейкопении
Инфекции
Одна из наиболее распространенных причин лейкопении – вирусные и генерализованные бактериальные инфекции. Патогенез снижения уровня лейкоцитов может быть различным – непосредственное повреждение клеток лимфотропными вирусами (ВИЧ, Варицелла-Зостер, корь), подавление образования в костном мозге, усиленная их потеря с экссудацией.
- Вирусные инфекции. Лейкопения развивается преимущественно за счет снижения содержания лимфоцитов (лимфопения). При инфекционном мононуклеозе, гриппе, вирусных гепатитах лейкоциты снижаются незначительно и быстро возвращаются к норме после выздоровления. При ВИЧ-инфекции уровень лимфоцитов нередко достигает нуля на стадии СПИДа. Даже после лечения значения лейкоцитов могут сохраняться низкими, так как препараты для терапии ВИЧ сами по себе способны вызвать лейкопению.
- Бактериальные инфекции. Лейкопения встречается только при тяжелых генерализованных инфекциях (менингококцемия, риккетсиозы, перитонит). Падение числа лейкоцитов является одним из критериев для диагностирования септического состояния и синдрома системного воспалительного ответа. Наблюдается в основном нейтропения, ее степень коррелирует с тяжестью заболевания. Регресс наступает практически сразу после проведения антибактериальной терапии.
Прием лекарственных препаратов
К развитию лейкопении способен привести широкий спектр лекарственных средств. Известно два основных механизма лекарственно-индуцированной лейкопении: токсическое повреждение костного мозга, ведущее за собой нарушение кроветворения, и образование иммунных комплексов, в результате чего вырабатываются антитела, атакующие собственные лейкоциты макроорганизма.
Лейкопения возникает в среднем на 15 сутки от начала приема лекарства. Степень тяжести может быть самой различной – от незначительного снижения количества белых кровяных клеток до агранулоцитоза. В связи с поражением всех 3-х ростков гемопоэза часто встречается сочетание с анемией и тромбоцитопенией (панцитопения). В большинстве случаев достаточно отмены лекарственного препарата. При развитии агранулоцитоза может потребоваться применение колониестимулирующих факторов. Медикаменты, наиболее часто вызывающие лейкопению:
- Цитостатики: циклофосфамид, хлопамбуцил, метотрексат.
- Тиреостатики: пропилтиоурацил, мерказолил.
- Нестероидные противовоспалительные средства: анальгин, амидопирин.
- Антибактериальные средства: левомицетин, сульфаниламиды.
- Противовоспалительные ЛС: D-Пеницилламин, сульфасалазин.
- Антипсихотические ЛС (нейролептики): аминазин, хлорпромазин.
- Противосудорожные ЛС: карбамазепин, диазепам.
Аутоиммунные воспалительные заболевания
Причиной лейкопении могут быть аутоиммунные заболевания. В этих случаях преимущественно снижаются лимфоциты и нейтрофилы. Существует два основных патогенетических механизма аутоиммунной лейкопении – образование антилейкоцитарных антител и снижение экспрессии на мембранах иммунных клеток специальных белков (CD55, CD59), которые защищают клетки от цитолиза. Лейкопения обычно умеренная, регрессирует во время ремиссии или под влиянием патогенетического лечения. Лейкопенический синдром характерен для следующих патологий:
- Заболевания суставов: ревматоидный артрит, синдром Фелти.
- Диффузные болезни соединительной ткани (коллагенозы): системная красная волчанка, синдром Шегрена.
- Демиелинизирующие заболевания: рассеянный склероз.
- Системные васкулиты: гранулематоз с полиангиитом, неспецифический аортоартериит Такаясу.
- Воспалительные заболевания кишечника (ВЗК): неспецифический язвенный колит, болезнь Крона.
Болезни крови
Механизмов лейкопении при гематологических патологиях несколько – замещение кроветворной ткани злокачественными клетками, фиброзной или жировой тканью, синтез антилейкоцитарных антител, дефицит некоторых химических элементов для гранулоцитопоэза (железа, цианкобаламина, фолиевой кислоты):
- Онкогематологические заболевания. Лейкопенией, вплоть до агранулоцитоза, могут дебютировать острые лейкозы (алейкемическая форма) – такое начало заболевания встречается примерно в 20% случаев. Почти всегда в анализе крови дополнительно выявляются тромбоцитопения и анемия. Лейкопения характерна для лимфогранулематоза (лимфомы Ходжкина). Уровень лейкоцитов нередко остается на низком уровне и после лечения.
- Гемолитические анемии. При аутоиммунных гемолитических анемиях, гемоглобинопатиях, наследственном микросфероцитозе возможна умеренная нейтропения. Примечательно, что падение уровня лейкоцитов происходит вне криза. Период гемолитического криза, напротив, сопровождается небольшим лейкоцитозом.
- Дизэритропоэтические анемии. При апластической анемии, а также длительно протекающей недостаточности витамина В12 и фолиевой кислоты из-за угнетения функционирования всех ростков кроветворения наблюдается панцитопения. Лейкопения при железодефицитной анемии развивается только при крайне выраженном дефиците железа и носит умеренный характер.
Лучевая болезнь
Действие ионизирующей радиации неблагоприятно сказывается на всем организме человека. В первую очередь и сильнее всего страдают органы с высокой скоростью клеточного обновления, к которым относится костный мозг. Под влиянием гамма-лучей, имеющих высокую проникающую способность, гемопоэтические стволовые клетки утрачивают митотическую активность.
Наследственные формы лейкопений
К первичным лейкопениям относятся генетические заболевания, обусловленные мутациями генов, регулирующих созревание или дифференцировку лейкоцитов. Некоторые мутации приводят к изменению структуры лейкоцитарных антигенов, из-за чего они подвергаются аутоиммунному разрушению. В подавляющем большинстве случаев встречаются первичные нейтропении.
Дебют наступает с первых лет жизни. Часть из этих болезней имеет доброкачественную природу (циклическая нейтропения, первичная иммунная нейтропения, синдром «ленивых лейкоцитов», синдром Генслена), снижение количества нейтрофилов при них незначительное, присоединяющиеся инфекции протекают в легкой форме, лейкопения регрессирует самостоятельно.
Другие наследственные лейкопении часто сопровождаются инфекционными осложнениями, которые зачастую становятся фатальными уже в детском возрасте: болезнь Костмана (генетически детерминированный агранулоцитоз), первичные иммунодефициты (синдром Ди Джорджи, Вискотта-Олдрича), синдром Чедиака-Хегаси. При этих болезнях для восстановления нормальных значений лейкоцитов требуется специфическое лечение.
Другие причины
- Белковое голодание.
- Переливание крови или лейкоцитарной массы.
- Эндокринные расстройства: гипотиреоз, акромегалия, гиперкортицизм.
- Заболевания, протекающие с гиперспленизмом: цирроз печени, малярия, висцеральный лейшманиоз.
- Болезни накопления: болезнь Гоше, болезнь Ниманна-Пика.
Диагностика
Лейкопения выявляется при клиническом исследовании крови. Ввиду многообразия этиологических факторов данного отклонения при его обнаружении следует обратиться к врачу-терапевту для тщательного сбора анамнеза, физикального осмотра, назначения дополнительного обследования:
- Анализы крови. Выполняется подсчет лейкоцитарной формулы, определяется концентрация маркеров воспаления – СОЭ, СРБ, прокальцитонина. Изучается наличие аутоантител (антител к ДНК, цитоплазме нейтрофилов, аЦЦП).
- Выявление инфекционного возбудителя. Методом иммуноферментного анализа идентифицируются антитела к возбудителям (вирусам, бактериям). Для подтверждения ВИЧ-инфекции назначается иммуноблоттинг. Проводится бактериальный посев крови, мокроты, мочи.
- Биопсия. При подозрении на лейкоз выполняется морфологическое исследование костного мозга, при котором обнаруживается гиперплазия гранулоцитарного ростка, большое количество бластных клеток. Для диагностики лимфом проводится аспирационная биопсия увеличенного лимфатического узла, в биоптате выявляется лимфоцитарная гиперклеточность, разрастание коллагена.
- Генетические исследования. Для подтверждения наследственных форм лейкопений необходимо обнаружение мутаций методом полимеразной цепной реакции и цитогенетическими исследованиями.

Коррекция
Конституциональная лейкопения не требует никакого вмешательства. Если причиной развития данного отклонения стал лекарственный препарат, необходима срочная его отмена. При выраженном снижении лейкоцитов или агранулоцитозе прибегают к введению гранулоцитарного колониестимулирующего фактора (Г-КСФ) или инфузии донорских гранулоцитов. Главное условие успешности терапии – лечение основной патологии:
- Элиминация возбудителя. Для лечения гриппа применяется осельтамивир, для борьбы с ВИЧ-инфекцией – антиретровирусные препараты (зидовудин, саквинавир). При бактериальной инфекции назначаются антибиотики.
- Противовоспалительная терапия. Чтобы достигнуть ремиссии аутоиммунных заболеваний, используются глюкокортикостероиды, иммуносупрессанты, производные 5-аминосалициловой кислоты.
- Химиотерапия. При подтверждении онкогематологической патологии назначаются комбинации химиотерапевтических средств – хлорамбуцил, винкристин, этопозид.
- Пересадка костного мозга. В случае неэффективности химиотерапии гемобластозов, а также при тяжелых первичных нейтропениях выполняется трансплантация гемопоэтических стволовых клеток.
Прогноз
Некоторые формы первичных лейкопений характеризуются высоким уровнем смертности (50-90%) среди детей от инфекционных осложнений. При вторичных лейкопениях прогноз в большей степени зависит от основного заболевания. Поэтому при любом уровне снижения лейкоцитов в крови показано тщательное обследование, направленное на выяснение причины и своевременное начало лечения.
1. Патофизиология системы крови. Часть II. Нарушения в системе лейкоцитов/ Николаева О.В., Кучерявченко М.А., Шутова Н.А. и др. – 2016.
4. Синдромная диагностика и базисная фармакология заболеваний внутренних органов. Том 2/ под ред. Г.Б. Федосеева, Ю.Д. Игнатова. – 2004.
ASIA-синдром – это комплекс аутоиммунных реакций, развивающихся у предрасположенных лиц в ответ на введение в организм веществ-адъювантов. Включает такие нозологии как силиконоз, макрофагальный миофасциит, поствакцинальный синдром и др. Различные формы синдрома имеют общие проявления: артралгию, миалгию, васкулит, немотивированный субфебрилитет, хроническую усталость. Диагноз устанавливается на основании предшествующего анамнеза, актуальных клинических и биохимических показателей крови, наличия антител, данных HLA-типирования, биопсии. Лечение проводится НПВС, глюкокортикоидами, цитостатиками.
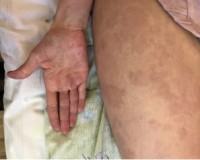
Общие сведения
ASIA-синдром (аутоиммунный синдром, вызванный адъювантами) впервые описан израильским иммунологом И. Шонфельдом в 2011 г. Второе, эпонимическое название патологии – синдром Шонфельда. Заболевание является предметом неутихающих дискуссий в научном сообществе. До настоящего времени не выработаны четкие критерии и не представлены неоспоримые доказательства его существования, а сама нозология не включена в МКБ-10. Шонфельда и его последователей обвиняют в антипрививочной пропаганде. Вместе с тем, описаны уже свыше 4 тыс. клинических случаев ASIA-синдрома, ему посвящены десятки статей и обсуждений на международных конгрессах.

Причины
Развитие ASIA-синдрома связывают с попаданием в организм адъювантов и возникновением гиперергического иммунного ответа. Адъюванты – это химические вещества, которые способны усиливать и пролонгировать антигенспецифическую иммунную реакцию, но не должны обладать собственной иммунореактивностью. В качестве таких соединений в современной фармакоиндустрии чаще всего используются соли аллюминия, кремния, сквален, силикон, многие другие компоненты, которые входят в состав вакцин, имплантов, филеров.
Согласно современным представлениям, ASIA-синдром развивается в результате наличия индивидуальной генетической предрасположенности, обусловленной носительством определенных мутаций HLA-генов (HLA-DRB1, HLA-DRB4, HLA-DQA1, HLA-DQB1 и пр.). Непосредственными причинами ASIA-синдрома называют:
- Иммунизацию. Вопрос о том, способны ли адъюванты вакцин вызвать аутоиммунные расстройства, является весьма спорным. С одной стороны, существуют исследования, достоверно опровергающие связь вакцинации с СКВ, рассеянным склерозом, СД , другими аутоиммунными патологиями. Между тем, сторонники ASIA-синдрома указывают на имеющуюся зависимость между вакцинацией против ВПЧ, гепатита В, гриппа и других инфекций и развитием аутоиммунных реакций.
- Имплантацию силиконовых протезов. Силиконовые импланты, используемые для увеличения груди, ягодиц, голеней, обладают определенной иммуногенностью, вызывая повышение уровня СРБ, РФ, провоспалительных факторов, аутоантител. Местные реакции представлены отторжением импланта или формированием фиброзной капсулы. В последние годы все чаще говорят о болезни грудных имплантов, хотя не все специалисты признают факт ее существования.
- Инъекции гиалуроновой кислоты. Описаны клинические наблюдения, когда, подкожное введение гиалуроновой кислоты самостоятельно или в комплексе с акриловыми гидрогелями вызывало развитие коллагенозов, аутоиммунных тиреопатий.
- Татуаж. Некоторые пигменты, содержащиеся в красителях для перманентного макияжа, способны вызывать системные реакции по типу васкулита, нефротического синдрома, гранулематозного поражения легких.
Патогенез
Механизм возникновения ASIA-синдром недостаточно изучен. Предполагается, что адъюванты вызывают иммунологические реакции несколькими путями. Будучи по своей природе не иммуногенными, эти вспомогательные вещества способствуют депонированию антигенов, с которыми они связаны, в месте введения и пролонгированному синтезу антител. Некоторые адъюванты стимулируют выработку провоспалительных факторов: цитокинов, хемокинов, интерлейкинов (IL-1β, IL-4, IL-6, IL-12, IL-18), которые поддерживают хроническую воспалительную реакцию.
Кроме этого, адъюванты способны индуцировать гуморальный иммунитет за счет стимуляции Th2-лимфоцитов. Наконец, адъюванты могут напрямую активировать главный комплекс гистосовместимости у генетически предрасположенных лиц.
Классификация
Термин «ASIA-синдром» объединяет в себе группу самостоятельных синдромов, имеющих собственные причины и клинические проявления. Общим критерием для них служит предполагаемая связь с введением в организм адъювантных веществ, провоцирующих аутоиммунную реакцию. Различают 5 форм ASIA-синдрома.
1. Силиконоз. Возникает менее чем у 1% в течение 6-15 лет после установки имплантата. Разрывы имплантов и миграция геля увеличивают риск возникновения аутоиммунных патологий. Соединения кремния, присутствующие в силиконовых протезах, могут способствовать развитию саркоидоза кожи и легких, ревматоидного артрита, болезни Шагрена, системного васкулита.
2. Поствакцинальный феномен. Связывают с присутствием в вакцинных препаратах таких адъювантов, как гидроксид алюминия. К проявлениям ASIA относят:
- синдром Гийена-Барре, развивающийся после введения противогриппозной и противогепатитной вакцины;
- ревматоидный артрит на фоне иммунизации против клещевого энцефалита, гриппа;
- СКВ, ассоциированную с иммунизацией против ВПЧ, краснухи, кори, туберкулеза, гепатита В.
3. Макрофагальный миофасциальный синдром. Считается, что всплеск заболеваемости макрофагальным миофасциитом ассоциирован с переходом к массовому введению вакцин в дельтовидную мышцу и четырехглавую мышцу бедра. Этим объясняется типичная локализация местного воспаления, специфические гистологические находки (отложения нанокристаллов гидроксида алюминия). Отмечается у пациентов после вакцинации по поводу гепатита А, В, столбняка.
4. Синдром «больного здания». О данном феномене говорят в том случае, если не менее 20% людей испытывают схожие патологические симптомы при нахождении в одном помещении. Чаще возникает у офисных работников, иногда у жильцов одного дома. Среди наиболее частых жалоб ‒ слезотечение, заложенность носа, зуд и сухость кожи, сонливость. Предполагают, что данный вариант ASIA-синдрома связан с химическими веществами, используемыми в системах для кондиционирования воздуха, возможно – антигенами плесени, фталатами.
5. Синдром войны в Персидском заливе. Впервые зафиксирован у военнослужащих, принимавших участие в боевых действиях в этом регионе в 1991 г. Причиной данного синдрома, сопровождавшегося мышечными и суставными болями, атаксией, цефалгией, лихорадкой, кожными высыпаниями, расстройствами ЖКТ, нарушениями сна, считают многократные вакцинации военных в сочетании с психологическим стрессом и повышенными физическими нагрузками.
Симптомы
Признаки ASIA-синдрома могут развиваться в широкие временные сроки – от 2-х дней до 20 и более лет после предполагаемого воздействия (иммунизации, аугментационной маммопластики, введения гиалуроновой кислоты, тутуажа). Ранние жалобы неспецифичны, включают необъяснимую слабость, персистирующий субфебрилитет, артралгии различной локализации или полиартрит, боли в мышцах и позвоночнике. В дальнейшем нарастает астения, может беспокоить бессонница, одышка.
Некоторые пациенты с различными вариантами ASIA-синдрома жалуются на появление геморрагической сыпи на коже, сухости во рту, выпадение волос, ломкость ногтей. Иногда присутствует феномен Рейно. Возможно развитие синдрома раздраженного кишечника. В поздние сроки может наблюдаться амнезия, когнитивное снижение, как следствие демиелинизации.
Отличительной особенностью ASIA-синдрома является регресс большинства клинико-лабораторных проявлений после удаления провоцирующего агента (силикона, пигмента и других).
Осложнения
От момента появления первых признаков синдрома Шонфельда до его диагностики проходят годы и десятилетия. Все это время больные получают неадекватное лечение, переносят частые госпитализации, страдают от снижения качества жизни. ASIA-синдром может приводить к манифестации различных аутоиммунных патологий: системного васкулита, ревматоидного артрита, СКВ, болезни Шегрена, рассеянного склероза. Длительное присутствие адъювантов в организме (например, силиконовых имплантов) сопровождается постоянной стимуляцией иммунных реакций, что является риск фактором возникновения псевдолимфомы, а также неходжкинской лимфомы.
Диагностика
Обследованием и наблюдением пациентов с проявлениями ASIA-синдрома занимаются врачи-иммунологи, ревматологи. В настоящее время для диагностики данной патологии предложены специальные критерии. К обязательным критериям относятся:
- связь симптомов с внешними воздействиями (инфекция, иммунизация, введение силикона);
- мышечный синдром (миалгия, миозит, парезы);
- суставной синдром (артралгии, артриты);
- астения (усталость, слабость, нарушения сна);
- психопатологические проявления (расстройство памяти, когнитивные дефицит);
- пирексия;
- ксеростомия.
Малые критерии ASIA-синдрома включают обнаружение Ат к предполагаемому адъюванту, специфических HLA-галотипов, признаки системных заболеваний, другие проявления (СРК).
- Исследование показателей крови. В крови увеличена СОЭ, определяется положительный СРБ, повышен уровень фибриногена, ЛДГ, ЩФ. Часто выявляются маркеры аутоиммунных заболеваний (anti-CCP, антинуклеарный фактор, Ат к dsДНК, РФ, Ат к антигену Sm и др).
- Биопсия тканей. Исследуются биоптаты кожи, мышц, сосудов, лимфоузлов, иногда внутренних органов. В очаге введения адъюванта развивается характерная гистологическая картина иммунного воспаления: лимфогистиоцитарная инфильтрация тканей, склероподобные и гранулематозные изменения.
- Инструментальные исследования. Для оценки целостности грудных имплантов выполняется УЗИ молочных желез, при необходимости – МРТ-контроль. При поражении внутренних органов назначается УЗИ почек, КТ легких. При синдроме Рейно производится капилляроскопия.
Лечение ASIA-синдрома
Для устранения патологических симптомов необходимо элиминировать провоцирующий фактор (удалить импланты и филеры, отказаться от использования кондиционера, сменить место работы/жительства). С целью купирования симптоматики используются НПВП (нимесулид, эторикоксиб, ибупрофен). При необходимости в схему базисной противовоспалительной терапии добавляют пульс-терапию метилпреднизолоном, пеницилламин, антиметаболиты (метотрексат).
Прогноз и профилактика
Корреляционная зависимость ASIA-синдрома от введения адъювантов нуждается в дальнейшем изучении и признании медицинским сообществом. На сегодняшний день влияние адъювантов на развитие системных заболеваний остается недоказанным. Клиника ASIA-синдрома часто исчезает после устранения триггера. Тем не менее, FDA рекомендует пластическим хирургам оказаться от имплантации грудных протезов с силиконовым гелем из-за их высокой иммуногенности в пользу имплантов с солевым раствором. Перед медицинскими манипуляциями, связанными с введением инородных веществ, необходимо проведение тщательного иммунологического обследования пациентов.
1. Современное представление о синдроме Шонфельда и возможность раннего скрининга пациентов, относящихся к группе риска/ Дубов В.С., Курындина И.А.// Научный диалог: Вопросы медицины. – 2017.
2. Аутоиммунный/воспалительный синдром, ассоциированный с адъювантами/ Раденска-Лоповок С.Г., Волкова П.// Архив патологии. – 2018. - №5.
3. The ASIA syndrome: basic concepts/ A. Watad, K. Sharif, Y. Shoenfeld// Mediterranean Journal of Rheumatology. – 2017.
Коллагенозы – группа заболеваний, объединенных однотипными функционально-морфологическими изменениями со стороны соединительной ткани (главным образом, коллагенсодержащих волокон). Характерным проявлением коллагенозов является прогрессирующее течение, вовлечение в патологический процесс различных внутренних органов, сосудов, кожи, опорно-двигательной систем. Диагностика коллагенозов основана на полиорганности поражения, выявлении положительных лабораторных маркеров, данных биопсии соединительной ткани (кожи или синовиальных оболочек суставов). Чаще всего для лечения коллагенозов применяются кортикостероиды, иммунодепрессанты, НПВС, аминохинолиновые производные и др.
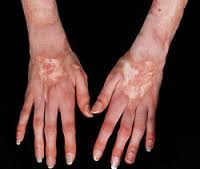
Общие сведения
Коллагенозы (коллагеновые болезни) – иммунопатологические процессы, характеризующиеся системной дезорганизацией соединительной ткани, полисистемным поражением, прогрессирующим течением и полиморфными клиническими проявлениями. В ревматологии к числу коллагенозов принято относить ревматоидный артрит, ревматизм, системную красную волчанку, системную склеродермию, узелковый периартериит, дерматомиозит, гранулематоз Вегенера и др. Эти заболевания объединены в единую группу на основании общего патоморфологического признака (фибриноидного изменения коллагена) и патогенетического механизма (нарушения иммунного гомеостаза).
Соединительная ткань формирует скелет, кожу, строму внутренних органов, кровеносные сосуды, заполняет промежутки между органами и составляет более половины массы человеческого тела. К основным функциям соединительной ткани в организме относятся защитная, трофическая, опорная, пластическая, структурная. Соединительная ткань представлена клеточными элементами (фибробластами, макрофагами, лимфоцитами) и межклеточным матриксом (основное вещество, коллагеновые, эластические, ретикулярные волокна). Таким образом, термин «коллагенозы» не в полной мере отражает происходящие в организме патологические изменения, поэтому в настоящее время данную группу принято называть «диффузными заболеваниями соединительной ткани».
Классификация коллагенозов
Различают врожденные (наследственные) и приобретенные коллагенозы. Врожденные соединительнотканные дисплазии представлены, в частности, мукополисахаридозами, синдромом Марфана, несовершенным остеогенезом, синдромом Элерса-Данлоса, эластической псевдоксантомой, синдромом Стиклера и др.
Приобретенные коллагенозы, в свою очередь, включают СКВ, склеродермию, узелковый периартериит, дерматомиозит, ревматоидный полиартрит, синдром Шегрена, ревматизм, системный васкулит, диффузный эозинофильный фасциит и др. Из них первые четыре нозологические единицы причисляют к большим коллагенозам, отличающимся истинно системным характером поражения и тяжестью прогноза; остальные – к малым коллагеновым болезням. Также принято выделять переходные и смешанные формы диффузных заболеваний соединительной ткани (синдром Шарпа).

Причины коллагенозов
Врожденные коллагенозы обусловлены наследственным (генетическим) нарушением структуры коллагена или обмена веществ. Менее изучена и понятна этиология приобретенных системной заболеваний соединительной ткани. Она рассматривается с точки зрения мультифакторной иммунопатологии, обусловленной взаимодействием генетических, инфекционных, эндокринных факторов и влияний внешней среды. Многочисленные исследования подтверждают связь между конкретными системными заболеваниями соединительной ткани и носительством определенных HLA-антигенов, главным образом, антигенов гистосовместимости II класса (HLA-D). Так, системная красная волчанка ассоциирована с носительством DR3-антигена, склеродермия - А1, В8, DR3 и DR5-антигенами, синдром Шегрена - с HLA-B8 и DR3. В семьях больных коллагенозами, чаще, чем в популяции в целом, системные заболевания регистрируются среди родственников первой степени родства.
В отношении инфекционных агентов, причастных к развитию коллагенозов, до сих пор ведутся научные исследования. Не исключается инфекционно-аллергический генез диффузных заболеваний соединительной ткани; рассматривается возможная роль внутриутробных инфекций, стафилококков, стрептококков, вирусов парагриппа, кори, краснухи, паротита, простого герпеса, цитомегаловируса, Эпштейна-Барр, Коксаки А и др.
Следует отметить связь коллагенозов с изменениями эндокринно-гормональной регуляции: с началом менструального цикла, абортами, беременностью или родами, климаксом. Внешнесредовые факторы, как правило, провоцируют обострение скрыто протекающей патологии либо выступают триггерами возникновения коллагенозов при наличии соответствующей генетической предрасположенности. Такими пусковыми механизмами могут являться стресс, травма, переохлаждение, инсоляция, вакцинация, прием лекарств и пр.
Патогенез и патоморфология коллагенозов
Патогенез коллагенозов можно представить в виде следующей общей схемы. На фоне бактериально-вирусной сенсибилизации организма формируются патогенные иммунные комплексы, которые оседают на базальной мембране сосудов, синовиальных и серозных оболочках и провоцируют развитие неспецифического аллергического воспаления. Эти процессы вызывают аутоаллергию и аутосенсибилизацию к собственным тканям, нарушение клеточного и гуморального факторов иммуногенеза, гиперпродукцию аутоантител к ядрам клеток, коллагену, эндотелию сосудов, мышцам.
Извращенные иммунные, сосудистые и воспалительные реакции при коллагенозах сопровождаются патологической дезорганизацией соединительной ткани. Патоморфологические изменения проходят 4 стадии: мукоидного набухания, фибриноидного некроза, клеточной пролиферации и склероза.
Коллагенозы сопровождаются различными патологоанатомическими изменениями, однако все заболевания объединяет диффузное вовлечение в патологический процесс соединительной ткани организма, которое может встречаться в различных сочетаниях. Так при узелковом периартериите преимущественно поражаются сосуды мышечного типа, что приводит к рубцеванию и запустеванию последних, поэтому в клиническом течении нередко отмечаются аневризмы сосудов, кровоизлияния, кровотечения, инфаркты. Для склеродермии типично развитие распространенного склероза (поражения кожи и подкожной клетчатки, пневмосклероза, кардиосклероза, нефросклероза). При дерматомиозите преобладает поражения кожи и мышц, а также расположенных в них артериол. Системная красная волчанка характеризуется полисиндромным течением с развитием дерматоза, полиартрита, синдрома Рейно, плеврита, нефрита, эндокардита, менингоэнцефалита, пневмонита, невритов, плекситов и пр.
Симптомы коллагенозов
Несмотря на многообразие клинико-морфологических форм коллагенозов, в их развитии прослеживаются общие черты. Все заболевания имеют длительное волнообразное течение с чередованием обострений и ремиссий, неуклонным прогрессированием патологических изменений. Характерна стойкая лихорадка неправильного типа с ознобами и профузными потами, признаки аллергии, необъяснимая нарастающая слабость. Общими для всех коллагенозов являются системный васкулит, мышечно-суставной синдром, включающий миалгии, артралгии, полиартриты, миозиты, синовиты. Часто отмечается поражение кожи и слизистых оболочек - эритематозная сыпь, петехии, подкожные узелки, афтозный стоматит и др.
Поражение сердца при коллагенозах может сопровождаться развитием миокардита, перикардита, миокардиодистрофии, кардиосклероза, артериальной гипертензии, ишемии, стенокардии. Со стороны органов дыхания отмечаются пневмониты, плевриты, инфаркт легкого, пневмосклероз. Почечный синдром включает в себя гематурию, протеинурию, амилоидоз почек, хроническую почечную недостаточность. Нарушения деятельности ЖКТ могут быть представлены диспепсией, желудочно-кишечными кровотечениями, приступами абдоминальных болей, симулирующими холецистит, аппендицит и др.
Полиморфизм клинической картины объясняется органоспецифичностью поражения при различных формах коллагенозов. Обострения диффузных заболеваний соединительной ткани обычно связаны с инфекциями, переохлаждением, гиперинсоляцией, травмами.
Диагностика коллагенозов
Основанием для предположения той или иной формы коллагеноза служит наличие классических клинико-лабораторных признаков. Типично появление в крови неспецифических маркеров воспаления: С-реактивного белка, повышение α2-глобулинов, фибриногена, серомукоида, СОЭ и др. Большое диагностическое значение имеет определение иммунологических маркеров, характерных для каждого заболевания: ЦИК, антинуклеарного и ревматоидного факторов, антител к одно- и двухспиральной ДНК, антистрептолизина-0, антител к ядерным антигенам, уровня комплемента и др. Нередко для постановки патоморфологического диагноза приходится прибегать к биопсии кожи, мышц, синовиальной оболочки суставов, почки.
Определенную помощь в диагностике коллагенозов может оказать рентгенологическое исследование костей и суставов, при котором выявляются общие (остеопороз, сужение суставных щелей), а также частные рентгенологические признаки (узурация суставных поверхностей при ревматоидном артрите, асептические некрозы суставных поверхностей при СКВ, остеолизы дистальных фаланг при склеродермии и т. п.). Для выявления характера и степени поражения внутренних органов используются ультразвуковые методы диагностики (ЭхоКГ, УЗИ плевральной полости, УЗИ почек, УЗИ органов брюшной полости), МРТ, КТ. Дифференциальная диагностика различных форм коллагенозов проводится ревматологом; при необходимости пациента консультируют другие специалисты: кардиолог, пульмонолог, иммунолог, дерматолог и др.
Лечение и прогноз коллагенозов
Течение большинства коллагеновых болезней прогрессирующее и рецидивирующее, что требует поэтапного, длительного, нередко пожизненного лечения. Чаще всего для терапии различных форм коллагенозов используются следующие группы препаратов: стероидные (глюкокортикоиды) и нестероидные противовоспалительные средства, цитостатики, аминохинолиновые производные, препараты золота. Дозировка и длительность курсов определяется строго индивидуально с учетом типа заболевания, остроты и тяжести течения, возраста и индивидуальных особенностей больного.
Для всех видов коллагенозов характерно хроническое прогрессирующее течение с многосистемным поражением. Назначение кортикостероидной или иммуносупрессивной терапии помогает уменьшить остроту клинических симптомов, привести к более или менее длительной ремиссии. Наиболее скоротечное развитие и тяжелое течение имеют так называемые большие коллагенозы. Гибель больных может наступить в результате почечной, сердечно-сосудистой, дыхательной недостаточности, присоединения интеркуррентной инфекции. Для профилактики обострений коллагенозов важно устранить очаги хронической инфекции, проходить диспансерное обследование, избегать избыточной инсоляции, переохлаждения и других провоцирующих факторов.

Коллагеноз представляет собой группу заболеваний, характеризующихся поражением соединительной ткани, в том числе и волокон, содержащих в своем составе коллаген. Коллагенозы относятся к группе патологий с участием тканей, богатых белком, поддерживающих на должном уровне функционирование органов и частей тела. Результатом коллагеноза становятся нарушения работы мышц, суставов и других органов, а также ухудшение состояния кожного покрова.
Симптомами коллагеноза могут быть:
- слабость;
- болезненные ощущения в мышцах и суставах;
- субфебрильная температура – повышение температуры тела на протяжении продолжительного временного отрезка в пределах 37 – 37,5°C;
- кожные высыпания;
- чрезмерная потливость.
Существует более 200 патологий соединительной ткани, симптомы и причины возникновения которых тесно взаимосвязаны. Попробуем разобраться с некоторыми самыми распространенными типами коллагенозов.
2. Наследственные заболевания соединительной ткани
Некоторые болезни соединительной ткани являются результатом изменений в определенных генах. Вот наиболее распространенные из них:
Синдром Элерса-Данло
Данный синдром представляет собой группу заболеваний наследственного характера, отличительной особенностью которых являются гипермягкие суставы, повышенная эластичность кожи, подверженные повреждениям кровеносные сосуды, аномальный рост рубцовой ткани и синяки. Симптоматика данного синдрома может варьироваться от легкой степени до высокой. В зависимости от конкретного вида Элерса-Данло признаки этого заболевания могут включать следующее:
- кровоточивость десен,
- слабые сосуды,
- медленное заживление ран,
- изогнутый позвоночник,
- плоскостопие,
- проблемы с легкими, сердечными клапанами и органами пищеварения.
Врожденный буллезный эпидермолиз
Люди с данным заболеванием имеют настолько хрупкую кожу, что практически любое соприкосновение с ней сопровождается возникновением тонкостенных волдырей с серозным содержимым. Подобные пузыри могут возникнуть при ударе, падении человека на землю и даже от трения одежды на определенных участках кожи.
В зависимости от какого-либо конкретного вида врожденного буллезного эпидермолиза подвергаться неблагоприятному воздействию могут дыхательные пути, пищеварительный тракт, мочевой пузырь, мышцы или другие органы. Как правило, буллезный эпидермолиз проявляется сразу при рождении ребенка, так как сам акт родов в некоторой степени является первой механической травмой.
Синдром Марфана
Клиническая картина данного заболевания характеризуется поражением большинства жизненно важных органов и систем: сердечно-сосудистой и центральной нервной системы, опорно-двигательного аппарата, органов зрения и дыхания. Люди с синдромом Марфана имеет высокий рост, а также чрезмерно длинные кости и тонкие «паукообразные» пальцы ног, рук.
Среди других проблем, сопровождающих синдром Марфана, можно выделить проблемы со зрением по причине аномального размещения хрусталика глаза и расширения аорты. Синдром Марфана провоцируется мутациями в гене, который регулирует структуру белка фибриллина.
Несовершенный остеогенез
Данная патология является врожденным расстройством, характеризующимся хрупкостью костей, низкой мышечной массой. Существует несколько типов этого заболевания. Специфические симптомы несовершенного остеогенеза зависят от конкретного вида заболевания и могут включать в себя следующие признаки:
- серый или синий оттенок склеры – белка глаз;
- тонкая кожа;
- снижение слуха;
- незначительное искривление позвоночника;
- проблемы с дыханием.
Причина возникновения данной патологии заключается в мутации генов COL1A1 и COL1A2, ответственных за коллаген типа 1, а также изменение качества протеина.
3. Аутоиммунные заболевания
Аутоиммунные заболевания представляют собой совокупность заболеваний, при которых под действием собственной иммунной системы происходит деформация и разрушение тканей, органов организма человека. Исследователи полагают, что это расстройство возникает у генетически восприимчивых людей. У них защитная иммунная система вырабатывает антитела, атакующие собственные ткани. К этому типу патологий можно отнести следующие заболевания.
Дерматомиозит и полимиозит
В основе этих заболеваний лежат воспалительные процессы, протекающие на фоне специфического действия иммунной системы человека. Дерматомиозит характеризуется воспалением кожного покрова, а полимиозит – мышц. Для симптоматики обоих заболеваний характерны:
- усталость,
- мышечная слабость,
- одышка,
- затруднение глотания,
- потеря в весе,
- лихорадка.
Ревматоидный артрит
При данном заболевании иммунная система атакует синовиальную оболочку – оболочку мембран, выстилающих полость суставов. В результате подобного воздействия она воспаляется, появляется боль и отечность, ощущение скованности во всем теле. Среди других симптомов ревматоидного артрита можно выделить:
- потерю аппетита;
- усталость;
- лихорадку;
- анемию.
Склеродермия
Этот термин обозначает группу заболеваний из группы коллагенозов, которые характеризуются уплотнением кожи, наращиванием рубцовой ткани и повреждением внутренних органов. Эти нарушения подразделяются на две основные категории: системная и очаговая склеродермия.
Синдром Шегрена
Синдром Шегрена представляет собой хроническое системное заболевание, при котором атаке иммунной системы подвергается слезные и слюнные железы, а также железы слизистых оболочек. Результатом данного патологического процесса становится дисфункция данных желез с последующим уменьшением количества вырабатываемого секрета. Основными синдрома Шегрена являются сухость в глазах и во рту, а также постоянная усталость и боль в суставах.
Системная красная волчанка
Системная красная волчанка, поражая капилляры и соединительную ткань, оказывает отрицательное влияние на весь организм в целом. Для симптоматики красной волчанки характерны следующие признаки:
- чувствительность к солнечному свету;
- высыпания на щеках и переносице;
- выпадение волос;
- нарушения работы почек;
- проблемы с концентрацией внимания и памятью;
- анемия.
Данный термин характерен более чем для 20 различных состояний, характеризующихся воспалением стенок сосудов. Как следствие, васкулит может ухудшать кровообращения органов и других тканей организма.
Смешанное заболевание соединительной ткани – смешанный коллагеноз.
При таком коллагенозе у людей выявляются черты одновременно нескольких болезней: красной волчанки, дерматомиозита, ревматоидного артрита и т.д. Многогранные проявления этой патологии у больных проявляются по-разному: кто-то жалуется на легкие симптомы, а у кого-то могут возникнуть и серьезные осложнения, в том числе и инфекции, инсульты, почечная недостаточность и другие опасные явления.
Лечение коллагеноза зависит от множества различных факторов: типа заболевания и его симптоматики, тяжести течения болезни, а также от индивидуальных особенностей организма больного. Чаще всего меры по лечению коллагеноза помогают если не вылечить болезнь полностью, то хотя бы контролировать неприятные симптомы коллагеноза.

Кальциноз кожи – одно из названий синдрома Профише (встречаются также синонимы «кожный камень», «болезнь Профише», «кальциевая подагра» и т.п.). Суть этого заболевания или, вернее, патологического процесса заключается в том, что твердые соли кальция, которые в норме циркулируют в организме преимущественно в растворенном, электролитном состоянии (не считая костных тканей и зубов), на фоне избыточной концентрации начинают откладываться в подкожной клетчатке и собственно коже.
Как правило, этот процесс носит вторичный характер и прогрессирует одновременно с обызвествлением других структур и органов (будучи лишь одним из проявлений общей тенденции), однако в некоторых случаях кожный кальциноз может развиваться и при нормальном содержании кальция в крови.
Чаще страдают женщины.
2. Причины
К настоящему времени окончательно прояснены не все причины и механизмы развития синдрома Профише. Достоверно установлено, что внутри- и подкожное отложение солей кальция может быть обусловлено опухолевыми процессами (в частности, костной локализации) или нарушениями метаболизма (как правило, при почечной дисфункции). Определенную роль играют нарушения общей гемодинамики и микроциркуляции, смещения кислотно-щелочного баланса, процессы рубцевания после травм, наследственные и аутоиммунные заболевания, прежде всего коллагенозы, – системная красная волчанка, склеродермия и т.д., а также болезнь Рейно.
В целом, по этиологическому критерию различают три основные формы кальциноза кожи: метастатическую (встречается, например, при остеомиелите или избытке витамина D), обменную и дистрофическую.
3. Симптомы и диагностика
Кальциноз кожи проявляется образованием внутрикожных плотных, легко пальпируемых узелков, которые длительное время могут оставаться безболезненными и не вызывают особого дискомфорта, поскольку не сопровождаются признаками воспаления, изменения цвета кожи и т.д. Однако на определенном этапе может начаться формирование т.н. «кальциевых гумм» – плохо заживляемых и, как правило, также безболезненных изъязвлений-фистул (свищей), наполненных белой крошащейся субстанцией.
Наиболее типичной локализацией образования и отложения кальцинатов являются кисти, пальцы, проекция суставов, при некоторых вариантах кальциноза – ягодицы, крайняя плоть у мужчин, кожный покров черепа у детей; или же кальциноз принимает генерализованный, распространенный характер.
Дальнейшее прогрессирование патологического процесса может привести к обызвествлению крупных суставов с серьезным ограничением их функции, – вплоть до полной неподвижности, – а также к развитию поздних воспалительных, дегенеративно-дистрофических и атрофических процессов.
Диагностика осуществляется клиническим методом, с учетом анамнеза и особенностей динамики. На этапе общего обследования и поиска первопричин назначают рентгенологические и лабораторные (биохимические) исследования. Могут также понадобиться биопсия, консультации профильных специалистов.
4. Лечение
Соединения, способные нормализовать уровень кальция и применяемые сегодня с этой целью, – хлорид аммония и йодид калия. Однако эти вещества сами по себе токсичны для человека, а при кальцинозе эффективны лишь в достаточно больших дозировках. Поэтому самолечение очень опасно; все назначения должны осуществляться и контролироваться врачом.
В зависимости от выявленных причин, обязательно назначают лечение первичного, основного заболевания (если только кальциноз не является идиопатическим или наследственным). При относительно небольшом количестве очагов обызвествления и определенных их размерах узелки могут быть удалены хирургически (в том числе путем, например, электрокоагуляции или лазерной деструкции), однако такое лечение проводится только на фоне поддерживающей консервативной терапии и является, по большому счету, паллиативом, – поскольку не устраняет причин и не исключает риск рецидивного образования кальцинатов в коже.
Важно соблюдать предписанную врачом диету, ограничивающую поступление кальция извне. Достаточно эффективны физиотерапевтические процедуры.
Прогноз неблагоприятен при генерализованных, тотальных формах кальциноза, либо же при вторичном кальцинозе на фоне онкологического процесса.
Заболевания ![частые заболевания]()
Жалобы и симптомы ![Жалобы и симптомы]()
- высыпания на лице
- высыпания на теле
- высыпания на половых органах
- покраснения и шелушения
- зуд и жжение
- появление новообразований на коже
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика ![Диагностика]()
- Дермоскопия
- Люминесценция
- Диаскопия
- Граттаж (поскабливание)
- Проба зондом пункция иглой
- Биопсия
Наши цены ![Типичные жалобы]()
- Консультация врача дерматолога - 3000 р.
- Удаление новообразований диаметром до 5 мм - от 300 р.
- Осмотр кожи под увеличением (дерматоскопия) - 500 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Читайте также:




