Что такое акантоз желудка
Обновлено: 19.04.2024
У 134 больных желчнокаменной болезнью изучено состояние слизистой оболочки пищевода, желудка и двенадцатиперстной кишки. В пищеводе в 54% случаев выявлены гиперкератоз и акантоз слизистой оболочки и в 17% признаки хронического эзофагита. При желчнокаменной болезни, протекающей самостоятельно, хеликобактерный гастрит обнаружен в 49% случаев, а при сочетании с язвенной болезнью двенадцатиперстной кишки в 70%. В слизистой оболочке двенадцатиперстной кишки у 72% больных желчнокаменной болезнью изменений найдено не было, в 28% изменения соответствовали хроническому умеренно выраженному дуодениту.
Течение желчнокаменной болезни (ЖКБ) сопровождается целым комплексом клинических симптомов со стороны верхнего отдела пищеварительного тракта. Вместе с тем характер патологических изменений со стороны пищевода, желудка и двенадцатиперстной кишки у больных ЖКБ изучен недостаточно. В то же время в литературе обсуждаются возможные патогенетические механизмы взаимосвязи изменений в гастродуоденальной зоне с патологией гепатобилиарной системы[1,8].
Цель работы - оценить состояние слизистой оболочки пищевода, желудка и двенадцатиперстной кишки у больных ЖКБ, в том числе и в сочетании с язвенной болезнью двенадцатиперстной кишки (ЯБДК).
Обследовано 134 больных ЖКБ в возрасте от 18 до 70 лет (103 женщины и 31 мужчина). Из них в 98 случаях ЖКБ протекала без сопутствующей патологии, а в 36 сочеталась с ЯБДК. В качестве контрольной группы обследовано 353 больных ЯБДК.
Клиническая картина у большинства больных характеризовалась симптомами, свидетельствующими о патологии желчного пузыря и желчевыводящих путей, основными из которых являлись боли в правом подреберье, временами усиливающихся до приступов желчных колик.
У части больных на первый план выступал симптомокомплекс разнообразных клинических проявлений в виде болевого, диспепсического или регуртационного синдромов, указывающих на патологию органов верхнего отдела пищеварительного тракта - ноющие боли и чувство тяжести в эпигастрии после еды, изжога, тошнота, отрыжка воздухом, чувство горечи во рту.
Диагноз ЖКБ и функциональное состояние желчного пузыря устанавливали по данным серийных ультразвуковых исследований и пероральной холецистографии. Наличие дуодено-гастрального и гастро-эзофагального рефлюкса определяли с помощью компьютерной внутрижелудочной рН-метрии.
Для оценки характера морфологических изменений со стороны верхнего отдела пищеварительного тракта всем больным проводили эзофагогастродуоденоскопию с множественными прицельными биопсиями из слизистой оболочки нижней трети пищевода, антрального и фундального отделов желудка, проксимальной части двенадцатиперстной кишки.
Биопсийный материал фиксировали в 10% нейтральном, забуференном по Лилли формалине. Серийные парафиновые срезы окрашивали гематоксилином и эозином. Для выявления Helicobacter pylori (HP) биопсийный материал окрашивали по методу Гимзы без дифференцировки. При изучении гистологических препаратов выделяли 3 степени обсеменения слизистой оболочки при увеличении х630 - слабая (+) - до 20 микробных тел в поле зрения, средняя (++) - до 50 микробных тел в поле зрения и высокая (+++) - более 50 микробных тел в поле зрения.
В гистологических препаратах полуколичественным методом при помощи визуально-аналоговой шкалы, предложенной модифицированной классификацией Сиднейской системы для оценки выраженности морфологических изменений слизистой оболочки желудка, определяли инфильтрацию нейтрофилами собственной пластинки слизистой оболочки, хроническое воспаление, атрофию, кишечную и желудочную метаплазию.
При исследовании биопсийного материала, полученного из нижней трети пищевода (таблица 1.), патологические изменения были выявлены у 36 из 52 больных ЖКБ (69,2%). Чаще всего (53,8%) изменения в слизистой оболочке пищевода характеризовались признаками гиперкератоза и акантоза, проявляющихся утолщением эпителия слизистой оболочки с удлинением межсосочковых отростков (рис. 1а и 16). Данное явление может быть обусловлено реакцией слизистой оболочки пищевода на билиарный рефлюкс, часто встречающегося у больных ЖКБ, а также возможным нарушением обмена витамина А у этих больных. Известно, что нарушение процессов кератинизапии с развитием гиперкератоза многослойного плоского эпителияпищевода является характерным признаком дефицита именно этого витамина [4,9].
Таблица 1. Характер патологических изменений в слизистой оболочке пищевода при ЖКБ, ЯБДК и ЖКБ и ЯБДК
При этом признаки хронического эзофагита выявлены у 30 % больных (у 11 из 36), что было в 2 раза чаще, чем у больных ЖКБ и ЯБДК, протекающей самостоятельно.
Эти данные превышали и показатели частоты выявления пептического эзофагита у больных только ЯБДП, полученные и другими исследователями [4].

Поделитесь информацией с друзьями
Пациентов, проходивших ЭГДС, волнует то обстоятельство, которое возникает по итогам биопсии слизистой пищевода и отражается в гистологическом отчете термином «лейкоплакия пищевода».
На сегодняшний день, чтобы критично и конструктивно подходить к этому термину нужно понять и принять следующие положения не только пациенту, но и врачам, выставляющие определение «лейкоплакия пищевода» на суд общественности:
- Лейкоплакия – это только клинический термин, используемый для обозначения белого пятна или бляшки, возникающее на поверхности слизистых оболочек с плоским эпителием, которое не снимается и не может быть охарактеризована клинически, как любое другое заболевание (например, сифилис, красный плоский лишай, волчанка и др.).
- Лейкоплакия имеет широкий диапазон возможных гистологических проявлений. Это может быть определенная степень утолщения верхних слоев эпителия (гиперкератоза), утолщения срединной зоны эпителия (акантоз) или атрофии, воспалительной клеточной инфильтрации, дисплазии или рака.
- Как и любое состояние, гистологические проявления лейкоплакии могут носить характер обычного простого поражения, так и атипического. При простой лейкоплакии обнаруживается нормальный плоский эпителий. При атипической лейкоплакии – атипический эпителий, с дисплазией.
Различие лейкоплакии полости рта и лейкоплакии пищевода
Лейкоплакия полости рта – это относительно распространенное, безболезненное поражение слизистой оболочки полости рта. Она возникает преимущественно у мужчин среднего и пожилого возраста и прочно ассоциируется с табакокурением и употреблением алкоголя. Всемирная организация здравоохранения считает лейкоплакию одним из наиболее распространенных предраковых или потенциально злокачественных нарушений и фактором риска развития плоскоклеточного рака.
Лейкоплакия пищевода – редкое состояние по сравнению с лейкоплакией полости рта. Связь с раком пищевода остается неясной, потому что заболеваемость лейкоплакией пищевода слишком низка. В англоязычной литературе, по видимому, чтобы меньше было путаницы в терминах аналогичное поражение в пищеводе вместо «лейкоплакия пищевода» называют «эпидермоидной метаплазией пищевода», редко встречающееся и недостаточно описанное в литературе. За 10 лет в 6-ти специализированных клиниках США было зафиксировано 18 случаев эпидермоидной метаплазии пищевода или лейкоплакии пищевода. В самих поражениях явно отсутствовали признаки плоскоклеточной атипии и дисплазии. Но у 17% пациентов в 2 см от очага наблюдались соседствующие плоскоклеточная дисплазия высокой степени и/или рак, требующие пристального наблюдения. Эти пациенты были прооперированы. Рецидивов у них не наблюдалось. У остальных пациентов при наблюдении до 8 лет ни у одного не было выявлено дисплазии или рака пищевода при биопсии.
Руководство к действию
Лейкоплакия пищевода – термин просто калькированный с термина лейкоплакия полости рта. Выставлять клинический термин – «лейкоплакия пищевода» в гистологическом описании не совсем корректно. Лечащий врач ждет от описания в первую очередь гистологические процессы, которые и проявляют это клиническое состояние – т.е. за счет чего произошло очаговое утолщение – за счет гиперкератоза поверхностных отделов плоскоклеточного эпителия пищевода, за счет акантоза срединной зоны эпителия, за счет отека и инфильтрации, атрофии? И следующий вопрос освещения в гистологическом отчете – имеются ли атипические формы клеток в материале, есть ли дисплазия? Обращать внимание и обсуждать с врачом расширенную тактику обследования и наблюдения необходимо, если имеется наличие атипии клеток и различных степеней дисплазии либо в смежных участках, либо в участках самого поражения.
Если у вас возникли дополнительные вопросы по лейкоплакии пищевода, то вы сможете задать их через форму на сайте справа или по электронной почте в разделе Контакты.
(Aatur D Singhi, Christina A Arnold, Clinton D Crowder, Dora M Lam-Himlin, Lysandra Voltaggio and Elizabeth A Montgomery. Esophageal leukoplakia or epidermoid metaplasia, Modern Pathology (2014) 27, 38–43)

Поделитесь информацией с друзьями
Это состояние наблюдается при усиленном делении плоскоклеточного эпителия пищевода (гиперплазии) и обычно рассматривается как доброкачественное.
При Национальной токсикологической программе в США (NTP) создан атлас неопухолевых поражений. Там дается определение этому поражению.
Гиперкератоз – это обычное для пищевода изменение и проявляется утолщением плоскоклеточного эпителия, ороговением его, и в дальнейшем приводящим к его отмиранию и слущиванию. Врач-гистолог может определить его в двух видах в зависимости от наличия ядра в клетке и назвать этот процесс, либо – ортокератоз (нет ядра), либо – паракератоз (есть ядро, но оно сморщенное, измененное). Сразу оговорюсь, что гиперкератоз не принято делить на ортокератоз и паракератоз в диагностике, но это должно быть отчетливо описано в гистологическом отчете.
Гиперкератоз – это частое сопровождение гиперплазии
Гиперкератоз часто наблюдается при плоскоклеточной гиперплазии, как правило, не диагностируется как отдельный процесс, хотя он, может быть упомянут в описании в гистологическом отчете.
Многие годы, были уверены, что единственным достоверным критерием эзофагита было наличие воспаления в слизистой пищевода. Тем не менее, в начале 20 века исследователями впервые была обнаружена плоскоклеточная гиперплазия пищевода у некоторых пациентов с клиническими симптомами рефлюкса, но нормальной или минимально измененной слизистой пищевода при эндоскопии. Это открытие стало ранним гистологическим признаком начального повреждения слизистой пищевода при рефлюксе. Обнаруженная закономерность также применима и у младенцев, и у детей старшего возраста.
При изучении гиперкератоза у животных в аноректальной зоне, избыток утолщенной слизистой, предположительно, уменьшается в результате механического удаления его путем прохождения пищи, т.е. слущивания. При анорексии (голодании) гиперкератоз наряду с наличием в пищеводе обычно также присутствует и в кардиальном отделе желудка. В таких ситуациях, в тканях мы не найдем никаких доказательств гиперплазии.
Если выставляется гиперкератоз без гиперплазии или когда он выраженный (распространенный), то процесс должен быть описан и оценен по степени тяжести на основании утолщения слизистой и обширности зоны поражения пищевода.
Рекомендации
На возникновение гиперкератоза влияет рацион питания с низким содержанием клетчатки, низким содержанием белка, или жидкие диеты, влекущие увеличение толщины эпителиального слоя. Кроме того, в опытах in vivo показано, что у животных, которые не едят, часто возникает гиперкератоз пищевода без сопутствующего усиления деления клеток (гиперплазии). Кроме того, витаминный дисбаланс и дефицит цинка может привести к паракератозу и связанного с ним плоскоклеточной гиперплазии.
Авторы
Linda H. Kooistra, DVM, PhD, DACVP Pathologist Charles River Laboratories, Inc. Research Triangle Park, NC
Abraham Nyska, DVM, Diplomate ECVP, Fellow IATP Expert in Toxicologic Pathology Visiting Full Professor of Pathology Sackler School of Medicine, Tel Aviv University Timrat Israel
Аденокарцинома желудка – это злокачественная опухоль желудка, происходящая из клеток железистого эпителия. На начальных стадиях может ничем себя не проявлять, в связи с чем ранняя диагностика затруднительна. В дальнейшем возникают и прогрессируют боль в эпигастрии, отсутствие аппетита, тошнота, отрыжка, потеря веса, слабость, апатия. Для подтверждения диагноза проводится ЭГДС с биопсией, определение онкомаркеров в крови, рентгенография желудка и др. Единственным радикальным методом лечения является хирургическое удаление опухоли. Лучевая и химиотерапия применяются как дополнительные методики или при наличии противопоказаний к хирургическому лечению.
МКБ-10
Общие сведения
Аденокарцинома желудка – злокачественная опухоль, происходящая из железистых клеток эпителия стенки желудка. Это заболевание составляет подавляющее большинство случаев рака желудка и занимает первое место среди онкопатологии во многих странах, в том числе в России, странах Скандинавии, Украине, Японии. Часто именно данная патология подразумевается под термином «рак желудка». Около 40% пациентов обращаются к гастроэнтерологу уже с запущенной стадией, и в ряде случаев из-за сопутствующей патологии невозможно проведение хирургического удаления опухоли. В то же время летальность при радикальном лечении составляет около 12%.
Причины
Точная этиология аденокарциномы желудка неизвестна. Причиной развития данной патологии считается длительное влияние канцерогенных агентов на фоне угнетения секреции и нарушений кровообращения. К развитию рака желудка предрасполагает ряд факторов. Процессы малигнизации имеют генетическую предрасположенность, зависят от особенностей питания, ряда бытовых факторов. Доказана связь частоты заболевания с инфицированием Helicobacter pylori – бактерией, вызывающей гастрит и язвенную болезнь желудка (у пациентов с наличием данного микроорганизма частота рака желудка вдвое выше).
Заболеваемость имеет возрастные особенности: аденокарцинома желудка чаще встречается после 55 лет. По данным специалистов в сфере клинической онкологии, мужчины страдают данным заболеванием в три раза чаще, чем женщины. Важную роль в развитии ракового процесса играют курение, алкоголь. Употребление крепких алкогольных напитков приводит к развитию очаговых пролиферативных процессов в слизистой желудка, а со временем – рака.
Также в развитии аденокарциномы желудка имеют значение такие факторы, как диета с низким содержанием пищевых волокон, витаминов, антиоксидантов, пернициозная анемия, хронический атрофический гастрит, аденоматозный полип желудка, гиперпластический гастрит. Среди эндогенных причин не исключают роль N-нитрозосоединений, синтезируемых в желудке при различных патологических состояниях. Массивный их синтез возникает при заболеваниях с анацидным состоянием.
Аденокарцинома практически никогда не возникает в здоровом желудке. В гастроэнтерологии выделяют предраковые (фоновые) заболевания и изменения слизистой желудка. К предраковым заболеваниям относятся состояния, которые потенциально могут привести к развитию рака: хронические гастриты, полипы, хронические язвы, оставшаяся после резекции часть желудка и другие. К предраковым изменениям слизистой желудка относят морфологически доказанные изменения, свидетельствующие о развитии процесса в направлении малигнизации (озлокачествления). Данные изменения объединяются термином «дисплазия».
Классификация
Выделяют следующие виды аденокарциномы желудка:
- язва-рак – опухоль имеет форму блюдца с изъязвлением в центральной зоне;
- скирр – патологический процесс распространяется на большую часть органа и проникает вглубь желудочной стенки;
- полипоидный рак – опухоль с четкими границами, визуально напоминающая полип;
- псевдоязвенный рак – данная форма в течение длительного времени напоминает проявления язвы желудка;
- тубулярная аденокарцинома – опухоль из клеток кубического, цилиндрического эпителия;
- слизистая аденокарцинома – опухоль из муцинозных (слизепродуцирующих) клеток.
Согласно классификации TNM, учитывающей степень инфильтрации органа, поражение регионарных лимфатических узлов и наличие метастазирования в отдаленные области, выделяют четыре стадии заболевания. Также существует гистопатологическая классификация, основанная на степени дифференцировки раковых клеток (высокая, средняя, низкая степень, недифференцированная аденокарцинома).
Симптомы аденокарциномы
Наиболее частыми симптомами аденокарциномы желудка являются боль, локализующаяся в эпигастральной области, интенсивность которой обычно не связана с приемом пищи, тошнота, рвота, отрыжка, отсутствие аппетита. Часто развиваются нарушения стула – запоры, диарея. Характерна потеря веса, слабость, апатия. Большое значение имеет выявление «малых» признаков (ощущение дискомфорта в эпигастрии, утрата удовлетворения от пищи, неприятный привкус, утомляемость, снижение трудоспособности, анемизация).
Симптомы заболевания зависят от локализации опухоли, характера ее роста, гистологических характеристик, изменений в других органах. Обычно местные симптомы появляются тогда, когда размеры образования мешают нормальной работе желудка. При наличии опухоли в антральном (выходном) отделе желудка возникает клиника пилоростеноза (сужения просвета пилоруса). Опухоль, локализованная в теле желудка, в течение длительного времени не проявляется, поскольку объем желудка достаточно большой. Такая форма обнаруживается обычно при достижении новообразованием значительных размеров и первыми признаками уже могут быть симптомы общей интоксикации.
При поражении кардиального отдела желудка (его верхней части) развиваются нарастающие признаки дисфагии – больному трудно глотать, необходимо тщательно пережевывать пищу и обильно запивать. При значительных размерах опухоли затруднено прохождение жидкой пищи. При прорастании опухоли желудка в соседние органы, развитии отдаленных метастазов клиника может быть разнообразной и зависит от локализации поражения.
Диагностика
При подозрении на аденокарциному желудка проводится углубленное выяснение анамнеза жизни и заболевания. Детальное выявление специфических симптомов, а также «малых» критериев позволяет предположить злокачественное поражение. Анамнез данного заболевания обычно короткий, характеризуется быстрым прогрессированием симптомов. При объективном обследовании врач-онколог тщательно обследует зоны наиболее частого метастазирования рака желудка: область шеи, печень, легкие, пупок, яичники. Для уточнения диагноза, проведения дифференциальной диагностики применяются:
- Гастроскопия. Позволяет визуализировать патологический очаг, взять образцы ткани из подозрительных участков для проведения гистологического и цитологического исследования.
- Рентгенография желудка. Дает возможность оценить нарушения анатомии внутренней стенки желудка. Определяются характерные для рака признаки: дефект заполнения, изменение контуров.
- Эндосонография. Для определения степени проникновения рака в стенку желудка, близлежащие органы, лимфатические узлы назначается эндоскопическое ультразвуковое исследование. В ходе данного теста возможно проведение тонкоигольной биопсии подозрительного участка (биопсия с ультразвуковым наведением).
- Анализы крови. Общий анализ крови подтверждает наличие анемии. Производится исследование крови на онкомаркеры: РЭА (раковый эмбриональный антиген), СА (раковый антиген).
- Гистологическое исследование. Обнаружение в биоптате раковых клеток является достоверным диагностическим признаком. Определение типа клеток, степени дифференцировки позволяет определить форму заболевания, спрогнозировать течение и составить оптимальную схему лечения.
Компьютерная томография (КТ), магнитно-резонансная томография (МРТ) при раке желудка позволяют выявить опухоль, но главным назначением данных методов является определение поражения близлежащих органов, наличия метастазов в регионарные, отдаленные группы лимфатических узлов, печень, легкие и другие органы. Томография дает возможность определить, какой метод лечения в данном случае будет наиболее эффективным. Дифференциальная диагностика аденокарциномы желудка проводится с гастритом, язвой (особенно каллезной), а также полипами желудка.
Лечение аденокарциномы желудка
Основным и единственно радикальным методом лечения является операция. Лучевая и химиотерапия при данной патологии в качестве самостоятельных методик применяются исключительно в случаях противопоказания к хирургическому вмешательству, а также при четвертой стадии.
Операция может быть проведена в двух вариантах: гастрэктомия (удаляется весь желудок с регионарными лимфоузлами, частью пищевода, тонкого кишечника, других близлежащих к опухоли тканей) или субтотальная резекция (удаляется часть органа с опухолью и небольшой участок окружающих тканей). Выбор тактики определяется размерами, локализацией опухоли, ее гистологическими характеристиками.
Если в ходе стандартной операции образование не может быть полностью удалено, но перекрывает желудок, вызывая существенные нарушения пищеварения, могут быть применены следующие методики:
- эндолюминальное стентирование – введение в желудок стента (трубки), позволяющее сохранить просвет органа. Проводится с целью обеспечения возможности пациента самостоятельно питаться.
- эндолюминальная лазерная терапия – метод эндоскопического лазерного воздействия, при котором раковые клетки удаляются лучом лазера как ножом.
Химиотерапия при аденокарциноме желудка не является высокоэффективным методом. Применяется перед хирургическим лечением с целью уменьшения размеров образования и улучшения результата лечения либо в случае противопоказаний или нецелесообразности проведения операции для улучшения состояния пациента. Как адъювантное лечение, назначается в сочетании с лучевой терапией после резекции с целью уничтожения оставшихся клеток опухоли.
Лучевая терапия также не применяется как самостоятельный метод. Используется в сочетании с оперативным лечением, при противопоказаниях к нему – с химиотерапией. Применяется для уменьшения симптоматики (болевого синдрома) как паллиативный метод.
Прогноз и профилактика
Прогноз при аденокарциноме желудка определяется стадией заболевания, локализацией опухоли. Аденокарциномы нижней части желудка, кардиального отдела обычно имеют лучший прогноз, поскольку ввиду особенностей расположения симптомы проявляются раньше, на более ранних стадиях, когда возможно проведение радикального лечения. Также прогноз зависит от гистологических характеристик рака: чем выше степень дифференцировки клеток, тем лучший результат лечения может быть достигнут.
В большинстве случаев аденокарцинома желудка диагностируется на поздних стадиях, на ранних выявляется лишь у 20% больных. Поздняя диагностика значительно ухудшает прогноз заболевания. Поэтому каждый пациент, находящийся на лечении в отделении гастроэнтерологии, при обнаружении потенциально опасных симптомов должен пройти необходимое обследование для исключения рака. Профилактика рака желудка заключается в рациональном питании, отказе от курения и употребления крепких спиртных напитков, ограничении продуктов, содержащих консерванты, красители.
2. Клинические рекомендации по диагностике и лечению больных раком желудка / Ассоциация онкологов России - 2014
Опухоли пищевода. Доброкачественные и злокачественные опухоли пищевода.
В дистальном отделе пищевода изредка наблюдают аденому, имеющую такое же строение, что и аденомы желудка. Она может развиваться из слизистой оболочки при так называемом пищеводе Баррета, когда в результате хронического рефлюкс-эзофагита и гегеротопяи (что менее вероятно) многослойный плоский эпителий нижней части пищевода замещается цилиндрическим эпителием с формированием структур, соответствующих слизистой оболочке фундального или кардиального отделов желудка, нередко с явлениями кишечной метаплазии.
Рак — наиболее часто встречающаяся злокачественная опухоль пищевода. Чаще наблюдают у мужчин? возраст большинства которых 50—70 лет. К предрасполагающим факторам относятся особенности питания — употребление очень горячей и грубой пищи; недостаток витаминов, особенно В2, А; железа, меди, цинка; вредные привычки (курение, алкоголь и др.); некоторые географические особенности местности; аномалии и посттравматические рубцовые изменения пищевода, грыжа пищеводного отверстия диафрагмы, тилоз (гиперкератоз ладоней и подошв), синдром Пламмера—Винсона (железодефицитная анемия, гипохлоргидрия, дисфагия), наблюдающийся преимущественно у жительниц стран Скандинавского полуострова в возрасте 40 -45 лет и др.
Заболеваемость раком пищевода колеблется в очень широких пределах, достигая наиболее высоких показателей в некоторых районах Ирана, Китая, Туркменской, Казахской, Узбекской ССР и др. Эпидемиологические исследования показали, что в этих районах среди населения чрезвычайно широко распространен хронический эзофагит (60—80% населения и более), который, очевидно, имеет значение в развитии рака пищевода. При гистологическом исследовании на фоне хронического эзофагита обнаруживают очаговые и диффузные атрофические и гиперпластические изменения многослойного плоского эпителия, пролиферацию базальных клеток, очаги дисплазии, внутриэпителиальный и ранний инвазивный рак.
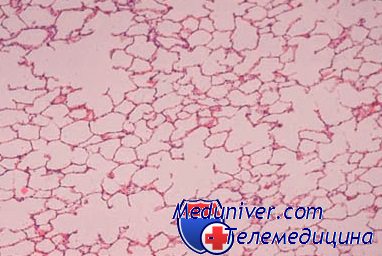
Такие же изменения часто можно обнаружить при раке пищевода, исследуя слизистую оболочку на различном расстоянии от опухоли. Эти изменения, по-видимому, являются основными этапами морфогенеза рака пищевода, что подтверждается динамическими наблюдениями, проведенными в районах Китая с повышенной заболеваемостью раком пищевода.
Предраковые изменения в многослойном плоском эпителии пищевода принципиально не отличаются от аналогичных изменений в шейке матки. Гистологическими критериями дисплазии являются усиление пролиферации и нарушение дифференцировки клеток. Количество базальных клеток, которые в норме занимают не более 15% толщины эпителиального пласта, при дисплазии увеличивается, клетки становятся более крупными, полиморфными, увеличивается число митозов. В зависимости от выраженности клеточных изменений и степени их распространения в эпителиальном пласте различают слабую» умеренную и тяжелую дисплазию. Выраженные полиморфизм и атипия клеток, большое количество митозов, утрата полярности расположения клеток и деления на слои при сохранении базальной мембраны характерны для внутриэпителиального рака.
В тех случаях, когда базальная мембрана не прослеживается, имеется тенденция к погружному росту и отшнуровка эпителиальных комплексов, изменения должны расцениваться как начало инвазивного рака.
При гистологическом исследовании, особенно по материалу эндоскопической биопсии, бывает трудно дифференцировать диспластические (предраковые) изменения и реактивную гиперплазию базальных клеток, которая может наблюдаться, например, при рефлюкс-эзофагите.
Трудности возникают также при дифференциальной диагностике тяжелой дисплазии, карциномы in situ и инвазивного рака. Для уточнения характера процесса необходимы динамическое наблюдение за такими больными и повторные биопсии.
Основная масса форм плоскоклеточного рака пищевода, видимо, развивается из покровного эпителия. Другим источником развития рака пищевода могут быть слизистые железы, в которых при хроническом гастрите также наблюдают атрофические и гиперпластические изменения, образование кист, пролиферацию резервных клеток, плоскоклеточную метаплазию и дисплазию эпителия. Из них могут возникать плоскоклеточный рак, аденокарцинома, железисто-плоскоклеточный рак, а также мукоэлидермоидная опухоль и аденокистозный рак (цилиндрома), аналогичные соответствующим опухолям слюнных желез. Аденокарциномы в пищеводе могут развиваться также от остатков цилиндрического эпителия, выстилающего пищевод на ранних стадиях эмбриогенеза, участков гетеротопии слизистой оболочки желудка.
Аденокарциномы дистальной части пищевода могут развиваться также на фоне так называемого пищевода Баррета. Во многих случаях труден или невозможен дифференциальный диагноз такой аденокарциномы и рака кардиального отдела желудка, прорастающего в пищевод.
Рак пищевода наиболее часто локализуется в средней его трети, затем следует нижняя треть пищевода; верхняя его треть поражается редко. Исключение составляет рак пищевода при синдроме Пламмера—Винсона, который наблюдается преимущественно у женщин 40—45 лет и поражает самый верхний отрезок пищевода.
Макроскопически большинство форм рака пищевода представляет собой изъязвленные блюдцеобразные или эндофитные опухоли, часто циркулярно охватывающие стенку, нередко на значительном протяжении. Экзофитные опухоли встречаются редко. Рак пищевода может распространяться по подслизистому слою далеко за пределы видимого очага опухоли, а также прорастать в прилежащие к пищеводу ткани и органы. Для суждения о степени распространенности процесса и радикальности оперативного вмешательства при исследовании удаленного отрезка пищевода необходимо изучение линий операционных разрезов и глубины прорастания стенки пищевода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

