Что показывает иммунограмма при герпесе
Обновлено: 23.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Генитальный герпес: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Генитальный герпес – хроническое рецидивирующее заболевание вирусной этиологии, передающееся преимущественно половым путем. Герпес считается крайне распространенным эрозивно-язвенным заболеванием половых органов - ежегодно в мире регистрируется 500 000 новых случаев обращений по этому поводу. В Российской Федерации у лиц старше 18 лет инфицированность вирусом, вызывающим генитальный герпес, составляет 17,2 случая на 10 000 населения.
В 70% случаев заболевание протекает бессимптомно, что и обусловило широкое распространение этой патологии.
Причины появления генитального герпеса
Генитальный герпес вызывает вирус простого герпеса (ВПГ) I и/или II типов. Вирус герпеса I типа чаще всего поражает слизистую оболочку рта и носит название орального (лабиального) герпеса. При заражении этим вирусом очаги поражения локализуются на лице в области губ.
Вирус герпеса II типа чаще вызывает генитальный герпес, однако оба типа могут провоцировать развитие патологии оральной и генитальной локализации. Для ВПГ II типа более характерно рецидивирующее течение, чем для ВПГ I.
- Половой путь – самый часто встречающийся путь передачи генитальной герпетической инфекции.
- Передача вируса бытовым путем является самой редкой.
- Аутоинокуляция – перенос вируса с зараженных участков слизистой на здоровые самим больным.
- Трансплацентарный – через плаценту от инфицированной матери плоду.
- Перинатальный – в процессе родов.
- Контактно-бытовой (при несоблюдении правил ухода и гигиены).
- Аутоинокуляция (см. выше).
- Беспорядочная половая жизнь без использования барьерной контрацепции (презервативов).
- Нарушение правил личной и бытовой гигиены.
- Снижение иммунитета (в силу наличия длительно текущих хронических заболеваний, несбалансированного питания, подверженности частым стрессам, нарушения режима сна).
- Первый эпизод развития клинической симптоматики генитального герпеса.
- Рецидивирующая герпетическая инфекция.
- Инфекция мочеполовых органов.
- у мужчин,
- у женщин.
- Инфекция прямой кишки и перианальной кожи.
- Герпес с типичной клинической картиной.
- Атипичное течение.
Если иммунная система справляется с вирусом на этом этапе, то формируется иммунитет и носительство вируса, не исключающее рецидива заболевания при ослаблении защитных функций организма.
Если у организма нет ресурсов противостоять ВПГ, то вирус проникает во внутренние органы и фиксируется на них. При снижении иммунитета, прочих вирусных инфекциях или при обострениях хронических заболеваний ВПГ из органов вновь выходит в кровь и с ее током разносится по организму.
Симптомы генитального герпеса
При первичном инфицировании инкубационный период составляет от 1 до 10 дней, а клинические проявления длятся от 18 до 24 дней с нарастанием симптоматики в течение недели. До возникновения очагов повреждения у 50% больных появляются продромальные симптомы - парестезии, чувство жжения в генитальной области, невралгии в ягодичной, паховой бедренной областях, дизурия - и продолжаются до 24 часов. В последующем вирусное повреждение эпителия проявляется в виде везикул на эритематозном фоне с дальнейшим характерным разрешением (образованием корочек). Симптомы общей интоксикации, свойственные любой вирусной инфекции, – недомогание, слабость, субфебрилитет, головная боль - развиваются, как правило, при первичном инфицировании, при рецидиве они минимальны.
Непервичная генитальная герпетическая инфекция протекает менее выраженно: длительность клинических проявлений составляет до 15 дней, реже наблюдается бессимптомное выделение вируса, длительность слущивания поврежденного эпителия составляет всего 4-5 дней.
Высыпания на половых органах и/или в перианальной области всегда носят пузырьковый характер, содержимое прозрачное, основание пузырьков гиперемировано (красного цвета); могут быть множественными и единичными.
Пораженная область слизистой оболочки отечная. У мужчин самая частая локализация высыпаний – мошонка, половой член, лобок, промежность, перианальная область.
У женщин – клитор, влагалище, вульва, лобок, шейка матки, перианальная область. В случае присоединения вторичной (чаще бактериальной) инфекции появляются гнойные и слизисто-гнойные выделения.
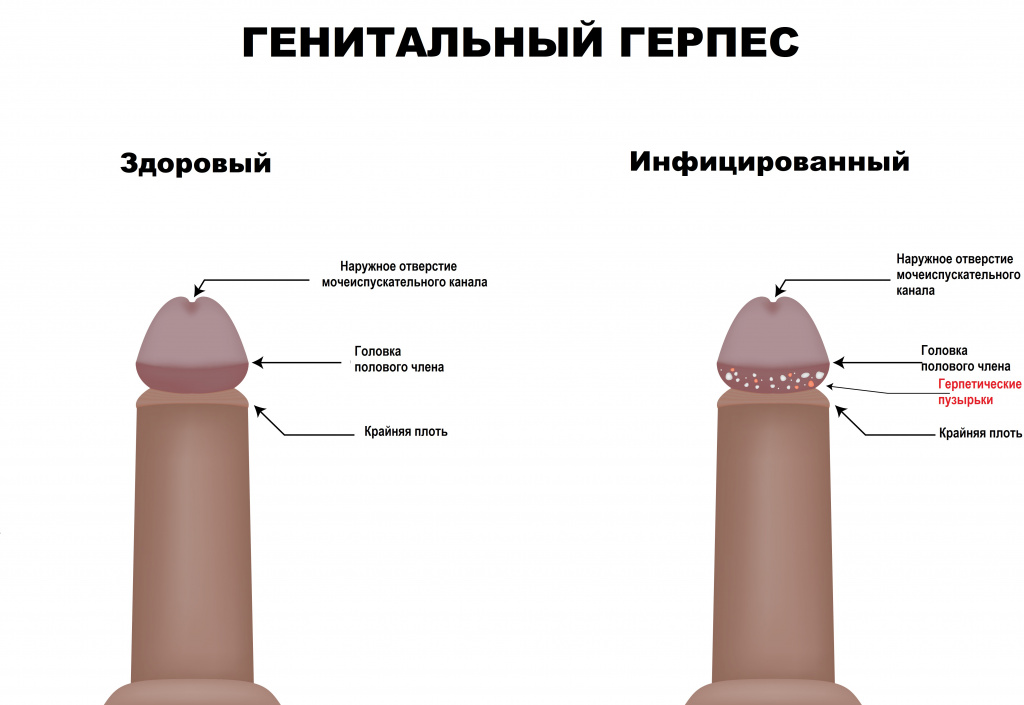
В случае обострения генитального герпеса присутствует боль при половом контакте.
Диагностика генитального герпеса
Диагностика этого заболевания строится на характерной клинической картине высыпаний и на выявлении ДНК вируса в крови или в отделяемом с пораженных тканей.
Необходимо сдать анализы крови для подтверждения инфицированности вирусом герпеса и определения активности процесса, для выявления ДНК вируса в эякуляте, секрете простаты, в соскобе клеток урогенитального тракта, а также в соскобах с конъюнктивы, кожи, слизистой оболочки носа, ротоглотки.
Раздельное определение ДНК-вируса простого герпеса 1 типа (губного или лабиального) и 2 типа (генитального) в сыворотке крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме реального времени. Термин "герпес" (от древнегреч. – ползти, ползучи.
1 ГОУ ВПО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого» Минздравсоцразвития России
Вирусы герпеса широко распространены в человеческой популяции, они способны поражать практически все органы и системы организма-хозяина, вызывая латентную, острую и хроническую формы инфекции. Вирусами герпеса инфицировано 65-90 % населения планеты. По данным ВОЗ, смертность, обусловленная герпесвирусами, занимает второе место после гриппа. Считается, что на территории России различными формами герпетической инфекции страдают около 20 млн человек. Особую актуальность герпетическая инфекция приобрела в связи с одновременной циркуляцией в организме человека нескольких серотипов вирусов одновременно. При герпесе, как и при других заболеваниях с персистенцией вируса, часто развиваются иммунодефицитные состояния, обусловленные недостаточностью различных звеньев иммунной системы и её неспособностью полностью элиминировать вирус из организма. По данным ряда исследователей, у больных с хронической герпесвирусной инфекцией в сравнении с контролем обнаружено достоверное повышение цито-токсических клеток (CD8), лейкоцитарного индекса интоксикации, снижение содержание Т-хелперов (CD4), T-клеток (CD3), иммуно-регуляторного индекса в периоде обострения заболевания. Изменения клеточного иммунитета зависело от периода заболевания и степени тяжести патологического процесса, то есть чем тяжелее протекало заболевание, тем выраженнее были иммунологические изменения. При наличии микст-инфекции (герпес 1, 2 типов в комплексе с цитомегаловирусом) авторы отмечали увеличение количества активированных T-лимфоцитов и клеток T-хелпера, тогда как смешанная инфекция (цитомегаловирусная инфекция и ВЭБ-инфекция) сопровождалась острым уменьшением в лимфоцитах CD3+/CD95+. Спектр клинических проявлений герпесвирусных инфекций отличается значительным разнообразием, однако все более характерным для данных инфекций становится атипичное течение с преобладанием первично-хронических и рецидивирующих форм. Все чаще хронические герпесвирусные инфекции ассоциируются с формированием у больных синдрома хронической усталости. В последние годы при изучении патогенеза герпесвирусных инфекций были получены доказательства ключевой роли иммунной системы и неспецифической резистентности организма в развитии особенностей течения заболевания. Это связано с тем, что нарушения иммунного реагирования являются немаловажным фактором, определяющим течение болезни и ее исход. Знание особенностей иммунопатогенеза хронической формы герпесвирусных инфекций позволит предупредить развитие активного непрерывно-рецидивирующего варианта заболевания и позволит наиболее эффективно определить тактику терапии, особенно у пациентов с часто рецедивирующими формами.

1. Воробьев А.А. Иммунология и аллергология. / А.А. Воробьев, А.С. Быков, А.В. Караулов. – 2006. – 287 с.
2. Герпесвирусные инфекции человека: руководство для врачей / В.А Исаков, Е.И. Архипова, Д.В. Исаков / под ред. В.А. Исакова – СПб.: СпецЛит, 2006. – 303 с.
4. Камбачокова З.А. Состояние клеточного и гуморального иммунитета у больных рецедивирующим генитальным герпесом // Медицинский вестник Башкорстана 2012. – № 1 (7). – С. 46–49.
5. Нагоев Б.С., Камбачокова З. А. Состояние клеточного иммунитета у больных герпесвирусными инфекциями // Вестник новых медицинских технологий. – 2011. – № 3 (18). – С. 325–327.
6. Синдром хронической усталости: диагностика и лечение / под ред. Ю.В. Лобзина. – СПб.: СпецЛит, 2005. – 79 с.
7. Соколова Т.Ф., Минакова Е.Ю., Долгих Т.И. Изучение иммунофенотипа лимфоцитов у пациентов с микст-инфекцией, вызванной вирусами семейства HERPESVIRIDAE // Медицинская иммунология. – 2010. – № 4–5 (12). – С. 433–436.
8. Черевко Н.А., Попова И.С., Климов В.В. и др. Особенности изменения популяционного иммунитета населения на фоне гепрес-инфицирования // Российский аллергологический журнал. – 2010. – № 1 (1). – С. 207–208.
9. Fatahzadeh M., Schwartz R.A. Human herpes simplex virus infections: epidemiology, pathogenesis, symptomatology, diagnosis, and management // J. Am. Acad. Dermatol. – 2007. – № 57 (5). – Р. 737–63; quiz 764–6.
10. Loutfy S.A., Alam El-Din H.M., Ibrahim M.F., Hafez M.M. Seroprevalence of herpes simplex virus types 1 and 2, Epstein-Barr virus, and cytomegalovirus in children with acute lymphoblastic leukemia in Egypt Kundi // Saudi Med J. – 2006. – № 27 (8). – Р. 1139–45.
11. Koelle D.M., Corey L. Herpes Simplex: Insights on Pathogenesis and Possible Vaccines // Annu Rev Med. – 2008. – № 59. – Р. 381–395.
12. Manchini, G. Immunochemical quantitation of antigens by single radical immunodiffusion / G. Manchini, A.O. Carbonara, J.F. Heremas // Immunochemistry. – 1965. – Vol. 2. – P. 235–254.
13. Wozniak M.A., Mee A.P., Itzhaki R.F. (January). Herpes simplex virus type 1 DNA is located within Alzheimer’s disease amyloid plaques // J Pathol. – 2009. – № 217 (1). – Р. 131–8.
Вирусы герпеса широко распространены в человеческой популяции, они способны поражать практически все органы и системы организма-хозяина, вызывая латентную, острую и хроническую формы инфекции [1, 2, 9]. Вирусами герпеса инфицировано 65–90 % населения планеты. По данным ВОЗ, смертность, обусловленная герпесвирусами, занимает второе место после гриппа. Считается, что на территории России различными формами герпетической инфекции страдают около 20 млн человек. Особую актуальность герпетическая инфекция приобрела в связи с одновременной циркуляцией в организме человека нескольких серотипов вирусов одновременно. При герпесе, как и при других заболеваниях с персистенцией вируса, часто развиваются иммунодефицитные состояния, обусловленные недостаточностью различных звеньев иммунной системы и её неспособностью полностью элиминировать вирус из организма [1, 9, 10]. По данным ряда исследователей, у больных с хронической герпесвирусной инфекцией в сравнении с контролем обнаружено достоверное повышение цито-токсических клеток (CD8), лейкоцитарного индекса интоксикации, снижение содержание Т-хелперов (CD4), T-клеток (CD3), иммуно-регуляторного индекса в периоде обострения заболевания. Изменения клеточного иммунитета зависело от периода заболевания и степени тяжести патологического процесса, то есть, чем тяжелее протекало заболевание, тем выраженнее были иммунологические изменения [3, 4, 11, 12]. При наличии микст-инфекции (герпес 1, 2 типов в комплексе с цитомегаловирусом) авторы отмечали увеличение количества активированных T-лимфоцитов и клеток T-хелпера, тогда как смешанная инфекция (цитомегаловирусная инфекция и ВЭБ-инфекция) сопровождалась острым уменьшением в лимфоцитах CD3+/CD95+ [5,10].
Спектр клинических проявлений герпесвирусных инфекций отличается значительным разнообразием, однако все более характерным для данных инфекций становится атипичное течение с преобладанием первично-хронических и рецидивирующих форм [1, 9]. Все чаще хронические герпесвирусные инфекции ассоциируются с формированием у больных синдрома хронической усталости [6, 13].
В последние годы при изучении патогенеза герпесвирусных инфекций были получены доказательства ключевой роли иммунной системы и неспецифической резистентности организма в развитии особенностей течения заболевания. Это связано с тем, что нарушения иммунного реагирования являются немаловажным фактором, определяющим течение болезни и ее исход. Знание особенностей иммунопатогенеза хронической формы герпесвирусных инфекций позволит предупредить развитие активного непрерывно-рецидивирующего варианта заболевания и позволит наиболее эффективно определить тактику терапии, особенно у пациентов с часто рецедивирующими формами.
Целью настоящей работы явилось изучение особенностей иммунного ответа при хронической герпетической инфекции и оценка эффективности сочетанной противовирусной и иммуномодулирующей терапии (Панавир и Глутоксим).
Материалы и методы исследования
Основную группу составили 30 пациентов обоего пола с хронической рецидивирующей инфекцией, вызванной вирусом простого герпеса (ВПГ), вирусом Эпштейна-Барр (ВЭБ), цитомегаловирусом (ЦМВ) или их сочетанием (микст-инфекция) возрастом от 20 до 50 лет. Отбор больных в группы осуществлялся методом сплошного наблюдения при обращении в консультативную поликлинику Красноярской краевой клинической больницы. Анализ результатов проводился при обострении заболевания.
Контрольную группу составили 36 практически здоровых на момент обследования человек, идентичных по полу и возрасту, без острых патологических процессов в течение 2-х месяцев, предшествующих обследованию, а также хронических заболеваний в анамнезе.
Для иммунологического исследования в утренние часы натощак согласно стандартной методике у всех пациентов проводилось взятие периферической крови из локтевой вены в вакуумные пробирки Green Vac-Tube (Южная Корея) с консервантом, содержащим раствор Li-гепарин и этилендитетрамин (ЭДТА).
Лимфоциты периферической крови выделяли в градиенте плотности фиколл-верографина по методу А. Boyum (1968). Определение в крови регуляторных субпопуляций лимфоцитов проводилось методом проточной цитофлуориметрии с помощью Epics XL («Beckman Coulter», США) с использованием панели сертифицированных моноклональных антител, меченных флуоресцеинизотиоционатом (FITC – Fluorescein Isothyocyanate, англ.), фикоэритрином (PE – Phycoerythrin, англ.), фикоэритрином-Техасским красным (ECD – Energy Coupled Dye или PE-TxR, англ.) линии IOTest («Beckman Coulter», США). Данным методом определялись соответственно кластеры клеточной дифференцировки (CD – Cluster of Differentiation, англ.) клеток человека: Т-лимфоциты, несущие CD3+, – маркер всех зрелых Т-клеток крови, CD4+ – маркер Т-хелперных клеток, CD8+ – цитотических Т-лимфоцитов. Рассчитывали соотношение CD4+/CD8+. Для удаления эритроцитов подготовку проб крови проводили по безотмывочной технологии с использованием следующих лизирующих растворов: OptiLyse C («Beckman Coulter», США). Для корректного исключения из зоны анализа всех частиц, которые не соответствовали по размерам и гранулярности живым лимфоцитам, вводили необходимые логические ограничения в гистограммы распределения частиц по малоугловому, боковому светорассеянию. Математическую обработку цитометрических данных проводили при помощи программ EXPO-32 и CXP v. 2.2 («Beckman Coulter», США). В каждой пробе анализировали не менее 104 клеток, используя трёхцветный цитометрический анализ.
Определение концентрации циркулирующих иммунных комплексов проводилось после инкубации сыворотки крови с раствором ПЭГ-6000 и последующим учетом результатов на фотоэлектроколориметре фильтр № 1 (длина волны 315 нм). Концентрация сывороточных иммуноглобулинов IgA, IgM, IgG измерялась методом Mancini [12]. Определение количественных показателей фагоцитарного звена производилась методом латексной агглютинации [7].
Иммуноферментным методом с использованием тест-систем фирмы «HUMAN» (Германия) определялись титры специфических антител (IgM и IgG) в сыворотке крови к указанным возбудителям и авидности специфических антител IgG к ВПГ, ЦМВ и IgG к VCA, EA, NA-антигенам ВЭБ.
Статистическая обработка результатов исследования проводилась с помощью непараметрического критерия Манна–Уитни (T) [8].
Результаты исследования и их обсуждение
Все пациенты с хронической формой герпесвирусной инфекции при осмотре предъявляли жалобы на наличие у них без видимых причин выраженной утомляемости, усталости и снижения работоспособности, которые отмечались в течение последних 1–3 лет. У 7 больных (23,33 %) на протяжении этого срока отмечалась постоянная температура до 37,2–37,5 °С с периодическими повышениями до 38 °С и ознобами. Значительная часть обследованных (21 человек; 70,00 %) предъявляли жалобы на эпизоды повышения температуры до 38°С, повторяющиеся 2–4 раза в год и продолжающиеся до 2–3 недель. Практически все пациенты (93,33 %) отмечали частые периодические боли в горле или повторные ОРВИ (5 и более раз в год). У большинства имели место разной степени выраженности головные боли, нарушения сна и ухудшение памяти (17 человек; 56,67 %), миалгия (66,67 %), артралгия (26,67 %) и мышечная слабость с быстрой утомляемостью (83,33 %). При осмотре у 22 больных (73,33 %) определялись увеличение и легкая болезненность лимфатических узлов, чаще – шейных, затылочных и нижнечелюстных, а у 7 человек (23,33 %) установлено наличие гепатоспленомегалии. Учитывая данную симптоматику, больным был выставлен диагноз СХУ (по МКБ 10 – G93.3).
В качестве стандартной терапии назначался Панавир – высокомолекулярный полисахарид, относящийся к классу гексозных гликозидов, обладающий противовирусным действием за счёт индукции интерферонов всех субклассов, а также Глутоксим, являющийся иммуномодулятором и системным цитопротектором за счёт влияния на внутриклеточные процессы тиолового обмена.
После лечения субфебрильная температура тела и боли в горле сохранялись лишь у 5 пациентов (16,7 %). Лимфаденопатия отмечалась всего у 8 пациентов (26,7 %), миалгии – у 7 (23,3 %), слабость, утомляемость – у 10 (33,3 %), а нарушения памяти и расстройства сна – у 9 (30 %).
Таким образом, после комбинированной противовирусной и иммуномодулирующей терапии отмечается значительная регрессия основных симптомов заболевания.
По сравнению с контрольной группой отмечалось уменьшение содержания IgА в сыворотке крови и увеличение уровня ЦИК, уровни же других классов иммуноглобулинов достоверно не различались. Также было отмечено уменьшение количества активно-фагоцитирующих клеток и подавление их поглотительной способности.
После лечения в группе больных с хронической герпесвирусной инфекцией наблюдалось стремление к нормализации иммунорегуляторного индекса за счёт роста процентного содержания CD4 и снижения уровня CD8, что связано с уменьшающейся вирусной нагрузкой. Отмечалась тенденция к увеличению уровня IgА в сыворотке крови и достоверное увеличение уровня IgG по сравнению с группой контроля, несколько уменьшался уровень ЦИК. По фагоцитарному звену отмечена нормализация показателей поглотительной активности (фагоцитарный индекс достоверно с контролем не различался).
По маркёрограмме герпесвирусных инфекций при сравнении групп между собой (табл. 2) значительно снижалось содержание Ig G EBNA к ВЭБ, практически не встречались маркёры активации ВЭБИ (Ig G EA к ВЭБ – у 3,33 %, Ig M VCA к ВЭБ – у 3,33 %), увеличивалась авидность Ig G VCA к ВЭБ. Отмечено снижение титра IgG к ВПГ и ЦМВ и увеличение авидности этих антител.
Показатели иммунного статуса больных хроническими герпесвирусными инфекциями до и после лечения (M ± m)
Мы успешно занимаемся лечением герпетических инфекций (цитомегаловирус, герпес 1 и 2 типа, герпес 6 типа, вирус Эпштейн-Барр и т.д.) и их осложнений. В нашей клинике пациентов с вирусами группы герпеса ведет врач иммунолог. По необходимости мы подключаем специалистов смежных специальностей, в зависимости от клинических проявлений герпетической инфекции.
В окружающей среде вирусы группы герпеса встречаются повсеместно. Носительство вирусов группы герпеса, если оно не вызывает болезни, – норма для здорового человека. При нормально работающей иммунной системе вирус герпеса работает подобно вакцине, стимулируя иммунную систему, создавая перекрестный иммунитет к другим инфекциям. В случае ослабления иммунной системы герпес может атаковать организм. Таким образом, если герпес в организме ведет себя агрессивно, это говорит о недостаточной защитной функции иммунитета, снижении иммунитета. Вирусы герпеса могут атаковать организм до тех пор, пока не будет восполнено недостающее звено иммунной защиты, поэтому и лечение цитомегаловируса, вируса Эпиштейн-Барр, и т.д. начинается с восстановления работы иммунной системы.
Причины снижения иммунитета к герпесу
- Нервное расстройство (тревога, нарушение сна)
- Бактериальные и грибковые инфекции (стрептококк, стафилококк, хронический тонзиллит, дисбактериоз кишечника, молочница)
- Дефицит витаминов Д, В, С, А. Е
- Эндокринные нарушения – инсулинорезистентность, снижение функции щитовидной железы, снижение продукции половых гормонов, высокий уровень гормона пролактина.
- Лечение препаратами, снижающими иммунитет
- Вирус простого герпеса типа 1 (Herpes simplex virus-1, HSV-1);
- Вирус простого герпеса типа 2 (Herpes simplex virus-2, HSV-2); ;
- Вирус Эпштейна — Барр (Epstein-Barr virus, EBV);
- Цитомегаловирус (Cytomegalovirus, CMV);
- Герпесвирусы человека типов 6, 7, 8 (HHV 6, 7, 8).
Симптомы герпетической инфекции
- Герпетические поражения слизистых оболочек полости рта (герпес часто появляется на губах) и генитальный герпес; , нервные расстройства;
- Герпетические поражения кожи и периферических нервов – герпес Зостер, попоясывающий лишай;
- Острые и хронические респираторные заболевания (например, фарингит, тонзиллит);
- Герпетические поражения глаз;
- Вирусные инфекции нервной системы;
- Поражение внутренних органов (печени, легких, органов пищеварения и др.);
- Злокачественные опухоли и болезни крови.
Лечение герпеса
Лечение цитомегаловируса, вируса Эпштейн-Барр, герпеса 1,2,6 типов в клинике “Эхинацея”
«Простерилизовать» живого человека от вирусов группы герпеса невозможно, да и не имеет смысла. Человек встречается с герпесвирусами повседневно, но в норме ничего плохого это не приносит. Заболевание наступает только при ослаблении иммунной защиты организма. Поэтому не имеет смысла лечить герпес как таковой, смысл лечения состоит в том, чтобы вернуть иммунной системе контроль над герпесом и уменьшить количество вирусов до подконтрольного иммунной системе.
В нашей клинике лечение герпетических инфекций строится по следующей схеме:
- В первую очередь мы установим почему ослаб иммунитет. Анализ крови – подробная иммунограмма поможет выяснить, что именно происходит с Вашей иммунной системой, какие звенья иммунитета ослабли. На основании иммунограммы мы сможем предложить лечение, направленное точно в цель.
- Также мы выполним обследование на другие инфекции (микоплазма, хламидия, йерсиния, токсоплазма и др.), которые могут «цепляться» к ослабленному организму при снижении иммунитета и тем самым ухудшать положение. Если инфекции обнаружены, врач рекомендует лечение, согласованное с общей программой.№
- Курс восстановления иммунной системы (иммунореабилитация). Современные лекарственные средства позволяют помочь именно тому звену иммунитета, которое оказалось ослабленным. Здесь важно подобрать лечение так, чтобы оно не стимулировало нормально работающие иммунные процессы. Так мы обеспечиваем безопасность лечения. По мере восстановления нормальной работы иммунитета влияние вирусов на здоровье будет становиться все меньше и меньше.
- Проведем контрольные анализы после курса лечения. Обычно мы выполняем их через 3-4 месяца и затем через полгода – год.
При необходимости курс лечения проводится совместно иммунологом и гинекологом, иммунологом и ЛОР врачом.
Будем рады помочь Вам в лечении цитомегаловируса, вируса Эпштейн-Барр вируса и других вирусов группы герпеса!
Ведущей деятельностью нашей клиники является лечение и диагностика заболеваний иммунной системы. Будем рады помочь Вам в восстановлении правильной работы иммунитета, проведении и расшифровки иммунограммы. Сдать анализ на иммунный статус (иммунограмму) в нашей клинике Вы можете 7 дней в неделю. По Вашему желанию предложим Вам помощь врача иммунолога.
Основная функция иммунной системы человека – это определение, нейтрализация и удаление из организма генетически чужеродных веществ. Это могут быть бактерии, вирусы, грибы, различные токсины и т.д. Если одно из звеньев иммунной системы ослабевает или наоборот, чрезмерно активируется – возможно заболевание. Это может быть инфекция (например, вирус герпеса, молочница и др.), аллергия, злокачественная опухоль (здоровая иммунная система ежедневно уничтожает появляющиеся опухолевые клетки), аутоиммунное заболевание (атака иммунитета против здоровых тканей организма). Разные клетки и молекулы иммунитета выполняют различную работу. Лекарств «для всего иммунитета» не бывает, поэтому до начала лечения нужно определить причину нарушения работы иммунитета (сделать иммунограмму). Иммунограмма – это серия анализов, которые помогают определить, где именно, в каком из процессов иммунитета произошла поломка. В показателях иммунограммы обычно видно, что некоторые процессы в иммунитете идут нормально, а некоторые подавлены или наоборот, чрезмерно активированы. Иммунологическое лечение должно попадать точно в цель, работать точно там, где есть нарушения. Главная задача любого лечения иммунитета – это помочь восстановиться ослабленным иммунным процессам, не мешать правильно работающим процессам, а чрезмерно активированные – «охладить». Просто сдать кровь на иммунограмму недостаточно: нужно соотнести показатели иммунограммы с общим состоянием организма, текущими заболеваниями, качеством сна и психического самочувствия.
Что такое иммунограмма?
Иммунограмма это комплексное исследование основных показателей иммунной системы человека. Обычно, основным материалом для исследования иммунного статуса служит венозная кровь, но для исследования могут использоваться слюна, ликвор и соскоб из носоглотки.
Что показывает иммунограмма? Основные параметры:
- Состояние клеточного иммунитета. Определяются маркеры иммунокомпетентных клеток, количество разных видов клеток иммунитета и их процентное соотношение. Виды клеток иммунитета – как рода войск: у каждого вида клеток своя работа.
- Состояние гуморального иммунитета. Исследуется уровень иммуноглобулинов IgA, IgG, IgM, IgE. Иммуноглобулины – это антитела, которые могут связывать чужеродные агенты. Исследуются циркулирующие иммунные комплексы (ЦИК).
- Интерфероновый статус. Исследуются интерфероны или интерфероновый статус. Интерфероны – это сигнальные молекулы, которые передают возбуждающие или тормозящие сигналы от клетки к клетке. Интерфероны обладают и прямым уничтожающим действием на вирусы и опухолевые клетки. Интерфероновый статус поможет оценить содержание интерферонов альфа и гамма в крови, способность клеток иммунной системы вырабатывать интерфероны.
- Система комплемента – компоненты комплемента С3 и С4. Комплемент – это элемент врожденного иммунитета т.е. комплекс белков, предназначенный для защиты организма от чужеродных агентов. Система комплемента работает вне зависимости от наличия/отсутствия иммунологической памяти к конкретным микробам: распознает микробы по их общим признакам.
- Функция фагоцитоза. Это способность иммунных клеток захватывать чужеродные организмы. Фагоцитирующая функция нейтрофилов, обычно, проверяется с помощью НСТ-теста (тест с нитросиним тетразолием).
- В ряде случае определяются аутоиммунные маркеры. Это циркулирующие иммунные комплексы, антинуклеарный фактор и различные аутоантитела, направленные против тканей собственного организма.
- Может определяться иммуноглобулин Е (IgE). IgE участвует в аллергических реакциях.
- Эозинофильный катионный белок (ECP). Белок, высвобождающийся при аллергическом процессе. По высокому уровню эозинофильного катионного белка можно определить текущий аллергический процесс, инвазию крупными паразитами.
- Состояние и работа вилочковой железы. Это железа, в которой созревают и проходят «обучение» Т-лимфоциты. Для этого можно посмотреть соответствующие маркеры в анализе крови на иммунный статус и оценить строение и размеры вилочковой железы с помощью компьютерной томографии (КТ органов грудной клетки).
| Клетки: | Маркеры: |
| В-лимфоциты | CD19, CD20, CD22 |
| Клетки естественные киллеры (NK-клетки) | CD3-CD16+CD56+ |
| Все Т-лимфоциты, включая Т-хелперы, Т-цитотоксические, Т-киллеры | CD3 |
| Т-киллеры | CD3+CD16+CD56+ |
| Т-хелперы | CD3+CD4+ |
| Цитотоксические Т-лимфоциты (старое название – Т-супрессоры) | CD3+СD8+ |
| Клетки, с которыми может соединяться интерлейкин-2. К ним относятся регуляторные Т-клетки, которые могут участвовать в торможении воспалительных реакций. | CD3+CD25+ |
Реже смотрятся другие специфические параметры (расширенная иммунограмма), в зависимости от целей и задач поисков.
Расшифровка иммунограммы – это процесс, который выполняется врачом по результатам исследования иммунограммы и других исследований, включая рентгеновские снимки, УЗИ и осмотр пациента. Без присутствия пациента иммунограмму достаточно трудно интерпретировать и не всегда это возможно сделать правильно. Например, если иммунитет был изначально снижен, а пациент заболел каким-то воспалительным заболеванием (к примеру, активировался вирус герпеса), то во время активного воспалительного процесса иммунитет будет работать более агрессивно и иммунограмма может стать ложно-нормальной. Картина чрезмерно активированного иммунитета может наблюдаться, если у пациента изначально был нормальный иммунитет, но он недавно переболел или перенес вакцинацию, травму. Расшифровка иммунограммы может проводиться одновременно с осмотром пациента в кабинете у врача иммунолога. Здесь важен полноценный физикальный осмотр пациента врачом иммунологом, с оценкой состояния лимфатических узлов, слизистых оболочек, органов дыхания, суставов, кожи и др. Это помогает правильно расшифровать и интерпретировать иммунограмму, с учетом персональных особенностей и текущего состояния здоровья.
Подготовка к исследованию иммунного статуса. Иммунограмма делается в комплексе с общим анализом крови. Сдавать кровь на иммунограмму нужно утром, натощак. Для того, чтобы избежать искажения результатов в анализе, мы рекомендуем воздержаться от приема алкоголя и курения за 1-2 дня до исследования иммунного статуса. Сдавать кровь на иммунограмму не рекомендуется во время менструации и на фоне острых инфекционных заболеваний, протекающих с высокой температурой.
Иммунограмму можно сдать в нашей клинике. По результатам исследования мы предложим Вам консультацию врача иммунолога, который даст расшифровку иммунограммы, порекомендует соответствующее лечение или направит надо дополнительное обследование, если требуется.
Стоимость анализа на иммунитет (иммунограммы) зависит от количества показателей, которые нужно учитывать при назначении лечения.
Зачем нужна иммунограмма
Мы можем предложить Вам полноценное лабораторное обследование иммунитета и помощь аллерголога-иммунолога при “расшифровке” анализов на иммунитет. Действует выгодное спецпредложение
| Вид иммунограммы | Результат иммунограммы |
| Иммунограмма стандартная |  |
| Иммунограмма расширенная |  |
| Интерфероновый статус |  |
Образцы результатов исследований с расшифровкой
Основные показания для обследования иммунитета
Мы обследуем иммунную систему, если заболевание протекает при ее участии. В основном, это:
Обследование на наличие инфекций
Одновременно с исследованием иммунной системы мы обычно уточняем наличие в организме инфекций и характер их взаимодействия с иммунитетом. Человек постоянно взаимодействует с микробами. В норме микробы оказываются под контролем иммунной системы и во внутренние среды организма не проникают. Но если работа иммунитета нарушена – заражение происходит легко. Лечение таких инфекций правильнее проводить в комплексе с восстановлением иммунной системы. Поэтому правильное обследование перед лечением – это «Иммунограмма + Инфекции». Действует выгодное спецпредложение
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Герпес: причины появления, симптомы, диагностика и способы лечения.
Определение
Герпесом, или герпетической инфекцией, называют несколько заболеваний, вызываемых вирусами отряда Herpesvirales семейства Herpesviridae.
Все они характеризуются поражением кожи, слизистых оболочек с локализацией либо в области глаз, носа и губ, гениталий, а также нервных волокон.
У лиц с иммунодефицитом могут наблюдаться генерализованные формы инфекции с вовлечением в процесс других органов и тканей.

Среди известных науке восьми типов герпеса самым распространенным является вирус герпеса простого типа (Herpes simplex virus).
Простой вирус герпеса достаточно неустойчив во внешней среде. В условиях комнатной температуры сохраняется до 24 часов, на металле — до 2 часов. Под действием температуры выше 50°C погибает за 30 минут, под действием спирта и хлорсодержащих веществ - в течение нескольких минут, при замораживании сохраняется до пяти суток.
Причины герпетической инфекции
Источником инфицирования всегда служит человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Возбудитель может передаваться воздушно-капельным, контактно-бытовым или половым путем, а также от матери плоду через плаценту, во время родов или грудного вскармливания.
К вирусу восприимчивы все люди, хотя у многих отмечаются бессимптомные формы заболевания. Попадая через слизистую рта, половых органов или дыхательные пути в организм человека, герпесная инфекция остается в нем навсегда. Вирус, скрытый внутри клетки-хозяина, не доступен для иммунных клеток, уничтожающих возбудителей. Вирус активизируется при ослаблении иммунитета в результате переохлаждения, перегрева, простудного заболевания, недостатка витаминов, переутомления, стресса, нехватки сна. Рецидив инфекции могут вызвать травмы, оперативные вмешательства, а также половой контакт при условии повреждения слизистой оболочки. Использование лекарственных и косметических средств, содержащих стероидные гормоны, также способствует манифестации вируса герпеса.
Классификация герпеса
В МКБ-10 (Международной классификации болезней) выделяют две группы заболеваний, связанных с вирусом простого герпеса:
- Инфекционные герпетические заболевания:
- герпетическая экзема (экзема Капоши);
- герпетический везикулярный дерматит;
- герпетический гингивостоматит и фаринготонзиллит;
- герпетический менингит;
- герпетический энцефалит;
- офтальмогерпес;
- диссеминированная герпетическая болезнь (герпетический сепсис);
- другие формы герпетических инфекций;
- неуточненная герпетическая инфекция.
- Генитальные герпетические инфекции:
- герпетические инфекции перианальных кожных покровов и прямой кишки;
- неуточненная аногенитальная герпетическая инфекция.
По клинической картине и локализации высыпаний:
- Типичные формы:
- герпес кожи — с поражением губ, крыльев носа, лица, рук, ягодиц и других частей тела;
- герпес глаз — иридоциклит, кератит, конъюнктивит, неврит зрительного нерва;
- герпес слизистых оболочек желудочно-кишечного тракта — стоматит, гингивит, фарингит, эзофагит;
- герпес половых органов — поражение слизистой оболочки полового члена, влагалища, вульвы, цервикального канала;
- герпес внутренних органов — гепатит, пневмония, панкреатит, трахеобронхит;
- герпес нервной системы — неврит, менингит, менингоэнцефалит, поражения бульбарных нервов, энцефалит;
- генерализованный простой герпес — висцеральная форма (пневмония, гепатит, эзофагит) и диссеминированная форма (сепсис).
- Атипичные формы:
- герпетиформная экзема Капоши — обширные сливающиеся высыпания по всему телу;
- абортивный герпес — почти незаметные папулы на грубой коже или дискомфорт без высыпаний;
- язвенно-некротический герпес — с развитием некроза тканей;
- эрозивно-язвенный герпес — с образованием язв и эрозий;
- геморрагический герпес — с кровянистым пропитыванием высыпаний и тканей;
- отечный герпес — с отеком тканей и болью в области губ и век;
- зостериформный простой герпес — с локализацией по ходу нервного ствола;
- диссеминированный герпес — с тенденцией перехода в генерализованную форму при ВИЧ;
- рупиоидный герпес — возникает на лице с присоединением вторичной бактериальной флоры;
- мигрирующий герпес — с тенденцией к изменению локализации высыпаний.
- латентная стадия — носительство с отсутствием симптомов;
- локализованная стадия — наличие одного очага поражения;
- распространенная стадия — наличие не менее двух очагов поражения;
- генерализованная стадия — висцеральная, диссеминированная.
При заражении герпесом детей в возрасте от 6 месяцев до 3 лет чаще всего развивается герпетический стоматит, для которого характерно острое начало с симптомами интоксикации и подъемом температуры.
На слизистой оболочке полости рта появляются сгруппированные пузырьки с прозрачным содержимым, на месте которых после вскрытия образуются болезненные эрозии. У детей старшего возраста первичный герпес характеризуется появлением зудящих пузырьков на красной кайме губ и коже носогубного треугольника. После их вскрытия остаются неглубокие язвочки, которые покрываются корочками. Корочки, отпадая, не оставляют следов на коже.
При первичном заражении взрослых вирусом простого герпеса симптомы более выражены, чем при дальнейших рецидивах. Больной испытывает озноб, головные боли, повышенную утомляемость, у него отсутствует аппетит, может наблюдаться расстройство сна. Покраснение, а затем характерные пузырьки появляются на губах, возле крыльев носа. В некоторых случаях увеличиваются подчелюстные лимфоузлы.
Герпетические нейроинфекции сопровождаются наиболее тяжелым течением, особенно если вирус поражает оболочки или ткань головного мозга.
В этих случаях симптомы включают головные боли, подъем температуры тела, напряжение затылочных мышц, психомоторное возбуждение (болезненное состояние, при котором наблюдается беспокойство и двигательная активность различной степени выраженности, вплоть до судорог). При несвоевременной диагностике заболевания существует риск летального исхода.
Офтальмогерпес сопровождается покраснением глаза, развитием блефаро- или кератоконъюнктивита, эрозиями роговицы.
Диагностика герпеса
Типичные случаи герпетической инфекции выявляются на основании клинической картины и анамнеза заболевания. Характерно его волнообразное течение со сменой периодов обострения и ремиссии.
Косвенным признаком служит склонность к простудным заболеваниям, чувствительность к переохлаждению, периодически возникающие состояния, сопровождаемые подъемом температуры, усталостью, депрессией.

При атипичных формах герпетической инфекции необходимы дополнительные обследования: клинический анализ крови, биохимический анализ крови (общий белок, белковые фракции, С-реактивный белок, АЛТ, АСТ, ЛДГ, креатинин, электролиты: калий, натрий, хлор, кальций) и клинический анализ мочи - для выявления поражения внутренних органов и предупреждения осложнений.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

