Что делать амиодарон раствор под кожу
Обновлено: 25.04.2024
Амиодарон при аритмии сердца - показания, противопоказания
Амиодарон имеет ряд преимуществ над остальными препаратами. Он высокоэффективен как при суправентрикулярных, так и при желудочковых нарушениях ритма сердца. Даже если аритмия рефрактерна к другим средствам антиаритмической терапии, назначение амиодарона оказывается успешным в 70% случаев.
Препарат имеет необычайно длинный период полувыведения (20-100 дней) и поэтому его принимают лишь 1 раз в сутки или даже реже. Он не оказывает существенного влияния на функцию желудочков, и его можно назначать пациентам с сердечной недостаточностью.
Вместе с тем амиодарон обладает рядом существенных нежелательных эффектов, поэтому длительно назначать его следует только больным с опасными для жизни или рефрактерными к другим препаратам нарушениями ритма сердца, или в тех случаях, когда риск развития побочных эффектов не столь значим в связи с общим плохим прогнозом (например, у лиц старческого возраста или пациентов с тяжелым поражением миокарда).
Несмотря на то что амиодарон эффективен в лечении желудочковых аритмий, недавно было показано, что у пациентов со сниженной функцией желудочков он не играет большой роли в «первичной профилактике» внезапной смерти, т.е. не предотвращает развития фатальных желудочковых нарушений ритма сердца у таких больных. Тем не менее многие пациенты с имплантированными дефибрилляторами нуждаются в приеме амиодарона с целью подавления желудочковых аритмий и, соответственно, снижения частоты срабатывания устройства.
Побочные эффекты амиодарона
При кратковременном парентеральном применении амиодарона возникновение побочных эффектов маловероятно, хотя описаны редкие случаи развития амиодарон-ассоциированного лекарственного гепатита. Введение в периферическую вену нередко сопровождается развитием флебита.
Длительный прием препарата внутрь, напротив, ассоциирован с высоким риском возникновения побочных эффектов.
Основные нежелательные эффекты амиодарона:
- Дерматологические: фотосенсибилизация и сине-серая пигментация
- Роговичные микродепозиты
- Дисфункция щитовидной железы: гипер- и гипотиреоз
- Фиброз легких
- Гепатит
- Нейропатия
- Миопатия
- Нарушения сна: бессонница, слишком яркие или кошмарные сновидения
- Тремор
- Алопеция
- Тахикардия типа «пируэт»
- Усиление действия варфарина
Дерматологические эффекты амиодарона
Фотосенсибилизация, т.е. повышение чувствительности кожи к воздействию ультрафиолетовых лучей, наблюдается у 2/3 пациентов. Несмотря на то что тяжелая фотосенсибилизация возникает лишь в незначительном числе случаев, о возможности ее развития следует предупреждать каждого, кто принимает амиодарон. При необходимости можно рекомендовать использовать специальную защитную одежду и защитные кремы, содержащие оксид цинка, избегать длительного пребывания на солнце.
Тяжелая реакция фотосенсибилизации является наиболее частой причиной отмены препарата, после которой симптомы могут сохраняться в течение года. Связь между типом кожи или дозой препарата и выраженностью этой реакции, по-видимому, отсутствует. У небольшого числа пациентов после длительного приема амиодарона развивается заметная сине-серая пигментация кожи, особенно в области носа и лба. Эта пигментация сохраняется в течение многих лет после отмены препарата.
Офтальмологические эффекты амиодарона
Тиреотропное действие амиодарона
Амиодарон содержит очень большое количество йода и вызывает умеренное увеличение сывороточного уровня тироксина и реверсивного трийодтиронина, а также снижение уровня сывороточного трийодтиронина. Концентрация тиреотропного гормона в сыворотке также может снижаться. Эти изменения на фоне терапии амиодароном свидетельствуют о нормальной функции щитовидной железы. Однако амиодарон может вызвать развитие как гипо-, так и гипертиреоза, что наблюдается у 15% пациентов.
Гипертиреоз может быть следствием активизации предсуществующей субклинической патологии щитовидной железы (которая, в свою очередь, может привести к увеличению синтеза тиреоидных гормонов) или следствием тиреоидита, развивающегося в исходно нормальной щитовидной железе и приводящего к усилению высвобождения ее гормонов. При развитии гипертиреоза часто ухудшается общее самочувствие пациента, наблюдаются снижение массы тела и другие признаки гиперфункции щитовидной железы.
Возможно рецидивирование аритмии, которую ранее удавалось контролировать лечением. В сыворотке повышается содержание как тироксина, так и трийодтиронина. Гипертиреоз может развиться достаточно остро и протекать тяжело. Он может возникнуть даже через много месяцев после прекращения приема амиодарона.
При развитии гипотиреоза в сыворотке крови снижается содержание тироксина, а уровень тиреотропного гормона повышается. Иногда данное состояние развивается без клинических проявлений. Показана заместительная терапия гормонами щитовидной железы. Отмена амиодарона не требуется. Обнаружение аутоантител к ткани щитовидной железы заставляет предположить наличие предсуществующей патологии железы и то, что гипотиреоз может прогрессировать даже после отмены амиодарона.
У больных, длительно принимающих амиодарон, состояние щитовидной железы необходимо контролировать каждые 6-12 месяцев. Всегда должен быть высокий уровень настороженности в плане возможного развития гипертиреоза у лиц, которые получают амиодарон или принимали его ранее.
Прочие побочные эффекты амиодарона
К другим серьезным побочным эффектам амиодарона относятся фиброз легких, гепатит, нейропатия и миопатия. Иногда несколько серьезных нежелательных эффектов проявляются одновременно. Как правило (но не всегда!), возникновение серьезных побочных эффектов связано с приемом высоких доз амиодарона.
Легочный фиброз - наиболее частая проблема. Клиническими проявлениями обычно становятся одышка (может быть выраженной) и обширные затемнения легочных полей, которые можно перепутать с отеком легких. Наличие предсуществующей патологии легких не влияет на риск этого осложнения. Как только диагноз поставлен, следует прекратить терапию амиодароном и провести короткий курс лечения глюкокортикостероидами. Часто наблюдается снижение диффузионной способности легких без каких-либо клинических проявлений.
Другими нежелательными эффектами являются тошнота, кожная сыпь, алопеция, тремор, тестикулярная дисфункция, бессонница и кошмарные сновидения, которые могут быть очень, яркими.
Важно отметить, что амиодарон потенцирует действие оральных антикоагулянтов, в результате чего дозу последних приходится уменьшать, обычно вдвое. Кроме того, препарат увеличивает концентрацию в плазме крови дигоксина, хинидина, верапамила, флекаинида и циклоспорина.
При некоторых формах аритмии основные преимущества амиодарона (высокая эффективность, отсутствие отрицательного инотропного действия и большая продолжительность действия) «перевешиваются» обширным списком побочных эффектов. Однако большинство из них являются обратимыми, и риск их развития не должен служить противопоказанием к назначению амиодарона пациентам с угрожающими жизни нарушениями ритма сердца, с короткой ожидаемой продолжительностью жизни, а также в тех случаях, когда другие антиаритмические препараты оказались неэффективны.

Дозировки и сроки применения амиодарона
Начало действия препарата существенно сдвинуто во времени. При приеме внутрь действие начинает проявляться на 3-7-е сутки лечения, а для развития максимального эффекта может потребоваться до 50 дней. При необходимости скорость наступления действия можно увеличить, назначив препарат в очень высоких дозах (например, по 600-1200 мг/сут.) в течение 1-2 нед. Затем дозу следует снизить до 400 мг/сут.
После достижения антиаритмического эффекта рекомендуется постепенное снижение дозы препарата, пока не будет определена минимальная эффективная доза. Обычно поддерживающая доза составляет 200-400 мг/сут. Для отдельных больных оказывается достаточным прием 200 мг через день. По опыту автора, при снижении суточной дозы у взрослых до уровня менее 300 мг/сут. рецидивы аритмии обычно возобновляются. При опасных формах аритмии не стоит рисковать и уменьшать дозу препарата ниже 300 мг/сут.
Препарат подвергается метаболизму в печени; почками не экскретируется. Основным метаболитом является дезэтиламиодарон, который сам по себе оказывает антиаритмическое действие. Очень высокая концентрация амиодарона и его метаболита наблюдается в легких, сердце, печени и жировой ткани.
При внутривенном введении действие развивается быстрее, чем при приеме внутрь, однако, в отличие от большинства других препаратов, немедленный антиаритмический эффект наблюдается редко. Как правило, он развивается через 1-24 ч. Если аритмия плохо поддается лечению, представляется целесообразным внутривенное введение амиодарона (несмотря на возможную задержку начала действия) вместо попыток примения других препаратов, которые менее эффективны и часто вызывают побочное действие.
Рекомендованная доза для внутривенного введения составляет 5 мг/кг за 30-60 мин с последующей инфузией 15 мг/кг в течение 24 ч. В экстренных ситуациях первичное внутривенное введение можно осуществлять с большей скоростью, однако вазодилатирующее действие амиодарона может привести к развитию выраженной артериальной гипотензии. Чтобы избежать развития флебита, препарат следует вводить через центральную вену. Если это невозможно, рекомендуется чаще менять места инфузии (обычно этого бывает достаточно).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что делать при попадании лекарств под кожу? Первая помощь при экстравазации
Лечение и первая помощь при экстравазации - попадании лекарств под кожу. Объем вмешательства зависит от стадии экстравазации, вводимого раствора и специфических антидотов. Схема лечения повреждений 3-4-й стадии не разработана. При отсутствии рандомизированных контролируемых исследований некоторые организации опубликовали протоколы лечения, основанные на собственном опыте, серии случаев и единичных достоверных данных.
1. Во всех случаях экстравазации - попадании лекарств под кожу выполняют следующее:
а. Немедленно прекращают внутривенную инфузию.
б. Убирают стягивающие повязки, которые могут действовать как жгут (например, при фиксации конечности).
в. Придают конечности возвышенное положение для уменьшения отека.
г. Местно применяют согревающие и охлаждающие пакеты, что спорно. Под действием тепла происходит местная вазодилатация, способствующая реабсорбции инфильтрированных растворов. Однако, согласно данным литературы, влажные согревающие пакеты могут вызывать мацерацию кожи.
2. Экстравазация 1-й и 2-й стадии:
а. Убирают внутривенный катетер.
б. Выбирают антидот.

Стадии экстравазации - попадания лекарств под кожу
3. Экстравазация 3-й и 4-й стадии:
а. Оставляют внутривенный катетер на месте и с помощью шприца объемом 1 мл аспирируют как можно больше введенной жидкости.
б. Убирают катетер, за исключением случаев, когда необходимо введение антидота.
в. Решают вопрос об использовании гиалуронидазы или антидота.
г. Метод многократных пункций. После экстравазации кислыми или гиперосмолярными растворами развивается напряженный отек с побледнением кожи над местом инфильтрации. Использование стилета после соблюдения мер асептики дает возможность свободно вытекать инфильтрированному раствору, при этом уменьшаются отек и вероятность развития некроза. Затем накладывают повязку, смоченную физиологическим раствором, в целях улучшения дренирования.
д. Промывание физиологическим раствором. Некоторые авторы рекомендуют использовать метод промывания физиологическим раствором подкожных тканей. После обработки и инфильтрации участка 1% лидокаином подкожно вводят 500-1000 ЕД гиалуронидазы. Затем выполняют четыре маленьких разреза скальпелем по периферии участка инфильтрации. Проводят промывание. Вводят физиологический раствор через катетер, установленный подкожно в один из разрезов, жидкость изливается через другой разрез. Образовавшееся вздутие массирующими движениями выдавливают в сторону разреза для облегчения удаления веществ, излившихся из сосуда.
4. Специфические антидоты лекарств:
а. Фентоламин:
(1) Применяют при лечении повреждений в результате экстравазации вазопрессоров, например допамина и адреналина, которые вызывают повреждение тканей за счет интенсивной вазоконстрикции и ишемии.
(2) Эффект развивается практически сразу. Наиболее эффективен в течение часа, но можно вводить до 12 ч. Биологический период полувыведения фентоламина при подкожном введении составляет менее 20 мин.
(3) Механизм действия: конкурентная блокада а-адренорецепторов, приводящая к расслаблению гладкомышечных клеток и гиперемии.
(4) Для новорожденных дозы не установлены. Они зависят от размера повреждения и массы тела новорожденного.
(5) Рекомендуемые дозы варьируют в пределах от 0,01 мг/кг на одно введение до 5 мл раствора с концентрацией 1 мг/мл.
(6) Раствор в концентрации 0,5-1,0 мг/мл вводят подкожно в инфильтрированную область после удаления внутривенного катетера.
(7) Меры предосторожности. Могут возникать гипотензия, тахикардия и нарушения ритма; следует вводить крайне осторожно у недоношенных; повторно вводить в малых дозах.
б. Нитроглицерин местно:
(1) Эффективен при лечении повреждений, обусловленных экстравазацией допамина.
(2) Механизм действия: расслабление гладких мышц сосудов.
(3) Применение: 2% нитроглицериновая мазь из расчета 4 мм/кг на пораженную область, возможно повторное применение каждые 8 ч, если перфузия тканей не улучшается.
(4) Также используют трансдермальные пластыри.
(5) Меры предосторожности. Всасывание через кожу может привести к гипотен-зии.
в. Тербуталин:
(1) Эффективен в лечении периферической ишемии, возникшей вследствие экс-травазации вазопрессоров у взрослых и детей старшего возраста; о применении в неонатологической практике публикации отсутствуют.
(2) Механизм действия: периферическая вазодилатация в результате активации бета2-адренорецепторов.
(3) Вводят подкожно в концентрации 0,5-1,0 мг/мл; дозы у взрослых варьируют от 0,5 до 1 мг.
5. Лечение раны после экстравазации - попадания лекарства под кожу:
Цель лечения раны у новорожденных с частичной или полной утратой кожи заключается в достижении заживления первичным или вторичным натяжением без образования рубцов, контрактур и проведения оперативного вмешательства. Используют разные схемы лечения в разных лечебных учреждениях.
а. Промывают поврежденную область стерильным физиологическим раствором.
б. На пораженный участок наносят сульфадиазиновую мазь и меняют повязки каждые 8 ч, осторожно очищая раневую поверхность, повторно наносят мазь. Сульфонамиды повышают риск ядерной желтухи, поэтому противопоказаны новорожденным в первые 30 дней жизни.
в. Аморфные гели на водяной основе, содержащие полимер карбоксиметилцеллюлозы, пропиленгликоль и воду, сохраняют рану влажной и облегчают ее заживление. Их выпускают в форме гелей и пленок, которые можно накладывать прямо на раневую поверхность и оставлять на месте при повторных перевязках. Гель легко удаляется с помощью физиологического раствора, его меняют каждые 3 дня. Более частую смену повязок проводят при избыточной экссудации.
г. Влажно-высыхающие повязки с физиологическим раствором и повязки с повидонйодом также эффективны. Обильное нанесение повидон-йода на открытую рану не рекомендуют у новорожденных с очень низкой массой тела, поскольку всасывание йода может угнетать функцию щитовидной железы.
д. Эффективность применения антибактериальных мазей не доказана.
е. Заживление раны оценивают каждый день. Для заживления необходимо от 7 дней до 3 мес.
ж. Если рана находится на сгибательной поверхности, выполняют пассивные упражнения в пределах физиологического объема при каждой смене повязки в целях предотвращения контрактур.
6. Консультация пластического хирурга:
а. Проводят при повреждениях всей толщины кожи и значительных по площади отдельных повреждениях, обусловленных экстравазацией.
б. Могут потребоваться ферментативная или хирургическая обработка раны или трансплантация кожи.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление амиодароном и его побочные эффекты
Амиодарон — йодированное производное бензофурана, химическая структура которого близка к структуре тироксина. В последнее время интерес клиницистов привлекает его способность устранять резистентные наджелудочковые и желудочковые аритмии и улучшать состояние пациентов с трудноизлечимой застойной сердечной недостаточностью. Наиболее тяжелая неблагоприятная реакция на терапевтическое применение амиодарона — быстро прогрессирующий дыхательный дистресс-синдром у взрослых.
а) Терапевтическая доза. Терапевтические ударные и поддерживающие дозы варьируют в широких пределах (400—2000 и 200—800 мг/сут соответственно). Об острых передозировках сообщалось редко. Проглатывание 8 г амиодарона здоровым взрослым человеком в одном случае вызвало не сильную брадикардию (на второй-третий день), удлинение интервала Q—Т и потоотделение без изменений кровяного давления. Побочных эффектов от применения терапевтических доз (например, светочувствительность, гипотиреоз, гинекомастия, гепатотоксичность, гипертиреоз, легочный фиброз, пигментация кожи, роговичные отложения) не наблюдалось после острых передозировок.
В этом случае появление симптомов и признаков задерживалось на несколько дней, вероятно, вследствие медленной абсорбции и длительного периода полужизни амиодарона. У одного пациента, проглотившего 15 г амиодарона, за синусовой брадикардией последовала блокада сердца I степени, потребовавшая применения электрокардиостимуляции. Прием 2600 мг препарата с целью суицида не вызвал ни клинических симптомов, ни изменений частоты сердечных сокращений или кровяного давления. Желудочковых аритмий не наблюдалось, но произошло удлинение интервала Q—T с инверсией зубца T в прекордиальных отведениях и временное исчезновение зубца R в отведениях от V1 до V4, что имитировало симптомы переднеперегородочного инфаркта миокарда.
У взрослого человека, проглотившего 3,4 г амиодарона, электрокардиограмма была нормальной. После промывания желудка и недолгой желудочковой тахикардии пациент выздоровел.

б) Токсикокинетика амиодарона. Пероральная абсорбция терапевтических доз происходит медленно, с широким диапазоном биодоступности (22— 86 %). Степень связывания амиодарона белками плазмы высокая (98 %). У добровольцев, которые получили терапевтические дозы, объем распределения был высоким (9—17 л/кг), а период полужизни долгим (3— 21 ч после введения однократной дозы и 52 сут после длительного введения препарата). В одном из случаев передозировки период полувыведения составил 31 ч. У пациентов после длительного лечения концентрации амиодарона и N-дезэтиламиодарона в сыворотке были примерно равными.
Терапевтическая концентрация в плазме составляет примерно 1—2,5 мг/л. Через почки экскретируется менее 1 % введенной дозы.
в) Взаимодействие лекарственных средств. Амиодарон способен вызвать увеличение сывороточной концентрации, усиление фармакологического действия и токсичности дигоксина, дилтиазема, хинидина, прокаинамида, пероральных антикоагулянтов и фенитоина.
г) Беременность. Амиодарон проникает через плаценту. Концентрация амиодарона в крови плода составляет примерно 10— 25 % концентрации в крови матери, что свидетельствует о наличии трансплацентарного барьера. Серьезные неблагоприятные последствия действия амиодарона при приеме матерью во время беременности следующие: гипотиреоз новорожденных, малый размер плода, не соответствующий сроку беременности, и недоношенность. Вскоре после рождения младенца с биохимическими и клиническими признаками гипотиреоза при рождении может потребоваться гормональная заместительная терапия.
В шести случаях, когда пациенткам в период беременности вводили амиодарон, все родившиеся младенцы оказались здоровыми, без зоба, роговичных микроотложений, гепатической дисфункции или легочного фиброза. Во время беременности зоб и гипотиреоз могут быть диагностированы у плода в матке с помощью ультразвуковой эхографии и посредством измерения уровня тиреотропного гормона в амниотической жидкости.
Если идентифицируется увеличение щитовидной железы, следует ставить вопрос о кесаревом сечении.
д) Механизм действия. Амиодарон увеличивает длительность потенциала действия клеток миокарда без изменения мембранного потенциала покоя. Следовательно, препарат меняет реполяризацию (удлинение интервала Q-T), не воздействуя на спонтанную (фаза 4) деполяризацию. Поскольку антиаритмические средства как класса I, так и класса II не обладают этими свойствами, амиодарон классифицируют как антиаритмическое средство класса III. Механизм действия амиодарона на тиреоидный метаболизм остается неясным, но, по всей вероятности, можно говорить о внутриклеточных процессах, а не о центральном или периферическом воздействий. Амиодарон обладает также способностью блокировать неконкурентные а- и b-рецепторы, что приводит к системному и коронарному расширению сосудов.
е) Клиническая картина отравления амиодароном. Тяжелые неблагоприятные реакции на терапевтические дозы амиодарона включают дыхательный дистресс-синдром с быстрым летальным исходом, полиморфную желудочковую тахикардию ("пируэтное" нарушение ритма), гипо- и гипертиреоз. Неблагоприятные клинические эффекты обычно наблюдаются после длительного применения амиодарона: это главным образом экстракардиальные эффекты, зависящие от дозы и концентрации препарата в тканях, обычно обратимые.
Как правило, они появляются, когда концентрация амиодарона (или дезэтиламиодарона, его основного метаболита) в плазме выше 1,5 мкг/мл.
- Кожа. Изредка отмечаются светочувствительность кожи и синее окрашивание ногтей.
- Глаза. Микроотложения амиодарона скапливаются в роговице почти у всех пациентов, принимающих этот препарат; они видны при осмотре со шелевой лампой и в редких случаях вызывают ухудшение зрения.
- Щитовидная железа. У 2—7 % пациентов развивается гипотиреоз и у 5— 16 % — гипертиреоз с потенциальным ухудшением любой аритмии. Гипертиреоз, по-видимому, чаще развивается у пациентов с зобом. Амиодарон, регулярно принимаемый в дозе 200 мг/сут, выделяет в кровоток от 5 до 10 мг йодида. Для индуцированного амиодароном тиреотоксикоза характерны снижение массы тела, слабость, возбуждение, гиперкинезия и рецидивы аритмии, по поводу которой пациент принимает это лекарство.
Изменения со стороны глаз и увеличение щитовидной железы часто отсутствуют. Тиреотоксикоз может развиться через несколько недель или месяцев после прекращения приема лекарства. Гипотиреоз может быть временным или персистентным и развивается у пациентов с уже существующими тироидными расстройствами или без них.
- Легкие. Амиодароновая интоксикация легких характерна для тех случаев, когда дозы выше 400 мг/сут применяются в течение по меньшей мере 2 мес. К факторам риска относятся преклонный возраст (> 60 лет), пониженная диффузионная емкость легких для окиси углерода (ДЛСО < 80 %) до лечения и повышенные концентрации дезэтиламиодарона в плазме (>2,3 мкг/мл). Установлено, что при прогнозировании токсичности амиодарона в каждом конкретном случае целесообразно учитывать предшествующие аномалии в функционировании легких, рентгенограммы грудной клетки или взаимосвязь препарат — доза.
Легочный синдром может быть аллергической реакцией. Легочная интоксикация часто проявляется как интерстициальная или альвеолярная инфильтрация, которая обычно бывает двусторонней. Она осложняет клиническое применение амиодарона примерно у 5—7 % пациентов. Симптомы проявляются или остро, напоминая инфекционный пневмонит, или медленно, с кашлем, одышкой при физическом напряжении и похуданием. Возможна лихорадка. В связи с длительным периодом полужизни амиодарона (до 54 сут) токсические эффекты могут сохраняться, несмотря на прекращение приема лекарства. Лечение предполагает прекращение приема амиодарона или уменьшение дозы до уровня ниже 400 мг/сут. Кортикостероиды вызывают рассасывание легочных инфильтратов.
- Печень. Гепатические аномалии, связанные с амиодароновой терапией, варьируют от временного повышения показателей при проведении стандартных тестов функции печени до тяжелой печеночной недостаточности. Сообщалось, что в ряде случаев печеночная недостаточность приводит к летальному исходу, когда аномалии в активности ферментов печени обусловлены курсом лечения, длившимся в среднем 10,4 мес, при средней кумулятивной дозе 104 г.
ж) Лабораторные данные отравления амиодароном:
- Вспомогательные методы. Часто для того, чтобы подтвердить диагноз "амиодароновая легочная интоксикация" и исключить другие диагнозы, например инфекцию или злокачественные новообразования, проводят бронхоскопию с бронхоальвеолярным лаважем и трансбронхоскопическую биопсию легких. Врач-клиницист должен также решить, нужны ли дополнительные исследования, например катетеризация легочных артерий, легочная ангиография и даже открытая биопсия легких.
- Тесты функции щитовидной железы. Повышение уровня тиреотропного гормона — явление временное, и постепенно он возвращается к показателям, отмечавшимся до лечения. Напротив, уровни тироксина и свободного тироксина остаются повышенными. Это состояние можно перепутать с гипертиреозом, который тоже встречается у некоторых пациентов, принимавших амиодарон. Бывает трудно провести разграничение между эутиреоидным пациентом, принимающим амиодарон, и пациентом, лечившимся амиодароном и ставшим гипертиреоидным.
В этой ситуации могут помочь сверхчувствительные методы анализа тиреотропного гормона и определение уровней трийодтиронина и свободного трийодтиронина.
- Тесты функции печени. Когда амиодарон принимают в дозах от 200 до 400 мг/сут, а концентрации амиодарона или дезэтиламиодарона ниже 1—5 мкг/мл, примерно у 10—20 % пациентов выявляется бессимптомное повышение уровней билирубина, трансаминазы и щелочной фосфатазы. Хотя случаи тяжелой интоксикации печени редки, в 6 случаях после длительного применения амиодарона в дозах от 200 до 600 мг/сут наступила смерть.
- Проаритмический эффект. Проаритмический эффект (например, "пируэтное" нарушение ритма) наблюдается не часто, исключение составляют пациенты старших возрастных групп, пациенты с гипокалиемией, а также пациенты, лечащиеся по поводу брадикардии или состояние которых осложнено желудочковой реполяризацией. У пациентов с гипертрофической кардиомиопатией амиодарон способен спровоцировать злокачественные аритмии или аномалии проведения.
з) Лечение отравления амиодароном. Пациентам должны помочь обычные терапевтические мероприятия. В связи с особенностями токсикокинетики амиодарона меры деконтаминации могут быть эффективными по прошествии нескольких часов после приема препарата. Лечение амиодароновой интоксикации легких заключается просто в прерывании применения препарата, хотя кортикостероиды могут ускорить выздоровление. Очень быстрая отмена кортикостероидов у некоторых пациентов вызывает рецидив.
У пациентов с синдромом Вольфа — Паркинсона — Уайта внутривенное введение амиодарона может вызвать тяжелую сердечно-сосудистую недостаточность и ширококомплексную брадикардию. Лечение включает применение изопреналина и кардиоверсии с использованием постоянного тока.
Если индуцирована брадикардия, показано применение b-адренергического агониста или водителя ритма. В случае гипотензии с нарушенной тканевой перфузией эффективны сосудосуживающие средства. Ни амиодарон, ни его метаболиты не подвергаются диализу. Поскольку для амиодарона характерны высокая степень связывания с белками и большой объем распределения, гемоперфузия для него, по-видимому, неприменима; однако имеющихся данных недостаточно, чтобы прийти к окончательному заключению относительно этого метода лечения. Холестирамин рекомендован в качестве средства, снижающего уровень энтерогепатической циркуляции амиодарона. По имеющимся данным, плазмаферез вызывает снижение концентраций амиодарона и его метаболита десметиламиодарона, а также концентраций свободного тироксина и тироксина.
Активированный уголь понижает степень абсорбции амиодарона. Промывание желудка необходимо проводить с подключением к пациенту кардиомонитора. Во время этой процедуры может развиться глубокая брадикардия. Для своевременного выявления признаков аритмии, брадикардии и блокады сердца пациента в течение 1—2 дней следует наблюдать в отделении медицинской помощи коронарным больным. Дальнейшего применения антиаритмических средств нужно по возможности избегать. Если брадикардия ставит под угрозу гемодинамическое состояние пациента, следует предусмотреть применение электрокардиостимуляции.
Неясно, следует ли осуществлять профилактическую кардиостимуляцию при значительном удлинении интервала P—R. Пероральный прием холестирамина (по 4 г в час в течение 4 ч) может сократить период полужизни амиодарона. В связи с возможностью замедления абсорбции амиодарона могут быть введены дополнительные дозы — до 12 ч. Холестирамин, по-видимому, уменьшает степень энтерогепатической циркуляции амиодарона.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Вероятность инфильтрации и экстравазального введения значительно уменьшается, если медицинская сестра понимает причины этих явлений, правильно выбирает вену для пункции или катетеризации и оборудование, а также тщательно следит за пациентом.
В соответствии со стандартами сестринской практики, инфильтрацией называется непреднамеренное введение раствора лекарственного средства в ткани, окружающие вену. Такие лекарственные средства могу вызывать раздражение окружающих тканей, если они окажутся в подкожной клетчатке, если же они выливаются на кожу, может развиваться контактный дерматит. Экстравазация — это введение значительного количества раствора лекарства мимо вены, и в некоторых случаев она сопровождается даже тканевыми некрозами.
В связи с этим, надо помнить, что некоторые растворы лекарственных средств не предназначены для ведения в периферические вены. Инфильтрация и экстравазация возникают чаще всего тогда, когда катетер не полностью находится в просвете вены, или же в стенке вены есть разрыв, который способствует утечке раствора. Причины этого явления:
- Катетер введен в вену неправильно;
- Вена повреждена, вокруг имеется отек клетчатки, который препятствует правильному току крови, раствор задерживается и вытекает в окружающие ткани;
- Внутри вены или вокруг катетера формируется тромб, который задерживает раствор, он выходит в окружающие ткани. Также при этом развиваются флебит или тромбофлебит;
- Катетер прокалывает или развивает противоположную стенку вены, что также может сопровождаться флебитом или тромбофлебитом;
- Катетер вытягивается из просвета вены при движении пациента или вследствие ненадежной фиксации.
Хотя чаще всего инфильтраты и экстравазаты возникают при инфузии в периферическую вену, эти осложнения могут развиваться и при использовании центральных венозных катетеров и имплантируемых портов. В этом случае последствия могут быть катастрофическими вследствие большого объема используемого раствора, и еще потому, что эти устройства используются для введения концентрированных и вязких растворов.
В большинстве случаев инфильтраты не приводят к тяжелому поражению тканей, но для пациента они очень некомфортны. Также приходится удалять катетер из вены и устанавливать новый, что может уменьшить число потенциально доступных вен, отнимает время и увеличивает затраты.
Самые серьезные последствия наступают, когда вне просвета сосудов оказываются раздражающие растворы, например, содержащие кальций, калий или препараты для химиотерапии. Повреждение тканей может напрямую зависеть от рН раствора: сильно щелочные или кислые растворы вызывают самые настоящие химические ожоги. Значительно концентрированные лекарственные препараты могут даже вызывать некроз тканей.
Степень повреждения при инфильтрации или экстравазации может зависеть от того, как быстро будут предприняты все меры, так как даже небольшое количество жидкости создает компрессию и повреждение. При раннем выявлении и лечении инфильтратов и экстравазатов можно предупредить повреждение нервов и тканей, и предупредить хирургическое вмешательство. Неспособность своевременно распознать эти осложнения может привести к стойкой деформации, и потере функции, даже в том случае, если пациенту будет проведена реконструктивная операция. Часто такие ошибки заканчиваются судебным процессом.
Чтобы избежать проблем, нужно быть настороженным в отношении признаков и симптомов инфильтрации и экстравазации, которые включают в себя:
- «Надутую» кожу, которая выглядит блестящей, натянутой и плотной;
- Отек в месте введения иглы или катетера;
- Холодная наощупь кожа;
- Дискомфорт;
- Замедление или прекращение инфузии;
- Утечка раствора лекарственного препарата вокруг места введения или под повязкой;
- Если над местом инфузии наложить жгут, инфузия не прекращается;
- Нет тока крови по катетеру, если пережать вену и опустить пакет с раствором (наличие крови не исключает инфильтрацию).
Дискомфорт и жжение при инфузии раздражающего или вязкого раствора может указывать на повреждение сосуда. Жалоба на боль в месте установки катетера или иглы в вену — это основной признак того, что нужно быстро вмешиваться. В этом случае необходимо принять следующие меры:
- Прекратить инфузию;
- Если нет противопоказаний, установить катетер в вену на другой руке;
- При инфильтрате — наложить компресс, если произошла экстравазация, особенно хлорида кальция — срочно приглашайте врача.
До введения вязкого, могущего вызвать сужение сосуда, или токсичного раствора лекарственного средства, необходимо знать, какие нейтрализующие вещества (антидоты) применяются при экстравазации и инфильтрации.
Для предотвращения инфильтрации, нужно выбирать подходящую вену. Выбирайте гладкую и упругую вену, которая не похожа на веревку с узлами. Избегайте сгибательных поверхностей суставов, так как здесь смещение катетера происходит особенно часто. Если такое место — единственное, куда можно установить катетер, используйте шину. Если пациент в сознании, инфузия долгая, а ему хочется двигаться, и например, читать книжку, то лучше избегать использования вен кисти.
Чаще всего оптимально катетеризировать вены предплечья, особенно внутренней его части. Кости — это естественная шина, вены достаточно хорошо фиксированы, поэтому вероятность смещения катетера значительно уменьшается.
Начинайте выбирать вену на предплечье так низко, насколько это вообще возможно (не стоит использовать место сделанной недавно венепункции), но не стоит ипользовать вены на внешней поверхности предплечья около запястья, так как там близко проходят нервы. Лучше не использовать вены внутренней части ниже локтя (антекубитальная ямка) — инфильтрацию в этой зоне очень легко просмотреть и она бывает немаленькой. При значительно инфильтрации в антекубитальной ямке жидкость сдавливает важные анатомические структуры и может привести к повреждению нервов и некрозу тканей.
Чтобы раствор лекарственного препарата максимально смешивался с кровью, выбирайте катетер минимально возможного диаметра, это позволит крови смешиваться с инфузатом, и обеспечить его адекватное разведение.
Всегда водите иглу срезом вверх, чтобы уменьшить риск сквозного прокола вены, тщательно фиксируйте катетер, чтобы он не смещался, особенно у детей и пожитых.
После того, как врач установит катетер в центральную вену, или медсестра — периферическую, место пункции проверяют каждые час-два, особенно если проводится длительная инфузия. Убедитесь, что место пункции вены хорошо видно (лучше применять прозрачные заклейки, а не марлевые салфетки).
Регулярно проверяйте, не появилось ли напряжения и отека в месте введения катетера. Спрашивайте пациента, нет ли боли, если говорить он не может, проверяйте место пункции чаще. Если вы заметите инфильтрацию или экстравазацию, сразу же прекращайте инфузию, и проверяйте, что произошло. Если инфильтрат большой, или раствор был раздражающий — немедленно зовите врача. Если катетер остался на месте, можно попробовать шприцом аспирировать часть попавшей в ткани жидкости, также через катетер можно вести антидот.
После удаления катетера больную руку надо держать в приподнятом положении (например, на подушке), и приложить холодный компресс, если это лекарства для химиотерапии — то теплый компресс. Если появляется некроз (обычно через может быть необходимой консультация хирурга.
Как документировать осложнения инфузионной терапии
Во-первых, нужно измерить участок измененных тканей, чтобы потом можно было оценить эффективность лечения. Обязательно нужно отслеживать состояние кожи и мягких тканей, чтобы избежать тяжелых осложнений, также это помогает оценить качество медицинской помощи.
Применение устройств для фиксации конечности, особенно в детской и гериатрической практике, может давать удивительные результаты: частота смещения катетеров может снизиться до нуля, и не будет тяжелых последствий. Соблюдение описанных выше несложных приемов может предотвратить осложнение. Ну а если оно все-таки возникло, то последствия можно сделать минимальными, если быстро и адекватно реагировать на случившееся.
Отдельно — о центральных венозных катетерах и имплантируемых портах
В соответствии с международными стандартами, раствор лекарственного средства, имеющий рН менее 5 и более 9, не должен вводиться через периферические вены. Например, это — ванкомицин (pH, ∼2.4) и фенитоин (pH, ∼12). То же самое касается и растворов, содержащих более 5% гидролизата белков, или 10% глюкозы.
Поскольку экстравазация такого раствора может иметь катастрофические последствия, то все их вводят через центральный венозный катетер или имплантируемый порт. Если приходится однократно вводить такой раствор в периферическую вену, то его вводят через толстый катетер, через боковой порт во время инфузии физиологического раствора, предпочтительнее иметь отдельный катетер для таких целей.
При введении вязкого или раздражающего раствора через центральный венозный катетер, всегда следует проверять обратный ток крови по катетеру, и часто делать это повторно во время инфузии. Если обратного тока крови нет, то это можно указывать на выход катетера из просвета вены, и утечке раствора в окружающие ткани. Также может быть тромбоз катетера — в этом случае срочно останавливайте инфузию и зовите врача во избежание тяжелых последствий.
Иногда врач проводит контрастное исследование под контролем рентгена, чтобы убедиться в проходимости катетера и может растворить тромб.
Если венозный доступ осуществляется через имплантируемый порт, важно выбирать иглу адекватной длины, чтобы она не выскочила из порта, и раствор не ушел бы в окружающую клетчатку. Если же игла окажется слишком длинной, то это может привести к повреждению мембраны порта, в результате чего экстравазация будет происходить уже через мембрану.
Когда инфузия лекарственного средства проводится через имплантируемый порт, нужно часто осматривать место установки порта, как и при работе с периферическим венозным катетером, чтобы своевременно выявить любую утечку или отек подкожной клетчатки рядом с портом. Если пациент жалуется на ЛЮБОЙ дискомфорт, немедленно прекращайте инфузию и посмотрите, что случилось. При подозрении на проблемы с портом — срочно зовите врача. Иногда порт может отсоединяться от катетера, и в этом случае пациенту нужна немедленная операция.
Шкала оценки инфильтравии в месте инфузии (Journal of Infusing Nursing, 2006)
0 баллов — нет никаких симптомов
1 балл — напряженная кожа, отек до 2.5 см в диаметре, холодная наощупь кожа, боль может быть, а может и не быть
2 балла — Кожа натянута, отек от 2 до 12 см в любом направлении, кожа холодная наощупь, боль может быть, а может и не быть
3 балла — кожа напряжена и просвечивает, большой отек — больше 15 см, в любом направлении, кожа холодная наощупь, боль средняя или умеренная, может быть онемение
4 балла — Кожа напряжена, просвечивает, плотная, может быть даже повреждена, обесцвечена, имеется выраженный отек, более 15 см, в любом направлении, отек глубокий, есть нарушения кровотка, боль от умеренной до выраженной, могут быть синяки
К последней, самой тяжелой степени инфильтрации, также относится утечка любого препарата крови, раздражающего или очень вязкого раствора.
Почему терапия аритмий считается одним из самых сложных разделов кардиологии? Как классифицируются аритмии? Какие группы лекарственных препаратов используются при лечении аритмий? Нарушения ритма сердца (аритмии) представляют собой один из самы
Почему терапия аритмий считается одним из самых сложных разделов кардиологии?
Как классифицируются аритмии?
Какие группы лекарственных препаратов используются при лечении аритмий?
Нарушения ритма сердца (аритмии) представляют собой один из самых сложных разделов клинической кардиологии. Отчасти это объясняется тем, что для диагностики и лечения аритмий необходимо очень хорошее знание электрокардиографии, отчасти — огромным разнообразием аритмий и большим выбором способов лечения. Кроме того, при внезапных аритмиях нередко требуется проведение неотложных лечебных мероприятий.
Одним из основных факторов, повышающих риск возникновения аритмий, является возраст. Так, например, мерцательную аритмию выявляют у 0,4% людей, при этом большую часть пациентов составляют люди старше 60 лет [1, 2, 4]. Увеличение частоты развития нарушений ритма сердца с возрастом объясняется изменениями, возникающими в миокарде и проводящей системе сердца в процессе старения. Происходит замещение миоцитов фиброзной тканью, развиваются так называемые «склеродегенеративные» изменения. Кроме этого, с возрастом повышается частота сердечно-сосудистых и экстракардиальных заболеваний, что также увеличивает вероятность возникновения аритмий [17, 18].
Основные клинические формы нарушений ритма сердца
- Экстрасистолия.
- Тахиаритмии (тахикардии).
- Наджелудочковые.
- Желудочковые.
По характеру клинического течения нарушения ритма сердца могут быть острыми и хроническими, преходящими и постоянными. Для характеристики клинического течения тахиаритмий используют такие определения, как «пароксизмальные», «рецидивирующие», «непрерывно рецидивирующие» [2].
Лечение нарушений ритма сердца
Показаниями для лечения нарушений ритма являются выраженные нарушения гемодинамики или субъективная непереносимость аритмии. Безопасные, бессимптомные или малосимптомные легко переносящиеся аритмии не требуют назначения специального лечения. В этих случаях основным лечебным мероприятием является рациональная психотерапия. Во всех случаях прежде всего проводится лечение основного заболевания.
Антиаритмические препараты
Основным способом терапии аритмий является применение антиаритмических препаратов. Хотя антиаритмические препаты не могут «вылечить» от аритмии, они помогают уменьшить или подавить аритмическую активность и предотвратить рецидивирование аритмий.
Любое воздействие антиаритмическими препаратами может вызывать как антиаритмический, так и аритмогенный эффект (то есть, наоборот, способствовать возникновению или развитию аритмии). Вероятность проявления антиаритмического эффекта для большинства препаратов составляет в среднем 40–60% (и очень редко для некоторых препаратов при отдельных вариантах аритмии достигает 90%). Вероятность развития аритмогенного эффекта составляет в среднем примерно 10%, при этом могут возникать опасные для жизни аритмии. В ходе нескольких крупных клинических исследований было выявлено заметное повышение общей летальности и частоты случаев внезапной смерти (в 2 — 3 раза и более) среди больных с органическим поражением сердца (постинфарктный кардиосклероз, гипертрофия или дилатация сердца) на фоне приема антиаритмических препаратов класса I, несмотря на то что эти средства эффективно устраняли аритмии [7, 8, 9].
Согласно наиболее распространенной на сегодняшний день классификации антиаритмических препаратов Вогана Вильямса, все антиаритмические препараты подразделяются на 4 класса:
I класс — блокаторы натриевых каналов.
II класс — блокаторы бета-адренергических рецепторов.
III класс — препараты, увеличивающие продолжительность потенциала действия и рефрактерность миокарда.
IV класс — блокаторы кальциевых каналов.Применение комбинаций антиаритмических препаратов в ряде случаев позволяет достичь существенного повышения эффективности антиаритмической терапии. Одновременно отмечается уменьшение частоты и выраженности побочных явлений вследствие того, что препараты при комбинированной терапии назначают в меньших дозах [3, 17].
Следует отметить, что показаний для назначения так называемых метаболических препаратов пациентам с нарушениями ритма не существует. Эффективность курсового лечения такими препаратами, как кокарбоксилаза, АТФ, инозие-Ф, рибоксин, неотон и т. п., и плацебо одинаковы. Исключение составляет милдронат, препарат цитопротективного действия, имеются данные об антиаритмическом эффекте милдроната при желудочковой экстрасистолии [3].
Особенности лечения основных клинических форм нарушений ритма
Экстрасистолия
Клиническое значение экстрасистолии практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) наличие экстрасистолии не влияет на прогноз и не представляет опасности для жизни. У больных с органическим поражением миокарда, например с постинфарктным кардиосклерозом, экстрасистолия может рассматриваться в качестве дополнительного прогностически неблагоприятного признака. Однако независимое прогностическое значение экстрасистолии не определено. Экстрасистолию (в том числе экстрасистолию «высоких градаций») даже называют «косметической» аритмией, подчеркивая таким образом ее безопасность.
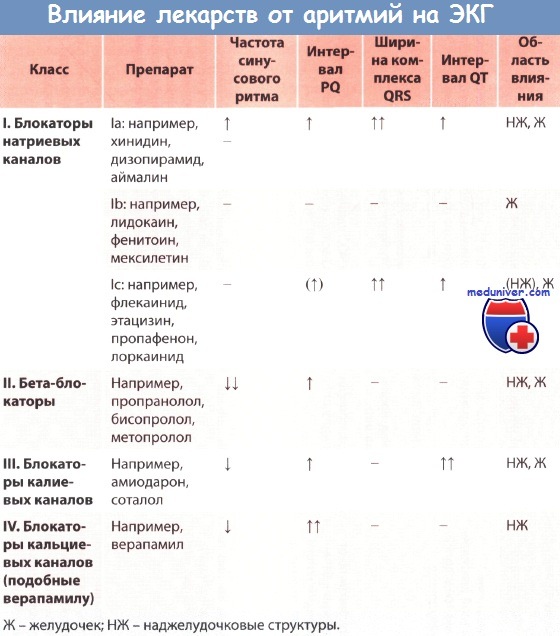
Как было уже отмечено, лечение экстрасистолии с помощью антиаритмических препаратов класса I C значительно увеличивает риск смерти. Поэтому при наличии показаний лечение начинают с назначения β-блокаторов [8, 17, 18]. В дальнейшем оценивают эффективность терапии амиодароном и соталолом. Возможно также применение седативных препаратов. Антиаритмические препараты класса I C используют только при очень частой экстрасистолии, в случае отсутствия эффекта от терапии β-блокаторами, а также амидороном и соталолом (табл. 3)
Тахиаритмии
В зависимости от локализации источника аритмии различают наджелудочковые и желудочковые тахиаритмии. По характеру клинического течения выделяют 2 крайних варианта тахиаритмий (постоянные и пароксизмальные. Промежуточное положение занимают преходящие или рецидивирующие тахиаритмии. Чаще всего наблюдается мерцательная аритмия. Частота выявления мерцательной аритмии резко увеличивается с возрастом больных [1, 17, 18].
Мерцательная аритмия
Пароксизмальная мерцательная аритмия. В течение первых суток у 50% больных с пароксизмальной мерцательной аритмией отмечается спонтанное восстановление синусового ритма. Однако произойдет ли восстановление синусового ритма в первые часы, остается неизвестным. Поэтому при раннем обращении больного, как правило, предпринимаются попытки восстановления синусового ритма с помощью антиаритмических препаратов. В последние годы алгоритм лечения мерцательной аритмии несколько усложнился. Если от начала приступа прошло более 2 суток, восстановление нормального ритма может быть опасным — повышен риск тромбоэмболии (чаще всего в сосуды мозга с развитием инсульта). При неревматической мерцательной аритмии риск тромбоэмболий составляет от 1 до 5% (в среднем около 2%). Поэтому, если мерцательная аритмия продолжается более 2 суток, надо прекратить попытки восстановления ритма и назначить больному непрямые антикоагулянты (варфарин или фенилин) на 3 недели в дозах, поддерживающих показатель международного нормализованного отношения (МНО) в пределах от 2 до 3 (протромбиновый индекс около 60%). Через 3 недели можно предпринять попытку восстановления синусового ритма с помощью медикаментозной или электрической кардиоверсии. После кардиоверсии больной должен продолжить прием антикоагулянтов еще в течение месяца.
Таким образом, попытки восстановления синусового ритма предпринимают в течение первых 2 суток после развития мерцательной аритмии или через 3 недели после начала приема антикоагулянтов. При тахисистолической форме сначала следует уменьшить ЧСС (перевести в нормосистолическую форму) с помощью препаратов, блокирующих проведение в атриовентрикулярном узле: верапамила, β-блокаторов или дигоксина.
Для восстановления синусового ритма наиболее эффективны следующие препараты:
- амиодарон - 300-450 мг в/в или однократный прием внутрь в дозе 30 мг/кг;
- пропафенон - 70 мг в/в или 600 мг внутрь;
- новокаинамид - 1 г в/в или 2 г внутрь;
- хинидин - 0,4 г внутрь, далее по 0,2 г через 1 ч до купирования (макс. доза - 1,4 г).
Сегодня с целью восстановления синусового ритма при мерцательной аритмии все чаще назначают однократную дозу амиодарона или пропафенона перорально. Эти препараты отличаются высокой эффективностью, хорошей переносимостью и удобством приема. Среднее время восстановления синусового ритма после приема амиодарона (30 мг/кг) составляет 6 ч, после пропафенона (600 мг) — 2 ч [6, 8, 9].
При трепетании предсердий кроме медикаментозного лечения можно использовать чреспищеводную стимуляцию левого предсердия с частотой, превышающей частоту трепетания, — обычно около 350 импульсов в минуту, продолжительностью 15–30 с. Кроме того, при трепетании предсердий очень эффективным может быть проведение электрической кардиоверсии разрядом мощностью 25–75 Дж после в/в введения реланиума.
Постоянная форма мерцательной аритмии. Мерцание предсердий является наиболее часто встречающейся формой устойчивой аритмии. У 60% больных с постоянной формой мерцательной аритмии основным заболеванием являются артериальная гипертония или ИБС. В ходе специальных исследований было выявлено, что ИБС становится причиной развития мерцательной аритмии примерно у 5% больных. В России существует гипердиагностика ИБС у больных с мерцательной аритмией, особенно среди людей пожилого возраста. Для постановки диагноза ИБС всегда необходимо продемонстрировать наличие клинических проявлений ишемии миокарда: стенокардии, безболевой ишемии миокарда, постинфарктного кардиосклероза.
Мерцательная аритмия обычно сопровождается неприятными ощущениями в грудной клетке, могут отмечаться нарушения гемодинамики и, главное, повышается риск возникновения тромбоэмболий, прежде всего в сосуды мозга. Для снижения степени риска назначают антикоагулянты непрямого действия (варфарин, фенилин). Менее эффективно применение аспирина [1, 17, 18].
Основным показанием для восстановления синусового ритма при постоянной форме мерцательной аритмии является «желание больного и согласие врача».
Для восстановления синусового ритма используют антиаритмические препараты или электроимпульсную терапию.
Антикоагулянты назначают, если мерцательная аритмия наблюдается более 2 суток. Особенно высок риск развития тромбоэмболий при митральном пороке сердца, гипертрофической кардиомиопатии, недостаточности кровообращения и тромбоэмболиях в анамнезе. Антикоагулянты назначают в течение 3 недель до кардиоверсии и в течение 3 — 4 недель после восстановления синусового ритма. Без назначения антиаритмических препаратов после кардиоверсии синусовый ритм сохраняется в течение 1 года у 15 — 50% больных. Применение антиаритмических препаратов повышает вероятность сохранения синусового ритма. Наиболее эффективно назначение амиодарона (кордарона) — даже при рефрактерности к другим антиаритмическим препаратам синусовый ритм сохраняется у 30 — 85% больных [2, 12]. Кордарон нередко эффективен и при выраженном увеличении левого предсердия.
Кроме амиодарона для предупреждения повторного возникновения мерцательной аритмии с успехом используются соталол, пропафенон, этацизин и аллапинин, несколько менее эффективны хинидин и дизопирамид. При сохранении постоянной формы мерцательной аритмии больным с тахисистолией для снижения ЧСС назначают дигоксин, верапамил или β-блокаторы. При редко встречающемся брадисистолическом варианте мерцательной аритмии эффективным может быть назначение эуфиллина (теопек, теотард).
Проведенные исследования показали, что две основные стратегии ведения больных с мерцательной аритмией — попытки сохранения синусового ритма или нормализация ЧСС на фоне мерцательной аритмии в сочетании с приемом непрямых антикоагулянтов — обеспечивают примерно одинаковое качество и продолжительность жизни больных [17].
Пароксизмальные наджелудочковые тахикардии
Пароксизмальные наджелудочковые тахикардии, встречающиеся гораздо реже, чем мерцательная аритмия, не связаны с наличием органического поражения сердца. Частота их выявления с возрастом не увеличивается.
Купирование пароксизмальных наджелудочковых тахикардий начинают с применения вагусных приемов. Наиболее часто используют пробу Вальсальвы (натуживание на вдохе около 10 с) и массаж сонной артерии. Очень эффективным вагусным приемом является «рефлекс ныряния» (погружение лица в холодную воду) — восстановление синусового ритма отмечается у 90% больных. При отсутствии эффекта от вагусных воздействий назначают антиаритмические препараты. Наиболее эффективны в этом случае верапамил, АТФ или аденозин.
У больных с легко переносящимися и сравнительно редко возникающими приступами тахикардии практикуется самостоятельное пероральное купирование приступов. Если в/в введение верапамила оказывается эффективным, можно назначить его внутрь в дозе 160–240 мг однократно, в момент возникновения приступов. Если более эффективным признается в/в введение новокаинамида — показан прием 2 г новокаинамида. Можно иcпользовать 0,5 г хинидина, 600 мг пропафенона или 30 мг/кг амиодарона внутрь.
Желудочковые тахикардии
Желудочковые тахикардии в большинстве случаев возникают у больных с органическим поражением сердца, чаще всего при постинфарктном кардиосклерозе [13, 14].
Лечение желудочковой тахикардии. Для купирования желудочковой тахикардии можно использовать амиодарон, лидокаин, соталол или новокаинамид.
При тяжелых, рефрактерных к медикаментозной и электроимпульсной терапии, угрожающих жизни желудочковых тахиаритмиях применяют прием больших доз амиодарона: внутрь до 4 — 6 г в сутки перорально в течение 3 дней (то есть по 20 — 30 табл.), далее по 2,4 г в сутки в течение 2 дней (по 12 табл.) с последующим снижением дозы [6, 10, 15, 16].
Предупреждение рецидивирования тахиаритмий
При частых приступах тахиаритмий (например, 1 — 2 раза в неделю) последовательно назначают антиаритмические препараты и их комбинации до прекращения приступов. Наиболее эффективным является назначение амиодарона в качестве монотерапии или в комбинации с другими антиаритмическими препаратами, прежде всего с β-блокаторами.
При редко возникающих, но тяжелых приступах тахиаритмий подбор эффективной антиаритмической терапии удобно проводить с помощью чреспищеводной электростимуляции сердца — при наджелудочковых тахиаритмиях — и программированной эндокардиальной стимуляции желудочков (внутрисердечное электрофизиологическое исследование) — при желудочковых тахиаритмиях. С помощью электростимуляции в большинстве случаев удается индуцировать приступ тахикардии, идентичный тем, которые спонтанно возникают у данного больного. Невозможность индукции приступа при повторной электрокардиостимуляции на фоне приема препаратов обычно совпадает с их эффективностью при длительном приеме [17, 18]. Следует отметить, что некоторые проспективные исследования продемонстрировали преимущество «слепого» назначения амиодарона и соталола при желудочковых тахиаритмиях перед тестированием антиаритмических препаратов класса I с помощью программированной электростимуляции желудочков или мониторирования ЭКГ.
При тяжелом течении пароксизмальных тахиаритмий и рефрактерности к медикаментозной терапии применяют хирургические способы лечения аритмий, имплантацию кардиостимулятора и кардиовертера-дефибриллятора.
Подбор антиаритмической терапии у больных с рецидивирующимим аритмиями
С учетом безопасности антиаритмических препаратов оценку эффективности целесообразно начинать с β-блокаторов или амиодарона. При неэффективности монотерапии оценивают действенность назначения амиодарона в комбинации с β-блокаторами [17]. Если нет брадикардии или удлинения интервала РR, с амиодароном можно сочетать любой β-блокатор. У больных с брадикардией к амиодарону добавляют пиндолол (вискен). Показано, что совместный прием амиодарона и β-блокаторов способствует значительно большему снижению смертности пациентов с сердечно-сосудистыми заболеваниями, чем прием каждого из препаратов в отдельности. Некоторые специалисты даже рекомендуют имплантацию двухкамерного стимулятора (в режиме DDDR) для безопасной терапии амиодароном в сочетании с β-блокаторами. Антиаритмические препараты класса I применяют только при отсутствии эффекта от β-блокаторов и/или амиодарона. Препараты класса I C, как правило, назначают на фоне приема бета-блокатора или амиодарона. В настоящее время изучается эффективность и безопасность применения соталола (β-блокатора, обладающего свойствами препаратов класса III).
П. Х. Джанашия, доктор медицинских наук, профессор
Н. М. Шевченко, доктор медицинских наук, профессор
С. М. Сорокoлетов, доктор медицинских наук, профессор
РГМУ, Медицинский центр Банка России, МоскваЧитайте также:

