Чем отличается папиллома от полипа на шейке матки
Обновлено: 28.04.2024
В течение жизни многие женщины сталкиваются с заболеваниями молочной железы. Хорошая новость в том, что большинство из них никак не связано с раком и приходится на доброкачественные новообразования. Однако в России многие из этих состояний диагностируются как предраковые заболевания, что приводит к ненужному и, порой, вредному лечению. Мы рассмотрели основные такие диагнозы и международные стандарты их лечения.
Для начала стоит отметить, что изменения груди — это нормально. Большинство из них связаны с естественными процессами — состояние груди может меняться до и во время менструации, беременности или менопаузы. Также на него влияют возраст и принимаемые женщиной гормоны и контрацептивы.
Миф 1: фиброаденомы нужно удалять
Это не так. Фиброаденомы — это небольшие новообразования в груди по форме напоминающие твердые шарики, которые легко перемещаются при нажатии и не вызывают болевых ощущений. Чаще всего фиброаденомы появляются у молодых женщин в возрасте 20-30 лет, риск их появления снижается у женщин в период после менопаузы.
Некоторые фиброаденомы можно прощупать самостоятельно. Но большинство выявляется во время маммографии или ультразвука. Показанием к удалению фиброаденомы считается быстрый рост новообразования. В остальном врачи сходятся во мнении, что фиброаденомы не требуют удаления, если они:
— не влияют на форму груди;
— не мешают самой женщине.
В некоторых случаях удаление подобных новообразований скорее противопоказано — например, у пациенток с множественными, но не растущими фиброаденомами. Поскольку при удалении опухолей могут быть задеты или удалены и здоровые ткани молочной железы.
Миф 2: мастопатия — это предраковое заболевание
Вовсе нет. На самом деле, мастопатия даже не входит в международную классификацию болезней, поскольку является нормальным состоянием груди в определенные жизненные периоды. Появление мастопатии связывают с изменением гормонального уровня в организме, именно поэтому симптомы могут усиливаться и уменьшаться в течение цикла.
Более половины женщин в возрасте 20-50 лет сталкиваются с мастопатией. При этом состоянии характерны изменения текстуры ткани молочной железы — она становится более узловатой, появляются бугорки внутри груди. У многих мастопатия протекает почти бессимптомно, у других же появляются ярко выраженные симптомы, такие как:
— боль или дискомфорт в груди, которые обычно становятся сильнее перед началом менструации и уменьшаются во время критических дней;
— грудь кажется опухшей и тяжелой;
— повышается чувствительность груди;
— боль или дискомфорт в подмышечных впадинах;
— могут образовываться «шишки» в груди, которые увеличиваются перед началом менструации, и уменьшаются после нее;
— также могут появляться зеленые или темно-коричневые выделения из груди.
Мастопатия не повышает риски возникновения рака груди. Согласно международным рекомендациям это состояние также не требует лечения, если симптомы выражены в слабой или средней степени. Для уменьшения дискомфорта могут быть рекомендованы обезболивающие, теплые компрессы, а также более облегающий бюстгальтер.
Лечение мастопатии необходимо только если симптомы мешают женщине и вызывают сильную боль в груди. В таком случае врач может назначить гормональную терапию. Хирургическое вмешательство не рекомендуется.
Миф 3: мастит способствует появлению рака груди
Нет, это не правда. Мастит — это воспаление тканей молочной железы, в большинстве случаев вызванное инфекцией или закупоркой молочных протоков. При мастите грудь может покраснеть и стать теплой на ощупь, появляются болевые ощущения. В некоторых случаях заболевание также вызывает схожие с гриппом симптомы — повышение температуры и появление головных болей. Обычно мастит проявляется только на одной груди.
Наиболее часто это заболевание появляется у женщин, кормящих грудью. По данным ВОЗ в 95% случаев заболевание появляется в первые 12 недель после родов. Инфекция развивается из-за закупорки молочного протока или попадания бактерий внутрь соска при кормлении.
Согласно международным исследованиям, мастит не влияет на повышение риска развития рака молочной железы. При лечении не рекомендуется хирургическое вмешательство. Антибиотики, назначенные лечащим врачом, помогут снять боль и температуру. В случае возникновения абсцесса груди (скопления гноя) требуется удалить его хирургическим путем и затем принимать антибиотики.
Миф 4: все кисты необходимо удалять
Не совсем так. Все зависит от размера кисты. Кисты представляют собой мягкие, легко перемещающиеся комки внутри груди. По форме они обычно круглые или овальные, наполнены жидкостью. Кисты могут появиться в одной или обеих железах. В некоторых случаях также могут возникнуть болевые ощущения в груди перед началом менструации.
Кисты — одно из самых распространенных доброкачественных поражений молочной железы, встречающееся у каждой третьей женщины в возрасте от 35 до 50 лет. Эти новообразования не являются раковыми и не увеличивают шансы развития онкологического заболевания. Однако множественные кисты могут затруднить выявление и диагностику других новообразований в тканях молочной железы.
Небольшие кисты обычно не причиняют неудобств женщине, поэтому они не требует особого лечения или удаления. Многокомпонентные кисты незначительно повышают риск развития рака молочной железы в будущем. Поэтому врач может порекомендовать сделать биопсию ткани груди. Крупные кисты (могут достигать до 2,5-5 см в диаметре) также могут вызывать дискомфорт и болевые ощущения, поскольку оказывают давление на соседние ткани. В таком случае следует обратиться к врачу для удаления жидкости из кисты, это поможет уменьшить неприятные ощущения.
Удаление кист хирургическим путем рекомендуется крайне редко. Хирургическое лечение назначают, если киста содержит жидкость кровяного оттенка или регулярно появляется через определенное время и вызывает неудобства.
Миф 5: травмы груди приводят к раку
Исследований, подтверждающих такую связь, нет.
Посттравматические олеогранулёмы (некроз жировых тканей) молочной железы возникают после операций или лучевой терапии, а также в результате травмирования жировых тканей груди. Это доброкачественное заболевание, при котором в жировых тканях появляются небольшие круглые и твердые новообразования, кожа вокруг которых выглядит покрасневшей и поврежденной. Обычно эти новообразования не вызывают болевых ощущений, но иногда некроз жировых тканей также сопровождается появлением кист, наполненных маслянистой жидкостью. Однако не стоит переживать из-за этого — небольшие кисты не требуют удаления и могут со временем исчезнуть самостоятельно.
Постравматические олеогранулёмы могут появляться у женщин и мужчин любого возраста, но наиболее они распространены среди женщин с избыточным весом и большим размером груди.
Согласно международной практике, удаление посттравматических олеогранулём не требуется, поскольку обычно они не вызывают болевых ощущений и не несут в себе риск развития рака молочной железы. Кроме того, операция может привести к поражению соседних тканей. Однако хирургическое вмешательство рекомендовано в следующих случаях:
— если биопсия ткани не дает достаточно информации, чтобы быть уверенным в диагнозе;
— новообразования не исчезают со временем, но становятся больше;
— если постравматические олеогранулёмы вызывают дискомфорт.
Миф 6: цистаденопапилломы повышают риск рака
Цистаденопапиллома, или внутрипротоковая папиллома — это небольшое доброкачественное образование внутри молочного протока, расположенное ближе к соску. Оно может сопровождаться прозрачными или кровяными выделениями из одной груди и болевыми симптомами. Чаще всего с заболеванием сталкиваются женщины от 35 до 50 лет.
Исследования доказывают, что одиночные папилломы не повышают риск развития рака молочной железы. Однако следует проявить осторожность и сделать биопсию, если:
— у женщины множественные папилломы;
— есть семейная история раковых заболеваний/ предрасположенность;
— папилломы появились в возрасте до 35 лет.
Лечение внутрипротоковых папиллом предполагает хирургическое удаление опухоли.
За помощь в научном редактировании статьи мы благодарим врача-онколога, резидента Высшей школы онкологии Александра Петрачкова
Profilaktika.Media - некоммерческий проект. Если материал вам понравился и полезен для вас, вы можете помочь проекту . Так наши журналисты смогут делать понятные и нужные инструкции чаще. Спасибо!
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисовой Элины Вячеславовны, гинеколога со стажем в 35 лет.
Над статьей доктора Борисовой Элины Вячеславовны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
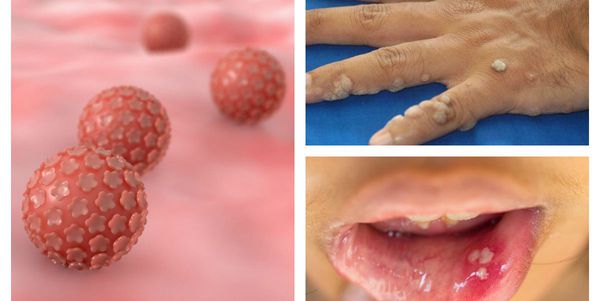
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
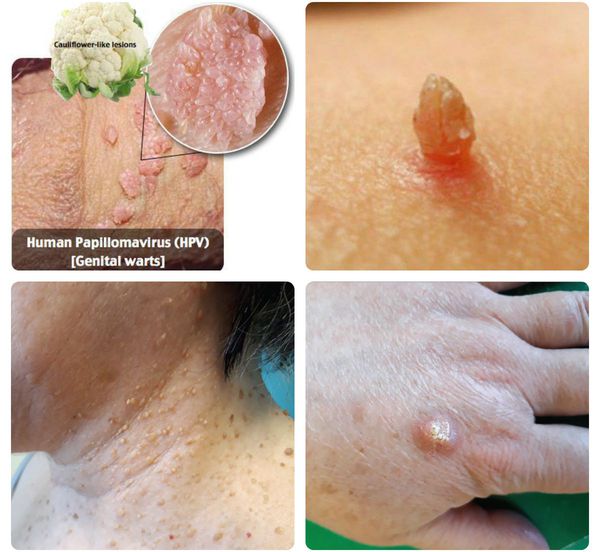
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
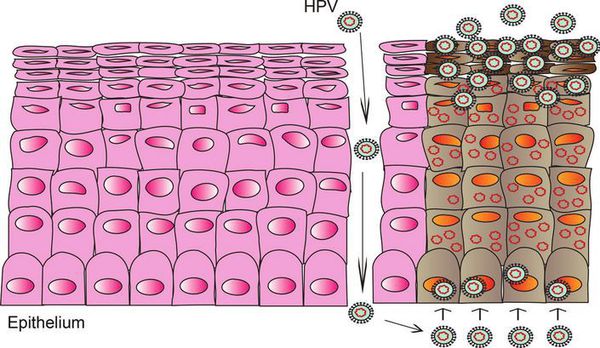
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
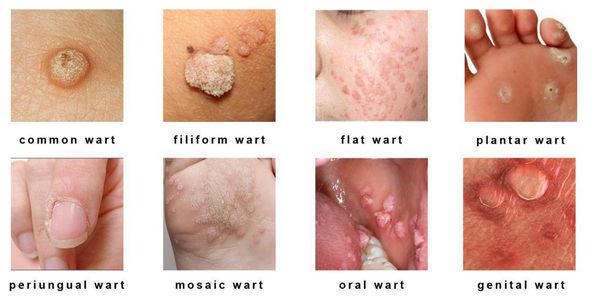
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
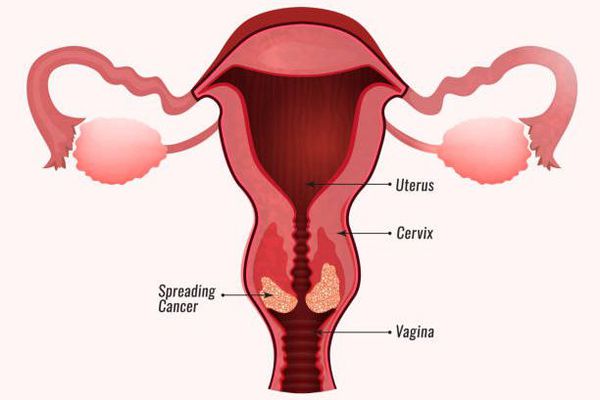
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
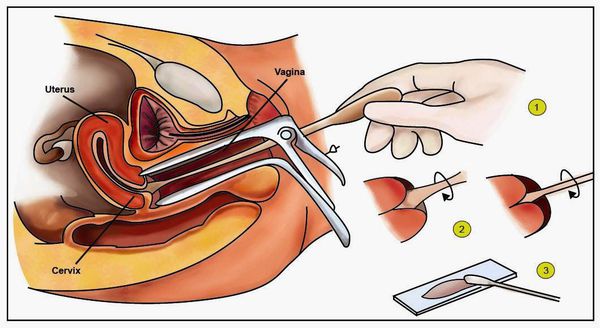
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
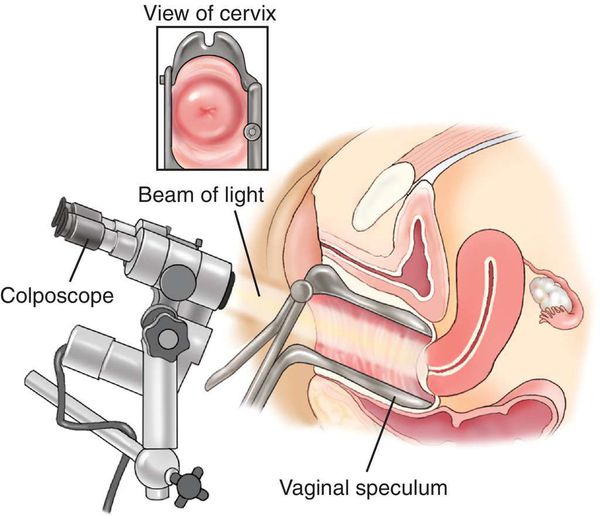
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
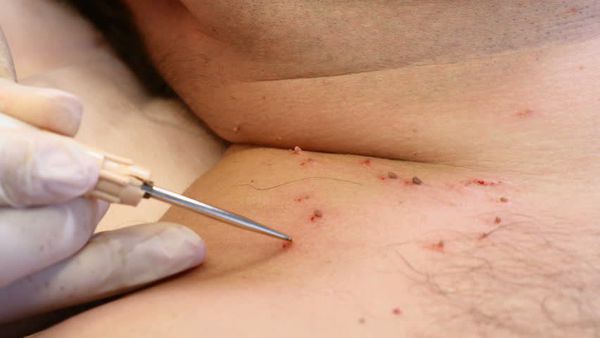
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
В отличие от дисплазий, другие заболевания шейки матки не становятся причиной развития злокачественных опухолей, поэтому подходы к лечению этих болезней должны быть более сдержанными. Однако распознать такие заболевания – не всегда простая задача. Если есть сомнения, врач должен провести биопсию, чтобы исключить предрак или рак шейки матки.
Как и дисплазии, большинство доброкачественных заболеваний шейки матки протекает бессимптомно. Лишь некоторые пациентки могут жаловаться на выделения из половых путей (особенно после полового контакта) или болезненные половые акты.
Эктопия
Влагалищная часть шейки матки покрыта многослойным плоским эпителием, а цервикальный канал (канал, соединяющий матку и влагалище – прим. авт.) – однослойным цилиндрическим. Один эпителий сменяется другим в области наружного зева (место, где цервикальный канал открывается во влагалище – прим. авт.) – эта область называется зоной трансформации. Она выглядит как стык двух цветов – бледно-розового и красного. В норме зона трансформации поднимается в цервикальный канал. В таком случае доктор видит бледно-розовую равномерно окрашенную шейку матки. Зона трансформации может располагаться на видимой части шейки матки. Однослойный эпителий тонкий, сквозь него просвечивают кровеносные сосуды, поэтому гинеколог видит красное пятно вокруг наружного зева шейки матки. Такая картина называется эктопией цилиндрического эпителия или просто эктопией.
Эктопия шейки матки, которую в России традиционно называют «эрозией» – самая частая находка при гинекологическом осмотре. Согласно Международной Федерации цервикальной патологии и кольпоскопии (IFCPC), эктопия шейки матки относится к числу нормальных кольпоскопических картин. Это значит, что эктопия не требует лечения.
Но в нашей стране ее лечат множеством методов – прижигают, замораживают, выпаривают лазером, иссекают, чтобы разрушить зону трансформации и цилиндрический эпителий. После любого из перечисленных воздействий на месте эктопии остается рубец. Он может вызывать сужение шейки матки со всеми последствиями – нарушением родовой деятельности и оттока крови из полости матки.
Эктропион
По своей природе очень близок к эктопии, поэтому их определения в зарубежной литературе часто одинаковые. В более узком смысле эктропион – это выворот канала шейки матки после родов, при котором цилиндрический эпителий виден на влагалищной части шейки матки. Эктропион не требует лечения. Изредка он вызывает обильные слизистые выделения. В этом случае врач может назначить лечение – пластику шейки матки или прижигание.
Кисты
Другой вид кист – мезонефральные. Они также называются кистами гартнерова хода. Мезонефральные кисты образуются из остатков Вольфова протока, который в норме исчезает в эмбриональном периоде. При тщательном исследовании конизатов (удаленных фрагментов) шейки матки, остатки Вольфова протока обнаруживаются в 15-20% образцов. Как и наботовы кисты, мезонефральные не требуют лечения, если не вызывают симптомов.
Некистозные образования
К некистозным образованиям шейки матки относятся полипы, эндометриоз, кондиломы, папилломы и лейомиомы.
Полип шейки матки – самая частая доброкачественная опухоль этого органа. Это нарост, который появляется на шейке матки. Пик заболеваемости регистрируется в возрасте старше 40 лет. Причины развития полипов неизвестны. Полипы шейки матки могут быть связаны с хроническим воспалением, а также с гормональными изменениями, так как гиперплазию эндометрия (утолщение слизистой оболочки матки и развитие в ней большого количества желез – прим. авт.) и полипы шейки матки часто обнаруживают одновременно.
Полипы шейки матки практически всегда доброкачественные. Лишь в редких случаях врачи могут обнаружить опухоли шейки матки – лимфому или аденосаркому, маскирующиеся под полипы.
Эндометриоз шейки матки – черные или красные точки размером 2-5 мм. Это достаточно редкая локализация эндометриоза. Заболевание может протекать бессимптомно, либо быть причиной выделений, болезненных половых актов или менструаций. Последние два проявления с большей вероятностью обусловлены эндометриозом в других локализациях. Бессимптомный эндометриоз шейки матки не требует лечения. Если пациентку беспокоят выделения из половых путей – как правило, кровянистые выделения при половых актах – врач может провести иссечение эндометриоидных очагов.
Кондиломы и папилломы шейки матки. Несмотря на похожие названия и внешний вид – выросты в виде цветной капусты – эти заболевания отличаются. Кондиломы связаны с ВПЧ низкого онкогенного риска (чаще всего 6 и 11 типы). Папилломы шейки матки не связаны с ВПЧ, причина их развития неизвестна. Кондиломы и папилломы крайне редко бывают злокачественными. В некоторых случаях они могут вызывать кровянистые выделения, например, при половых контактах. И те, и другие новообразования нужно удалять.
Лейомиома. Шейка матки редко становится основным и единственным местом проявления заболевания – в 19 из 20 случаев миомы развиваются в теле матки.
У лейкоплакии нет симптомов. Врач-гинеколог при осмотре видит ее как белесоватые наложения на шейке матки. Это депозиты кератина, который вырабатывается эпителиальными клетками. Основная опасность лейкоплакии шейки матки в том, что скрывается под ней, потому что синтез кератина также может происходить в участках дисплазии или рака шейки матки. Биопсия обязательна, если лейкоплакия обнаружена в зоне трансформации, потому что большинство дисплазий появляется именно там.
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
Мишень вируса
ВИЧ-инфекция вызывается рок-звездой вирусной концертной сцены, ретровирусом со сложной белковой оболочкой, которая позволяет «хозяину» мутировать и оставаться невидимым для иммунитета. Это одна из самых неуправляемых инфекций: несмотря на наличие доступной терапии, сохраняется высокий риск развития различных онкологических заболеваний.
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток - одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
СПИД-индикаторные опухоли
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
Опухоли, связанные с ВПЧ
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
Также для предотвращения ИРШМ девочкам с сопутствующей ВИЧ-инфекцией старше 9 лет и до 26 лет крайне рекомендуется вакцинация от ВПЧ-инфекции (вакцины: 2-валентный Церварикс, 4-валентный Гардасил, в Европе/США - 9-валентный Гардасил-9). Кроме ИРШМ и дисплазии вульвы и влагалища у женщин, вакцинация предотвращает развитие рака анального канала. У ВИЧ+ гетеросексуальных мужчин и МСМ риск этого вида рака возрастает в 19 раз.
О чем еще нужно знать
У пациентов с ВИЧ-инфекцией повышается риск развития:
Гепатоцеллюлярная карцинома
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Неходжкинские лимфомы (НХЛ)
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Одними из причин развития лимфом у ВИЧ-позитивных пациентов считаются состояние «хронического воспаления» во время какой-либо длительной инфекции (например, инфекции Helicobacter pylori, вирусного гепатита C) и аутоиммунные заболевания, предшествующие диагнозу.
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.

В настоящее время полипы матки довольно распространенная патология, с которой гинекологам приходится сталкиваться в амбулаторной практике. Эти образования часто остаются бессимптомными, но если они растут из слизистой оболочки в полости матки, они могут быть одной из наиболее распространенных причин аномального кровотечения из половых путей у женщин.
Симптоматические полипы матки — важное показание обратиться к гинекологу и принять решение об их удалении.
Полипы матки – что это такое?
Полип матки представляет собой протрузию, доброкачественную гипертрофию слизистой оболочки каплевидной, округлой формы. В подавляющем большинстве полипы — доброкачественные поражения и не имеют тенденции быть злокачественными.
Полипы матки обычно диагностируются случайно, потому что они часто не дают никаких симптомов в течение длительного времени. Патология обнаруживается у 5-12% женщин, а самая высокая заболеваемость полипами матки приходится на репродуктивный возраст. Однако они могут возникать и после менопаузы.
Полипы шейки матки и тела матки – причины и диагностика
Среди полипов можно выделить две основные группы, относящиеся к разным частям одного и того же органа. Это полипы шейки матки и полипы полости матки. Несмотря на схожее по звучанию название и близость обеих структур (шейки матки и полости матки), это самостоятельные варианты заболевания, с разными методами диагностики и дальнейшего ведения.
Бывает и так, что оба типа полипов сосуществуют друг с другом у одной и той же пациентки. Их часто путают с миомой матки, но это также два совершенно разных заболевания.
Полипы шейки матки
Полипы шейки матки обычно не являются поводом для беспокойства с точки зрения онкологии, так как риск трансформации их в злокачественную форму составляет всего 0,1%. Обычно полип шейки матки может быть диагностирован во время классического гинекологического осмотра с использованием зеркала.
Во время осмотра шейного диска врач может заметить поражение, выходящее из цервикального канала, обычно достигающее до 3 см. Реже полип прячется внутри канала.
В отличие от полипов матки, ультразвук обычно не может выявить полипы шейки матки, если они не достигают больших размеров.
Полипы эндометрия
Как и в случае с полипами шейки матки, полипы полости матки (тела) обычно не являются поводом для беспокойства по поводу рака, поскольку частота их малигнизации составляет около 1%. Важно отметить, что они также не классифицируются как предраковое состояние.
Однако симптомы, которые могут давать эти новообразования, характерны и для других заболеваний, именно поэтому исключение ракового процесса является золотым стандартом ведения в случае полипов полости матки. Причины возникновения этих полипов до конца не изучены, но считается, что решающую роль играет повышенная концентрация женских половых гормонов – эстрогенов.
Полипы полости матки могут достигать размеров до нескольких, реже десятка, сантиметров. Они встречаются поодиночке или группой, а к слизистой они фиксируются толстым основанием или выступающей ножкой. Частота возникновения полипов эндометрия увеличивается с возрастом.
При подозрении на полип тела матки, или полип эндометрия, врач начнет консультацию с проведения опроса о тревожных симптомах. Дальнейшее лечение будет включать гинекологическое обследование, не способное визуализировать полипы полости матки, но выявляющее сопутствующие патологии, и ультразвуковое исследование – самый простой способ увидеть возможное изменение между 5-м и 10-м днем цикла. Именно в эти дни слизистая оболочка, выстилающая матку, еще относительно тонкая и не успела вырасти с продолжительностью цикла.
Полипы шейки матки – симптомы
Полипы шейки матки могут вызывать неприятные симптомы, однако чаще патология остается бессимптомной. Если симптомы есть, то это:
- кровянистые выделения между месячными;
- кровянистые выделения после полового акта;
- выделения из влагалища с примесью крови или без нее.
Также было доказано, полипоз может быть причиной повышенной предрасположенности к интимным инфекциям.
Симптомы полипов эндометрия
К симптомам полипов тела матки относятся:
- кровянистые выделения между менструациями;
- длительные или более обильные ежемесячные кровотечения, чем раньше;
- иногда бывают и кровянистые выделения из влагалища.
Эти симптомы могут также возникать после менопаузы, что должно побудить больную к более широкой диагностике и исключению ракового процесса, дающего аналогичную симптоматику.
Полипы шейки матки – лечение
В случае визуализации поражения, которое по своим особенностям напоминает полип шейки матки, гинеколог назначает полипэктомию, удаляя полип с помощью специальных инструментов для его «скручивания».
Процедура обычно короткая – до нескольких минут и проводится в рамках одного дня. В зависимости от решения врача и восприятия боли пациенткой, процедура может проводиться под коротким, внутривенным наркозом или даже без анестезии.
Удаление полипа шейки матки обычно также сопровождается процедурой кюретажа канала полости матки, что особенно важно в связи с возможным рецидивом полипа после его неполного удаления, а также для исключения возможного ракового процесса.
После процедуры, полученный в ходе нее материал передается на гистопатологическое исследование для окончательного подтверждения диагноза. В зависимости от лаборатории, обычно приходится ждать результата около 3-4 недель.
Лечение полипов полости матки
В случае подозрения на полип в полости матки дальнейшее лечение включает в себя выполнение гистероскопии, а значит и обследования, которое заключается во введении небольшой камеры через шейку матки внутрь матки и визуальной оценке ее полости.
Специальный инструмент гистероскоп дает возможность удалить очаг поражения вместе с кюретированным материалом из полости матки. Удаленные ткани отдают на гистопатологическое исследование, как в случае с полипами шейки матки. Процедура обычно длится до нескольких минут и проводится под коротким, внутривенным наркозом.
Удаление полипа шейки матки – рекомендации после операции. Полипы матки и влияние на фертильность
Влияние на фертильность и дальнейшие рекомендации после процедуры обусловлены типом полипа. Полипы на шейке матки не оказывают существенного влияния на фертильность и показаний к сохранению перерыва в усилиях забеременеть после процедуры удаления нет.
Если полип шейки матки обнаружен во время беременности, решение о его удалении обычно откладывается до родов. Бывает и так, что полип самопроизвольно отпадает во время родов под влиянием гормонов.
В свою очередь, в случае полипов эндометрия бывает, что они препятствуют имплантации эмбриона в полости матки. Это означает бесплодие, поэтому женщинам детородного возраста часто рекомендуется их удалять. После процедуры по удалению полипа из тела матки рекомендуется трехмесячный перерыв до зачатия.
Читайте также:

