Чем мазать донорское место после пересадки кожи
Обновлено: 15.04.2024
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Комплексное лечение длительно незаживающих ран разной этиологии
Журнал: Клиническая дерматология и венерология. 2013;11(3): 101‑106
Третьякова Е.И. Комплексное лечение длительно незаживающих ран разной этиологии. Клиническая дерматология и венерология. 2013;11(3):101‑106.
Tret'iakova EI. Combination treatment for persistent wounds of various etiologies. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):101‑106. (In Russ.).
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Представлены результаты наружного лечения 2% кремом Аргосульфан 47 больных с длительно не заживающими ранами разной этиологии. В результате комплексного лечения полная эпителизация трофических язв у больных с хронической венозной недостаточностью, облитерирующим эндоартериитом и липоидным некробиозом наступила у 10 (41,7%) пациентов, частичный регресс - у 14 (58,3%). Явления пиодермии разрешились у 7 (87,5%) больных, значительно уменьшились - у 1 (12,5%). Трещины в области ладоней и подошв на фоне разрешения тилотической экземы заэпителизировались у всех 15 (100%) пациентов. Крем Аргосульфан в комплексной терапии больных с длительно не заживающими ранами оказался высокоэффективным, отличался хорошей переносимостью, удобством в применении.
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Важнейшей медико-социальной проблемой является лечение длительно не заживающих ран разной этиологии. Трофические язвы и глубокие трещины кожи в области нижних конечностей, а также хронические язвенные пиодермии резко снижают качество жизни и надолго ограничивают активность больных. Особое место в лечении и профилактике этих заболеваний, предупреждающей развитие инфекционного процесса в ране и являющейся барьером на пути распространения инфекции, занимает местная терапия.
Современные высокоэффективные средства для местного лечения длительно не заживающих ран имеют ряд лечебных качеств, которые позволяют применять их с учетом фаз раневого процесса. Они должны обладать противовоспалительным и протеолитическим действием, иметь широкий антибактериальный спектр воздействия, сохранять активность в кислой среде, не вызывать явлений гипергрануляции и пигментации, иметь гипоаллергенные качества, быть нетоксичными и удобными в применении.
Существует много комбинированных препаратов для местного лечения, содержащих антибиотики или сульфаниламиды в сочетании друг с другом и/или разными антисептиками. Для таких препаратов характерно более медленное развитие микробной резистентности и более широкий охват бактериальных агентов — возбудителей инфекций.
Присутствующие в составе крема ионы серебра усиливают антибактериальное действие сульфаниламида — тормозят рост и деление бактерий путем связывания с дезоксирибонуклеиновой кислотой микробной клетки [1]. Постепенное высвобождение ионов серебра подавляет рост патогенной микрофлоры на протяжении длительного периода нахождения повязки на ране, что важно при высоком риске реинфекции госпитальными штаммами и является постоянным барьером на пути распространения инфекции.
Кроме того, ионы серебра ослабляют сенсибилизирующие свойства сульфаниламида. Существует мнение, согласно которому аппликация на кожу и слизистые оболочки сульфаниламидов нежелательна в связи с невысокой активностью и риском возникновения аллергической реакции. При нанесении такой мази на ожоговую или инфицированную поверхность могут наблюдаться жжение и боль [1]. Гидрофильная основа крема Аргосульфан, имеющая оптимальный рН и содержащая большое количество воды, обеспечивает его увлажняющее и аналгезирующее действие и приводит к уменьшению сроков заживления ран.
Благодаря минимальной резорбции Аргосульфан-крем, нанесенный даже на обширные раневые поверхности, не оказывает токсического действия, так как сульфатиазол серебра обладает небольшой растворимостью, благодаря чему концентрация лекарственного средства в ране длительно поддерживается на одинаковом уровне. Незначительное количество сульфатиазола серебра, оказавшегося в кровотоке, в печени подвергается ацетилированию и в моче находится в виде неактивных метаболитов и частично в неизмененном виде [1]. В связи с отсутствием системной абсорбции препарата можно использовать крем Аргосульфан в сочетании с другими препаратами. Повязки с кремом Аргосульфан, содержащие ионы серебра, безболезненны при наложении на раневую поверхность, не присыхают к ране и легко удаляются с ее поверхности, обладают мягким подсушивающим эффектом, хорошо проникают в некротизированную ткань и экссудат. Тканевый детрит, пропитанный препаратом, образует «защитную подушку», под которой идет форсированное образование грануляций и эпителизация.
Мы применяли крем Аргосульфан при длительно не заживающих ранах у больных с трофическими язвами разной этиологии, липоидном некробиозе, хронической язвенной и язвенно-вегетирующей пиодермиях, глубоких трещинах, осложняющих течение тилотической экземы.
Появление трофических язв может осложнить течение многих заболеваний – от болезней системы кровообращения до нарушений обмена веществ, причем развитие язвенного дефекта сопровождается как нарушением нормального кровообращения, так и изменением иннервации. Именно поэтому процесс выздоровления может потребовать применения комплексного воздействия и достаточно продолжительного лечения.
Различают варикозные, ишемические и нейротрофические язвы [2—5]. Наибольшую группу (1—2% взрослого населения) составляют больные с хронической венозной недостаточностью (ХВН) нижних конечностей, развивающейся при нарушении венозного оттока и повышении давления внутри капилляров. Основные причины ХВН — варикозное расширение вен и посттромбофлебитический синдром. При повреждении клапанов глубоких вен голени нарушается функция мышечно-венозной помпы и возникает ретроградный ток крови. Повреждение прободающих вен, которые соединяют поверхностные вены с глубокими, усугубляет венозную недостаточность. Из-за отложения фибрина в периваскулярном пространстве и угнетения тканевого фибринолиза развиваются склероз и облитерация лимфатических и мелких кровеносных сосудов. Периваскулярный фиброз нарушает доставку питательных веществ к эпидермису, что приводит к образованию варикозных трофических язв [2—5].
Ишемические язвы формируются при заболеваниях периферических артерий, в частности при облитерирующем атеросклерозе (ОАС). ОАС всегда сопровождается поражением кожи — от постепенно нарастающей ишемии до инфаркта, т.е. некроза, развивающегося при внезапном нарушении кровоснабжения в результате атероэмболии — закупорки мелких артерий фрагментами атеросклеротических бляшек. Ишемические язвы локализуются на часто травмируемых участках и местах сдавления, сопровождаются выраженными болевыми ощущениями. Смешанные язвы развиваются у больных, страдающих и ХВН, и ОАС, у которых клинически присутствуют черты обоих заболеваний [4, 5].
Причиной нейротрофических язв являются поражение чувствительных и двигательных нервов, нарушения кровообращения и атеросклероз при сахарном диабете и его осложнениях, вторичном гиперпаратиреозе, гранулематозном воспалении в ответ на дегенерацию коллагена при липоидном некробиозе [6, 7].
Липоидный некробиоз — редкий хронический дерматоз сосудисто-обменного характера, который обычно относят к группе локализованных липоидозов кожи. Провоцирующими факторами при липоидном некробиозе в 1 /3 случаев является сахарный диабет, еще у 1 /3 — нарушение толерантности к глюкозе, поэтому необходимы семейный анамнез и исследования для выявления скрытых форм сахарного диабета. Началу заболевания нередко предшествует травма. Дегенерация коллагена приводит к усиленной агрегации тромбоцитов, микроангиопатиям, поражению артериол, склерозированию и облитерации сосудов в очагах некробиоза. Сосудистые нарушения приводят к нарушению трофики и некробиотическим изменениям дермы с последующим отложением в ней липидов. Заболевание часто имеет длительное рецидивирующее течение, его выраженность не зависит от тяжести сахарного диабета, формирующиеся трофические язвы сопровождаются выраженными болевыми ощущениями и заживают, как правило, с формированием грубого рубца [6, 7].
Без специального лечения трофические язвы характеризуются низкой тенденцией к заживлению и длительным рецидивирующим течением [8, 9]. Общепризнано, что оперативное лечение ХВН и ОАС лучше выполнять после заживления трофической язвы или тщательной санации ее поверхности. Однако консервативное лечение с применением устаревших малоэффективных местных медикаментозных средств часто осложняется дерматитом, экземой, рожистым воспалением, что отодвигает сроки выполнения сосудистой операции. На выбор лекарственного препарата влияют фаза течения заболевания и выраженность воспалительной реакции (I фаза — предъязвенное состояние; II фаза — дистрофические изменения, некроз, воспаление кожи и прилежащих тканей; III фаза — очищение язвы и регенерация; IV фаза — эпителизация и рубцевание), осложнения (микозы, экзема, пиодермии, рожистое воспаление, рецидивирующий тромбофлебит, малигнизация и др.), видовой состав микрофлоры язвы. В многочисленных бактериологических исследованиях качественного состава микрофлоры поверхности трофических язв выявлена полирезистентная грампозитивная и грамнегативная микрофлора. Содержание микроорганизмов в индуративно измененных тканях, окружающих язву, иногда достигает 10 7 -10 9 микробных тел на 1 г ткани раны, что указывает на высокий риск генерализации инфекционного процесса [10]. Как правило, выделяемые микроорганизмы высокорезистентны не только к традиционным антибактериальным препаратам, но и к наиболее часто используемым в таких случаях местным средствам — растворам фурацилина, хлоргексидина, синтомициновой эмульсии, мазям с антибиотиками (тетрациклином, гентамицином) и др. На стадиях грануляции и эпителизации, для их ускорения, а также при осложнении ран дерматитом, экземой или другими проявлениями аллергии на традиционные препараты, средством выбора могут стать соли серебра, учитывая их высокую эффективность в подавлении как грампозитивной, так и грамнегативной микрофлоры, лучшую переносимость и редкость аллергических реакций даже у пациентов с отягощенным аллергоанамнезом.
Пиодермии (гнойничковые заболевания кожи) представляют собой группу дерматозов, в основе которых лежит гнойное воспаление кожи и ее придатков, а также подкожно-жировой клетчатки. На долю пиодермий приходится 1 /3 всех случаев заболеваний кожи [4, 5]. Развитию пиодермий способствуют микротравмы, мацерация и загрязнение эпидермиса, повышенное потоотделение, переохлаждение, перегревание, эндокринопатии (сахарный диабет), гипогаммаглобулинемия, недостаточное поступление белков, гиповитаминоз, нарушения иммунитета и тяжелые соматические заболевания, переутомление, хронические интоксикации, персистирующие очаги стафилококковой инфекции. Наиболее частыми возбудителями пиодермий являются золотистый и эпидермальный стафилококк (80—90% больных), в 10—15% случаев выявляется смешанная инфекция (стафилококк в сочетании со стрептококком, синегнойной палочкой, протеем, кишечной палочкой и др.) [1, 4, 10].
Хронические язвенная и язвенно-вегетирующая пиодермии относятся к глубоким стрептостафилококковым пиодермиям, характеризуются образованием плохо заживающих язвенных гнойных поражений кожи и подлежащих тканей. Нередко заболевание сопровождается ухудшением общего состояния, повышением температуры тела, слабостью, явлениями интоксикации, лимфангиитами и лимфаденитом. Язвенная пиодермия (стрептостафилококковое импетиго) проявляется фликтенами, эктимами, располагающимися на фоне эритемы. Высыпания, как правило, диссеминированные, захватывают обширные участки кожного покрова. Под корками характерно образование глубоких язв с вялыми грануляциями на дне и воспаленными мягкими краями. Стрептостафилококковое импетиго нередко является осложнением зудящих дерматозов (экземы, чесотки, атопического дерматита и др.). Хроническая язвенно-вегетирующая пиодермия характеризуется язвенными образованиями неправильной формы с выраженными вегетациями в области краев и дна. Нередко вокруг язвы присутствует застойно-розовый венчик гиперемии. Характерно хроническое течение с периодическими обострениями с появлением новых язв или серпигенизации основного язвенного образования.
Терапия пиодермий должна быть этиопатогенетической. При лечении хронических, рецидивирующих и глубоких форм пиодермий используют антибиотики (местно и системно), антисептические растворы, по показаниям глюкокортикостероиды, иммуномодуляторы, витамины, проводят вскрытие пустул и абсцессов, при необходимости — удаляют и выскабливают вегетации и некротические ткани.
Тилотическая (роговая) экзема — хроническое упорно рецидивирующее аллергическое заболевание кожи, разновидность истинной экземы. Тилотическая экзема проявляется гиперкератозом ладоней и подошв с образованием грубых роговых и корковых наслоений, сухостью кожи, а также глубокими болезненными длительно не заживающими, нередко кровоточащими трещинами. Данное заболевание характеризуется поливалентной сенсибилизацией и аутосенсибилизацией, протекает на фоне нейроэндокринных сдвигов, сопровождается изменениями в центральной и вегетативной нервной системе, нарушениями обменных процессов и трофики тканей [4, 5]. Поражение подошв и ладоней, как правило, симметричное, трещины формируются на фоне эритемы, шелушения, особенно на участках наибольшего давления и нагрузки, в том числе и на боковых поверхностях пальцев. Воспаление может быть выражено на ограниченном участке или занимать всю подошву и/или ладонь, боль в области трещин может быть более интенсивной, чем зуд. Тенденция к углублению трещин связана с возрастом пациента, длительностью болезни, холодным временем года и наличием фоновых заболеваний.
В трещины на подошвах легко может проникать пиогенная инфекция, развиваться рожистое воспаление или пиодермии. Тилотическая экзема резистентна к лечению, склонна к рецидивированию, к улучшению состояния приводят частое и сильное увлажнение кожи и немедленное прекращение ношения влажной обуви [11].
Под нашим наблюдением находились 47 больных (13 мужчин, 34 женщины) в возрасте 44—75 лет с трофическими язвами, развившимися на фоне ХВН и облитерирующего эндартериита, нарушениях кровоснабжения и трофики при липоидном некробиозе, а также с пиодермиями и тилотической экземой. Длительность заболевания составляла от 2 мес до 4 лет. Все больные в составе комплексной терапии наружно применяли крем Аргосульфан.
У 11 (23,4%) больных имелись варикозные, у 5 (10,6%) — смешанные трофические язвы, у 8 (17%) — трофические язвы при липоидном некробиозе; у 8 (17%) — хроническая язвенная и хроническая язвенно-вегетирующая пиодермии, у 15 (32%) — тилотическая экзема с глубокими трещинами на ладонях и подошвах.
У 22 (46,8%) больных дерматозы протекали на фоне эндокринных заболеваний: у 4 (8,4%) — сахарного диабета, у 2 (4,2%) — нарушений толерантности к глюкозе, у 5 (10,6%) — узлового зоба, у 1 (2,1%) — гипотиреоза, у 1 (2,1%) — патологии надпочечников. У 2 (4,2%) больных был выявлен хронический бронхит, у 3 (6,3%) — хронический гастрит, у 5 (10,6%) — хронический панкреатит, у 2 (4,2%) — вирусный гепатит С, у 10 (21,3%) — гипертоническая болезнь, у 9 (1%) — ишемическая болезнь сердца, у 2 (4,2%) — миома матки.
При бактериологических исследованиях качественного состава микрофлоры с поверхности очагов (язв, трещин) у 29 (61,7%) больных выявлен золотистый и эпидермальный стафилококк, у 18 (38,3%) — смешанная инфекция (стафилококки в сочетании со стрептококком, кишечной палочкой, бактероидами, протеем, дрожжевыми грибами) в количестве 104—105 микробных тел на 1 г ткани раны.
Всем пациентам назначался охранительный режим. Предлагалось ограничить пребывание в вертикальном положении с целью уменьшения статической нагрузки, размещать пораженную конечность в возвышенном положении. Рекомендовалось уменьшить потребление с пищей соли и экстрактивных продуктов, больным с тилотической экземой назначалась гипоаллергенная диета, пациентам с липоидным некробиозом — диета с ограничением углеводно-жировой нагрузки.
В составе комплексной терапии все больные получали сосудистые препараты и венопротекторы (пентоксифиллин, детралекс, эскузан), антиагреганты (курантил), десенсибилизирующие средства (глюконат кальция, тиосульфат натрия), улучшающие трофику (солкосерил, актовегин) и антигистаминные (супрастин, тавегил, лоратадин) препараты. Пациентам с трофическими язвами, липоидным некробиозом, пиодермиями проводилось лечение антибиотиками цефалоспоринового ряда, иммуномодуляторами (метилурацил, виферон, циклоферон), витаминами (мильгамма), с тилотической экземой — препаратами витамина А (аевит, ретинола пальмитат), с липоидным некробиозом — препаратами липоевой кислоты (берлитион).
В качестве наружного средства все больные использовали 2% крем Аргосульфан. После очищения 0,1% водным раствором хлоргексидина и/или хирургической обработки раневых поверхностей препарат слоем 2—3 мм ежедневно 2 раза в сутки наносили на очаги поражения на трещины или язвы с середины к краям до полного впитывания. На очаги, имеющие большую площадь, крем Аргосульфан наносили ежедневно под окклюзионную повязку на ночь. Рана во время лечения покрывалась препаратом полностью, если ее часть открывалась, крем наносили дополнительно. Курс комплексного лечения составлял 25—30 сут.
Болевых ощущений, а также местных и общих аллергических реакций при использовании крема Аргосульфан не наблюдалось.
Крем Аргосульфан при местном лечении длительно не заживающих ран позволил добиться улучшения у всех больных. В результате комплексной терапии полная эпителизация трофических язв у больных с ХВН, ОАС и липоидным некробиозом наступила в 10 (41,7%) случаях, частичный регресс (уменьшение размеров, воспалительных и дистрофических изменений кожи, появление зрелых грануляций и краевой эпителизации с минимально выраженной пигментацией) — в 14 (58,3%). Явления пиодермии разрешились у 7 (87,5%) пациентов, значительно уменьшились (с резким замедлением роста микрофлоры до 102 микробных тел на 1 г ткани раны) — у 1 (12,5%). Отсутствие под повязкой с кремом Аргосульфан гипергрануляций в ране способствовало формированию негрубых подвижных слабопигментированных рубцов. Трещины в области ладоней и подошв на фоне разрешения тилотической экземы эпителизировались у всех 15 (100%) пациентов.
Поскольку крем Аргосульфан — препарат длительного применения, что обусловлено медленным восстановлением физиологических процессов в эпидермисе и дерме, больным с трофическими язвами и пиодермией мы рекомендовали использовать его по ранее применяемой схеме амбулаторно в течение 1—2 мес после окончания курса лечения в стационаре (до полного заживления или пересадки кожи).
Таким образом, 2% крем Аргосульфан в комплексной терапии больных с длительно не заживающими ранами оказался высокоэффективным как на стадии формирования трофических язв, так и в период заполнения глубоких ран грануляционной тканью, что во многих случаях привело к самостоятельному заживлению их под повязкой. Препарат отличался хорошей переносимостью, удобством в применении, позволил значительно снизить стоимость лечения больного в стационаре и успешно продолжить лечение амбулаторно.
Кожный трансплантат-это часть здоровой кожи, удаленная из одной области вашего тела, чтобы восстановить поврежденную или отсутствующую кожу где-то еще на вашем теле. Эта кожа не имеет своего собственного источника кровотока.
Изучение того, как ухаживать за кожными лоскутами и трансплантатами, может помочь им быстрее вылечиться и уменьшить рубцы.
Почему выполняется операция кожного лоскута или трансплантата
Кожный лоскут-это здоровая кожа и ткань, которая частично отделяется и перемещается, чтобы покрыть близлежащую рану.
- Кожный лоскут может содержать кожу и жир, или кожу, жир и мышцы.
- Часто кожный лоскут все еще прикреплен к своему первоначальному месту на одном конце и остается соединенным с кровеносным сосудом.
- Иногда лоскут перемещается на новое место и кровеносный сосуд хирургическим путем пересоединяется. Это называется свободным клапаном.
Кожные трансплантаты используются для лечения более серьезных, крупных и глубоких ран, в том числе:
- Раны, которые слишком велики, чтобы зажить самостоятельно
- Ожоги
- Потеря кожи от серьезной инфекции кожи
- Хирургическое вмешательство при раке кожи
- Венозные язвы, язвы под давлением или диабетические язвы, которые не заживают
- После мастэктомии или ампутации
Участок, из которого берется кожа, называется донорским участком. После операции у вас будет две раны, сам трансплантат или лоскут и донорский участок. Донорские участки для трансплантатов и лоскутов подбираются на основании:
- Насколько близко кожа соответствует области раны
- Насколько заметен будет шрам с места донора
- Насколько близок донорский участок к ране
Часто донорский участок может быть более болезненным после операции, чем рана из-за вновь открытых нервных окончаний.
Уход за кожными лоскутами и трансплантатами
Вам нужно будет ухаживать за лоскутом или трансплантатом, а также за донорским участком. Когда вы вернетесь домой после операции, у вас будет повязка на ваших ранах. Повязка делает несколько вещей, в том числе:
- Защитите вашу рану от микробов и уменьшите риск инфекции
- Защитите область по мере ее заживления
- Впитайте любые жидкости, которые вытекают из вашей раны
Для ухода за трансплантатом или лоскутом сайта:
- Возможно, Вам потребуется отдохнуть в течение нескольких дней после операции, так как ваша рана заживает.
- Тип повязки у вас есть зависит от типа раны и где она находится.
- Держите повязку и область вокруг нее чистой и свободной от грязи или пота.
- Не позволяйте повязке промокнуть.
- Не трогайте повязку. Оставьте его на месте до тех пор, пока ваш врач рекомендует (около 4-7 дней).
- Принимайте любые лекарства или обезболивающие, как указано.
- Если это возможно, постарайтесь поднять рану так, чтобы она была выше вашего сердца. Это помогает уменьшить отек. Возможно, вам придется делать это сидя или лежа. Вы можете использовать подушки, чтобы поддержать область.
- Если ваш врач говорит, что это нормально, вы можете использовать пакет со льдом на повязке, чтобы помочь с отеками. Спросите, как часто вы должны применять пакет со льдом. Обязательно держите повязку сухой.
- Избегайте любых движений, которые могут растянуть или повредить лоскут или трансплантат. Избегайте попадания или натыкаясь на область.
- Вам нужно будет избегать напряженных физических упражнений в течение нескольких дней. Спросите вашего доктора на сколько времени.
- Если у вас есть вакуумная повязка, вы можете иметь трубку, прикрепленную к повязке. Если трубка отваливается, сообщите об этом своему врачу.
- Вы, вероятно, увидите своего врача, чтобы изменить повязку в течение 4-7 дней. Возможно, Вам потребуется изменить повязку на лоскут или трансплантат вашим врачом несколько раз в течение 2-3 недель.
- Как сайт лечит, вы можете быть в состоянии ухаживать за ним в домашних условиях. Ваш врач покажет вам, как ухаживать за вашей раной и наносить повязки.
- Сайт может стать зудящим, как он лечит. Не царапайте рану и не ковыряйте ее.
- Нанесите солнцезащитный крем SPF 30 или выше на хирургические участки, если они подвергаются воздействию солнца.
Для ухода за донорским участком:
- Оставьте повязку на месте. Держите его в чистоте и сухости.
- Ваш врач удалит повязку примерно через 4-7 дней или даст вам инструкции по ее удалению.
- После того, как повязка будет удалена, вы можете оставить рану открытой. Однако, если он находится в области, которая покрыта одеждой, вы захотите покрыть сайт, чтобы защитить его. Спросите своего врача, какой тип повязки использовать.
- Не наносите никаких лосьонов или кремов на рану, если ваш врач не говорит вам об этом. Когда область заживает, она может зудеть и могут образоваться струпья. Не выковыривайте струпья и не царапайте рану, когда она заживет.
Купание или душевая кабина
Ваш врач даст вам знать, когда это нормально, чтобы купаться после операции. Иметь в виду:
- Возможно, вам придется принимать губчатые ванны в течение 2-3 недель, пока ваши раны находятся на ранних стадиях заживления.
- После того, как вы получите право купаться, душ лучше, чем ванны, потому что рана не впитывается в воду. Промачивание раны может привести к ее повторному открытию.
- Будьте уверены, чтобы защитить ваши повязки во время купания, чтобы держать их сухими. Ваш врач может посоветовать закрыть рану полиэтиленовым пакетом, чтобы сохранить ее сухой.
- Если ваш доктор дает ОК, то нежно прополощите вашу рану с водой по мере того как вы купаете. Не трите и не скребите рану. Ваш врач может рекомендовать специальные очищающие средства для использования на ваших ранах.
- Аккуратно промокните сухую область вокруг раны чистым полотенцем. Дайте ране высохнуть на воздухе.
- Не используйте мыло, лосьоны, порошки, косметику или другие средства по уходу за кожей на вашей ране, если это не указано вашим врачом.
В какой-то момент во время процесса заживления вам больше не понадобится повязка. Ваш врач скажет вам, когда вы можете оставить свою рану открытой и как ухаживать за ней.
tagPlaceholder Tags: 7 , медсправка, медсправки для гаи , медсправка для гибдд, права, остеопат , медкомиссия для поступления, больничный лист, врачи УЗИ, справка медсправка для детей в
Самым большим преимуществом свободной пересадки лоскутов средней толщины является то, что большие участки кожных покровов могут быть пересажены без того, чтобы был причинен какой бы то ни было ущерб (функциональный или косметический) на месте донорской раны. Однако условием осуществления этого основного преимущества на практике является беспрепятственное заживление донорской раны, которое наиболее успешно обеспечивается соответствующим лечением при оставлении этой раны открытой.
Как правило, иссечение лоскута проводится при местном инфильтрационном обезболивании, которое выполняется от центра к периферии на основе принципов, проиллюстрированных на стр. 25.
В целях равномерного распределения обезболивающей жидкости и достижения равномерной поверхности по донорскому участку до тех пор похлопывают шпателем, пока он не становится гладким и не появляется слабое покраснение. Под действием похлопывания сосуды расширяются, что значительно улучшает условия реваскуляризации трансплантата.

Перед началом иссечения донорский участок смазывается физиологическим раствором поваренной соли или каким-нибудь маслом, чтобы он стал скользким.

После этого следует само иссечение трансплантата. Поверхность донорской раны — до окончания вмешательства на месте воспринимающего ложа — покрывается салфетками, смоченными в теплом физиологическом растворе поваренной соли, что способствует гемостазу.

В конце операции на поверхность донорской раны накладывается одинарный слой импрегнированной марли, по размерам соответствующей донорской ране, и уже в операционной, путем обдувания теплым воздухом начинают высушивать этот участок.
После возвращения больного в палату участок донорской раны иммобилизуется (конечность помещается на санки Брауна). Над донорским участком с помощью шин Крамера или специальных металлических конструкций создается защитная решетка. Эта решетка необходима для того, чтобы защитить открытую донорскую рану от прикосновения постельного белья.
Из засохшей на импрегнированном бинте крови за 24 часа образуется абсолютно сухая, твердая корка, через 2—3 дня она позволяет одеть на больного пижаму. В это время больной уже может вставать.
Образовавшаяся корка тесно спаивается с основанием раны, образуя прочное и в то же время гибкое защитное покрытие.
Раневая поверхность донорской раны эпителизуется прежде всего с краев. О развитии процесса эпителизации свидетельствует отслоение краев корки, которое наблюдается на 8—10 день после операции.
Поднявшиеся края корки следует ежедневно обрезать, чтобы они не могли, случайно зацепившись за белье больного, сорвать еще плотно прилегающие части и, возможно, вызвать кровотечение и даже привести к возникновению инфекции.
Для защиты еще плотно прилегающих участков корки и залеченных участков, покрывшихся тонким слоем нового эпителия, используется пластубол.

Спустя 10—14 дней после операции эпителизация заканчивается, корка окончательно отслаивается, об иссечении трансплантата на месте донорской раны свидетельствует лишь светлое пятно на коже.
Однако в некоторых случаях донорские раны приходится временно перевязывать (у больных, оперировавшихся под общим наркозом, у маленьких детей и пр.). В таких случаях через 24 часа после операции повязка снимается и начинается — как бы несколько отсроченное — лечение открытой раны по вышеописанному методу.

В медицинской практике, к сожалению, нередки случаи получения серьезных травм, при которых пересадка кожи на поврежденном участке необходима. Чтобы избежать осложнений после операции, за травмированным местом требуется особый уход и наблюдение у врача. Однако процесс реабилитации не всегда проходит гладко — после пересадки кожи может начаться образование рубцов. Как ухаживать за прооперированной раной, чтобы после полного заживления не осталось следов от несчастного случая? Читайте в этой статье.
Общая информация

Хирургическое вмешательство путем пересадки кожи называется дерматопластикой. Операцию назначают при лечении ожогов и ран большой площади пострадавшим любого возраста, а также в ряде других случаев:
- ожоги;
- раны, в том числе после хирургического вмешательства;
- диабетическая стопа, сопровождаемая язвенными дефектами, которые плохо поддаются консервативным методам лечения;
- операции, связанные с дефектами конечностей, а также слоновостью.
Кожная пластика противопоказана при повышенной температуре, инфицировании раны и при наличии декомпенсации соматических болезней. Материал для пересадки кожи может быть взят из 3 источников:
- кожа самого пациента или донора;
- кожный покров животных, после специальной подготовки;
- искусственные материалы из биологических полимеров и клеточных покрытий.
Материал подбирается исходя из клинических показаний и его доступности. По классификации операций дерматопластики выделяют следующие разновидности хирургического вмешательства:
Предполагает использование собственной кожи пациента. Проводится, если дефекты кожи занимают не более 35–50% от всего тела. Со здоровой части спины или ноги срезают тонкий слой кожного покрова и пересаживают его на травмированную область.
В этом способе особенно сложен процесс реабилитации. Согласно исследованиям, после устранения аутодермопластикой до 10% ожогов первой степени, от 55 до 62% ожогов второй степени и от 30 до 40% ожогов третьей степени развиваются келоидные и гипертрофические рубцы.
Именно они являются самыми проблемными и чувствительными из возможных шрамов, поскольку в процессе развития доставляют неудобство человеку: эстетически портят внешний вид, вызывают зуд, покраснение, повышенную температуру в месте травмы. А гипертрофический рубец со временем еще и разрастается в размерах, захватывая здоровые участки кожи.
Назначается, если поврежденная кожа составляет более 50% от всего тела или при наличии противопоказаний к проведению аутодермопластики. При этом используется донорский, животный или синтетический кожный покров.
Проводится в немногих медицинских центрах, имеющих крупные научные подразделения. Для операции используется биологический материал, взятый у самого больного.
По срокам проведения и реабилитации дерматопластику разделяют на первичную и вторичную. Первичная проводится при госпитализации пациента, не дожидаясь регенеративных процессов в дерме. Вторичная трансплантация проводится через неделю, когда начинает формироваться грануляционная ткань из незрелых соединительных тканей.
Кроме этого, в хирургии существуют понятия свободной и несвободной пересадки кожи. В первом случае лоскут кожи полностью переносят на поверхность раны, а во втором — участок кожи имеет питательную ножку, обеспечивающую лучший заживляющий эффект.
При тяжелых ожогах и обширной площади поражения необходимо обращение к комбустиологу. Этот врач занимается лечением сложных травм и тесно сотрудничает с рентгенологом, анестезиологом, трансплантологом и другими специалистами.
Комбустиологи используют следующие методы работы:
- Лечение под повязкой. Ожог обрабатывают антисептиком и назначенными медикаментами, накладывают повязку. Бинты должны быть стерильны, обязательно менять их каждый оговоренный промежуток времени.
- Терапия в безбактериальной среде. Пострадавший с открытыми ожогами находится в специальном стерильном боксе. Этот метод применяется в случаях, когда невозможно наложить повязку либо по причине больших площадей раны, либо ее трудной доступности (промежность, лицо).
- Некроэктомия и работа со струпом. Гнойники и мертвые клетки удаляются с помощью хирургического вмешательства.
- Пересадка кожи. Ее принято считать завершающим этапом терапии. Проводится при больших площадях поражения, когда естественная регенерация клеток невозможна.
Эксперт в области хирургии знает десятки операций по трансплантации кожи. Однако во всех случаях за прооперированной частью тела необходимо тщательно ухаживать, чтобы избежать возникновения раны после пересадки кожи.

Уход после пересадки кожи
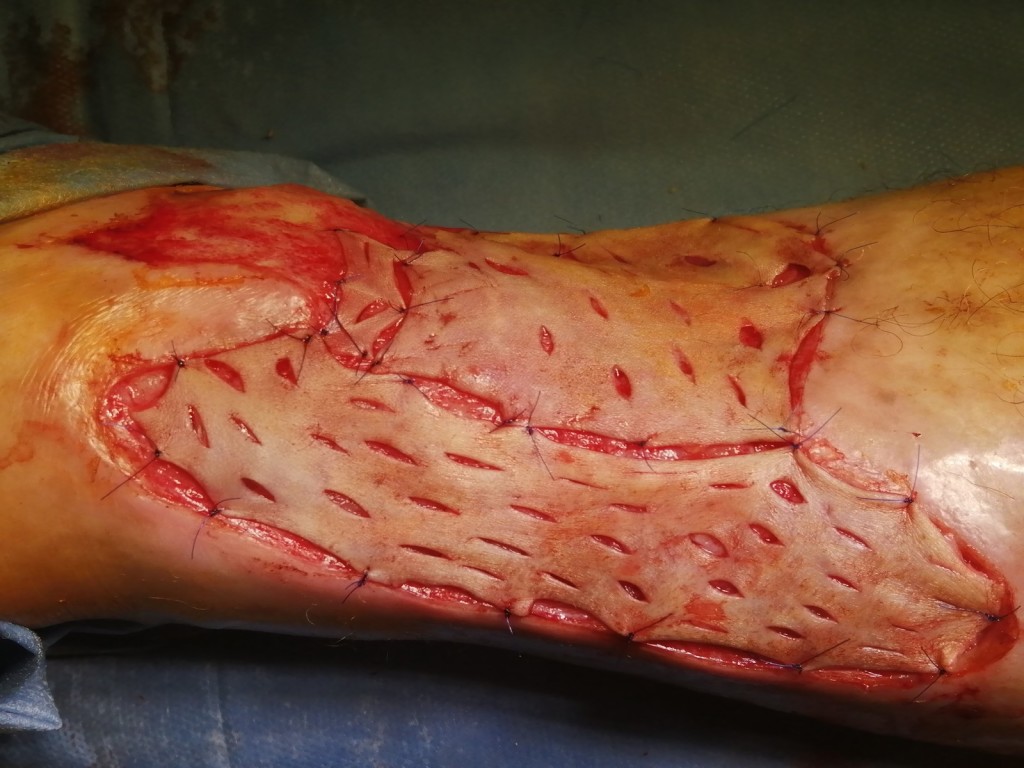
Скорость заживления после операции зависит от того, насколько точно вы будете следовать рекомендациям врача. Сам процесс регенерации проходит в три этапа:
- Адаптивные изменения в пересаженной коже. Инородный фрагмент адаптируется к новым условиям и начинает взаимодействовать с организмом. Этот процесс протекает за 2–3 дня.
- Период регенерации (заживления). Проходит полная адаптация пересаженной кожи, донорские клетки полностью заменяются на новые, синтезируются белки соединительной ткани. Процесс проходит за 3 месяца.
- Стабилизация. Восстанавливается нормальная структура кожи, пересаженные участки становятся идентичны «родной» коже. Этап проходит за 6–18 месяцев.
После проведения операции пересаженная кожа прирастает к телу за 7–10 дней. Менять повязку рекомендуется на 2–3 день, причем снимать старый бинт послойно: нижние слои прилипают к незажившей ране и при неосторожном движении есть риск ее открыть вновь. Далее повязку следует менять ежедневно при помощи медсестры или врача. Для ускоренного заживления и профилактики инфицирования рану обрабатывают антисептиками и делают аппликации медикаментозными препаратами, которые назначает врач. Помимо перевязок, существует ряд рекомендаций, которые следует соблюдать прооперированному пациенту:
- исключить термическое и механическое воздействие на поврежденную область — не носить колючую, синтетическую и ограничивающую движения одежду;
- не мочить прооперированное место, при соблюдении личной гигиены закрывать его полиэтиленом или другим водоотталкивающим материалом;
- не снимать самостоятельно повязку;
- пить много жидкости, для взрослого — порядка 2-2,5 л воды в сутки;
- исключить из рациона острые, соленые и копченые продукты, добавить витамины, макроэлементы и белковую пищу;
- отказаться от употребления алкоголя и курения.
После снятия повязки врач назначает обезболивающие препараты, а также противовоспалительные и противорубцовые средства. С этими задачами успешно справляется гель Ферменкол — уникальный ферментный комплекс природного происхождения на основе коллагеназы камчатского краба. Данный гель применяется для устранения гипертрофических и келоидных рубцов после операции, ожога, травмы, а также в комплексной терапии контрактур. Почему Ферменкол используется в качестве мази после пересадки кожи:
- обновляет кожу до 90%;
- охлаждает, снимает чувство стягивания и зуда;
- выравнивает рельеф, нормализует окраску, повышает эластичность кожи;
- не содержит гормонов, в составе только натуральные ингредиенты и зеленый консервант;
- можно применять во время беременности, лактации и детям с 0 лет;
- действует местно, не затрагивая интактные (здоровые) ткани.
Гель Ферменкол наносят аппликационно (мажут тонким слоем 2–3 раза в день на чистую сухую кожу) несколько раз в сутки. Это способствует формированию нормотрофического мягкого рубца, который исчезает самостоятельно спустя несколько месяцев. Курс применения в этом случае длится 30–40 дней.
Для достижения максимального эффекта специалисты рекомендуют совмещать Ферменкол с физиотерапией: электрофорез, фонофорез, микротоки. Если прооперированное место имеет большую площадь, специалисты могут назначить курс фонофореза с гелем Ферменкол (воздействие ультразвуком).
В случае застарелых грубых рубцов — электрофорез с набором Ферменкол (воздействие электрическим током). Физиотерапия с Ферменкол существенно ускоряет процесс обновления кожи за счет положительного воздействия самих процедур и более глубокого проникновения активных компонентов в дерму. Данный метод зарекомендовал себя более эффективно, чем аппликации (накожное применение).
Так, для прохождения курса электрофореза Ферменкол применяется в виде специального раствора, который можно приобрести как отдельно, так и в комплекте с портативным аппаратом для домашних процедур. Для курса фонофореза подойдет гель Ферменкол, его также возможно приобрести как отдельно, так и в комплекте с аппаратом для фонофореза, который пригодится в каждой домашней аптечке.
Какие могут быть осложнения при заживлении рубца после пересадки кожи
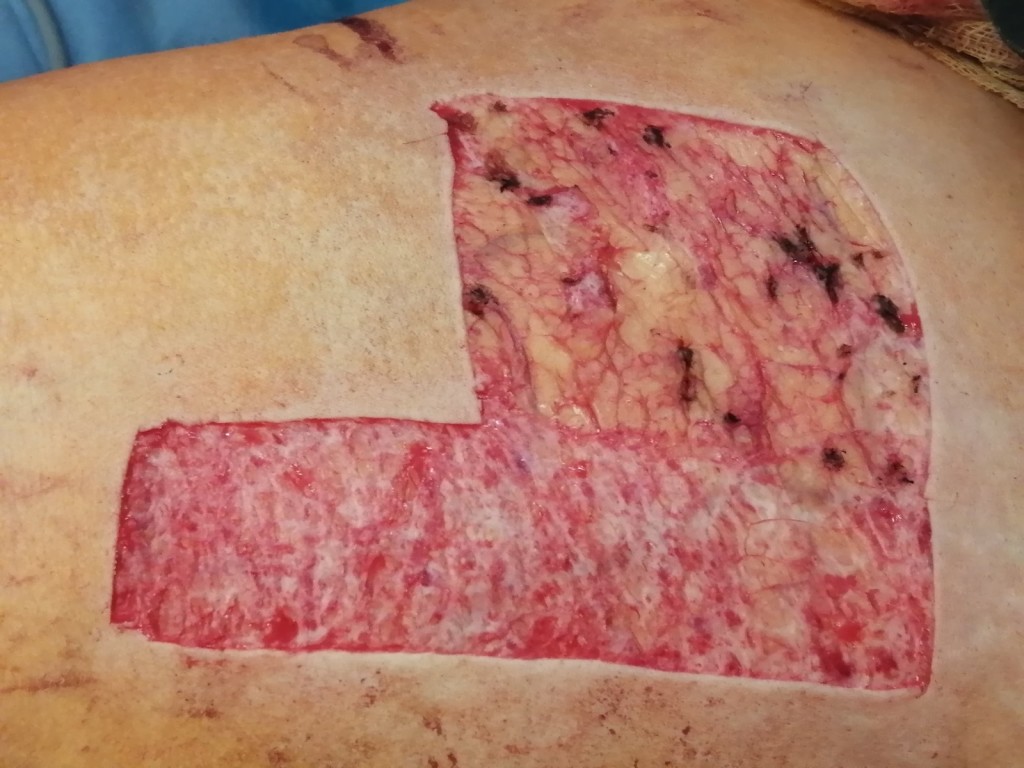
Если в реабилитационном периоде была занесена инфекция или рана подвергалась травмированию, возможно формирование грубого келоидного или гипертрофического рубца. Эти виды шрамов не исчезают самостоятельно, в случае с келоидным — наоборот, способны увеличиваться со временем, затрагивая здоровые соседние ткани.
Стоит учитывать, что у взрослых и у детей процесс развития шрамов протекает с разной скоростью. Детская кожа реактивно реагирует на ожоги 3А и 3Б степени бурным ростом послеожоговых рубцов, причем активный рост наблюдается даже на донорских участках. Если у взрослого человека рубцы созревают и начинают регрессировать в течение года, то у маленьких детей этот процесс может занять 2–3 года.
Применение Ферменкола при послеожоговых рубцах целесообразно, так как входящая в его состав коллагеназа избирательно разрушает избыточный патологический коллаген — основную составляющую рубцовой ткани. На сегодняшний день аналогов Ферменколу по силе проявления активности к патологическому коллагену не существует. При выборе способа коррекции следует учитывать множество факторов. Чтобы достичь максимального эффекта при коррекции именно послеожоговых рубцов, одного геля недостаточно. При таких рубцах детям показан электрофорез с набором для энзимной коррекции (2–3 курса по 10–15 процедур в год), а аппликации гелем Ферменкол показаны в перерывах между курсами физиопроцедур.
Также после пересадки новой кожи могут образоваться келоидные рубцы в области суставов, препятствующие нормальному функционированию конечности и способные привести к необратимым деформациям. Чем раньше начнется лечение, тем быстрее кожа приобретет эстетически приятный, здоровый вид! Купить продукцию Ферменкол вы можете на официальном сайте или в аптеке вашего города. Будьте здоровы!
ФГБОУ ВПО «Ульяновский государственный университет», Ульяновск, Россия;
ГУЗ «Центральная городская больница Ульяновска», Ульяновск, Россия
Ульяновский государственный университет, Ульяновск
Оценка местного лечения ран донорских мест у пациентов с глубокими ожогами
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(11): 49‑52
ФГБОУ ВПО «Ульяновский государственный университет», Ульяновск, Россия;
ГУЗ «Центральная городская больница Ульяновска», Ульяновск, Россия
Цель исследования — оценить влияние местного лечения ран донорских мест у обожженных на частоту развития осложнений и определить основные факторы риска осложнений со стороны ран донорских мест. Материал и методы. Выборку составили 486 пациентов с глубокими ожогами, которым выполнена свободная аутодермопластика расщепленными трансплантатами. В основной группе (n=56) лечение ран донорских мест осуществляли с помощью влагосберегающих повязок DDB-M. В контрольной группе (n=430) лечение проводили традиционным способом под однократно наложенными влажно-высыхающими марлевыми повязками. Результаты. В рамках исследования выявлена структура осложнений со стороны ран донорских мест, а также основные факторы риска нагноений.
ФГБОУ ВПО «Ульяновский государственный университет», Ульяновск, Россия;
ГУЗ «Центральная городская больница Ульяновска», Ульяновск, Россия
Ульяновский государственный университет, Ульяновск
Наиболее частым способом оперативного вмешательства при лечении глубоких ожогов является свободная аутодермопластика расщепленными трансплантатами [1—3], которая сопровождается образованием ран донорских мест. Традиционным способом местной терапии таких ран остается лечение под марлевыми влажно-высыхающими повязками с растворами антисептиков в сочетании с физическими методами высушивания раневой поверхности [4]. Срок их заживления, по данным разных авторов [5—8], варьирует от 7 до 26 дней и может осложняться нагноением раны и длительным ее заживлением в 5—70% случаев. Кроме того, при глубоких ожогах площадью 15% поверхности тела (ПТ) появляется дефицит донорских ресурсов аутокожи, при глубоких ожогах свыше 20% ПТ он становится выраженным [5, 9], поэтому важно быстрое и неосложненное заживление донорских ран. Среди факторов, способствующих развитию осложнений со стороны ран донорских мест, выделяют избыточную толщину трансплантата, тяжелое общее состояние пациента, нерациональную локализацию донорских мест, неправильное лечение, преклонный возраст [5]. Известен способ лечения ран донорских мест под пленочной полиэтиленовой повязкой DDB-M, заживление ран донорских мест при этом происходит в среднем через 6,3±1,2 сут без развития осложнений [10].
Цель исследования — оценить влияние местного лечения ран донорских мест у обожженных на частоту развития осложнений и определить факторы риска осложнений со стороны ран донорских мест.
Материал и методы
Проведено ретроспективное одноцентровое исследование медицинской документации взрослых пациентов с ожогами, находившихся на лечении в ожоговом отделении ГУЗ «Центральной городской клинической больницы» Ульяновска с 2011 по 2015 г. Критерии включения: пациенты старше 18 лет; пациенты с ожогами II—IIIАБ—IV степени (II—III степени по МКБ-10) с общей площадью поражения до 40% ПТ; пациенты, которым выполняли свободную аутодермопластику расщепленными трансплантатами. Критерии исключения: пациенты младше 18 лет; пациенты, переведенные в другие лечебные учреждения до момента заживления ран донорских мест; пациенты с ожогами II—IIIАБ—IV степени (II—III степени по МКБ-10) с общей площадью поражения более 40% ПТ; пациенты, которым не выполняли свободную аутодермопластику расщепленными трансплантатами. Из 780 пациентов с глубокими ожогами, пролеченных в 2011—2015 гг. в ожоговом отделении ГУЗ «ЦГКБ» Ульяновска, в исследование вошли 486 (63,8%) больных с глубокими ожогами, из них 308 (63,4%) мужчин, 178 (36,6%) женщин, средний возраст больных составил 53 (28; 77) года.
Формирование аутодермотрансплантатов у всех пациентов осуществляли электродерматомом ДЭ-60−01, толщина аутодермотрансплантатов составила 0,3—0,4 мм, ширина — до 60 мм. Для сравнения эффективности способов местного лечения ран донорских участков все пациенты, вошедшие в ретроспективное исследование, были разделены на две группы. В основной группе (n=56) после проведения интраоперационного гемостаза марлевыми салфетками с раствором адреналина 1:400 раны донорских мест закрывали пленочными повязками DDB-M. Повязки на ранах фиксировали к здоровым участками кожи и между собой полосками лейкопластыря, затем закрывали марлевыми салфетками и фиксировали турами бинта. Смену повязок проводили через 24—48 ч. Лечение заканчивали после полной эпителизации раны.
В контрольной группе (n=430) лечение осуществляли традиционным способом — под однократно наложенными влажно-высыхающими марлевыми повязками с раствором йодофоров (йодопирон, бетадин и др.) в сочетании с дополнительными методами физического высушивания ран с помощью тепловентиляторов, инфракрасной лампы, флюидизирующих кроватей Редактрон и Сатурн-90, согласно клиническим рекомендациям [4]. Наложению повязки с антисептиком предшествовал интраоперационный гемостаз марлевыми салфетками с раствором адреналина 1:400, как и в основной группе. При нагноении ран донорских участков проводили местное лечение с использованием марлевых повязок с мазями на водорастворимой основе (левомеколь, левосин, дермазин и др.), а также системную антибиотикотерапию с учетом чувствительности микрофлоры.

По данным статистического анализа, пациенты основной и контрольной групп были сопоставимы по всем анализируемым показателям (табл. 1). Таблица 1. Характеристика пациентов, вошедших в группы исследования, Ме (10%; 90%)
При анализе лабораторных данных особое внимание уделяли лейкоцитарному индексу интоксикации (ЛИИ) как объективному показателю степени выраженности воспаления и эндогенной интоксикации. ЛИИ в исследовании определяли по формуле Кальф—Калифа. Статистическую обработку данных проводили с помощью программы IBM SPSS Statistics 20. Анализ вида распределения данных выполняли с помощью теста Шапиро—Уилка. Меры центральной тенденции и дисперсии количественных признаков в случае нормального распределения признаков описывали средней арифметической и средним квадратическим отклонением (M±s), а в случае распределения отличного от нормального — медианой (Me) и 80% интерпроцентильным размахом (между 10-й и 90-й процентилями). Проверку статистических гипотез выполняли с применением критерия χ 2 , точного критерия Фишера, критерия U Манна—Уитни для независимых выборок, однофакторного дисперсионного анализа (ANOVA) с проверкой равенства дисперсий по критерию Ливена. Относительную силу взаимосвязи между факторами риска и исходами определяли с помощью регрессионного анализа как отношение шансов с 95% доверительным интервалом. Уровень статистической значимости при проверке статистических гипотез в данном исследовании принимался равным 0,01.
Результаты и обсуждение

В результате ретроспективного исследования выявлены основные виды осложнений ран донорских мест (табл. 2). Таблица 2. Структура и частота осложнений в группах исследования

ЛИИ у тяжелообожженных в основной и контрольной группах продемонстрировал статистически достоверные различия на 5-е сутки после операции (табл. 3), Таблица 3. Динамика лейкоцитарного индекса интоксикации в послеоперационном периоде у тяжелообожженных пациентов на 10-е сутки в основной группе он практически соответствовал норме в отличие от контрольной группы (p<0,0001), что свидетельствует об эффективности местного лечения пленочной влагосберегающей повязкой DDB-M.
В основной и контрольной группах статистически достоверных различий по частоте кровотечений из ран донорских мест не выявлено (p=0,431), что свидетельствует о низкой гемостатической эффективности обоих способов лечения ран донорских мест. Пленочная влагосберегающая повязка DDB-M, выполняя роль капиллярного дренажа, способствует выделению крови из-под повязки в послеоперационном периоде. Длительное заживление ран донорских мест наблюдалось у 10 (2,3%) пациентов контрольной группы, в основной группе таких случаев не отмечено, однако статистически достоверных различий между группами не выявлено (p=0,614). Тем не менее установлено статистически значимое различие (p<0,0001) по срокам заживления ран донорских мест — в основной группе раны заживали в среднем на 5 дней раньше. Так, в основной группе раны зажили через 7 (6; 9) сут, в контрольной — через 12 (9; 20,9) сут; U-критерий по тесту Манна—Уитни составил 1164.

У всех пациентов с длительным заживлением ран донорских мест отмечено их нагноение, однако статистический анализ показал, что нагноение ран не являлось достоверным предиктором длительного заживления ран донорских мест (χ 2 =9,206; p=0,02). Единственным статистически достоверным фактором длительного заживления было ожоговое истощение (χ 2 =10,696; p=0,01). Анализ данных литературы и результаты ретроспективного исследования позволили выявить основные факторы нагноения ран донорских мест: преклонный возраст, «неудобную» локализацию донорских мест, площадь ожога, традиционный способ лечения, наличие психических заболеваний различного генеза [5]. Оценка значимости номинальных факторов риска нагноения ран приведена в табл. 4. Таблица 4. Оценка значимости номинальных факторов риска нагноения ран

Статистический анализ показал, что среди номинальных факторов информационно значимыми факторами риска нагноения оказались «неудобная» локализация ран донорских мест, традиционный способ местного лечения, ожоговое истощение и психические заболевания различного генеза (p <0,0001). Последний фактор риска нагноения ран объяснялся тем, что у пациентов с психическими расстройствами сложно высушить рану донорского места, такие пациенты также часто снимают повязки и не выполняют рекомендации лечащего врача. Оценка количественных факторов риска приведена в табл. 5. Таблица 5. Оценка значимости количественных факторов риска нагноения
При изучении количественных факторов риска установлено, что такой параметр, как возраст пациентов, не превышал порога статистической значимости, т. е. не являлся предиктором нагноения. А такие факторы, как площадь поражения (p<0,0001), срок выполнения операции с момента травмы (p=0,001) и индекс Франка (p<0,0001), достоверно влияли на риск нагноения ран донорских мест.
Заключение
В структуре осложнений со стороны ран донорских мест преобладает нагноение (23,7%). Местное лечение ран донорских мест под пленочной повязкой DDB-M достоверно снижает риск возникновения нагноения, однако точных данных о влиянии данного способа на риск кровотечения из ран донорских мест и на вероятность их длительного заживления не получено.
Ретроспективное исследование показало, что прогностически значимыми факторами ослож-нений являются площадь поражения и, как следствие, «неудобная» локализация донорских мест, а также психические заболевания, ожоговое истощение, срок оперативного восстановления кожных покровов и традиционный способ местного лечения.
Читайте также:

