Чем лечить узловую эритему на ногах при беременности
Обновлено: 24.04.2024
Acosta K, Haver M, Kelly B. Etiology and Therapeutic Management of Erythema Nodosum During Pregnancy.
Этиология и лечение узловатой эритемы при беременности. Обновление
1. Введение
Узловатая эритема (УЭ) является наиболее распространенной формой панникулита. Она характеризуется острым началом эритематозными, нежными узлами в классических случаях с симметричной локализацией на разгибательных поверхностях нижних конечностей. Узлы округлые, слегка повышающиеся, 1-6 см в диаметре, иногда сливающиеся. Поражения могут иногда располагаться на лодыжках, бедерах, руках, лице, шее и туловище. Симптомы достигают максимума в 1-2 недель, а затем проходят сами через 1-6 недель, иногда сохраняются до 12 недель. Изъязвления узлов являются редкостью, и они разрешаются без рубцов, но могут оставлять гиперпигментацию (эритема contusiformis). Также могут наблюдаться системные симптомы, такие как лихорадка, озноб, недомогание, артралгии, а иногда и желудочно-кишечные симптомы.
Женщины болеют в 3-5 раз чаще чем мужчины. Хотя УЭ может возникнуть в любом возрасте, оно является наиболее распространенным в 3-4 десятилетии жизни. Развитие УЭ наблюдается при многих системных заболеваниях, и может зависеть от многих факторов, включая возраст, расу, пол, и географическое положение пациента. В 30-50% случаев УЭ причину установить не удается и устанавливается диагноз идиопатической УЭ. Идентифицируемые причины УЭ включают саркоидоз , инфекции, злокачественные опухоли, аутоиммунные заболевания, препараты и беременность. Типы инфекций разнообразны и включают вирусные инфекции, такие как гепатит С, вирус Эпштейна-Барра, грибковые инфекции, такие как гистоплазмоз, дерматомикозы, кокцидиоидомикоз, бластомикоз и бактериальные инфекции, включая туберкулез, иерсиниоз, кампилобактерии, сифилис и стрептококковую инфекцию.
Стрептококковая инфекция, как представляется, наиболее распространенная инфекционная причина и наиболее частая причина у детей. В одном из исследований наиболее распространенной причиной УЭ был признан саркоидоз, в то время как другие исследования указывали на инфекции, как наиболее частую причину. В редких случаях УЭ связана с беременностью и приемом оральных контрацептивов (КОК). Заболеваемость УЭ в связи с беременностью, как сообщается, встречаетсяв в 4,6 - 6% всех случаев.
Целью данной работы является изучение этиологии УЭ во время беременности и возможных вариантов, доступных для лечения. Поиск литературы (август 2012) проводили с использованием Овидия MEDLINE. В параметры поиска были включены узловатая эритема, беременность, лечение, этиология, оральные контрацептивы, кортикостероиды, НПВС, йодид калия, этанерцепт, инфликсимаб, гидроксихлорохин, ихтиол, колхицин и дапсон.
2. Диагностика
Клинических результатов зачастую достаточно для установления диагноза УЭ, но в некоторых случаях рекомендуется биопсия. УЭ дифференцируют с индуративной эритемой, узелковым периартериитом, сифилитическими гуммами, поверхностным тромбофлебитом, узловыми лепридами бактериальным целлюлитом, лимфомами и саркоидозом. Обследование направлено на исключение или уменьшение многочисленных причин УЭ. Необходим тщательный сбор анамнеза о всех последних заболеваниях.
Все пациенты должны пройти обследование с рентгеном грудной клетки и общеклиническими анализами. При назначении рентгенологического исследования грудной клетки у беременной пациентки важно учитывать воздействие ионизирующего излучения на плод.Рентгенография грудной клетки обеспечивает очень небольшое излучение радиации для плода, порядка 0.0007 Гр, и представляет минимальный тератогенный риск, особенно если область живота правильно защищена свинцовым фартуком. Могут быть обнаружены лейкоцитоз и повышенная скорость оседания эритроцитов.
Другие тесты, такие как посев из носоглотки, титры антистрептолизина, на сывороточный ангиотензин-превращающий фермент, внутрикожные тесты на туберкулез, кокцидиоидомикозом, бластомикоз, и гистоплазмоз назначаются по показаниям. Так как УЭ может быть связана с различными патологическими процессами, важно исключение их в первую очередь, и только после этого связывать УЭ с беременностью.
3. Этиология во время беременности
Этиология УЭ во время беременности не полностью понятна, но, по всей видимости, связана с иммунными механизмами, обусловленными гормональными изменениями, происходящими во время беременности. Эта ассоциация подтверждается тем фактом, что КОК были также связаны с развитием УЭ, и заболеваемость УЭ резко сократилась с введением низких доз гормональных таблеток в 1980-е годы. Однако, недавнее исследование показало, что гормоны были наиболее частыми препаратами, вызывающими УЭ и наиболее частой причиной всех случаев рецидивирующей УЭ. Кроме того, в недавнем докладе описали беременную женщину, у которой развилась УЭ при получении ежедневных внутримышечных инъекций прогестерона (для вспомогательной репродуктивной терапии) и впоследствии после отмены препарата наблюдалось разрешение панникулита. Эти авторы предполагают, что в будущем возможно увеличение частоты УЭ во время беременности, т.к. вспомогательная репродуктивная терапия становится все более популярной.
Давно замечено, что аутоиммунными заболеваниями чаще страдают женщины. Это указывает на роль половых гормонов в развитии этих заболеваний. Половые гормоны модулируют врожденную и адаптивную иммунную систему. Эстрогены, как было отмечено, перестраивают иммунную систему со сдвигом к Т-хелперам 2-го порядка, тем самым ухудшая болезненные процессы, которые вызваны циркулирующими антителами. Кроме того, эстрогены вызывают быстрое созревание В-клеток и способствуют лимфопоэзу в тканях за пределами костного мозга, что может привести к аутореактивности. В исследованиях на мышах эстрогены подавляют апоптоз аутореактивными В-клетками. Это может быть связано с тенденцией к развитию аутоиммунных заболеваний у женщин. Прогестерон, с другой стороны, оказывает более подавляющее действие на иммунную систему. Эффект митогенов на пролиферацию Т-клеток снижается от прогестерона, и прогестерон может быть ответственным за снижение иммунного ответа организма на развивающийся плод во время беременности.
Существуют доказательства , указывающие на роль иммунных комплексов при УЭ. Во-первых, прямая иммунофлюоресценция поражений показывает отложения иммуноглобулинов и комплемента в стенках пораженных сосудов. Повышение иммунных комплексов было обнаружено у пациентов с вторичной УЭ при туляремии, саркоидозе и туберкулезе. В одном из исследований УЭ сывороточные уровни комплемента были нарушены у 18 из 22 больных. Наиболее распространенным нарушением было присутствие C3i, который генерируется путем расщепления С3 сложной опосредованной активацией иммунной системы комплемента.
Иммунные комплексы, поэтому, вероятно присутствуют у большинства пациентов с УЭ. Это открытие может также объяснить сопровождающие УЭ симптомы артралгии, лихорадки и недомогание, которые похожи на сывороточную болезнь и другие болезни, вызванные циркулирующими иммунными комплексами. Неясно, как именно иммунные комплексы влияют на патогенез УЭ, но возможно, что они вызывают повреждение ткани путем активации системы комплемента и развития воспалительной клеточной инфильтрации тканей с выходом медиаторов воспаления.
Механические факторы также могут вносить свой ??вклад в развитие УЭ во время беременности таким же образом, как и механические / анатомические факторы могут способствовать возникновению УЭ исключительно на передней поверхности голеней. Некоторые авторы считают, что передняя поверхность голеней имеет относительно редкую артериальную сеть, а отеки ног во время беременности могут способствовать УЭ. Другие факторы, помимо женских половых гормонов должны играть определенную роль в развитии УЭ во время беременности, т.к. у некоторых женщин наблюдался только один эпизод УЭ несмотря на последующие беременности или воздействие КОК. Поэтому, половые гормоны, скорее всего играют косвенную роль в патогенезе УЭ, возможно, индуцируя условия, благоприятные для развития УЭ.
4. Лечение
УЭ является саморегрессирующим процессом и поэтому немедикаментозные методы лечения, такие как постельный режим и эластичные бинты могут быть достаточными для контроля симптомов. В тех случаях, когда УЭ является результатом основного заболевания, лечение их приводит к разрешению поражений. Аспирин, НПВС, йодид калия, а иногда и системные кортикостероиды, назначаются с целью устранения боли, и ускорения восстановления, но многие из этих препаратов противопоказаны при беременности. Другие лекарственные средства, такие как ингибиторы фактора некроза опухоли (TNF)-α, колхицин, и гидроксихлорохин относят к препаратам с доказанной эффективностью при лечении УЭ.
УЭ можно лечить раствором йодистого калия в дозе 900 мг в день в течение 2-4 недель. Точный механизм действия препарата неясен, но эффект связывают с увеличение выработки в организме гепарина, способствующего снижению реакции гиперчувствительности замедленного типа. Другое исследование показывает, что йодид калия ингибирует хемотаксис нейтрофилов, которые также могут модулировать иммунный ответ при УЭ. Йодистый калий у беременых относят к категории D по FDA США и он противопоказан во время беременности, особенно во втором и третьем триместрах, т.к. легко проникает через плаценту и может вызвать зоб или гипотиреоз плода и новорожденного.
Еще одним средством для лечения УЭ являются НПВП. Они снимают боль и уменьшают воспаление путем ингибирования циклооксигеназы, которая ингибирует выработку простагландинов. НПВП также снижают продукциюпровоспалительных цитокинов Т-клеток. Сообщается об эффективности при лечении УЭ оксифенбутазона в дозе 400 мг / день и индометацина по 100-150 мг / день, напроксена 1000 мг / день в течение 2-3 недель. Важно отметить, что эти пациенты не были беременными во время лечения.
НПВП у беременных относятся к категории C и, как правило, не рекомендуются в течение первого триместра в связи с возможностью тератогенных эффектов, таких как пороки сердца и других дефектов. Использование НПВС в течение третьего триместра беременности может привести к порокам сердца. Индометацин также был связан с некротическим энтероколитом, внутрижелудочковым кровоизлиянием, и бронхолегочной дисплазией. Кроме того, НПВП подавляют и пролонгируют беременность. Однако если выгода перевешивает риск, НПВП можно вводить при бдительном наблюдении за пациентом акушера-гинеколога. Патология почек, анемия, желудочно-кишечные кровотечения, и взаимодействие с другими препаратами может также являться относительным противопоказанием к назначению НПВП любому пациенту.
Кортикостероиды модулируют иммунную систему в широком спектре направлений на долгий срок путем связывания с внутриклеточными рецепторами, которые, за счет изменения экспрессии генов, уменьшают продукцию провоспалительных цитокинов, таких как интерлейкин-1 и интерлейкин-6, а также уменьшают активацию ядерного фактора-kB, который увеличивает апоптоз активированных клеток. С помощью этих механизмов кортикостероиды подавляют иммунную систему и уменьшают воспаление. Кортикостероиды при беременности относят к категории D в первом триместре и к категории С в течение второго и третьего триместров.
Системные кортикостероиды, такие как преднизолон, кажется, представляют риск развития орофациальных расщелин у плода, если их вводят в первом триместре, но они не считаются основным тератогенным риском. Системные кортикостероиды эффективно уменьшают развитие УЭ. УЭ во время беременности, как сообщается, можно успешно лечить системным введением преднизолона, а также дефлазакорта. Coaccioli и др. отметили, что ежедневные инъекции дефлазакорта были эффективными при УЭ в течение третьего триместра беременности в одном случае.
Инфликсимаб был эффективен у детей при лечении УЭ вызванной болезнью Крона. Важно понимать, что разрешение УЭ в этом случае не может быть непосредственно отнесено к инфликсимабу, так как есть вероятность того, что инфликсимаб подействовал на основной процесс- воспалительное заболевание кишечника, который затем привел в разрешению УЭ. Инфликсимаб при беременности относится к категории B и считается безопасным для использования во время беременности. Хотя есть ограниченные данные его воздействия на плод во время беременности, материнские пособия по всей видимости, существенно перевешивают риски для плода.
Хлорохин хорошо переносимый препарат с нескоторыми побочными эффектами, и, хотя не имеет разрешения FDA у беременных, было показано, что у женщин, принимающих этот препарат во время беременности не имеется повышенного риска неблагоприятных для плода эффектов. Сообщается об эффективном лечении случаев хронической УЭ гидроксихлорохином.
Внутриочаговое введение кортикостероидов, дапсон и ихтиоловые аппликации были предложены в качестве возможных вариантов лечения, но никакой информации относительно эффективности этих методов лечения в литературе найти не удалось. Внутриочаговое введение кортикостероидов может быть полезным непосредственным введением препарата в ткань, что позволяет избежать системной иммуносупрессии.
Возможные осложнения могут включать в месте инъекции реакции на препарат ввиде отека и эритемы. Дапсон, отнесенный при беременности к категории C, используется для профилактики малярии и некоторых дерматологических заболеваний, включая проказу. Использование дапсона во время беременности считается безопасным, поскольку он не оказывает заметной фетотоксичности и не вызывает врожденные дефекты.
Что такое узловатая эритема? Причины возникновения, диагностику и методы лечения разберем в статье доктора Загидулины Марии Валерьевны, дерматолога со стажем в 13 лет.
Над статьей доктора Загидулины Марии Валерьевны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Узловатая эритема — это воспаление подкожно-жировой клетчатки, которое сопровождается появлением болезненных пальпируемых подкожных узелков красного или фиолетового цвета. Чаще всего они появляются на голенях, иногда в других областях.
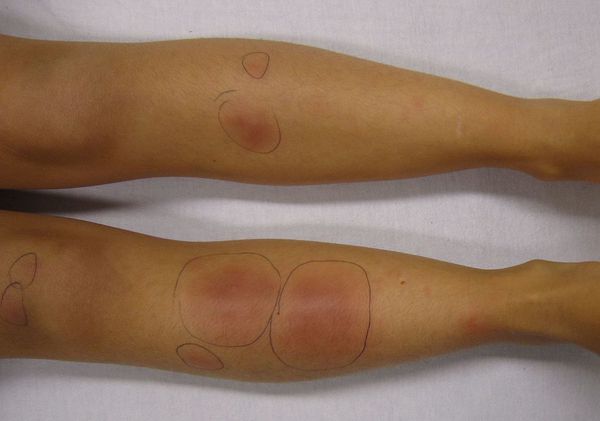
Это заболевание обусловлено повышенной иммунной реакцией организма на возбудителя [1] [3] . Несмотря на многочисленные исследования данной патологии, причины возникновения узловатой эритемы и механизм её развития изучены недостаточно. Однако существует теория о том, что основной причиной узловатой эритемы могут быть различные инфекционные заболевания.
Таблица 1. Причины узловатой эритемы.
К факторам риска появления узловатой эритемы относятся грибковые заболевания, воспалительные заболевания желудочно-кишечного тракта, нарушения гормонального фона, туберкулёз, приём различных лекарственных средств [2]
Важную роль играют провоцирующие факторы, такие как смена климата, переходное время года, стрессы, перепады температуры (переохлаждение), варикоз нижних конечностей и др. Заболевание имеет сезонность, обычно появляется ранней весной и поздней осенью, что обусловлено частыми простудными заболеваниями, ангинами, снижением иммунитета.
Заболеваемость узловатой эритемой в разных странах может варьировать от 1 до 5 случаев на 100 000 населения в год [12] . Это зависит от распространённости болезней, которые могут вызвать узловатую эритему, в конкретной местности. В основном узловатая эритема выявляется у людей 20-30 лет [2] [12] . Именно в этом возрасте человек впервые встречается со многими инфекциями.
Женщины, которые имеют ген HLA В8, более подвержены возникновению узловатой эритемы, что может подтверждать факт наследственной предрасположенности к данному заболеванию [4] . HLA (Human Leukocyte Antigen — человеческий антиген лейкоцитов) отвечает за распознавание чужеродных клеток и активацию иммунного ответа на них. При запуске этого механизма мы видим клиническую картину воспаления, причиной которого является реакция иммунной системы.
Известно, что HLA В8 располагает к нескольким группам заболеваний, в том числе к узловатой эритеме. И так запрограммировано, что чаще он встречается у женщин [11] . Именно поэтому женщины болеют гораздо чаще, чем мужчины (примерно в 3-6 раз) [12] . Если не брать в расчёт изменение генома, то узловатая эритема встречается пропорционально одинаково у мужчин и женщин, так как стрептококковой инфекции и другим заболеваниям они подвержены одинаково.
Узловатая эритема чаще выявляется у населения Европы, в частности в Скандинавии, при этом у азиатов её диагностируют редко, так как ген HLA B8 у них почти не встречается [11] [13] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы узловатой эритемы
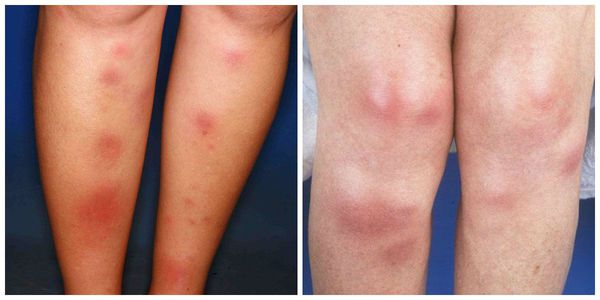
Узелки могут сливаться между собой, образуя красные уплотнения. В редких случаях они распространяются на кожу бёдер, задней поверхности рук, шеи и даже лица [6] . Узлы прощупываются нечётко, так как вокруг них имеется отёк [7] . По центру узлы имеют возвышение. Как правило, на 3-10 день узлы становятся плотными и болезненными, поэтому их часто принимают за абсцессы. Но уже на 10-14 день они постепенно размягчаются и спадают.
На 10-14 день узлы из красных превращаются в синие или сине-багровые, что визуально напоминает обычный синяк. Вся клиническая картина держится примерно 14-20 дней, после этого кожа на месте узлов и вокруг них начинает шелушиться [9] . Такой симптом довольно характерен для узловатой эритемы, что позволяет диагностировать её и на поздних стадиях. Язв не возникает, что также является диагностически важным признаком при постановке диагноза. Параллельно могут беспокоить боли в суставах и мышцах.
На месте узлов, как правило, ничего не остаётся, они исчезают бесследно. Повторное возникновение узловатой эритемы наблюдается нечасто [6] .
Для детей характерно более лёгкое течение болезни, узлов обычно немного. Боли в суставах бывают редко [7] .
Патогенез узловатой эритемы
Кожа — это показатель здоровья всего организма, поэтому любые изменения должны направлять врача и пациента на поиск их причины.
Узловатая эритема начинается с того, что бактерии, вирусы или другие агенты попадают в организм. Они могут проникнуть извне или из очага инфекции, который находится в организме, например в кишечнике, миндалинах и т. д. В ответ на их внедрение срабатывает иммунная система, начинают вырабатываться антитела — белки, которые связываются с антигенами (возбудителями), маркируют их или нейтрализуют самостоятельно. Комплексы, состоящие из антител и антигенов, называются циркулирующими иммунными комплексами (ЦИК). С током крови ЦИК разносятся по организму и задерживаются в различных органах и тканях. В том числе иммунные комплексы оседают в подкожно-жировой клетчатке, стенках сосудов и вокруг венул, находящихся в соединительнотканных перегородках подкожной клетчатки .
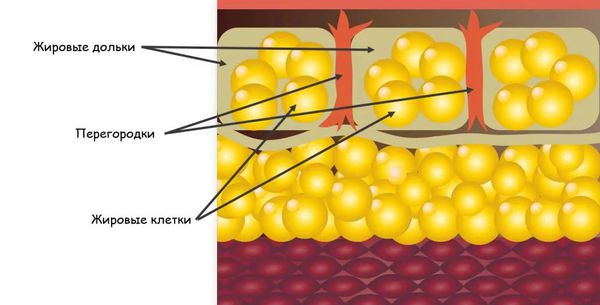
В результате возникает избыточная иммунная реакция местного характера, которая характеризуется воспалением и повреждением тканей. Это приводит к образованию узлов на коже.
Сочетание воспалительного процесса с расширением сосудов обусловливает красное окрашивание узлов в первые дни заболевания, а изменения в подкожно-жировой клетчатке приводит к образованию узлов, которые прощупываются под кожей [4] . По некоторым источникам инфекционные агенты параллельно могут вызывать развитие васкулита (воспаления стенок сосудов), что усугубляет течение узловатой эритемы [5] .
Можно сделать вывод, что большую роль в процессе развития узловатой эритемы играет чрезмерный иммунный ответ организма на внедрение инфекции, вируса или другого возбудителя. Как это происходит, до сих пор до конца не изучено. И почему организм реагирует так бурно, тоже точно неизвестно.
Классификация и стадии развития узловатой эритемы
По возникновению узловатая эритема бывает двух видов::
- Первичная (идиопатическая) — узловатая эритема протекает самостоятельно, без наличия других заболеваний.
- Вторичная — есть основное заболевание, на фоне которого возникла узловатая эритема.
Таблица 2. Узловатая эритема по течению и клиническим проявлениям.
Заболевание проходит три стадии:
Осложнения узловатой эритемы
Осложнения узловатой эритемы напрямую связаны с основным заболеванием. Нужно отметить, что и сама узловатая эритема является следствием запущенного процесса в организме.
Опасность острой узловатой эритемы заключается в её переходе в хроническую форму, так как при рецидивирующем характере заболевания возможно тяжёлое течение.
В единичных случаях осложнением патологии у детей может быть поражения глаз. В основном речь идёт о патологии переднего отрезка глаза: эписклерит (воспаление соединительного слоя между склерой и конъюнктивой), пигментная эпителиопатия (снижение остроты зрения вследствие появления множественных очагов сероватого или беловатого цвета) [9] .
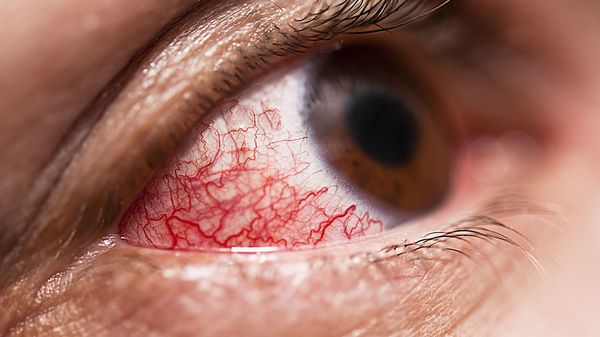
Диагностика узловатой эритемы
Диагностика узловатой эритемы начинается со сбора анамнеза. При этом необходимо учитывать:
- чем болел пациент в последнее время, не было ли заболевания, которое могло спровоцировать узловатую эритему.
- приём лекарственных препаратов;
- наследственность;
- заболевания печени, поджелудочной железы;
- поездки в другие страны, смена климата и т. д.
Минимальный перечень лабораторных исследований:
- Общий анализ крови. Как правило, показывает повышение скорости оседания эритроцитов (СОЭ), что отображает картину воспаления. Лейкоциты чаще остаются в пределах нормы.
- Биохимический анализ крови: печёночные ферменты (АЛТ, АСТ), амилаза, липаза, трипсин, ферритин. Печень является индикатором очищения организма, изменения показателей печени показывают нарушение процессов в организме.
- Иммунологическое обследование:
- С-реактивный белок (СРБ) — белок острой фазы воспаления, повышается при развитии узловатой эритемы и при некоторых других заболеваниях. Одним из первых повышается в крови, говорит об общем процессе воспаления, не является специфичным, а лишь направляет врача в диагностике заболевания.
- Антистрептолизин О (АСЛ-О). Повышение этого показателя говорит о наличии стрептококковой инфекции в организме, в частности гемолитического стрептококка, который вызывает ангины, тонзиллит, фарингит и другие инфекции, которые могут спровоцировать развитие узловатой эритемы. Увеличение АСЛ-О в крови можно увидеть через неделю от начала заболевания (например ангины). Для достоверности анализ сдают двукратно, с интервалом 2-4 недели. Если уровень значительно повышен, это подтверждает причину возникновения узловатой эритемы
Для исключения воспалительного процесса в организме выполняют следующие исследования:
- Внутрикожный туберкулиновый тест. Реакция манту выполняется всем для исключения туберкулёза [7] .
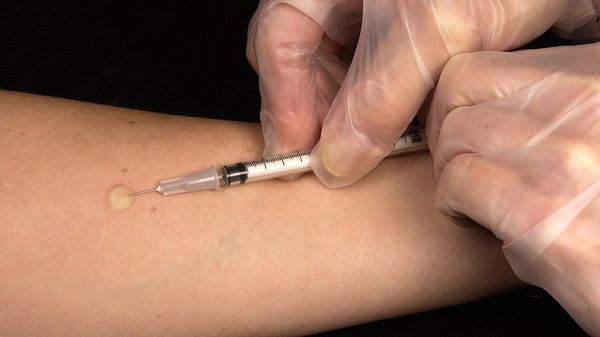
- Рентгенограмма или компьютерная томография органов грудной клетки. Данное обследование зависит от жалоб, от клиники, оснащения больницы др. В некоторых случаях могут провести рентгенограмму, а затем при необходимости компьютерную томографию. В других случаях сразу выполняют КТ внутренних органов для исключения и\или выявления саркоидоза [8] .
- Биопсия узла (редко). Гистологический анализ показывает наличие или отсутствие характерных клеток для узловатой эритемы в материале [7] .
Дифференциальная диагностика проводится со следующими заболеваниями:
- кольцевидная эритема;
- клещевая мигрирующая эритема;
- эритема Базена;
- гранулематозный саркоидоз;
- ревматологические заболевания;
- рожа;
- узелковый полиартериит;
- спонтанный панникулит;
- синдром Свита [7] .
Лечение узловатой эритемы
Как будет проходить лечение, амбулаторно или стационарно, зависит от жалоб пациента, клинической картины и тяжести заболевания.
Показания к госпитализации:
- Неэффективное амбулаторное лечение.
- Ухудшение клинической картины, распространённость кожного процесса, его усиление.
- Наличие основного заболевания, которое обострилось и ухудшает самочувствие пациента [7] .
В остальных случаях лечение и необходимое дообследование проводят в амбулаторных условиях.
Лечение включает в себя:
- Постельный режим. Он необходим, так как долгое хождение или сидение вызывает у пациента выраженную отёчность ног, которая усиливается, при этом нарастает боль в ногах. В связи с этим рекомендуется по возможности держать ноги в приподнятом положении, а при значительном дискомфорте бинтовать их обычными или эластическими бинтами или носить эластические чулки [8] .
- Лекарственная терапия. Обычно проводится симптоматическое лечение, либо лечение, зависящее от основного заболевания, при его выявлении. Может включать:
- Для обезболивания — НПВС (нестероидные противовоспалительные средства).
- Одновременно назначаются сосудистые препараты ( пентоксифиллин ) для улучшения микроциркуляции, что способствует более быстрому разрешению процесса.
- В случаях с выраженным отёчным синдромом к лечению добавляют мочегонные препараты.
- При необходимости назначают антибактериальные, противовирусные препараты [7] .
- В условиях стационара включают инфузионную терапию.
- Назначаются витамины, препараты кальция для поддержания иммунитета и снижения реактивности организма.
- Местно на узлы применяют:
- раствор диметилсульфоксида 33 % (аппликации);
- НПВС мази и гели;
- клобетазола дипропионат 0,05 % (мазь);
- ангиопротекторы для улучшения микроциркуляции ( "Троксевазин") .
- Физиотерапевтические методы : электрофорез, фонофорез с гидрокортизоном 1 % (мазь) на узлы [7] .
При хроническом течении терапия направлена большей частью на лечение основного заболевания. Оно проводится по клиническим общепринятым рекомендациям. Следует разобраться в причине возникновения узловатой эритемы, выявить возбудителя, тогда врач сможет назначить лечение, которое будет направлено на профилактику рецидивов. В следующие 2-3 месяца после окончания терапии пациентам нужно беречь своё здоровье, так как процесс снова может активироваться.
Учитывая инфекционную природу заболевания, важным направлением в исследованиях, посвящённых узловатой эритеме, является разработка различных схем и методов антиинфекционной терапии в комплексном лечении рассматриваемой патологии [10] .
Прогноз. Профилактика
Прогноз для жизни при узловатой эритеме в большинстве случаев благоприятный. Как правило, при остром течении заболевание резко возникает и так же резко исчезает без последствий для организма. Рецидивы заболевания возникают редко. Иногда они наблюдаются при узловатой эритеме, связанной со стрептококковыми или нестрептококковыми инфекциями верхнего респираторного тракта. В некоторых случаях хроническое течение возможно у пациентов с заболеваниями сердечно-сосудистой системы [8] . В этом случае прогноз полностью зависит от особенностей заболевания, сил организма и эффективности лечения.
С целью профилактики узловатой эритемы при возникновении ангин, гайморитов и герпетических инфекций нужно обязательно обращаться к врачу, делать анализы для выявления возбудителя, проходить терапию, специфичную для данного возбудителя. Так можно обезопасить себя от возникновения узловатой эритемы и многих других процессов.
Профилактика рецидивов в первую очередь направлена на полноценное лечение основного заболевания, также важно избегать провоцирующих факторов. После основного лечения следует наблюдаться у дерматолога и необходимых специалистов, продолжать лечение с профилактической целью и проходить полное клиническое обследование до нормализации показателей анализов.
Рекомендуется защищаться от простудных заболеваний, повышать иммунитет, для этого сбалансированно питаться, заниматься физической активностью, особенно в течение года после болезни. При плохом самочувствии или ОРВИ обращаться к своему лечащему врачу для предотвращения рецидива. Врачам следует аккуратно назначать вакцинации и новые лекарственные средства [3] .
Что такое многоформная экссудативная эритема (МЭЭ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Фоминых Софьи Юрьевны, дерматолога со стажем в 23 года.
Над статьей доктора Фоминых Софьи Юрьевны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Многоформная экссудативная эритема (МЭЭ) — это острое аллергическое заболевание, при котором на коже и слизистых оболочках появляются различные по виду высыпания — пятнистые, папулёзные и пузырные.
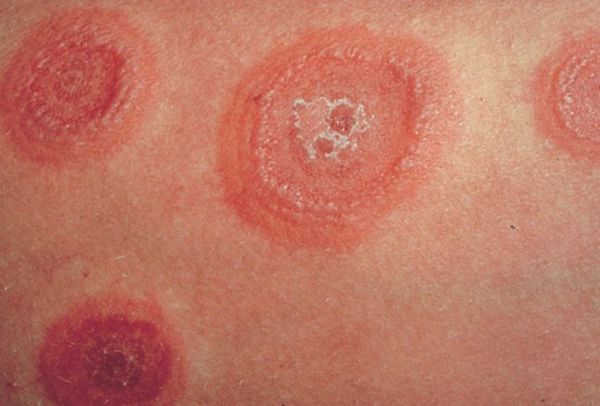
МЭЭ обычно болеют люди молодого и среднего возраста. У пациентов мужского пола это заболевание встречается несколько чаще, чем у женщин.
Известны две основные разновидности МЭЭ:
- инфекционно-аллергическая (идиопатическая или истинная) — составляет около 80 % всех случаев МЭЭ и является следствием аллергической реакции на хронический очаг инфекции в организме;
- токсико-аллергическая — развивается, как правило, на фоне применения некоторых лекарственных средств, таких как амидопирин, барбитураты, сульфаниламиды и тетрациклины [7] .
Для инфекционно-аллергической МЭЭ характерна весенне-осенняя сезонность. Одного очага хронической инфекции недостаточно, чтобы данное заболевание развилось или обострилось. Для этого необходимо определённое сочетание триггерных, т. е. провоцирующих факторов, например:
- иммунодефицит (обратимый, преходящий, циклический);
- переохлаждение;
- ультрафиолетовое облучение;
- некоторые консерванты в составе пищевых продуктов (бензоаты, формальдегид и т. д.);
- психоэмоциональный стресс;
- патология пищеварительного тракта (хронический гастрит, дисбактериоз);
- аутоиммунные заболевания и онкопатология; , ангина и другие заболевания.
Не исключается и наличие наследственной предрасположенности к ММЭ.
Причиной инфекционно-аллергической МЭЭ, которая приводит к развитию болезни, чаще всего является герпесвирус человека, вирус Эпштейна — Барр, цитомегаловирус, а также возбудители вирусных гепатитов, микобактерии, микоплазменная, стрептококковая и грибковые инфекции, паразиты. Наиболее распространённый вид инфекционно-аллергической МЭЭ — герпес-ассоциированная МЭЭ [4] [12] [13] .
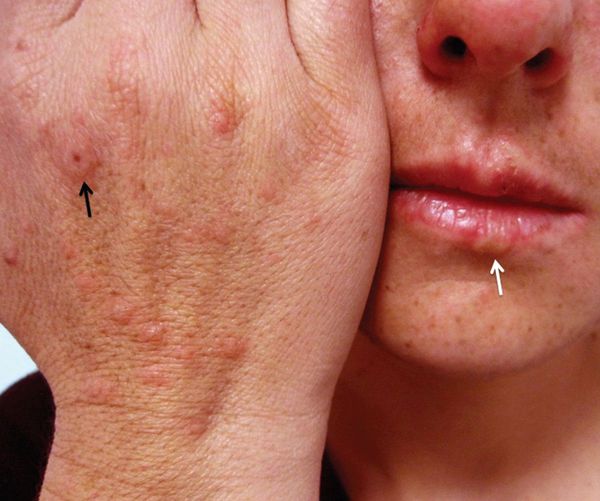
Считается, что герпесвирусная инфекция [1] [2] [5] становится причиной подавляющего большинства случаев МЭЭ. Чаще всего обнаруживается связь с вирусом простого герпеса первого типа [8] [10] [11] , реже — второго.
В пользу инфекционно-аллергической формы МЭЭ свидетельствует наличие продромального периода (предшествующего болезни), склонности к сезонности высыпаний и хроническое рецидивирующее течение.
Эксперты ВОЗ отмечают, что рост заболеваемости простым герпесом в настоящий момент заставляет рассматривать его в числе первоочередных проблем, наряду с ВИЧ-инфекцией и гриппом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы многоформной экссудативной эритемы
Для инфекционно-аллергической МЭЭ, включая герпес-ассоциированную [13] , характерно острое начало заболевания. Оно может проявляться повышением температуры, общей слабостью, ломотой в теле, головной болью, болезненными ощущениями в горле и другими симптомами.
Нередко за несколько дней до обострения МЭЭ у пациентов активируется герпетическая инфекция — проявляется герпес на губах или возникает рецидив генитального герпеса [8] .
Высыпания, характерные для МЭЭ, обычно начинают появляться через 1-2 дня после начала продромальных явлений. При этом общие симптомы обычно идут на спад.
Локализация сыпи весьма разнообразна. Она может появиться как на коже, так и на слизистых оболочках.
Кожные проявления
На коже обычно отмечаются чётко очерченные округлые красно-розовые пятна и плоские отёчные папулы, которые увеличиваются в размерах от 2-3 мм до 3 см в диаметре. При инфекционно-аллергической форме пятна обычно несколько мельче и не склонны к слиянию. Они могут доставлять зуд и жжение.
Преимущественная локализация высыпаний — на разгибательной стороне рук и ног, тыльной стороне стоп и кистей, на лице и в области гениталий. В основном они располагаются на теле симметрично, часто группами в виде дуг, гирлянд.
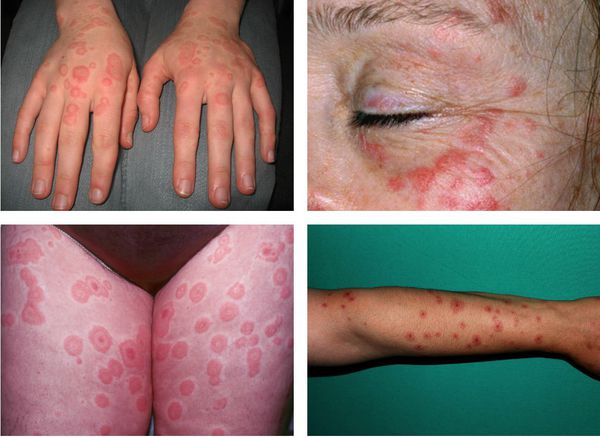
По мере роста папулы её центр начинает западать и менять окраску на более синюшную, по периферии остаётся красно-розовый ободок — таким образом элементы сыпи приобретают характерный вид "мишени" (иногда их сравнивают с "бычьим глазом" или "кокардой") [4] .
После в их центре образуются пузыри — везикулы и буллёзные элементы. Они содержат серозный или кровянистый экссудат. Лопаясь, пузыри формируют желтоватые или коричнево-бурые корочки, эрозированные поверхности.
В итоге на теле пациента одновременно присутствуют элементы разной степени развития — пятна, папулы и пузыри, переходящие в корочки и эрозии. Именно поэтому эритема именуется многоформной.
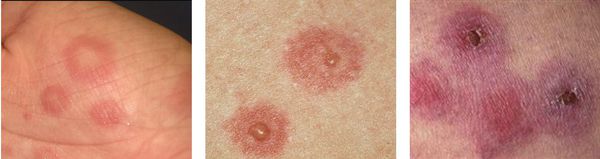
С интервалами в несколько дней могут образовываться новые группы высыпаний. Это может затянуть процесс. Но обычно окончательный регресс наступает приблизительно в течение двух недель.
Частота обострений может варьировать от 1-2 до 5-12 раз в год. В редких тяжёлых случаях одно обострение может переходить в другое, практически без светлого промежутка. За это время предыдущие высыпания полностью не разрешаются.
Высыпания на слизистых оболочках
Могут появляться единичные элементы на слизистой полости рта, который не причиняют особого беспокойства. В более тяжёлых случаях поражения бывают настолько обширными и болезненными. Они затрудняют речь и приём даже однородной и жидкой пищи [12] [13] .
Образующиеся пузыри лопаются довольно быстро, поэтому пациент не успевает их заметить — обычно обнаруживаются уже эрозии, на которых иногда можно увидеть плёнчатые фибринозные налёты светлого или бурого оттенка.
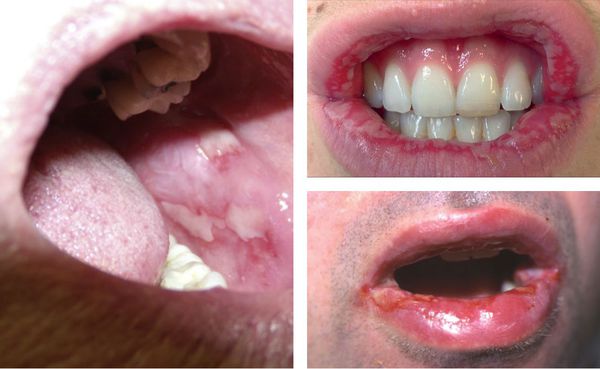
В области красной каймы губ могут возникнуть весьма болезненные, растрескивающиеся кровянистые корки, которые не позволяют больному полноценно открывать рот.
Реже высыпания обнаруживаются на слизистых глаз и половых органов. В осложнённых случаях возможно присоединение вторичной инфекции, образование рубцов и синехий (спаек).
Патогенез многоформной экссудативной эритемы
На современном этапе любая разновидность мультиформной экссудативной эритемы рассматривается как сдвиг адаптации защитных механизмов в сторону гиперчувствительности [4] .
МЭЭ — это смешанная аллергическая реакция, в которой просматриваются особенности, характерные для гиперчувствительности как немедленного, так и замедленного типа. Зачастую у пациента явно прослеживается так называемая общая атопическая предрасположенность — исходно у него могут отмечаться, к примеру, признаки пищевой аллергии, атопический ринит, бронхиальная астма и дерматит.
При герпес-ассоциированной МЭЭ у пациентов резко повышается уровень иммуноглобулинов класса Е (IgE) и снижается продукция иммуноглобулинов класса А (IgA), которые обеспечивают "первую линию" защиты кожи и слизистых оболочек. Также отмечается понижение выработки альфа- и гамма-интерферона и образование циркулирующих иммунных комплексов с вирусом простого герпеса.
Вирус повреждает генетический аппарат не только клеток эпидермиса, но и иммунокомпетентных клеток, изменяет состояние их рецепторов, выработку специфических ферментов и провоспалительных цитокинов. В то же время может наблюдаться Т-клеточный и нейтрофильный иммунодефицит, повышение количества В-лимфоцитов. Всё это нарушает связь между различными звеньями иммунитета, искажает нормальный иммунный ответ, заставляет организм проявлять агрессию к собственным тканям, в данном случае — к клеткам эпидермиса и эндотелия сосудов кожи.
Всё вышеперечисленное приводит к образованию лимфоцитарного инфильтрата вокруг кровеносных сосудов кожи, иногда с признаками геморрагии. В базальном слое эпидермиса развивается внутри- и внеклеточный отёк. Сам слой расслаивается, в нём возникают некротические изменения с образованием толстостенных булл.
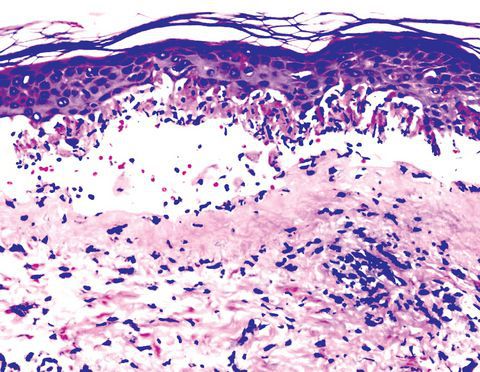
Степень тяжести патологических проявлений при герпес-ассоциированной МЭЭ во многом зависит от выраженности имеющихся иммунных сдвигов, которые, в свою очередь, могут являться причиной наличия хронического инфекционного очага в организме.
Классификация и стадии развития многоформной экссудативной эритемы
В зависимости от степени выраженности симптомов [3] [12] выделяют две формы МЭЭ:
- малая — поражений слизистых нет или они очень слабо выражены, почти нет общих симптомов;
- большая — протекает с тяжёлым поражением слизистых оболочек, ярко выраженными общими симптомами.
По первичным элементам сыпи, преобладающим в клинической картине МЭЭ, различают пять форм заболевания:
- эритематозная — ограниченное покраснение кожи;
- папулёзная — появление красноватых плотных узелков;
- эритематозно-папулёзная — образование папул с ярко-красными краями и потемневшим центом;
- везикуло-буллёзная — формирование эритематозных бляшек с пузырьком в центре;
- буллёзная — превращение пузырьков в эрозии, которые покрываются корочками.
Воспалительный процесс в зависимости от гистопатологической картины поражения кожи разделяют на три типа [3] :
- эпидермальное воспаление — нарушается наружный слой кожи;
- дермальное воспаление — изменяется толстый слой кожи под эпидермисом;
- смешанное (эпидермо-дермальное) воспаление.
По степени тяжести МЭЭ может быть лёгкой, средней, среднетяжёлой и тяжёлой. В качестве критериев тяжести рассматривают количество и размер буллёзных элементов, наличие поражений слизистых оболочек полости рта и гениталий, температуру тела. Отдельно выделяют часто рецидивирующую форму.
Общепринятой классификации герпес-ассоциированной МЭЭ в настоящее время не существует. В её развитии, как и в развитии МЭЭ, различают два периода:
- продромальный — период активации вирусного процесса;
- буллёзный — период разгара заболевания.
Осложнения многоформной экссудативной эритемы
Осложнения чаще всего развиваются при тяжёлых формах заболевания, а также у людей, организм которых по различным причинам ослаблен [12] [13] .
При обширных поражениях слизистой полости рта резкая болезненность высыпаний затрудняет нормальный гигиенический уход. Когда во рту изначально присутствовали очаги инфекции, возможно развитие такого осложнения, как фузоспирохетоз. Это стоматологическое заболевание характеризуется образованием толстого желтоватого дурно пахнущего налёта на слизистой полости рта, языке и зубах.
Затруднённый приём пищи при генерализованном поражении слизистой полости рта может приводить к истощению пациента.
При локализации высыпаний на слизистой носа возможно развитие ринита с носовыми кровотечениями.
Эрозии на слизистой половых органов могут заживать с образованием синехий (спаек, сращений).
В 22% случаев через эрозивные дефекты покровов проникает вторичная бактериальная инфекция. Это чревато гнойно-септическими осложнениями, образованием более глубоких поражений, на месте которых в редких случаях могут образовываться рубцы.
Поражение слизистой оболочки глаз может осложняться конъюнктивитом и кератитом (кератоконъюнктивитом) [3] .
К числу редких и наиболее серьёзных осложнений можно также отнести постгерпетическую невралгию, пневмонию, почечную недостаточность.
Диагностика многоформной экссудативной эритемы
Для постановки диагноза "МЭЭ" в типичном случае врачу-дерматологу достаточно характерной клинической картины и данных опроса пациента. Имеют значение сведения о хронических очагах инфекции, недавних рецидивах герпетических высыпаний и провоцирующих факторах.
Лабораторные анализы (например, общий анализ крови) в нетяжёлых случаях могут не показать никаких отклонений. При тяжёлых формах отмечается повышение СОЭ и умеренный лейкоцитоз — небольшое повышение уровня лимфоцитов в крови.
Для уточнения диагноза нужно исключить другие, схожие по симптоматике заболевания — пузырчатку, узловатую эритему, системную красную волчанку, вторичный сифилис и другие. С этой целью выполняют цитологическое исследование мазков-отпечатков, взятых с поверхности высыпаний, а также изучение клеток поражённой ткани под микроскопом.
Наличие герпетической инфекции в организме при необходимости можно подтвердить несколькими способами:
- ПЦР-диагностика на инфекции, передающиеся половым путём;
- серологическое обследование на наличие антител к вирусу простого герпеса;
- оценка иммунного статуса.
Дифференциальную диагностику герпес-ассоциированной МЭЭ необходимо проводить с узловатой и кольцевидной эритемой Дарье, токсидермиями, вторичным сифилисом, системной красной волчанкой, герпетическим стоматитом, болезнью Кавасаки, уртикарным васкулитом, красным плоским лишаем (эрозивной формой).
Лечение многоформной экссудативной эритемы
Основные задачи лечения:
- уменьшить тяжесть общих проявлений и количество высыпаний во время обострений;
- сократить длительность рецидивов;
- предотвратить осложнения;
- в межрецидивный период повысить сопротивляемость организма, сократить частоту рецидивов.
При любой форме МЭЭ используют десенсибилизирующую терапию и антигистаминные (противоаллергические) препараты.
При поражении слизистых оболочек рта и половых органов назначаются орошения и полоскания составами, успокаивающими воспаление и подавляющими инфекцию — "Ротокан", настой ромашки и т. п.
Ускорить очищение эрозий от налётов и некротических тканей помогают местные ферментные препараты. Также применяются кератопластические средства и препараты, способствующие регенерации и ускорению эпителизации повреждений.
Показаниями для госпитализации может послужить тяжёлое течение заболевания, а также неэффективность амбулаторного лечения. В нетяжёлых случаях вполне допустимо лечение в домашних условиях, без особых ограничений.
Изоляции больного не требуется, так как он не представляет опасности для здоровья окружающих. Пациенту рекомендуется гипоаллергенная диета, химически и термически щадящая, гомогенная пища (особенно при высыпаниях на слизистой рта), пить достаточное количество воды.
Лечение герпес-ассоциированной МЭЭ
Тактика лечения при герпес-ассоциированной МЭЭ зависит от степени выраженности тех или иных симптомов, стадии развития процесса, частоты и тяжести обострений [3] [4] . Например, если рецидивы возникают часто, высыпания обильны и им характерны некротические изменения, то нередко применяются глюкокортикоиды [14] .
Когда в возникновении заболевания очевидна роль герпесвируса, показан приём синтетических ациклических нуклеозидов — ацикловир, валацикловир [14] , фамцикловир.
В случае торпидного (вялого) течения герпес-ассоциированной МЭЭ рекомендовано профилактическое, противорецидивное и превентивное (предупреждающее) лечение. Для этого длительными курсами применяют препараты, содержащие ацикловир.
Применение антибиотиков в лечении герпес-ассоциированной МЭЭ оправдано лишь при наличии признаков вторичной бактериальной инфекции — нарастание интоксикации и появление гнойного отделяемого.
Чтобы предупредить присоединение вторичной инфекции, эрозированные участки и пузыри обрабатывают растворами антисептиков, например, фукорцином, фурацилином или хлоргексидином.
Прогноз. Профилактика
В большинстве случаев МЭЭ прогноз для жизни и здоровья благоприятный, за исключением редких особо тяжёлых форм болезни у людей с пониженной резистентностью организма.
Рубцы при заживлении повреждений не образуются, за редким исключением. Иногда на месте бывших элементов сыпи изменяется окрас кожи.
Рецидивировать МЭЭ может приблизительно в 30 % случаев. Особое внимание следует уделять тяжёлым поражениям слизистой оболочки и бактериальной суперинфекции [15] .
В качестве первичной профилактики рекомендуется минимизировать риск заражения герпетической инфекцией:
- соблюдать нормы личной гигиены;
- избегать случайных половых связей;
- практиковать защищённый секс.
Чтобы сохранить сопротивляемость организма инфекциям в норме, нужно рационально питаться, соблюдать оптимальный режим труда и отдыха, полноценно спать, регулярно закаляться, отказаться от вредных пристрастий.
Меры неспецифической вторичной профилактики формируются с учётом возможных триггерных факторов. Целесообразно обратить внимание на следующие моменты:
- регулярное прохождение профилактических осмотров и своевременная санация (очищение) хронических очагов инфекции, при ассоциации с герпесвирусной инфекцией — противовирусная терапия;
- защита от избыточного облучения солнечным светом и ультрафиолетового облучения;
- уменьшение вероятности переохлаждения;
- исключение стрессовых воздействий и т. п.
Для предупреждения рецидивов герпес-ассоциированной МЭЭ применяется герпетическая поливакцина, которая вводится по особой схеме. Её эффективность достигает более 70 %: она в 2-4 раза уменьшает частоту рецидивов.
Сокращению числа рецидивов также способствует длительный превентивный приём синтетических ациклических нуклеозидов, препаратов интерферона [6] , его индукторов и целого ряда неспецифических иммуномодуляторов [9] .
Acosta K, Haver M, Kelly B. Etiology and Therapeutic Management of Erythema Nodosum During Pregnancy.
Этиология и лечение узловатой эритемы при беременности. Обновление
1. Введение
Узловатая эритема (УЭ) является наиболее распространенной формой панникулита. Она характеризуется острым началом эритематозными, нежными узлами в классических случаях с симметричной локализацией на разгибательных поверхностях нижних конечностей. Узлы округлые, слегка повышающиеся, 1-6 см в диаметре, иногда сливающиеся. Поражения могут иногда располагаться на лодыжках, бедерах, руках, лице, шее и туловище. Симптомы достигают максимума в 1-2 недель, а затем проходят сами через 1-6 недель, иногда сохраняются до 12 недель. Изъязвления узлов являются редкостью, и они разрешаются без рубцов, но могут оставлять гиперпигментацию (эритема contusiformis). Также могут наблюдаться системные симптомы, такие как лихорадка, озноб, недомогание, артралгии, а иногда и желудочно-кишечные симптомы.
Женщины болеют в 3-5 раз чаще чем мужчины. Хотя УЭ может возникнуть в любом возрасте, оно является наиболее распространенным в 3-4 десятилетии жизни. Развитие УЭ наблюдается при многих системных заболеваниях, и может зависеть от многих факторов, включая возраст, расу, пол, и географическое положение пациента. В 30-50% случаев УЭ причину установить не удается и устанавливается диагноз идиопатической УЭ. Идентифицируемые причины УЭ включают саркоидоз , инфекции, злокачественные опухоли, аутоиммунные заболевания, препараты и беременность. Типы инфекций разнообразны и включают вирусные инфекции, такие как гепатит С, вирус Эпштейна-Барра, грибковые инфекции, такие как гистоплазмоз, дерматомикозы, кокцидиоидомикоз, бластомикоз и бактериальные инфекции, включая туберкулез, иерсиниоз, кампилобактерии, сифилис и стрептококковую инфекцию.
Стрептококковая инфекция, как представляется, наиболее распространенная инфекционная причина и наиболее частая причина у детей. В одном из исследований наиболее распространенной причиной УЭ был признан саркоидоз, в то время как другие исследования указывали на инфекции, как наиболее частую причину. В редких случаях УЭ связана с беременностью и приемом оральных контрацептивов (КОК). Заболеваемость УЭ в связи с беременностью, как сообщается, встречаетсяв в 4,6 - 6% всех случаев.
Целью данной работы является изучение этиологии УЭ во время беременности и возможных вариантов, доступных для лечения. Поиск литературы (август 2012) проводили с использованием Овидия MEDLINE. В параметры поиска были включены узловатая эритема, беременность, лечение, этиология, оральные контрацептивы, кортикостероиды, НПВС, йодид калия, этанерцепт, инфликсимаб, гидроксихлорохин, ихтиол, колхицин и дапсон.
2. Диагностика
Клинических результатов зачастую достаточно для установления диагноза УЭ, но в некоторых случаях рекомендуется биопсия. УЭ дифференцируют с индуративной эритемой, узелковым периартериитом, сифилитическими гуммами, поверхностным тромбофлебитом, узловыми лепридами бактериальным целлюлитом, лимфомами и саркоидозом. Обследование направлено на исключение или уменьшение многочисленных причин УЭ. Необходим тщательный сбор анамнеза о всех последних заболеваниях.
Все пациенты должны пройти обследование с рентгеном грудной клетки и общеклиническими анализами. При назначении рентгенологического исследования грудной клетки у беременной пациентки важно учитывать воздействие ионизирующего излучения на плод.Рентгенография грудной клетки обеспечивает очень небольшое излучение радиации для плода, порядка 0.0007 Гр, и представляет минимальный тератогенный риск, особенно если область живота правильно защищена свинцовым фартуком. Могут быть обнаружены лейкоцитоз и повышенная скорость оседания эритроцитов.
Другие тесты, такие как посев из носоглотки, титры антистрептолизина, на сывороточный ангиотензин-превращающий фермент, внутрикожные тесты на туберкулез, кокцидиоидомикозом, бластомикоз, и гистоплазмоз назначаются по показаниям. Так как УЭ может быть связана с различными патологическими процессами, важно исключение их в первую очередь, и только после этого связывать УЭ с беременностью.
3. Этиология во время беременности
Этиология УЭ во время беременности не полностью понятна, но, по всей видимости, связана с иммунными механизмами, обусловленными гормональными изменениями, происходящими во время беременности. Эта ассоциация подтверждается тем фактом, что КОК были также связаны с развитием УЭ, и заболеваемость УЭ резко сократилась с введением низких доз гормональных таблеток в 1980-е годы. Однако, недавнее исследование показало, что гормоны были наиболее частыми препаратами, вызывающими УЭ и наиболее частой причиной всех случаев рецидивирующей УЭ. Кроме того, в недавнем докладе описали беременную женщину, у которой развилась УЭ при получении ежедневных внутримышечных инъекций прогестерона (для вспомогательной репродуктивной терапии) и впоследствии после отмены препарата наблюдалось разрешение панникулита. Эти авторы предполагают, что в будущем возможно увеличение частоты УЭ во время беременности, т.к. вспомогательная репродуктивная терапия становится все более популярной.
Давно замечено, что аутоиммунными заболеваниями чаще страдают женщины. Это указывает на роль половых гормонов в развитии этих заболеваний. Половые гормоны модулируют врожденную и адаптивную иммунную систему. Эстрогены, как было отмечено, перестраивают иммунную систему со сдвигом к Т-хелперам 2-го порядка, тем самым ухудшая болезненные процессы, которые вызваны циркулирующими антителами. Кроме того, эстрогены вызывают быстрое созревание В-клеток и способствуют лимфопоэзу в тканях за пределами костного мозга, что может привести к аутореактивности. В исследованиях на мышах эстрогены подавляют апоптоз аутореактивными В-клетками. Это может быть связано с тенденцией к развитию аутоиммунных заболеваний у женщин. Прогестерон, с другой стороны, оказывает более подавляющее действие на иммунную систему. Эффект митогенов на пролиферацию Т-клеток снижается от прогестерона, и прогестерон может быть ответственным за снижение иммунного ответа организма на развивающийся плод во время беременности.
Существуют доказательства , указывающие на роль иммунных комплексов при УЭ. Во-первых, прямая иммунофлюоресценция поражений показывает отложения иммуноглобулинов и комплемента в стенках пораженных сосудов. Повышение иммунных комплексов было обнаружено у пациентов с вторичной УЭ при туляремии, саркоидозе и туберкулезе. В одном из исследований УЭ сывороточные уровни комплемента были нарушены у 18 из 22 больных. Наиболее распространенным нарушением было присутствие C3i, который генерируется путем расщепления С3 сложной опосредованной активацией иммунной системы комплемента.
Иммунные комплексы, поэтому, вероятно присутствуют у большинства пациентов с УЭ. Это открытие может также объяснить сопровождающие УЭ симптомы артралгии, лихорадки и недомогание, которые похожи на сывороточную болезнь и другие болезни, вызванные циркулирующими иммунными комплексами. Неясно, как именно иммунные комплексы влияют на патогенез УЭ, но возможно, что они вызывают повреждение ткани путем активации системы комплемента и развития воспалительной клеточной инфильтрации тканей с выходом медиаторов воспаления.
Механические факторы также могут вносить свой ??вклад в развитие УЭ во время беременности таким же образом, как и механические / анатомические факторы могут способствовать возникновению УЭ исключительно на передней поверхности голеней. Некоторые авторы считают, что передняя поверхность голеней имеет относительно редкую артериальную сеть, а отеки ног во время беременности могут способствовать УЭ. Другие факторы, помимо женских половых гормонов должны играть определенную роль в развитии УЭ во время беременности, т.к. у некоторых женщин наблюдался только один эпизод УЭ несмотря на последующие беременности или воздействие КОК. Поэтому, половые гормоны, скорее всего играют косвенную роль в патогенезе УЭ, возможно, индуцируя условия, благоприятные для развития УЭ.
4. Лечение
УЭ является саморегрессирующим процессом и поэтому немедикаментозные методы лечения, такие как постельный режим и эластичные бинты могут быть достаточными для контроля симптомов. В тех случаях, когда УЭ является результатом основного заболевания, лечение их приводит к разрешению поражений. Аспирин, НПВС, йодид калия, а иногда и системные кортикостероиды, назначаются с целью устранения боли, и ускорения восстановления, но многие из этих препаратов противопоказаны при беременности. Другие лекарственные средства, такие как ингибиторы фактора некроза опухоли (TNF)-α, колхицин, и гидроксихлорохин относят к препаратам с доказанной эффективностью при лечении УЭ.
УЭ можно лечить раствором йодистого калия в дозе 900 мг в день в течение 2-4 недель. Точный механизм действия препарата неясен, но эффект связывают с увеличение выработки в организме гепарина, способствующего снижению реакции гиперчувствительности замедленного типа. Другое исследование показывает, что йодид калия ингибирует хемотаксис нейтрофилов, которые также могут модулировать иммунный ответ при УЭ. Йодистый калий у беременых относят к категории D по FDA США и он противопоказан во время беременности, особенно во втором и третьем триместрах, т.к. легко проникает через плаценту и может вызвать зоб или гипотиреоз плода и новорожденного.
Еще одним средством для лечения УЭ являются НПВП. Они снимают боль и уменьшают воспаление путем ингибирования циклооксигеназы, которая ингибирует выработку простагландинов. НПВП также снижают продукциюпровоспалительных цитокинов Т-клеток. Сообщается об эффективности при лечении УЭ оксифенбутазона в дозе 400 мг / день и индометацина по 100-150 мг / день, напроксена 1000 мг / день в течение 2-3 недель. Важно отметить, что эти пациенты не были беременными во время лечения.
НПВП у беременных относятся к категории C и, как правило, не рекомендуются в течение первого триместра в связи с возможностью тератогенных эффектов, таких как пороки сердца и других дефектов. Использование НПВС в течение третьего триместра беременности может привести к порокам сердца. Индометацин также был связан с некротическим энтероколитом, внутрижелудочковым кровоизлиянием, и бронхолегочной дисплазией. Кроме того, НПВП подавляют и пролонгируют беременность. Однако если выгода перевешивает риск, НПВП можно вводить при бдительном наблюдении за пациентом акушера-гинеколога. Патология почек, анемия, желудочно-кишечные кровотечения, и взаимодействие с другими препаратами может также являться относительным противопоказанием к назначению НПВП любому пациенту.
Кортикостероиды модулируют иммунную систему в широком спектре направлений на долгий срок путем связывания с внутриклеточными рецепторами, которые, за счет изменения экспрессии генов, уменьшают продукцию провоспалительных цитокинов, таких как интерлейкин-1 и интерлейкин-6, а также уменьшают активацию ядерного фактора-kB, который увеличивает апоптоз активированных клеток. С помощью этих механизмов кортикостероиды подавляют иммунную систему и уменьшают воспаление. Кортикостероиды при беременности относят к категории D в первом триместре и к категории С в течение второго и третьего триместров.
Системные кортикостероиды, такие как преднизолон, кажется, представляют риск развития орофациальных расщелин у плода, если их вводят в первом триместре, но они не считаются основным тератогенным риском. Системные кортикостероиды эффективно уменьшают развитие УЭ. УЭ во время беременности, как сообщается, можно успешно лечить системным введением преднизолона, а также дефлазакорта. Coaccioli и др. отметили, что ежедневные инъекции дефлазакорта были эффективными при УЭ в течение третьего триместра беременности в одном случае.
Инфликсимаб был эффективен у детей при лечении УЭ вызванной болезнью Крона. Важно понимать, что разрешение УЭ в этом случае не может быть непосредственно отнесено к инфликсимабу, так как есть вероятность того, что инфликсимаб подействовал на основной процесс- воспалительное заболевание кишечника, который затем привел в разрешению УЭ. Инфликсимаб при беременности относится к категории B и считается безопасным для использования во время беременности. Хотя есть ограниченные данные его воздействия на плод во время беременности, материнские пособия по всей видимости, существенно перевешивают риски для плода.
Хлорохин хорошо переносимый препарат с нескоторыми побочными эффектами, и, хотя не имеет разрешения FDA у беременных, было показано, что у женщин, принимающих этот препарат во время беременности не имеется повышенного риска неблагоприятных для плода эффектов. Сообщается об эффективном лечении случаев хронической УЭ гидроксихлорохином.
Внутриочаговое введение кортикостероидов, дапсон и ихтиоловые аппликации были предложены в качестве возможных вариантов лечения, но никакой информации относительно эффективности этих методов лечения в литературе найти не удалось. Внутриочаговое введение кортикостероидов может быть полезным непосредственным введением препарата в ткань, что позволяет избежать системной иммуносупрессии.
Возможные осложнения могут включать в месте инъекции реакции на препарат ввиде отека и эритемы. Дапсон, отнесенный при беременности к категории C, используется для профилактики малярии и некоторых дерматологических заболеваний, включая проказу. Использование дапсона во время беременности считается безопасным, поскольку он не оказывает заметной фетотоксичности и не вызывает врожденные дефекты.
Читайте также:

