Чем лечить ожог от фарматекса
Обновлено: 24.04.2024
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Произведено и расфасовано:
Упаковка и выпускающий контроль качества:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Фарматекс
Суппозитории вагинальные белого цвета, цилиндрической формы с конусообразным концом.
| 1 супп. | |
| бензалкония хлорида 50% водный раствор | 37.8 мг, |
| что соответствует содержанию бензалкония хлорида | 18.9 мг |
Вспомогательные вещества: гипролоза - 9.1 мг, жир твердый Witepsol S 51 - 1553.1 мг.
5 шт. - блистеры (1) - пачки картонные.
5 шт. - блистеры (2) - пачки картонные.
Фармакологическое действие
Антисептик со спермицидным действием. Является четвертичным аммониевым соединением, относится к катионовым сурфактантам.
Спермицидное действие обусловлено способностью активного вещества разрушать мембраны сперматозоидов (сначала жгутиков, затем головок), что приводит к невозможности оплодотворения яйцеклетки поврежденным сперматозоидом.
Эффект развивается через 5-10 мин после введения во влагалище.
Не влияет на нормальную микрофлору влагалища и на менструальный цикл.
In vitro бензалкония хлорид активен в отношении Neisseria gonorrhoeae, Chlamydia spp., Trichomonas vaginalis, Herpes simplex типа 2, Staphylococcus aureus. Мало активен в отношении Gardnerella vaginalis, Candida albicans, Haemophilus ducreyi и Treponema pallidum. Не активен в отношении Mycoplasma spp.
Фармакокинетика
Бензалкония хлорид не всасывается в слизистую оболочку влагалища, удаляется простым промыванием водой и с нормальными физиологическими выделениями. При местном применении практически не всасывается.
«МЕДЛАЙН Экспресс», №5(173), май, 2004, стр. 23-25.
К.М. Ломоносов, О.Л. Иванов.
Кафедра кожных и венерических болезней ММА им. И.М. Сеченова, Москва.
Любая перенесенная инфекция, передающаяся половым путем (гонорея, трихомониаз, хламидиоз, уреаплазмоз), равно как и другие экзогенные факторы часто приводят к нарушению местного гомеостаза влагалища. В результате нарушения гуморальных факторов (системы комплемента, лизоцима, опсининов, фибронектина, бета-лизина и др.) в комплексе с клеточными факторами (макрофагами, полиморфноядерными лейкоцитами, Т-лимфоцитами) и элементами местного иммунитета (IgA-антитела) происходит нарушение защитных барьеров, обеспечивающих динамическое равновесие между макроорганизмом и нормальной микрофлорой, что приводит к развитию часто рецидивирующих бактериальных вагинозов эндогенного происхождения [4, 6, 7].
Проводимые во время обострения бактериального вагиноза лечебные мероприятия приводят лишь к временному улучшению. К сожалению, они не способны предотвратить рецидивы вагиноза. Все это заставляет искать новые средства, способные не только воздействовать на активно пролиферирующие условно-патогенные микроорганизмы, но и на факторы, предрасполагающие к этим состояниям.
Учитывая имеющиеся данные о способности препарата Фарматекс восстанавливать местный иммунитет после перенесенных ИППП [2], мы провели изучение течения бактериального вагиноза у женщин, регулярно использующих Фарматекс в качестве контрацептивного средства.
Препарат Фарматекс выпускается компанией «Лаборатория Иннотек Интернасиональ» (Франция) в виде вагинальных свечей, его действующим веществом является хлористый бензалконий. Общее название хлористого соединения - диметил-алкил-бензил-аммония-хлористый бензалконий. Хлористый бензалконий был открыт в 1937 году и представляет собой смесь различных хлористых соединений бензалкония, содержащих бензольное ароматическое кольцо и боковую цепь от С8 до С18. Хлористый бензалконий является катионным веществом, изменяющим поверхностное натяжение клеточной мембраны, и при введении во влагалище покрывает слизистую поверхность, образуя пленку. В течение нескольких секунд он иммобилизует сперматозоиды, разрушает их клеточную мембрану и вызывает коагуляцию цервикальной слизи. Поэтому основное показание к его применению - местная контрацепция для женщин репродуктивного возраста. Цепь С14, содержащаяся в хлористом бензалконии, обладает также выраженным бактерицидным действием за счет содержания углерода. Проведенные многочисленные исследования препарата in vitro показали его активность в отношении Neisseria gonorrhoeae, Chlamydia spp., Trichomonas vaginalis, Staphylococcus aureus, вируса герпеса 2-го типа [3, 5].
Материалом для данного исследования послужили наблюдения за 55-ю женщинами, страдающими часто возникающим (не реже 1 раза в 1-3 месяца) неспецифическим бактериальным и/или кандидозным вагинозом.
Возраст пациенток варьировал от 18 до 41 года, в среднем 28,3 ± 1,2 лет. Причем наибольшее количество пациенток наблюдалось в возрастной группе от 26-ти до 35-ти лет, т.е. они находились в наиболее трудоспособном и репродуктивном периоде.
Жалобы пациенток были в основном однотипными и заключались в появлении, часто без видимых причин, необильных рецидивирующих выделений из влагалища (лейкоррея), нередко со зловонным запахом, которые могли исчезать произвольно с течением времени или требовали проведения местных лечебных процедур. Часть пациенток отмечало небольшой зуд в области влагалища.
Таким образом, у всех женщин в анамнезе были жалобы, указывающие на бактериальный вагиноз.
Длительность данного состояния варьировала от полугода до 5-ти лет. У всех пациенток обострения случались 1 раз в 1-3 месяца, в среднем - 1 раз в 2 месяца.
Часто возникновение выделений большинство пациенток связывало с перенесенными инфекциями, передаваемыми половым путем, - 21 (38,2%) (4 - после перенесенной гонореи, 8 - после урогенитального хламидиоза, 5 - трихомониаза, 3 - уреаплазмоза, 1 - генитального герпеса). У 9-ти (16,4%) пациенток выделения возникали без видимых причин. Распределение пациенток в зависимости от причин возникновения выделений представлено в таблице 1.
Таблица 1
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ РЕЦИДИВИРУЮЩИХ ВЫДЕЛЕНИЙ
| Причины | Всего (%) |
| ИППП | 21 (38,2%) |
| Искусственное прерывание беременности | 5 (9,1%) |
| Роды | 7 (12,7%) |
| Пневмония | 1 (1,8%) |
| Гнойный аппендицит | 1 (1,8%) |
| Хронический тонзиллит | 1 (1,8%) |
| Цистит | 1 (1,8%) |
| ОРВИ | 2 (3,6%) |
| Перемена климата (смена места жительства) | 1 (1,8%) |
| Частая смена половых партнеров | 6 (10,9%) |
| Без видимых причин | 9 (16,4%) |
На момент обращения к нам все пациентки были в фазе ремиссии. При осмотре лишь у 4-х (7,3%) имелась небольшая гиперемия влагалища.
Всем пациенткам проводилось комплексное клинико-лабораторное обследование, включавшее бактериоскопию материала из уретры, цервикального канала и заднего свода влагалища; бактериологическое исследование микрофлоры влагалища (с определением титра в исследуемом материале микроорганизмов семейства Entherobacteriaceae, Streptococcaceae, Staphylococceae) и на кандидозы; исследование местного иммунитета цервикальной слизи, поскольку шейка матки является основным барьером защиты, которая синтезирует факторы специфического и неспецифического иммунитета. При исследовании местного иммунитета определяли 11 белков цервикального секрета: иммуноглобулины G, М, A, sIgA, комплемент С3, С4, орсомукоид, трансферрин, фибриноген, лизоцим, иммунные комплексы (ИК). Концентрацию IgA, IgM, IgG и sIgA определяли методом радиальной иммунодиффузии в 1,5%-ном геле арагозы по Манчини.
Уровень компонентов комплемента определяли методом молекулярного тестирования путем добавления к цервикальной слизи реагента, который представлял собой комплемент сыворотки человека, истощенный по испытуемому компоненту и, таким образом, лимитирующий активацию комплемента на уровне собственного компонента исследуемой цервикальной слизи. Концентрацию компонентов комплемента учитывали на фотометре «Labsystems Multiskan MS».
Лизоцим, орсомукоид, трансферрин и фибриноген определяли нефелометрическим методом по О.В. Бухарину, основанным на способности ферментов лизировать клеточную культуру Micrococcus Lisodeicticus.
Полученные результаты исследования подвергали статистической обработке с помощью стандартных методик на базе электронной таблицы «QUATTRO PRO для Windows» версия 5 и электронной базе данных «Microsoft Access 97».
При бактериоскопическом исследовании материала, взятого из уретры, цервикального канала и заднего свода влагалища, ни у кого из наших пациенток не было выявлено инфекций, передаваемых половым путем, таких как гонорея, трихомониаз, хламидиоз, уреаплазмоз, цитомегаловирусная инфекция, генитальный герпес.
По результатам анализа общей микроскопической картины влагалищных мазков мы разделили наших пациенток на три группы, отражающие состояние биоценоза влагалища (по Кира Е.Ф., 1995) [1]:
1. Нормоценоз, характеризующийся доминированием лактобацилл, отсутствием грамотрицательной микрофлоры, спор, мицелия, псевдогифов, наличием единичных лейкоцитов и «чистых» эпителиальных клеток. Подобная картина отражает типичное состояние нормального биотопа влагалища.
2. Промежуточный тип биоценоза влагалища, характеризующийся умеренным или незначительным количеством лактобацилл, наличием грамположительных кокков, грамотрицательных палочек; обнаруживаются лейкоциты, моноциты, макрофаги, эпителиальные клетки.
3. Дисбиоз влагалища, выражающийся в незначительном количестве или полном отсутствии лактобацилл, обильной полиморфной грамотрицательной и грамположительной палочковой и кокковой микрофлорой, наличием ключевых клеток, вариабельным количеством лейкоцитов, отсутствием или незавершённостью фагоцитоза.
В результате обследования у 26-ти (47,3%) пациенток отмечался нормоценоз, у 24-х (43,6%) - промежуточный тип и только у 5-ти (9,1%) имелся дисбиоз влагалища, что соответствует клиническому диагнозу бактериального вагиноза.
Таблица 2
ПАТОЛОГИЧЕСКИЕ РЕЗУЛЬТАТЫ БАКТЕРИОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ ОТДЕЛЯЕМОГО ВЛАГАЛИЩА
| Бактерии - участники микробного биоценоза гениталий (КОЕ/мл) | Число случаев, когда количество бактерий превышало норму (% от общего числа с патологией) |
| Эшерихии | 6 (16,2%) |
| Протей вульгарный | 11 (29,7%) |
| Клебсиелла | 6 (16,2%) |
| Энтерококки | 24 (64,9%) |
| Стафилококк золотистый | 9 (24,3%) |
| Кишечная палочка | 12 (32,4%) |
| Грибы рода кандида | 15 (40,5%) |
| Лактобактерии (< 10 в 5) | 13 (35,1%) |
Таблица 3
СОДЕРЖАНИЕ БЕЛКОВ ЦЕРВИКАЛЬНОГО СЕКРЕТА

* - значение показателей ниже нормы: ** - значение показателей выше нормы:
Данные изменения четко коррелируют с данными бактериоскопического и бактериологического исследований. При промежуточном типе или дисбиозе влагалища отклонения показателей местного иммунитета более выражены, чем при нормоценозе.
Таким образом, у подавляющего большинства женщин, предъявляющих жалобы на возникновение беспричинно рецидивирующих патологических выделений (лейкоррею), отмечается формирование сапрофитических микробных ассоциаций, не свойственных нормальному физиологическому состоянию, и признаки супрессии местного иммунного ответа в сочетании с иммуновоспалительной реакцией без выраженных клинических проявлений, что и объясняет наличие данной симптоматики.
В соответствии с поставленными задачами все наши пациентки использовали при половой жизни в качестве контрацептивного средства Фарматекс в виде вагинальных суппозиториев, вводя свечу глубоко во влагалище за 5 минут до полового акта. Частота применения Фарматекса у наших обследуемых составила в среднем около 100 раз в течение 12 месяцев.
Переносимость препарата была хорошей, лишь 2 пациентки отказались от применения препарата в связи с развитием у полового партнера явлений баланопостита.
В процессе наблюдения за ними в течение 12-ти месяцев лишь у 9-ти пациенток однократно и у 3-х дважды возникали патологические выделения, которые спонтанно исчезали в течение 3-6-ти дней.
Во время применения Фарматекса через 6 и 12 месяцев проводили повторные бактериоскопические, бактериологические и иммунологические исследования.
В результате бактериоскопического исследования материала, взятого из уретры, цервикального канала и заднего свода влагалища, у всех наших пациенток отмечалась выраженная тенденция к нормализации биоценоза влагалища. Так, при обследовании, проведенном через 12 месяцев с момента применения Фарматекса, ни у одной пациентки не выявлена микроскопическая картина, характерная для дисбиоза влагалища, и только у 15-ти (28,3%) отмечается пограничный тип биоценоза.
Аналогичная тенденция прослеживается и при бактериологическом обследовании. Так, у 29-ти пациенток (54,7%) имелась картина дисбиоза влагалища против 37-ми (67,3%) до начала применения Фарматекса. Необходимо отметить, что в группе пациенток с дисбиозом также имелась положительная тенденция, заключавшаяся в уменьшении количества колониеобразующих единиц бактерий по сравнению с начальным их уровнем и уменьшении количества видов бактерий, характеризующих картину дисбиоза.
При исследовании местного иммунитета цервикальной слизи имелась четкая тенденция к нормализации местного иммунного ответа у всех пациенток (таблица 3).
Полученные нами результаты объясняются непосредственным местным воздействием на слизистую оболочку влагалища, цервикального канала и частично уретры основного компонента Фарматекса -хлористого бензалкония.
Выводы:
1. Инфекции, передаваемые половым путем, являются наиболее частыми (38,2%) причинами развития рецидивирующего бактериального вагиноза;
2. У 14,5% пациенток, страдавших рецидивирующим бактериальным вагинозом, микроскопическая картина соответствовала норме, и только при бактериологическом исследовании обнаружена повышенная обсемененность влагалища различными микробными ассоциациями;
3. Препарат Фарматекс помимо своего основного -контрацептивного действия оказывает нормализующее влияние на количество условно-патогенной флоры влагалища, восстанавливая местный иммунитет, что способствует сокращению рецидивов бактериального вагиноза.
Литература:
1. Кира Е.Ф. Бактериальный вагиноз. - Санкт-Петербург, ООО «Нева-Люкс» -2001. - С. 363.
2. Ломоносов К.М., Иванов О.Л. Фарматекс как средство нормализации микробного биоценоза влагалища после перенесенных инфекций, передаваемых половым путем // Российский журнал кожных и венерических болезней. - 2002. - № 2. - С. 61 - 63.
3. Bourbon P., Thuries S., Zerbib S. Les ammonium quaternaries en therapeutique locale vaginale // Rev. Fr. Gynecol. Obstet. - 1989. - Vol. 84. - P. 11-13.
4. Kutteh W.H., Mestecky S.A. Secretory immunity in the famale reproductive tract // Am. J. Reprod. Immunol. - 1994. - Vol. 17, № 1. - P. 40 - 46.
5. Wainberg M., Spira B., Bleau G., Thomas R. Inactivation of Human Immunodeficiency Virus Type 1 in Tissue Culture Fluid and in Genital Secretions by the Spermicide Benzalkonium Chloride // Journal of Clinical Microbiology. - 1990. - № 1. - P. 156 - 158.
6. White H.D., Yeaman G.R., Givan A.L., Wira C.R. Mucosal immunity in the female reproductive tract: cytotoxic T lymphocyte function in the cervix and vagins of premenopausal and postmenopausal women // Am. J. Reprod. Immunol. - 1997. - Vol. 37, № 1. - P. 30-38.
7. Wira C.R., Rossoll B.M., Antigen-presenting cells in the female reproductive tract: influence of sex hormones on antigen presentation in the vagins // Immunol. - 1995. - Vol. 84, № 4. - P. 505 - 508.
Для цитирования: Ломоносов К.М. Влияние фарматекса на течение бактериального вагиноза. РМЖ. 2005;5:246.
Любая перенесенная инфекция, передаваемая половым путем (гонорея, трихомониаз, хламидиоз, уреаплазмоз), равно как и другие экзогенные факторы, часто приводит к нарушению местного гомеостаза влагалища. В результате расстройства гуморальных факторов (системы комплемента, лизоцима, опсининов, фибронектина, b–лизина и др.) в комплексе с клеточными факторами (макрофагами, полиморфноядерными лейкоцитами, Т–лимфоцитами) и элементами местного иммунитета (Ig А–антитела) происходит нарушение защитных барьеров, обеспечивающих динамическое равновесие между макроорганизмом и нормальной микрофлорой, что вызывает развитие часто рецидивирующих бактериальных вагинозов эндогенного происхождения [4,6,7].
Проводимые во время обострения бактериального вагиноза лечебные мероприятия приводят лишь к временному улучшению. К сожалению, они не способны предотвратить рецидивы вагиноза. Все это заставляет искать новые средства, способные не только воздействовать на активно пролиферирующие условнопатогенные микроорганизмы, но и на факторы, предрасполагающие к таким состояниям.
Учитывая имеющиеся данные о способности препарата Фарматекс восстанавливать местный иммунитет [2], мы провели изучение течения бактериального вагиноза у женщин, регулярно использующих его в качестве контрацептивного средства.
Препарат «Фарматекс» выпускается в виде вагинальных свечей, действующим веществом которого является хлористый бензалконий. Общее название хлористого соединения – диметил–алкил–бензил–аммония–хлористый бензалконий. Хлористый бензалконий, открытый в 1937 г., представляет собой смесь различных хлористых соединений бензалкония, содержащих бензольное ароматическое кольцо и боковую цепь от С8 до С18. Хлористый бензалконий является катионным веществом, изменяющим поверхностное натяжение клеточной мембраны и при введении во влагалище покрывает слизистую поверхность, образуя пленку. В течение нескольких секунд он иммобилизирует сперматозоиды, разрушает их клеточную мембрану и вызывает коагуляцию цервикальной слизи, поэтому основное показание к его применению – местная контрацепция для женщин репродуктивного возраста. Цепь С14, содержащаяся в хлористом бензалконии, обладает также выраженным бактерицидным действием за счет содержания углерода. Проведенные многочисленные исследования препарата in vitro показали его активность в отношении Neisseria gonorrhoeae, Chlamydia spp., Trichomonas vaginalis, Staphylococcus aureus, вируса герпеса 2 типа [3,5].
В исследование были включены 55 женщин, страдающих часто возникающим (не реже 1 раза в 1–3 мес.) неспецифическим бактериальным и/или кандидозным вагинозом.
Возраст пациенток варьировал от 18 лет до 41 года, составив в среднем 28,3±1,2 года. Причем самой многочисленной оказалась группа от 26 до 35 лет, т.е. та, где находились больные наиболее трудоспособного и репродуктивного возраста.
Из сопутствующей патологии лидировали заболевания желудочно–кишечного тракта (хронический гастрит, дисбактериоз кишечника, желчно–каменная болезнь, п=17) и ЛОР–органов (хронический тонзиллит, хронический фарингит, хронический гайморит, п=8).
В основном больные предъявляли жалобы на появление, часто без видимых причин, необильных рецидивирующих выделений из влагалища (лейкоррея), нередко со зловонным запахом, которые могли исчезать произвольно с течением времени или требовали проведения местных лечебных процедур. Часть пациенток отмечали небольшой зуд в области влагалища.
Таким образом, у всех больных в анамнезе зафиксированы жалобы, указывающие на бактериальный вагиноз. Продолжительность заболевания варьировала от полугода до 5 лет. Обострения у всех пациенток возникали 1 раз в 1–3 мес, в среднем 1 раз в 2 мес.
Чаще наличие выделений большинство пациенток (21, или 38,2%) связывали с перенесенными ИППП (4 – с гонореей, 8 – с урогенитальным хламидиозом, 5 – с трихомониазом, 3 – с уреаплазмозом, 1 – с генитальным герпесом). У 9 (16,4%) больных выделения появлялись без видимых причин. Распределение пациенток в зависимости от причин возникновения выделений представлено в таблице 1.
39 (71%) пациенток неоднократно обращались к различным специалистам (венерологу, гинекологу), обследовались лабораторно, но явных причин возникновения обострений выявлено не было. Наиболее частые диагнозы: урогенитальный кандидоз (18) и гарднереллез (7). Больные получали самую разнообразную терапию, включающую антибиотики, дифлюкан, нистатин, трихопол, флагил, местные средства (тержинан, клион Д, полижинакс, клотримазол и др.) с временным эффектом.
На момент обращения к нам все пациентки находились в фазе ремиссии. При осмотре лишь у 4 (7,3%) выявлена небольшая гиперемия влагалища.
Все больные прошли комплексное клинико–лабораторное обследование, включавшее бактериоскопию материала из уретры, цервикального канала и заднего свода влагалища; бактериологическое исследование микрофлоры влагалища (с определением титра в исследуемом материале микроорганизмов семейства Entherobacteriaceae, Streptococcaceae, Staphylococceae) и на кандидозы; исследование местного иммунитета цервикальной слизи, поскольку шейка матки является основным барьером защиты, которая синтезирует факторы специфического и неспецифического иммунитета. При исследовании местного иммунитета определяли уровень 11 белков цервикального секрета: Ig G, Ig A, Ig M, slg А, комплемента С3=, С4=, орсомукоид, трансферрин, фибриноген, лизоцим, иммунные комплексы (ИК). Концентрацрпо иммуноглобулинов вычисляли методом радиальной иммунодиффузии в 1,5%–ном геле арагозы по Манчини.
Уровень компонентов комплемента выявляли методом молекулярного тестирования путем добавления к цервикальной слизи реагента, который представлял собой комплемент сыворотки человека, истощенный по испытуемому компоненту и таким образом лимитирующий активацию комплемента на уровне собственного компонента исследуемой цервикальной слизи. Концентрацию компонентов комплемента учитывали на фотометре «Labsystems Multiskan MS».
Содержание лизоцима, орсомукоида, трансферрина и фибриногена определяли нефелометрическим методом по О.В. Бухарину, основанном на способности ферментов лизировать культуру Micrococcus lisodeicticus.
Полученные результаты статистически обрабатывали с помощью стандартных методик на базе электронной таблицы «QUATTRO PRO для Windows» (версия 5) и электронной базе данных «Microsoft Access 97».
При бактериоскопическом исследовании материала, взятого из уретры, цервикального канала и заднего свода влагалища, ни у кого из пациенток не выявлено таких ИППП, как гонорея, трихомониаз, хламидиоз, уреаплазмоз, цитомегаловирусная инфекция, генитальный герпес.
По результатам анализа общей микроскопической картины влагалищных мазков мы разделили пациенток на три группы, отражающие состояние биоценоза влагалища [Кира Е.Ф., 1995] [1].
1. Нормоценоз, характеризующийся доминированием лактобацилл, отсутствием грамотрицательной микрофлоры, спор, мицелия, псевдогифов, наличием единичных лейкоцитов и «чистых» эпителиальных клеток. Подобная картина отражает типичное состояние нормального биотопа влагалища.
2. Промежуточный тип, отличающийся умеренным или незначительным количеством лактобацилл, наличием грамположительных кокков, грамотрицательных палочек; обнаруживаются лейкоциты, моноциты, макрофаги, эпителиальные клетки.
3. Дисбиоз влагалища, выражающийся в незначительном количестве или полном отсутствии лактобацилл, обильной полиморфной грамотрицательной и грамположительной палочковой и кокковой микрофлорой, наличием ключевых клеток, вариабельным количеством лейкоцитов, отсутствием или незавершенностью фагоцитоза.
Обследование больных привело к следующим результатам: у 26 (47,3%) отмечался нормоценоз, у 24 (43,6%) – промежуточный тип и только у 5 (9,1%) – дисбиоз влагалища, что соответствует клиническому диагнозу бактериального вагиноза.
При более глубоком исследовании бактериальной флоры влагалища (бактериологическом исследовании), которое позволяет в полной мере оценить качественные и количественные показатели микрофлоры, наблюдалась несколько иная картина. Так, только у 18 (32,7%) пациенток количество бактерий оказалось в пределах нормы. У остальных 37 (67,3%) наблюдался дисбиоз влагалища, что выражалось различными микробными ассоциациями (табл. 2).
Таким образом, у 8 (14,5%) пациенток с нормальной микроскопической картиной при бактериологическом исследовании обнаружена повышенная обсемененность различными микробными ассоциациями, что можно характеризовать, как бактериальный вагиноз, который не диагностируется простой микроскопией.
Результаты проведенного параллельно исследования местного иммунитета цервикальной слизи пациенток выявили в отличие от группы здоровых доноров выраженные сдвиги (табл. 3). Так. у больных отмечались достоверное снижение содержания Ig M, Ig A, slg А, некоторое повышение уровня ИК, что свидетельствует об антигенной атаке во влагалищном секрете. Некоторое снижение содержания орсомукоида, лизоцима, трансферрина говорит о супрессии местного иммунитета. Незначительный подъем уровня С4 и тенденцию к комплементарному каскаду СЗ, можно объяснить наличием небольшой, клинически не выраженной воспалительной реакции.
Указанные изменения четко коррелировали с данными бактериоскопического и бактериологического исследований. При промежуточном типе или дисбиозе влагалища отклонения показателей местного иммунитета выражены в большей степени, нежели при нормоценозе.
Таким образом, у подавляющего большинства женщин, предъявлявших жалобы на возникновение беспричинно рецидивирующих патологических выделений, отмечались формирование сапрофитических микробных ассоциаций, не свойственных нормальному физиологическому состоянию, и признаки супрессии местного иммунного ответа в сочетании с иммуновоспалительной реакцией без выраженных клинических проявлений, что и объясняет наличие данной симптоматики.
В соответствии с поставленными задачами все пациентки использовали (в среднем около 100 раз в течение 12 мес.) при половых контактах в качестве контрацептивного средства Фарматекс в виде вагинальных суппозиториев, вводя свечу глубоко во влагалище за 5 мин. до полового акта.
В целом переносимость препарата оказалась хорошей, лишь 2 больные отказались от его применения в связи с развитием у полового партнера явлений баланопостита.
В процессе наблюдения за пациентками в течение 12 мес лишь у 9 из них однократно и у 3 дважды появлялись патологические выделения, которые спонтанно исчезали в течение 3–6 дней.
Во время применения Фарматекса через 6 и 12 мес проводили повторные бактериоскопические, бактериологические и иммунологические исследования.
Бактериоскопическое исследование материала, взятого из уретры, цервикального канала и заднего свода влагалища, показало выраженную тенденцию к нормализации биоценоза влагалища у всех пациенток. Так, при обследовании, проведенном через 12 мес. с момента применения Фарматекса, ни у одной из них не выявлена микроскопическая картина, характерная для дисбиоза влагалища, и только у 15 (28,3%) диагностирован промежуточный тип биоценоза.
Аналогичная тенденция прослеживалась и при бактериологическом обследовании. Так, у 29 (54,7%) больных наблюдался (до начала применения Фарматекса у 37 (67,3%)) дисбиоз влагалища. Необходимо отметить, что в группе пациенток с дисбиозом также имелась положительная тенденция, которая заключалась в уменьшении количества колониеобразующих единиц бактерий по сравнению с их начальным уровнем, а также количества видов бактерий, характеризующих картину дисбиоза.
При исследовании местного иммунитета цервикальной слизи имелась четкая тенденция к нормализации местного иммунного ответа у всех больных (табл. 3).
Полученные нами результаты объясняются непосредственным местным воздействием на слизистую оболочку влагалища, цервикального канала и частично уретры основного компонента фарматекса – хлористого бензалкония.
Выводы
1. ИППП являются наиболее частыми (38,2%) причинами развития рецидивирующего бактериального вагиноза.
2. У 14,5% пациенток, страдавших рецидивирующим бактериальным вагинозом, микроскопическая картина соответствовала норме, и только при бактериологическом исследовании обнаружена повышенная обсемененность влагалища различными микробными ассоциациями.
3. Помимо основного контрацептивного действия, Фарматекс оказывает нормализующее влияние на количество условно–патогенной флоры влагалища, восстанавливая местный иммунитет, что способствует сокращению числа рецидивов бактериального вагиноза.
Литература
1. Кира Е.Ф. Бактериальный вагиноз. – СПб, 2001. – С. 363.
2. Ломоносов К.М., Иванов О.Л. Фарматекс как средство нормализации микробного биоценоза влагалища после перенесенных инфекций, передаваемых половым путем // Российский журнал кожных и венерических болезней. – 2002, № 2. – С. 61–63.
3. Bourbon P., Thuries S., Zerbib S. Les ammonium quaternaries en therapeutique locale vaginale // Rev. Fr. Gynecol. Obstet. – 1989. – Vol. 84. – P. 11–13.
4. Kutteh W.H., Mestecky S.A. Secretory immunity in the famale reproductive tract // Am. J. Reprod. Immunol. – 1994. – Vol. 17, N 1. – P. 40–46.
5. Wainberg M., Spira В., Bleau G., Thomas R. Inactivation of human immunodeficiency virus type 1 in tissue culture fluid and in gemtal secretions by the spermicide benzalkonium chloride // J. Clin. Microbiol. – 1990. – Vol. 47, N 1. –P. 156–158.
6. White H.D., Yeaman G.R., Givan A.L., Wira C.R. Mucosal immunity in the famale reproductive tract: cytotoxic T lymphocyte function in the cervix and vagins of premenopausal and postmenopausal women // Am. J. Reprod. Immunol. – 1997. – Vol. 37, N 1. – P. 30 – 38.
7. Wira C.R., Rossoll B.M. Antigen–presenting in the female reproductive tract: influence of sex hormones on antigen presentation in the vagins // Immunol. –1995. – Vol. 84, N 4. – P. 505–508.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Для цитирования: Логинов Л.П. Современные принципы местного лечения термических ожогов. РМЖ. 2001;3:123.
НИИ скорой помощи имени Н.В. Склифосовского
О громный накопленный в мире опыт местного лечения больных с ожогами, изучение обширной литературы, посвященной ожоговой патологии (Т.Я. Арьев, 1971; Н.И. Атясов, 1972; В. Рудовский и соавт., 1980; М.И. Кузин и соавт., 1982; Б.С. Вихриев, В.М. Бурмистров, 1986), позволяет в настоящее время сформулировать некоторые неоспоримые постулаты.
• Местное лечение поверхностных ожогов I-II степени, даже обширных, не представляет серьезных трудностей. Они при лечении любыми средствами заживают в течение 7-12 дней.
• Cубдермальные ожоги IIIА степени нуждаются в более длительной консервативной терапии, которое не исключает возможности применения хирургического лечения у ограниченного числа больных. Подобные ожоги заживают в сроки от 3 до 6 нед.
• Глубокие ожоги IIIБ - IV cтепени нуждаются в хирургическом лечении.
• Местное консервативное лечение глубоких ожогов является лишь вспомогательным, оно преследует цель в кратчайшие сроки подготовить ожоговую рану к свободной пересадке кожи - заключительному этапу по восстановлению утраченного кожного покрова.
Исходя из вышеизложенного, представляется целесообразным поделиться нашим многолетним опытом местного лечения глубоких ожогов. В настоящей работе приведена лишь небольшая часть средств для местного лечения ожогов, которые применялись наиболее часто. Весь перечень подобных препаратов весьма велик и вряд ли целесообразно их перечислять.
На догоспитальном этапе при наличии ограниченных ожогов лучшей первичной повязкой является сухая асептическая повязка, при обширных ожогах для этих целей используют стандартные контурные повязки или стерильные простыни. Первичная повязка не должна содержать жиры и масла в связи с возникающими впоследствии трудностями при туалете ран, а также красители, т.к. они могут затруднить распознавание глубины поражения. Самым действенным мероприятием на догоспитальном этапе является криообработка ожоговых поверхностей. Это достигается обливанием пораженного участка в течение 10-15 мин холодной водой или использованием для этих целей льда, снега в чистом целлофановом пакете или готового криопакета. Криообработка прекращает действие термического агента на ткани пострадавшего и способствует благоприятному течению ожогов в последующем.
При поступлении в ожоговый центр пострадавшим выполняют первичную обработку ожоговых ран, характер и объем которой зависит от площади и глубины ожогового поражения. При наличии ограниченных поверхностных ожогов (не более 20% поверхности тела) без признаков ожогового шока обычно выполняют тщательный туалет ожоговых ран, заключающийся в удалении десквамированного эпидермиса, инородных тел, пузырей, в обильном промывании антисептическими растворами и наложении мазевой повязки. Если имеются обширные ожоги кожи, сопровождающиеся шоком, первичную обработку при поступлении не выполняют. Больного заворачивают в стерильную простыню, а отсроченный первичный туалет производят после стабилизации общего состояния. Глубокие ожоги обрабатывают так же, как и поверхностные, с той лишь разницей, что накладывается повязка с антисептическими растворами.
Нередко уже при поступлении может возникнуть необходимость в срочном оперативном вмешательстве. Подобная ситуация возникает при наличии циркулярных ожогов шеи, конечностей или грудной клетки. В этих случаях скальпелем без дополнительного обезболивания делают продольное рассечение струпа (некротомия) до жизнеспособных кровоточащих тканей. Такая простая манипуляция приводит к улучшению кровоснабжения пораженных участков, предупреждает углубление ожогового поражения, а при ожогах грудной клетки в значительной степени улучшает дыхательные экскурсии.
Местное лечение глубоких ожогов имеет свои конкретные задачи в разных фазах течения раневого процесса. Вскоре после получения ожога в период острого воспаления и нагноения лечение направлено на борьбу с раневой инфекцией и должно способствовать ускоренному отторжению некротических тканей. Для этого проводят частые (вплоть до ежедневных) перевязки с растворами йодсодержащих препаратов (йодопирон, йодовидон, повидон-йод и др.), хлоргексидина, диоксидина, фурацилина, повиаргола, лавасепта, плевасепта и т.п. Для борьбы с инфекцией в настоящее время хорошо себя зарекомендовал современный отечественный антисептик мирамистин, который применяется в 0,01% концентрации (С.В. Смирнов, Л.П. Логинов, 2000). В первой фазе раневого процесса при наличии влажных струпов или в период активного механического удаления их, используются углеродные перевязочные материалы. Эти материалы обладают хорошей сорбционной способностью, что приводит к уменьшению гнойного отделяемого, подсушиванию струпов и, как следствие, значительному уменьшению интоксикации организма. В конце данной фазы раневого процесса для борьбы с инфекцией также используют мази на водорастворимой основе (левомеколь, диоксиколь, сильвацин и др.).
С целью отторжения омертвевших тканей используются протеолитические ферменты животного происхождения (трипсин, хемотрипсин, панкреатин), бактериальные ферменты (стрептокиназа, коллагеназа, террилитин и др.), растительные ферменты (папаин и др.). Следует учитывать тот факт, что ферменты не действуют на плотный ожоговый струп. Поэтому применение ферментов наиболее показано в процессе механического удаления некрозов либо при наличии влажных струпов.
Кератолитические средства (молочная, салициловая, карболовая кислоты, мочевина) в нашей практике находят ограниченное применение, поскольку они усиливают местный воспалительный процесс в ране, вызывающий усиление интоксикации. Эти средства используются нами лишь при ограниченных ожогах у пострадавших, не подлежащих оперативному лечению по тем или иным причинам (отказ от операции, тяжелая сопутствующая патология).
При консервативном лечении глубоких ожогов самопроизвольное отторжение нежизнеспособных тканей можно ожидать лишь через 4-6 нед после травмы. Такие длительные сроки подготовки ожоговых ран к свободной пересадке кожи - конечному этапу хирургического лечения обожженных - непозволительны, так как за это время состояние больных может ухудшиться за счет присоединения осложнений, и выполнение операции у многих из них становится проблематичным. Поэтому мы, как и комбустиологи всего мира, стремимся выполнить закрытие ран аутотрансплантатами в максимально короткие сроки. Это достигается хирургическими методами лечения: некротомией, некрэктомией и свободной пересадкой кожи. Идеальным методом хирургического лечения глубоких ожогов является радикальное иссечение нежизнеспособных тканей с одномоментной кожной пластикой образовавшегося дефекта в первые 2-3 дня после получения ожогов. Однако трудность диагностики глубины поражения, травматичность самой операции, отсутствие уверенности в полном удалении мертвых тканей приводят к тому, что ее возможно выполнять лишь у ограниченного числа обожженных с площадью глубокого ожога не более 10% поверхности тела.
Для удаления остатков нежизнеспособных тканей используются частые (вплоть до ежедневных) перевязки с антисептическими растворами, ферментами, антибиотиками. В дальнейшем при начинающемся росте грануляционной ткани переходют на мазевые повязки (2% фурацилиновая мазь, левомеколь, диоксиколь и др.). Хорошо себя зарекомендовала мазь Лавендула, содержащая антисептик мирамистин и фермент бактериального происхождения ультрализин. Мирамистин хорошо подавляет грамотрицательную и грамположительную микрофлору, а ультрализин способствует протеолизу и удалению оставшихся мертвых тканей.
В этот же период применяются различные мази на трикотажной сетчатой основе. Среди них заслуживают внимания однослойные мазевые повязки с 5% диоксидиновой мазью. Обычно после 2-3 перевязок мы могли отметить уменьшение гнойного отделяемого, активизацию роста грануляционной ткани, снижение микробной обсемененности ожоговых ран. Важным преимуществом данной повязки является также то, что она легко и безболезненно удаляется с поверхности раны на очередной перевязке.
В этой же фазе раневого процесса (регенерация) с используются препараты, стимулирующие рост грануляций: салфетки с гиалуроновой кислотой, бальзамические повязки и т.п. Не потеряла своего значения ксенотрансплантация свиной кожи для временного покрытия обширных ожоговых поверхностей с целью защиты их от внутрибольничной инфекции и уменьшения потерь белков, электролито и, жидкостей.
Показателем готовности раны к закрытию ее аутотрансплантатами считается наличие ярко-красного грануляционного покрова с необильным гнойным отделяемым с выраженной каймой краевой эпителизации, отсутствие остатков нежизнеспособных тканей.
Обязательным условием для выполнения операции свободной пересадки кожи является отсутствие гипопротеинемии (общий белок не менее 60 г/л), гипоальбуминемии (белковый коэффициент не менее 1), анемии (гемоглобин не ниже 90 г/л). Временным противопоказанием к операции считается наличие в ране b-гемолитического стрептококка. К удалению грануляций перед аутодермопластикой мы прибегаем крайне редко, так как почти всегда удается добиться хорошего состояния последних и есть надежда на хорошее приживление трансплантатов.
Ожоговые раны на площади до 15-20% поверхности тела обычно закрываем в один этап, более обширные ожоговые раны нуждаются в 2-3-, а иногда и в 4-5-этапных операциях. Срезание кожных лоскутов выполняем дерматомами с ручным или электрическим приводом под общим обезболиванием. Проблема дефицита донорских ресурсов при этом решается с помощью сетчатых аутодермотрансплантатов с коэффициентом растяжения от 1:2 до 1:6. Повторное срезание кожных лоскутов с зажившего донорского участка также позволяет решать проблему дефицита донорских ресурсов. Быстрой эпителизации донорских ран способствует наложение после операции однослойных мазевых повязок с 5% диоксидиновой мазью: при толщине срезанных трансплантатов 0,3 мм донорские раны эпителизировались за 10-12 дней. Закрытие всех ожоговых ран аутотрансплантатами производим за 2-2,5 месяца с момента ожогового поражения.
В послеоперационном периоде местное лечение также не утратило своей значимости. Речь идет о больных, у которых имеет место частичное расплавление кожных лоскутов и образование между ними множества гранулирующих ран. В данной ситуации полезными оказываются различные губчатые покрытия (коласпон, дигиспон, биотравм, гешиспон и др.), которые способны не только реально стимулировать репаративные процессы, но и обладают противовоспалительным действием. К сожалению, в настоящее время многие из них в связи с тяжелой экономической ситуацией в стране не выпускаются отечественной промышленностью. Для борьбы с избыточными грануляциями применяем мази с гидрокортизоном.
Описанное выше хирургическое лечение обширных глубоких ожогов укладывается в понятие “активная хирургическая тактика”, сформулированное 40 лет назад Н.И. Атясовым. В процессе оперативного лечения обожженных не потеряли своего значения и физические методы воздействия на раневой процесс (УВЧ, УФО, лазеротерапия, кровати “Клинитрон”, потолки с инфракрасным излучением и т.п.). Местное лечение обширных глубоких ожогов проводится на фоне интенсивной инфузионно-трансфузионной терапии, позволяющей поддерживать показатели гомеостаза в пределах нормальных значений.
Первый опыт применения для закрытия ран после глубоких ожогов эпидермальных кератиноцитов, выращенных вне организма больного, показал его перспективность в решении проблемы дефицита донорских ресурсов (А.В.Васильев и соавт., 1994). Теоретически этот метод предполагает создание безграничных донорских ресурсов, т.к. из маленького кусочка кожи выращиваются эпителиальные пласты, превышающие площадь этой кожи в 100 и более раз. Однако трудоемкость, сложность и большая стоимость выращивания кератиноцитов не позволяют в настоящее время внедрить этот метод в практическую медицину.
Активная хирургическая тактика позволила улучшить результаты лечения тяжело обожженных, расширить границы выживаемости при крайне тяжелых ожогах, сохранять жизнь некоторым больным с глубокими ожогами на площади 50 - 60% и более поверхности тела.
1. Т.Я. Арьев. Ожоги и отморожения. “Медицина”, 1971.
2. Н.И. Атясов. Система активного хирургического лечения тяжело обожженных. Г., 1972.
3. В. Рудовский и соавт. Теория и практика лечения ожогов М., “Медицина”, 1980.
4. М.И. Кузин и соавт. Ожоговая болезнь. М., “Медицина”, 1982.
5. Б.С. Вихриев, В.М. Бурмистров. Ожоги. Л., “Медицина”, 1986.
6. С.В. Смирнов, Л.П. Логинов. Результаты лечения ожоговых ран с использованием отечественного антисептика мирамистина. В мат. симпоз. “Мирамистин - новый отечественный антисептик широкого спектра действия”. М., 2000, с.17
7. А.В. Васильев и соавт. Применение выращенных эпителиальных пластов для лечения обожженных. Травматология и ортопедия, 1994; 4: 34-9.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Сегодня лечение ожогов является актуальной проблемой. По данным госстата за 2018 год не менее 30000 людей подверглись термическим или химическим повреждениям. Это одна из самых распространенных бытовых травм. Однако часто ожог можно получить и на производстве, где не соблюдаются условия безопасности.
При возникновении ожогов надо суметь вовремя оказать правильную первую помощь. От того, как быстро вы окажете помощь себе или пострадавшему человеку, будет зависеть его дальнейшее состояние и скорость лечения.
Организм человека способен сам регенерировать и убирать легкие ожоги без серьезных последствий для здоровья. Более серьезные ожоги требуют неотложной медицинской помощи для предотвращения осложнений. За подобными ранами нужно следить, не допускать проникновения инфекции и регулярно обрабатывать противовоспалительными лекарствами или накладывать противоожоговые салфетки.
Если вы оказались рядом с обожженным, вам твердо нужно знать, как лечить ожог, иначе вы причините своими действиями больше вреда, чем пользы.
Причины ожогов
Ожог может произойти вследствие воздействия:
- огня;
- горячей жидкости или пара;
- горячего металла, стекла или других предметов;
- электрического тока;
- радиации (рентгеновское излучение или лучевая терапия);
- ультрафиолета (солнце или солярий);
- активных химических веществ.
Стоит отметить, что причины ожогов могут быть и иными, но все виды такого рода травм классифицируются в зависимости от степени нанесенного повреждения и симптоматики:
- Первая степень. Таким ожогом затрагивается только внешний слой кожных покровов. Травма характеризуется покраснением, отечностью и болевыми ощущениями. Пострадавшему оказывается первая помощь и назначается непродолжительный курс лечения.
- Вторая степень. Этот ожог ведет к поражению не только эпидермиса, но и подлежащего слоя – дермы. Повреждение характеризуется покраснением, побелением или пятнистостью кожи, болью и отечностью. Возможно развитие пузырей от ожогов и сильного болевого синдрома.
- Третья степень. При таком повреждении затрагивается жировой слой под кожными покровами. Обгоревшие участки тела обугливаются, чернеют или белеют. Часто ожогами третьей степени нарушается работа нервной и дыхательной системы.
Первые действия для нейтрализации термических ожогов
- как можно дальше убрать пострадавшего от источника тепла;
- если тлеет одежда или снаряжение, следует немедленно от нее избавиться. Если одежда прилипла к коже, надо аккуратно срезать ее или снять;
- к месту повреждений приложить сухой лед или использовать холодную воду;
- обработать поврежденные участки тела мазью от ожогов;
- в случае серьезных травм обратиться вызвать скорую.
Нейтрализация химических ожогов
- промыть пораженное место сильным потоком воды. Ни в коем случае не следует обрабатывать рану маслом.
- если получен ожог от негашеной извести или серной кислоты, его следует
- обработать сухой салфеткой, использование воды недопустимо;
- нанести стерильную антисептическую повязку.
Случаются ситуации, когда люди получают тяжелые ожоги. Лечение их вне стационара требует специальных знаний и навыков. Если человек ими не обладает - лучше немедленно обратиться к врачу.
Степень ожогов
Существует три основных степени ожогов: первая, вторая и третья. Оценка каждой степени основана на серьезности повреждения кожи: первая степень является самой незначительной, а третья - самой серьезной.
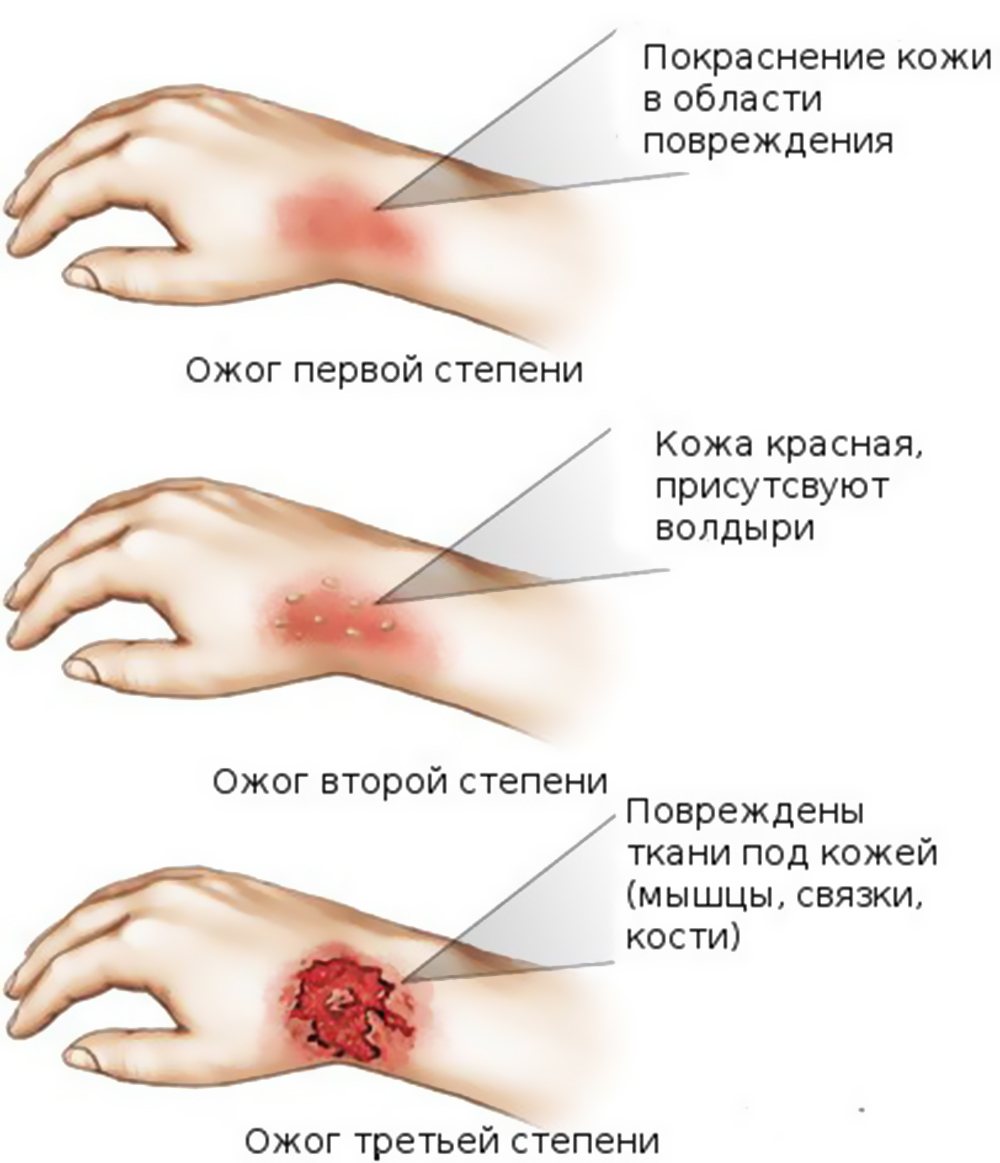
Признаки повреждений выглядят следующим образом:
- ожоги первой степени: происходит нарушение эпидермального слоя, кожа красная, чуть вздувшаяся;
- ожоги второй степени: появляются волдыри и наблюдается отслоение кожи;
- ожоги третьей степени: наблюдается некроз тканей, кожа становится белой, образуется корка;
Есть также ожоги четвертой степени. Эта степень включает в себя все симптомы ожога третьей степени. Повреждения проникают за пределы кожи и распространяются на сухожилия и кости. Именно в этом случае остаются шрамы после ожога.
Химические и электрические ожоги требуют немедленной медицинской помощи, поскольку они могут повлиять на внутренние органы, даже если внешние повреждения едва видимы.
Тип ожога не зависит от причины его возникновения. Ошпаривание, например, может вызвать все три типа ожога – термический, химический и физический, в зависимости от того, насколько горячая жидкость и как долго она остается в контакте с кожей.
Лечение после ожогов

Мазь или гель от ожога кипятком хорошо помогает при кухонных проблемах. Если были получены ожоги второй или третьей степени требуется стационарное лечение. Его следует проходить в клинике под присмотром врачей. Терапевт порекомендует, чем обработать ожог или как лечить ожог с волдырями.
Как лечить ожоги с волдырями в домашних условиях
- ни в коем случае не прокалывайте волдырь - это может привести к образованию инфекции;
- промыть ожог под прохладной проточной водой;
- нанесите противоожоговый крем или гель с обезболивающим эффектом тонким слоем;
- наложить бинт на место ожога после обработки;
- обрабатывать ожог с волдырем и менять повязку ежедневно.
Восстановление кожи после ожога
Что помогает от ожогов, так это точное соблюдение гигиены и регулярная обработка раны.
После получения травмы, на коже сразу же образуется волдырь, наполненный прозрачной плазмой, которая может просачиваться сквозь обожженные ткани. При правильной обработке можно избежать воспаления и нагноения, и регенерация пройдет быстрей.
Уже через несколько дней пузыри от ожогов начнут спадать и отшелушиваться, под волдырем начнет образовываться новая кожа. В это время раны могут чесаться, но прикасаться к пораженному участку нельзя - к концу первой недели зуд пройдет сам собой.
Если рану запустить в ней может развиться процесс нагноения. Он может сопровождаться повышением температуры, внезапной слабостью и ознобом. При таком анамнезе регенерация кожных покровов может затянуться на недели. В этом случае вероятно появление уплотненных наростов и валиков.
Как предотвратить появление рубцов после ожога?
Рубцы от ожогов появляются в зависимости от особенностей организма пострадавшего. В любом случае их появление можно предотвратить, своевременно используя противорубцовые гели и мази, а также специальные силиконовые покрытия для ран и увлажняющие кремы.
Лечение рубцов и шрамов после ожогов
Если вас интересует, как избавиться от внешних последствий ожога, нужно знать, что при серьезных нарушениях кожного покрова, шрам останется в любом случае. Здесь потребуется помощь косметолога, который поможет восстановить нормальный вид кожи.
Обычно для подобной операции используется методика иссечения рубца, после чего на ткани накладывается несколько косметических швов. Когда швы снимают, поврежденный участок обрабатывают мазями, которые препятствуют образованию новых шрамов на коже.
Для особо сложных случаев, например, при ожогах кипятком, используется методика лазерной шлифовки. Современное оборудование позволяет полностью удалить шрамы и достичь идеальной кожи. Если же сила ожога незначительна, рекомендуется химический пилинг с фруктовыми кислотами.
Средства от ожогов
Чем же лечить ожог, и какую оперативную помощь можно оказать самостоятельно в полевых или домашних условиях?

Использование кремов типа Левомиколя или Спасателя гарантированно помогает при незначительных повреждениях, таких как краткое прикосновения к горячей кастрюле. Декспантенол очень хорошо работает при ожогах первой степени. Если же степень повреждений более серьезна, кремы могут использоваться только как профилактическое средство и надеяться на них как не стоит.
Такие средства от ожогов, как спреи или гели - например, Гидрогель противоожоговый Burnshield, являются более эффективными, так они дисперсны и лучше впитываются кожей. Эти препараты сочетают в себе две функции – противовоспалительную и обезболивающую.
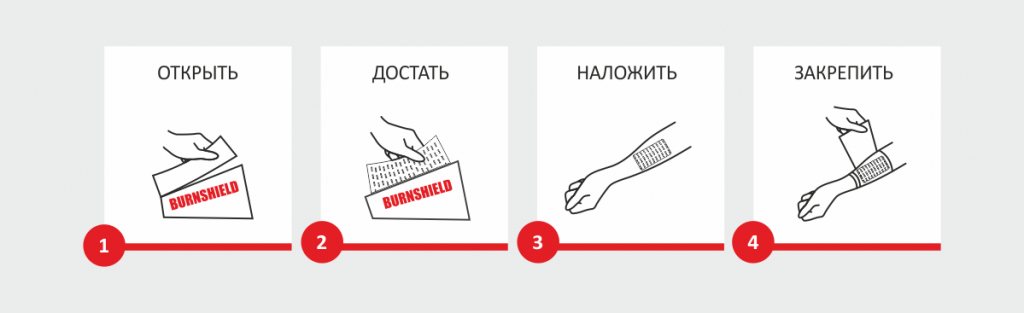
Есть еще один вид обработки – специальные противоожоговые повязки. Их рекомендуют, когда пациенту нужно быть на открытом воздухе. Такие повязки не допускают попадания в рану грязи и пыли.
Что нельзя использовать для лечения ожога
При получении ожога любой степени в лечебных целях не следует пользоваться:
- масло;
- мед и прополис;
- лед;
- зубная паста;
- химические вещества.
Чтобы снизить риск общих ожогов
В быту можно достаточно просто снизить риск ожогов, следует только соблюдать несколько рекомендаций:
- нельзя оставлять готовящуюся или уже приготовленную пищу на плите без присмотра;
- сковородки размещаются на плите рукоятками к ее задней части;
- любую горячую жидкость нужно размещать в недоступном для ребенка и животного месте – кипяток является частой причиной термического ожога;
- нельзя хранить электрические приборы рядом с водой;
- не стоит готовить в легковоспламеняющейся одежде;
- следует заблокировать ребенку доступ к электро- и газовым приборам;
- на розетки, которые не используются, нужно надеть защитные колпачки;
- не следует курить дома;
- датчики дыма требуют регулярного обслуживания и замены батареек;
- дом или квартиру нужно оснастить огнетушителем;
- причиной химических ожогов являются химикаты – их необходимо хранить в месте, которое недоступно для ребенка и животного.
Куда обратиться при ожоговых травмах?
У человека не всегда может получиться эффективно убрать волдыри от ожогов или оказать требуемую помощь дома, и тогда не нужно терять время и заниматься самолечением.
В случае осложнений следует незамедлительно обратиться к вашему лечащему терапевту. Специалист скажет, какие анализы требуется сделать, определит по признакам ожога степень и разработает курс лечения с учетом специальных средств.
Читайте также:

