Бесплодие при системной красной волчанке
Обновлено: 28.04.2024
Характерная черта современной медицины — большой объем специфической информации и глубина понимания проблемы врачами различных специальностей. Это делает необходимым условием успешной медицинской практики взаимодействие специалистов различного профиля при лечении многих пациентов. Как пример — совместный интерес акушеров-гинекологов и ревматологов к системной красной волчанке (СКВ), обусловленный тем, что этим заболеванием страдают преимущественно женщины детородного возраста, которые хотели бы иметь детей и при этом предпринимают попытки беременеть. Но наличие серьезного хронического заболевания и необходимость постоянного приема лекарств будущей матерью повышают риск неблагоприятного течения заболевания в период беременности и развития ее осложнений.
Все эти риски можно снизить до минимума, если запланировать наступление беременности на фоне отсутствия или снижения активности СКВ, а также тщательно контролировать активность заболевания во время беременности и после родоразрешения. Эти задачи призвано решить сотрудничество наших врачей ревматологов и акушеров-гинекологов, что находит отражение в «историях борьбы» со счастливым финалом — рождением малышей у женщин, которые еще пару десятков лет назад и мечтать не могли о таком счастье.
Клинический случай. Пациентка И., 32 года, в настоящее время наблюдается врачом-ревматологом с диагнозом СКВ. До достижения возраста 28 лет считала себя абсолютно здоровой. В 2015 г. течение первой беременности осложнилось симтомами преэклампсии с прогрессирующей тромбоцитопений (снижения количества тромбоцитов), что потребовало досрочного родоразрешения.
Через несколько месяцев при обследовании по поводу возможной мочевой инфекции был диагностирован тромбоз нижней полой вены, по поводу чего пациентка велась совместно сосудистыми хирургами НИИ СП им. Н.В. Склифосовского и консультативной гемостазиологической бригады 52-й городской больницы. Как причина данного осложнения была заподозрена и, в дальнейшем, подтверждена генетическая тромбофилия.
Наследственная тромбофилия — генетически обусловленная предрасположенность к повышенному тромбообразованию. Беременность сопровождается физиологической гиперкоагуляцией, которая представляет собой защитный механизм, препятствующий развитию кровотечений в родах или при угрозе прерывания/прерывании беременности. При наложении этих двух факторов риск тромбозов многократно увеличивается, что может стать причиной множества акушерских осложнений.
Подобранная терапия эффективно купировала тромботическое состояние, но сохранялась тромбоцитопения, никак не укладывающаяся ни в имеющийся диагноз, ни в наблюдаемую клиническую картину.
Пристальное внимание врачей не было напрасным, через некоторое время появились новые симптомы: боли в суставах кистей и стоп, сыпь под воздействием солнечных лучей, продолжало снижаться зрение. После непростого диагностического поиска ревматологами ГКБ № 52 был установлен диагноз СКВ и начато патогенетическое лечение.
Системная красная волчанка (СКВ) — хроническое аутоиммунное заболевание с поражением соединительной ткани и сосудов, при котором организм начинает реагировать на собственные клетки как на чужеродные образованием иммунных комплексов. Запускается воспалительный процесс, затрагивающий многие органы и системы: почки, легкие, сердце, кожу, суставы, глаза, клетки крови.
В октябре 2018г. дополнительные задачи поставила наступившая вторая беременность. Появление дополнительных симптомов потребовало диагностических вмешательств и участия других специалистов, в частности, гематологов и офтальмологов. В результате к родам пациентка пришла с диагнозом: системная красная волчанка хронического течения, низкой степени активности с поражением суставов, кожи, системы крови, глаз, АНФ (-),Ат к ДНК (-). АФС-тромбоз нижней полой вены, ВА (+), Наследственная тромбофилия.
Принимая во внимание высокий риск отслойки сетчатки во время естественных родов и наличие рубца на матке, решено родоразрешить пациентку путем планового кесарева сечения. И 14 июля 2019 года в результате плановой операции кесарево сечение родилась живая доношенная девочка 3200г/51см с оценкой по Апгар 7-8 баллов.
Совместное ведение родов и раннего послеродового периода акушерами и ревматологами с привлечением специалистов по проблемам системы свертывания увенчалось успехом. Послеродовой период протекал без осложнений. На 5-е сутки мама и ребенок выписаны домой. Женщина продолжает наблюдаться у ревматолога амбулаторно.
Пациентку наблюдали:
Врач ревматолог, заведующая отделением ревматологии Загребнева А. И.
Врач ревматолог, заведующая КДО ГКБ № 52 Ткаченко С. Н.
Руководитель гематологической службы ГКБ № 52 Мисюрина Е. Н.
Руководитель выездной реанимационной гематологической бригады ГКБ № 52, главный внештатный специалист трансфузиолог Буланов А. Ю.
Зам.главного врача по акушерству и гинекологии Грабовский В. М.
Заведующая родильным домом ГКБ № 52 Кокая. И. Ю.
Врачи акушеры-гинекологи: Осокин И. П., Ефремов А. Н.
Давний интерес к проблеме беременности при системной красной волчанке (СКВ) определил тот факт, что заболевание поражает преимущественно женщин детородного возраста. Несколько десятков лет назад существовало неоспоримое мнение, что больные волчанкой не могут иметь детей и при возникновении беременности необходим аборт. Сегодня, к счастью, это не так.
Взгляд в историю
СКВ – хроническое аутоиммунное заболевание соединительных тканей и сосудов, при котором механизм защиты в организме начинает реагировать на собственные клетки как на чужеродные. Это становится причиной запуска воспалительного процесса, влияющего на многие органы: почки, кожу, суставы, сердце, клетки крови и легкие. Тяжелое воспаление может привести к хроническим болям, повреждению тканей и внутренних
органов. СКВ проявляется периодически, но очень редко исчезает полностью. Большинство пациентов испытывают слабые симптомы болезни, которые время от времени сменяются обострениями с резко повышающейся усталостью, лихорадкой, сыпью, болью в суставах, отеками, выпадением волос, повышенной чувствительностью к свету и резкой потерей массы тела. После очередного обострения заболевание переходит в стадию ремиссии. 90% заболевших СКВ составляют молодые женщины. Объясняется это гормональными особенностями женского организма, повышенной склонностью к продукции глобулинов, а также теми процессами, которые происходят в матке во время менструации, – например, это возможное образование аутоантител к отторгающимся клеткам эндометрия.

Один из первых обзоров на тему «СКВ и беременность» был опубликован 60 лет назад – в 1955 г. В нем было проанализировано течение 87 беременностей при СКВ и констатировано, что в 47% случаев в период беременности отмечается обострение заболевания, которое может приводить к смерти пациентки. В течение нескольких десятилетий после того, как был сделан подобный вывод, женщинам с СКВ беременность не рекомендовалась – из-за риска не только обострения заболевания, но и потери плода. Однако улучшение диагностики болезни, разработка современных методов лечения и, как следствие этого, улучшение прогноза заболевания позволили ревматологам пересмотреть свои представления о возможности беременности при СКВ. И сегодня большинство пациенток благополучно вынашивают ребенка. Но для этого требуется решать проблему, так сказать, многопланово, с рассмотрением многих вопросов.
Актуальные задачи
А вопросов немало. Вот основные из них: взаимовлияние СКВ и беременности; влияние заболевания матери на развитие плода и здоровье будущего ребенка; возможность и безопасность применения лекарственных препаратов при беременности; особенности ведения родов у пациенток с СКВ; возможность грудного вскармливания ребенка при СКВ; безопасная контрацепция. Все это врачу и пациентке необходимо обсуждать еще на этапе планирования беременности.
Важный момент заключается в том, что фертильность – способность к зачатию и вынашиванию плода – у больных СКВ, как правило, не страдает. Некоторое снижение фертильности может наблюдаться лишь у пациенток с высокой активностью заболевания (но в этот период наступление беременности и не рекомендуется) или при вынужденной длительной терапии высокими дозами цитотоксических препаратов, например циклофосфана.
Моменты риска
Конечно, наличие серьезного хронического заболевания и необходимость постоянного приема лекарств будущей матерью повышают риск неблагоприятного течения заболевания в период беременности и осложнений последней. В первую очередь рискуют те, кто забеременел в то время, когда болезнь находилась в активной стадии. Риски следующие:
• преэклампсия – высокое артериальное давление и белок в моче характерны для примерно 13% беременных с СКВ (у всех беременных безотносительно диагнозов – от 3 до 8%), к группе риска относятся женщины с волчаночным нефритом;
• выкидыш – им заканчивается около 25% беременностей с СКВ (у всех беременных безотносительно диагнозов – 10–20%);
• преждевременные роды – у матерей с СКВ недоношенными рождаются около 25% детей, причем причиной преждевременного родоразрешения является не только заболевание, но и лекарственная терапия;
• нарушения роста плода – дети матерей с СКВ подвержены более высокому риску внутриутробной задержки роста, примерно в 15% беременностей с СКВ. При преэклампсии, а также при терапии стероидными или иммуносупрессивными препаратами во время беременности риск возрастает;
• образование тромбов в плаценте – у некоторых беременных с СКВ образуются антитела, приводящие к появлению в плаценте кровяных сгустков. Они препятствуют нормальному росту и функционированию плаценты и в итоге замедляют рост ребенка.
Однако все эти риски можно снизить до минимума, если запланировать наступление беременности на фоне отсутствия или снижения активности СКВ: при таком условии обострение наблюдается в 13–18% случаев и проявляется преимущественно кожными изменениями и болями в суставах. Оно не ухудшает исход беременности, которая, как правило, завершается родами в срок и рождением доношенного здорового ребенка. Напротив, если беременность не планируется и наступает при высокой активности болезни, протекающей с поражением почек, сердца, легких, центральной нервной системы, тогда частота обострений повышается до 60–70% и состояние может завершиться либо потерей плода, либо летальным исходом для самой пациентки. К тому же в этих случаях больная вынуждена принимать максимальные дозы глюкокортикоидов и других препаратов, увеличивающих риск лекарственных осложнений, неблагоприятных реакций, преждевременных родов. У таких пациенток поздний токсикоз развивается в 2,8 раза чаще, чем у здоровых беременных, артериальная гипертензия встречается у 37–56% больных, преждевременные роды отмечаются в 19–54% случаев, а частота кесарева сечения достигает 34%.
Опасные антитела
Среди факторов, способных негативно влиять на исход беременности при СКВ, особое значение придается позитивности по Ro/SSA- и/или La/SSB-антителам, которые обнаруживаются у 35% пациенток. Необходимо, планируя беременность, обладать четкой информацией на эту тему. Дело в том, что Ro/La-антитела способны передаваться от матери к плоду через плаценту, начиная с 14-й недели (процесс активизируется с 16–17-й недели), и могут вызывать развитие неонатальной волчанки (НВ). НВ – это редкое, пассивно приобретенное аутоиммунное заболевание, развивающееся у плода и у новорожденного, мать которого позитивна по Ro/La-антителам. Оно может проявляться двумя основными синдромами: поражением кожи и/или сердца (наиболее тяжелое его проявление – полная поперечная блокада сердца), иногда – с другими системными проявлениями. При этом поражение кожи отмечается у 7–16% новорожденных, а сердца – у 2% плодов и новорожденных. Если поражение кожи, нередко провоцируемое проведением ультрафиолетового облучения ребенка по поводу, например, желтухи новорожденного, может проходить самостоятельно, то развитие атриовентрикулярной блокады сердца может стать причиной гибели плода и показанием к досрочным родам
с последующей установкой искусственного водителя ритма у младенца.
Но не все так страшно. Своевременная диагностика этого состояния и необходимая коррекция проводимой терапии способны повлиять на течение и исход беременности. А переданные младенцу материнские антитела исчезают в течение первых 6 месяцев его жизни.
Другим неблагоприятным фактором является присутствие в организме матери антифосфолипидных антител (аФЛ), которые могут приводить к ранней или поздней потере беременности, развитию тяжелого позднего токсикоза беременности (преэклампсии и эклампсии) – состояния, опасного для жизни беременной. Поэтому среди беременных с СКВ в группу повышенного риска осложненного течения заболевания входят не только пациентки с поражением почек и центральной нервной системы, но также больные с сопутствующим антифосфолипидным синдромом (АФС), который диагностируется на основании наличия у пациентки в прошлом артериальных и/или венозных тромбозов, повторных случаев потери беременности и высоко/умеренно позитивных аФЛ.
Все выше сказанное определяет важность планирования беременности при СКВ. Незапланированная беременность, наступившая в период обострения СКВ, может негативно сказаться как на здоровье женщины, отягощая симптомы заболевания, так и на исходе беременности.
Планируем правильно

Итак, планирование беременности рекомендуется в период отсутствия или низкой активности СКВ, длящийся не менее полугода, считая от последнего обострения заболевания, а также на фоне приема низких доз основных лекарств, контролирующих активность болезни.
Прежде всего необходим тщательный контроль состояния беременной, который проводится в тесном контакте ревматолога, акушера-гинеколога (а при необходимости и врачей других специальностей) и пациентки в течение всего периода беременности и первое время после родов. Как правило, при беременности предполагается не менее 3 консультаций врача-ревматолога (по одному визиту в каждом триместре), во время которых проводится осмотр пациентки, сдаются анализы (клинический, биохимический и иммунологический анализ крови, общий анализ мочи, суточный анализ мочи на белок и др.), уточняется и проводится коррекция лекарственной терапии. Часто назначают и дополнительные исследования для контроля роста и развития плода – например, специфический анализ крови «на волчаночный антикоагулянт», помогающий контролировать тяжесть заболевания. Необходимы контроль артериального давления, ультразвуковое исследование для отслеживания роста ребенка, допплерометрия для выявления, соответствует ли норме поток крови через пуповину (особенно актуально в III триместре), фетальный мониторинг плода для проверки пульса ребенка и отслеживания признаков блокады сердца (если беременная имеет анти-Ro и анти-La антитела), нестрессовый тест для измерения частоты сердечных сокращений (ЧСС) ребенка в то время, когда он движется (на последних двух месяцах беременности), биофизический профиль для оценки развития ребенка и для определения, получает ли он достаточное количество кислорода в утробе матери.
При соблюдении перечисленных условий большинство беременностей при СКВ в настоящее время завершается благополучно. Многие женщины могут родить ребенка сами, если были тщательно обследованы и на момент родов не имеют симптомов СКВ. Правда, врачи нередко рекомендуют беременным с СКВ кесарево сечение. Основными показаниями для кесарева сечения могут быть сопутствующий АФС с поражением центральной нервной системы и поражение тазобедренных суставов с нарушением их функции.
Лекарственная терапия
Прием лекарств беременными с СКВ должен проходить с соблюдением двух основных принципов. Во-первых, спектр применяемых препаратов и их дозировки должны быть необходимыми и достаточными для подавления активности заболевания и обеспечения успешного протекания беременности, родов и послеродового периода; во-вторых, препараты должны минимально воздействовать на плод и его развитие.
Препаратами выбора для лечения беременных с СКВ являются преднизолон и метилпреднизолон (предпочтительно в дозах, не превышающих 15 мг/сут). Беременные не должны прекращать прием глюкокортикоидного
препарата (преднизолона или метипреда), и только врач-ревматолог может решить вопрос о дозе этих препаратов, согласно клинико-лабораторным показателям. Необоснованные отмена или изменение дозы чреваты обострениями СКВ или присоединением осложнений – высокого кровяного давления, диабета беременных, рецидивами хронических инфекций.
Исследования последних лет доказали большое значение приема аминохинолиновых препаратов (гидроксихлорохина) в предупреждении обострения СКВ в период беременности и после родов. Прием препарата рекомендуется в течение всей беременности.
Циклофосфан, метотрексат, микофенолата мофетил должны быть отменены до зачатия.
Лекарства с малоизученным действием на развитие беременности, плода и новорожденного (например, белимумаб, ритуксимаб) полностью отменяются.
Отдельного интереса заслуживает вопрос о возможности кормления ребенка грудью. Решается это индивидуально, и, как показывает опыт, при отсутствии активности СКВ и приеме низких доз глюкокортикоидов грудное вскармливание вполне возможно. Важно кормить малыша непосредственно перед приемом препаратов, чтобы он меньше получал их от мамы вместе с молоком.
А вот вопрос контрацепции у больных СКВ изучен недостаточно. Основной используемый метод – барьерный (презерватив, колпачки). Гормональная контрацепция может быть рекомендована лишь при неактивной СКВ и в отсутствие некоторых факторов: обострений СКВ в течение нескольких лет, антифосфолипидных антител в организме, а также высоких доз глюкокортикоидов в лекарственной терапии.
В завершение еще раз хочу подчеркнуть, что планирование беременности при СКВ, динамическое наблюдение у ревматолога и акушера-гинеколога с необходимой коррекцией терапии способствуют улучшению течения болезни в период беременности, успешным родам и последующему грудному вскармливанию. ■
Н.М. Кошелева,
ФГБНУ НИИР им. В.А. Насоновой
ПРОФИЛАКТИКА СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ ПРИ БЕРЕМЕННОСТИ
Правильное отношение к своему образу жизни во время беременности может помочь предотвратить вспышки заболевания и серьезно увеличить шансы родить здорового ребенка.
• Необходимо чаще и больше отдыхать. Все беременные нуждаются в продолжительном сне, а женщины с СКВ – еще больше.
• Нельзя долго находиться на солнце, особенно в весенне-летний сезон. Ультрафиолетовое излучение может вызвать обострение СКВ. Используйте также солнцезащитную одежду и крем от загара.
• Выполняйте рекомендации врача, не пренебрегайте никакими дополнительными обследованиями, даже если вам они кажутся лишними, так как вы себя чувствуете превосходно. Необходимо постоянно следить за появлением симптомов заболевания.
• Правильно питайтесь. Ешьте фрукты, овощи и цельные зерна – это обязательная часть здоровой диеты. Если у вас повышенное артериальное давление, снижайте количество употребляемой соли. Лучше всего обратиться к диетологу, который составит подробное меню с учетом вашего заболевания. Старайтесь придерживаться его.
• Никогда ничего не меняйте самостоятельно в своей лекарственной терапии.
Чтобы исследовать состояние у пациентов с СКВ, которые принимали или недавно прекратили принимать противомалярийные препараты, исследователи выявили 1573 потенциальных участника из долгосрочного наблюдательного когортного исследования в университетской клинике.
Из этой многочисленной группы было выделено 88 клинических случаев - пациентов, которые достигли клинической ремиссии в течение как минимум года и прекратили прием противомалярийной терапии.
Первая контрольная группа была представлена пациентами, которые достигли ремиссии и продолжали принимать лекарства. Также был произведен второй контроль, в результате чего общее количество участников исследования составило 173.
Все пациенты наблюдались не менее 2 лет.
Обострение СКВ было определено как любое увеличение показателей по шкале SLEDAI-2K, при значительном обострении – превышение нормы на 4 или более баллов.
Средний возраст исследуемых составил 44 года, средний возраст в контрольной группе - 46 лет.
Представителями обеих групп были преимущественно белокожие женщины.
Причины отмены препаратов включали собственную инициативу, ремиссию, а также токсическое повреждение сетчатки, кожи, слизистых оболочек и органов сердечно-сосудистой системы.
20 участников экспериментальной группы сообщили о неблагоприятных побочных эффектах противомалярийных препаратов, связанных с их высоким профилем токсичности.
Врачи также сравнили результаты 26 пожилых пациентов с волчанкой, которые принимали гидроксихлорохин в течение как минимум 5 лет до момента прекращения приема препарата, с 32 пациентами контрольной группы, которые продолжали принимать гидроксихлорохин на момент исследования.
Обострение СКВ произошло в 61,4% случаев по сравнению с 45,1% в контрольной группе (P = 0,002), причем наиболее распространенными вариантами обострений были обострения со стороны кожи и скелетно-мышечной системы.
После многомерного анализа риск обострения более чем в два раза возрастал у тех, кто прекратил лечение (отношение шансов, 2,26; 95% доверительный интервал, 1,24–4,11; P = 0,008).
Более чем в половине случаев (n = 46) противомалярийные препараты возобновляли после отмены, что в основном было связано с обострением заболевания.
Из группы пациентов, возобновивших лечение в связи с обострением СКВ: у 88% вновь был достигнут контроль над заболеванием \ произошло улучшение состояния, у оставшихся 12% случились новые обострения.
Из 88 пациентов 51 пациент резко прекратили прием терапии тогда, как 37 пациентов отмену препаратов производили постепенно.
У пациентов, придерживающихся постепенной отмены, было меньше обострений (45,9%) по сравнению с пациентами, прекратившими лечение внезапно (72,6%).
После многофакторного анализа риск обострения более чем в три раза увеличился для группы внезапной отмены лекарств (OR 3,42; 95% ДИ 1,26-9,26; P = 0,016).
Пациенты, снизившие дозу противомалярийных препаратов, позднее возобновили полноценную терапию по сравнению с группой резкой отмены лекарств (37,8% против 62,7%; P = 0,02).
Только у 5 пожилых пациентов из каждой группы - 19,2% в группе отмены и 15,6% в группе пролонгирования терапии произошел эпизод обострения СКВ (OR 1,28; 95% ДИ 0,31-5,30; P = 0,73). Большинство обострений были кожными и скелетно-мышечными по своей природе; ни в одной из групп не было развития серьезных патологических состояний.
Медленное снижение дозы или продолжение приема противомалярийных препаратов может помочь предотвратить обострение болезни у пациентов с СКВ, достигших клинической ремиссии в течение как минимум года.
У пожилых пациентов с СКВ, которые постепенно прекращают прием гидроксихлорохина, также отсутствует повышенный риск обострения болезни.

Новость
Знаменитый телесериал «Доктор Хаус» запоминается не только циничным и сварливым нравом главного героя — гения медицинской диагностики, — но и аутоиммунным заболеванием системной красной волчанкой, появляющейся там едва ли не в каждой серии и даже ставшей своеобразным рефреном сериала.
Автор
Редакторы
Системная красная волчанка — это мультифакторное заболевание, развивающееся на основе генетического несовершенства иммунной системы и характеризующееся выработкой широкого спектра аутоантител к компонентам клеточного ядра. Молекулярно-генетические основы болезни изучены довольно плохо, в связи с чем специфического лечения до сих пор не создано, а в основе проводимой в клинике патогенетической терапии лежат иммунодепрессанты — глюкокортикостероиды и цитостатики. И вот, после более чем 50 лет попыток разработать специфическое лечение волчанки, произошел сдвиг: Управление по контролю за качеством пищевых продуктов и лекарств США официально утвердило в качестве лекарства от волчанки препарат Бенлиста (Benlysta) на основе моноклональных антител, специфически блокирующих B-лимфоцит-стимулирующий белок (BLyS).
Системная красная волчанка (СКВ) — одно из самых распространённых аутоиммуных заболеваний, в основе которого лежит генетически обусловленное комплексное нарушение иммунорегуляторных механизмов. При заболевании происходит образование широкого спектра аутоантител к различным компонентам ядра клеток и формирование иммунных комплексов. Развивающееся в различных органах и тканях иммунное воспаление приводит к обширным поражениям микроциркуляторного кровяного русла и системной дезорганизации соединительной ткани [1], [2].
Патогенез СКВ
В патогенезе СКВ важное место отводится иммунным механизмам, многие аспекты которых, несмотря на интенсивное изучение, остаются невыясненными. СКВ характеризуется обескураживающей «пестротой» иммунологических феноменов, что связывают с изменением практически всех известных функций иммунокомпетентных клеток (рис. 1).

Рисунок 1. Патогенез СКВ
Волчанка во многом связана с нарушениями на уровне пролиферации различных клонов В-клеток, активируемых многочисленными антигенами, в роли которых могут выступать медицинские препараты, бактериальная или вирусная ДНК и даже фосфолипиды мембраны митохондрий. Взаимодействие антигенов с лейкоцитами связано либо с поглощением антигенов антиген-презентирующими клетками (АПК), либо с взаимодействием антигена с антителом на поверхности В-клетки.
В результате поочередной активации то T-, то B-клеток увеличивается продукция антител (в том числе, аутоантител), наступает гипергаммаглобулинемия, образуются иммунные комплексы, чрезмерно и неконтролируемо дифференцируются Т-хелперы. Разнообразные дефекты иммунорегуляции, свойственные СКВ, связаны также с гиперпродукцией цитокинов Th2-типа (IL-2, IL-6, IL-4, IL-10 IL-12).
Одним из ключевых моментов в нарушении иммунной регуляции при СКВ является затрудненное расщепление (клиренс) иммунных комплексов, — возможно, вследствие их недостаточного фагоцитоза, связанного, в частности, с уменьшением экспрессии CR1-рецепторов комплемента на фагоцитах и с функциональными рецепторными дефектами.
Распространённость СКВ колеблется в пределах 4–250 случаев на 100 000 населения; пик заболеваемости приходится на возраст 15–25 лет при соотношении заболевших женщин к мужчинам 18:1. Наиболее часто заболевание развивается у женщин репродуктивного возраста с увеличением риска обострения во время беременности, в послеродовом периоде, а также после инсоляции и вакцинации.
СКВ часто становится причиной инвалидности. В развитых странах в среднем через 3,5 года после постановки диагноза 40% больных СКВ полностью прекращают работать, — в основном, в связи с нейрокогнитивными дисфункциями и повышенной утомляемостью. К потере трудоспособности чаще всего приводят дискоидная волчанка и волчаночный нефрит.
Клинические проявления СКВ чрезвычайно разнообразны: поражение кожи, суставов, мышц, слизистых оболочек, лёгких, сердца, нервной системы и т.д. У одного пациента можно наблюдать различные, сменяющие друг друга варианты течения и активности заболевания; у большинства больных периоды обострения заболевания чередуются с ремиссией. Более чем у половины больных есть признаки поражения почек, сопровождающиеся ухудшением реологических свойств крови [4].
Поскольку молекулярные и генетические механизмы, лежащие в основе заболевания, до сих пор как следует не изучены, специфического лечения волчанки до недавнего времени не существовало. Базисная терапия основана на приёме противовоспалительных препаратов, действие которых направлено на подавление иммунокомплексного воспаления, как в период обострения, так и во время ремиссии. Основными препаратами для лечения СКВ являются:
- глюкокортикоиды (преднизолон, метилпреднизолон);
- цитостатические препараты (циклофосфамид, азатиоприн, метотрексат, мофетила микофенолат, циклоспорин).
«Я знаю пароль, я вижу ориентир»
В конце 1990-х в биофармацевтической компании Human Genome Sciences (Роквилл, Мэриленд, США) открыли молекулярный путь, «сузив» который, можно в какой-то степени сдержать развитие СКВ. В этом пути участвует белок, получивший название «стимулятор B-лимфоцитов» (или BLyS), — цитокин из семейства фактора некроза опухолей. Было обнаружено, что ингибирование BLyS позволяет несколько сдержать разыгравшуюся иммунную систему и уменьшить число колоний B-лимфоцитов, производящих аутоантитела, атакующие здоровые ткани.
Исследователи, желая специфически блокировать BLyS, сделали ставку на человеческое моноклональное антитело, разработанное совместно с английской биотехнологической фирмой Cambridge Antibody Technology, и названное белимумаб (belimumab). В начале марта 2011 года американское Управление по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) впервые за 56 лет одобрило препарат, предназначенный для специфического лечения системной красной волчанки. Эти препаратом стал Бенлиста — коммерческое название антитела белимумаба, производством которого уже занимается компания GlaxoSmithKline. До того FDA одобряла для терапии СКВ гидроксихлорохин — лекарство от малярии; было это в 1956 году.
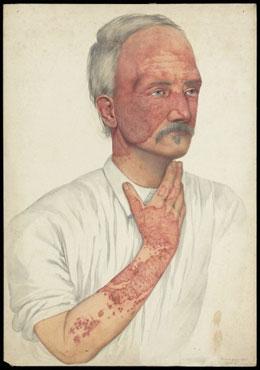
Рисунок 2. Человек, больной системной красной волчанкой (акварель 1902 года кисти Мэйбл Грин). Свое название заболевание получило ещё в средневековье, когда людям казалось, что характерная волчаночная сыпь на переносице напоминает волчьи укусы.
Дорога к этому свершению была долгой, потому что до 2009 года, когда белимумаб успешно прошел первые две фазы клинического тестирования, ещё ни одно лекарство против волчанки не добиралось до фазы III испытаний — рандомизированного мультицентрового исследования с участием большой популяции пациентов. (О процессе разработки лекарств и о клинических испытаниях см. «Драг-дизайн: как в современном мире создаются новые лекарства» [5].) Дело в том, что «строгая» система клинических проверок, основанная на идеологии доказательной медицины, просто не пропускала препараты-«кандидаты», оказывавшиеся на поверку просто неэффективными или опасными для здоровья пациентов.
«Под проекты разработки лекарств против волчанки было просто не получить финансирования, поскольку все знали, что эти разработки как одна проваливаются», — говорит Ричард Фьюри (Richard Furie), ревматолог из Нью-Йорка, руководивший клиническими исследованиями белимумаба. — «Люди открыто говорили: „вы никогда не добьетесь успеха [в клинических исследованиях]“» [6].
Целенаправленная терапия
Когда исследователи из Human Genome Sciences (HGS) открыли цитокин BLyS [7] на основе анализа генетической активности белых клеток крови, полной последовательности генома человека [8] еще не было. «Это было чудное время», — рассказал Дэвид Гилберт (David Hilbert), бывший руководитель исследований этой компании. — «Мы каждый день сидели над лимфоцитами и получали последовательности все новых и новых генов, про которые совершенно не было понятно, что они такое» [6].
В процессе исследования BLyS сотрудники HGS обнаружили, что количество этого цитокина сильно увеличивается при воспалении, а особенно — у больных волчанкой. Это была очень важная зацепка, хотя и было понятно с самого начала, что дорога предстоит нелёгкая, учитывая количество уже провалившихся клинических испытаний препаратов. Ситуация особенно осложнялась тем, что клинические проявления СКВ крайне разнообразны — от лёгкого дискомфорта у одних до тяжкого бремени на всю жизнь у других, — что и побудило, наверное, авторов «Доктора Хауса» включить волчанку в сериал в таком утрированном контексте.
Кстати, цитокину BLyS даже есть памятник, причем в процессе его синтеза на рибосоме: дочь основателя компании HGS, увлекающаяся молекулярной скульптурой [9], «позаимствовала» у отца белок для ваяния. Скульптура установлена в американском НИИ Колд Спринг Харбор.
Действие лекарств, селективно на молекулярном уровне «выключающих» некоторые ветви иммунитета, должно быть очень точным. Например, в 2008 закончились неудачей клинические испытания атацицепта (atacicept), ингибирующего не только BLyS, но и ещё один родственный белок. Тестирование на больных тяжелой формой волчанки — волчаночным нефритом — пришлось срочно прекратить из-за аномально высокого числа побочных инфекций у принимавших лекарство. Аналогичная ситуация была с антителом окрелизумабом (ocrelizumab), блокировавшим работу B-лимфоцитов по другому механизму.
Следующие на очереди
Белимумаб — только первое лекарство из находящихся на очереди в процессе тестирования у различных фармацевтических фирм (таких как Anthera, Eli Lilly и других). Часть разрабатываемых лекарств действуют также на BLyS, другие — ингибируют работу T-лимфоцитов, «атакуя» белок под «научным» названием B7-родственный белок, ещё один препарат ингибирует медиатор воспаления интерферон-γ. Самому же белимумабу пророчат светлое будущее — с точки зрения фармацевтических гигантов, это обозначает миллиардные продажи, выводящие препарат в заветный список «блокбастеров». Между прочим, это совершенно не обозначает полного излечения от болезни миллионам пациентов — эффективность препарата не такая уж и высокая (согласно официальной информации, помогает он одному пациенту из 11), тем более что тестирование проводили не на тяжелой форме заболевания [10]. Кроме того, белимумаб оказался неэффективен в лечении чернокожих пациентов. Впрочем, это все равно лучше, чем неспецифически «глушить» иммунитет пациентов. Жаль только, что большинству российских больных придется по старинке использовать преднизолон, хоть менее эффективный, но зато намного более дешевый, чем инновационный препарат «с пылу-жару».

Красная волчанка — это аутоиммунное заболевание. Симптомы волчанки включают: сыпь, эритему (часто эритема в форме бабочки), лишайник на лице (лишайниковая пластинка), гиперчувствительность к свету, артрит, изъязвление на слизистых оболочках.
Красная волчанка может встречаться в различных формах — наиболее распространёнными из них являются: системная красная волчанка и кожная красная волчанка, реже встречаются отёки.
Красная волчанка очень коварное и неприятное аутоиммунное заболевание. Его нелегко лечить и причины его возникновения не полностью известны.
Иногда волчанка ограничивается проявлением на коже (кожная красная волчанка — внешняя), но чаще всего она поражает весь организм, автоматически повреждая следующие органы: почки, сердце, лёгкие, нервную систему. Затем возникает системная красная волчанка (внутренняя).
Красная волчанка — симптомы
В 75 процентов случаев изменения сначала появляются на коже и слизистых оболочках. Они принимают форму сыпи (часто появляющейся после длительного пребывания на солнце), шелушащихся овальных пятен на коже головы или безболезненных язвах в полости рта.
Наиболее типичным симптомом волчанки является появление характерных пятен на щеках и носу.
Латинское название волчанки происходит от слова волчанка (волк), потому что на лице людей, страдающих этим заболеванием, есть характерная эритема — форма напоминает пятна (окрашивание меха) как на морде волка (иногда эритема может напоминать форму бабочки).
- боль в суставах;
- артрит;
- головные боли;
- изменения кожи;
- синдром Рейно — покраснение и кровоподтёки кожи рук;
- усталость и слабость в сочетании с потерей веса;
- септическая лихорадка;
- нарушение функции суставов (симптомы схожи с симптомами ревматоидного артрита).
Заболевания сердечно-сосудистой системы очень опасны своими последствиями. Это может привести к воспалению сердечной мембраны и инфаркту миокарда. Антитела, присутствующие в организме, которые повреждают клетки крови, также могут вызывать многочисленные гематологические нарушения.
Пациенты жалуются на выпадение волос, изменения на ногтях (часто ошибочно диагностируется микоз).
Диагностика волчанки
Диагностировать волчанку очень сложно — диагноз ставится до 60% случаев.
У пациентов с волчанкой изменения поражают дыхательную систему. Различают: острую и хроническую пневмонию, плеврит (воспаление, покрывающее лёгкие).
Волчанка также влияет на нервную систему, что может привести к хроническим головным болям, конвульсиям и даже нервно-психическим расстройствам. У многих пациентов волчанка поражает почки, что в крайних случаях может привести к полному повреждению почек.
Первые симптомы волчанки трудно уловить — в диагностике часто допускаются ошибки. Симптомы волчанки, как правило, очень разнообразны и могут напоминать другие заболевания. Вот почему постановка правильного диагноза может длиться годами.
Американское общество ревматологов разработало 11 критериев, из которых по меньшей мере четыре симптома говорят о диагнозе волчанка:
- эритема на лице;
- лишай;
- гиперчувствительность к солнечному свету;
- раны на слизистых оболочках;
- артрит;
- плеврит или перикардит;
- изменения в почках — от лёгких до очень тяжёлых;
- расстройства нервной системы;
- гематологические расстройства;
- иммунологические сбои;
- антиядерные антитела.
Причины возникновения
Причины волчанки до конца не выяснены, однако известно, что тенденция к развитию волчанки является наследственной. Волчанка является аутоиммунным заболеванием, которое означает, что организм, вместо того, чтобы защищаться от бактерий и вирусов, атакует собственные клетки и ткани.
Как часто возникает волчанка? Кому угрожает?
Волчанка очень редкая — болеют всего несколько десятков сотен тысяч человек. Мужчины болеют в девять раз реже.
Волчанка и беременность
При диагностике волчанки планирование беременности должно быть тщательно обсуждено с врачами и должно быть проведены специальные тесты.
Диагностированная волчанка не означает, что женщина не сможет забеременеть, однако, это заболевание увеличивает риск самопроизвольного аборта, а его симптомы усиливаются во время беременности. У детей и младенцев волчанка встречается крайне редко.
Читайте также:

