Белая кожа у новорожденных это всегда тяжелая патология
Обновлено: 29.04.2024

Бледность кожи у ребенка может зависеть от индивидуальных анатомо-гистологических особенностей кожи, низкого кровяного давления. Наиболее часто наблюдается бледность кожи вследствие анемии, недостаточности кровенаполнения периферических сосудов, отека. Так, недостаточная циркуляция крови в периферических сосудах может быть обусловлена уменьшением циркуляции крови на периферии (централизация кровообращения) или снижением сердечного выброса (острая левожелудочковая недостаточность при дифтерии — прививка от дифтерии ребенку — детская клиника «Маркушка», пневмонии, эндомиокардите, перикардите, стенозе устья аорты и др.). Непосредственными причинами бледности кожи могут быть гломерулонефрит, коллапс, шок, страх, холод, боль и др.
Диффузная бледность кожи у ребенка, детей
Диффузная бледность кожных покровов у ребенка, детей указывает на снижение гемоглобина в крови (нарушение образования эритроцитов: железодефицитная, гипо- и апластическая и другие анемии; острое или хроническое кровотечение: массивное или микрокровотечение; усиленное разрушение эритроцитов: гемолитическая анемия, гемоглобинопатии).
Бледность кожи ребенка, детей может быть связана с утолщением слоев тканей
Бледность кожи может быть связана с утолщением слоев тканей, лежащих над капиллярами, при отеках с тяжелой гипопротеинемией (гломерулонефрит, нефротический синдром, экссудативная энтеропатия, синдром мальабсорбции, ожоговая болезнь), гипотиреозе, гиповитаминозе А, конституционально обусловленном утолщении кожи.
Бледность кожи ребенка, детей: псевдоанемия
Важно отличать бледность кожи, связанную с изменением качественного или количественного состава крови, от бледности, обусловленной спазмом сосудов (псевдоанемии; при истинной анемии слизистые оболочки становятся бледными, при псевдоанемии остаются розовыми).
Бледность кожи ребенка, детей: оттенок
При некоторых состояниях бледность кожи у ребенка приобретает характерный оттенок: желтый — при гемолитической анемии; восковидный — при гипо- и апластических анемиях; цвета кофе с молоком — при инфекционном эндокардите; землисто-серый — при гнойносептических заболеваниях; зеленоватый — при хлорозе.
Бледность кожи может быть обусловлена дефицитом меланина при альбинизме, фенилкетонурии (болезнь Феллинга).

Цвет кожи ребенка определяется относительным содержанием в ней меланина, оксигемоглобина, восстановленного гемоглобина и каротина, толщиной рогового слоя, степенью кровоснабжения.
Меланин — основной пигмент, от которого зависит цвет кожи, волос и глаз
Меланин является основным пигментом, от которого зависит цвет кожи, волос и глаз (детский окулист — клиника «Маркушка»). Он выполняет функции фильтра, уменьшающего опасное воздействие на кожу ультрафиолетовых лучей и таким образом предотвращающего острую реакцию на солнечные ожоги и хроническое воздействие лучевой энергии. Цвет кожи определяется содержанием меланина в кератиноцитах, представляющих собой клетки-рецепторы меланинсодержащих органелл (меланосом), формируемых меланоцитами. Консультация детский дерматолог Москва — поликлиника «Маркушка».
Цвет кожи ребенка, детей определяется генетическими или конституциональными факторами: сохранение цвета и изменение
В норме цвет кожи детерминирован генетическими или конституциональными факторами и сохраняется на некоторых участках тела (область ягодиц), поскольку кожа не подвергается внешним воздействиям, или цвет ее изменяется под воздействием солнечных лучей (загар), в результате усиленной пигментации под влиянием гормонов, стимулирующих меланоциты.
Система меланоцитов состоит из самих меланоцитов (отросчатые клетки, функционально связанные с некоторыми кератиноцитами), локализующихся на границе дермы и эпидермиса, в волосяных луковицах, увеальном тракте, пигментном эпителии сетчатки, внутреннем ухе и мягкой мозговой оболочке. Эта система аналогична хромаффинной системе, клетки которой также являются производными нервного гребня и обладают биохимическими механизмами для гидроксилирования тирозина в ДОФА. Однако в хромаффинной системе ферментом служит не тирозиназа, а тирозингидроксилаза, а ДОФА превращается в адренохром, а не в тирозиномеланин.
У человека тирозиназа (медьсодержащая оксидаза) активирует процесс гидроксилирования тирозина в ДОФА и дофхинон. Ионы цинка активируют превращение дофахрома в 5,6-гидроксиндол, а меланосомы содержат цинк в высокой концентрации.
Пигментация зависит от четырех факторов: образования меланосом, их меланизации и секреции, непостоянной агрегации и разрушения меланосом во время их перехода в кератиноциты.
В увеальном тракте и пигментном эпителии сетчатки меланин защищает глаз от видимой и длинноволновой части лучистой энергии, тогда как ультрафиолетовая радиация задерживается роговицей.
Загар у ребенка, защита от ультрафиолетового излучения
У человека система защиты от ультрафиолетового излучения высоко развита, воздействие этой части электромагнитного спектра ведет к активации сложного механизма (загар) образования плотных, содержащих хромопротеин органелл (меланосомы) и их доставки к эпидермальным клеткам, внутри которых рассеивают и абсорбируют ультрафиолетовые лучи, удаляют обладающие повреждающим действием свободные радикалы, образующиеся в коже в результате воздействия ультрафиолетовой радиации.

Кожа ребенка, как и взрослого человека, состоит из эпидермы, дермы (собственно кожи) и гиподермы (подкожной клетчатки). Однако по своим морфологическим и функциональным особенностям она отличается значительным своеобразием, особенно у детей раннего возраста.
Хороший детский дерматолог Москва — поликлиника «Маркушка».
Эпидермис имеет очень тонкий роговой слой, состоящий из 2-3 рядов слабо связанных между собой и слущивающихся клеток, и активно разрастающийся основной слой. Основная перепонка, разделяющая эпидермис и дерму, у детей раннего возраста недоразвита, рыхла, вследствие чего при патологии эпидермис может отделяться от дермы пластами (десквамативная эритродермия). Для детской кожи особенно характерно хорошее кровенаполнение, связанное с густой сетью широких капилляров, что придает кожным покровам вначале ярко-розовый, затем нежно-розовый цвет.
Дерма состоит из сосочкового и ретикулярного слоев, в которых слабо развиты эластические, соединительнотканные и мышечные элементы.
Сальные, потовые железы у ребенка, волосы на голове новорожденных детей
Сальные железы у ребенка хорошо функционируют уже внутриутробно, образуя творожистую смазку, покрывающую его тело при рождении. У новорожденных и детей 1-го года жизни на коже лица заметны желтовато-белые точки — избыточное скопление секрета в кожных сальных железах. У детей, предрасположенных к экссудативному диатезу, на щеках образуется тонкая, так называемая молочная корка, а на волосистой части головы — гнейс (жирная себорея).
Потовые железы у новорожденных сформированы, но в течение первых 3-4 мес. жизни обнаруживается их некоторая функциональная недостаточность, что связано с несовершенством центра терморегуляции.
Волосы на голове новорожденных детей вполне развиты, но не имеют сердцевины, сменяются несколько раз на 1-м году жизни. Кожа на спине и плечах покрыта пушком, более выраженным у недоношенных. Брови и ресницы выражены слабо, рост их усиливается на 1-м году, а к 3-5 годам жизни они становятся, как у взрослых людей. Ногти обычно хорошо развиты и доходят до кончиков пальцев у доношенных новорожденных.
Подкожная жировая клетчатка у ребенка, детей
Состав подкожной жировой клетчатки у детей разных возрастов различен: у детей раннего возраста в ней содержится большее количество твердых жирных кислот (пальмитиновой и стеариновой) и меньше — жидкой олеиновой кислоты, что и обусловливает более плотный тургор тканей у детей 1 -го года жизни, более высокую точку плавления жира и наклонность к образованию локальных уплотнений и отека кожи и подкожной клетчатки с образованием склеремы и склередемы. Важно отметить, что состав подкожного жирового слоя у грудных детей близок по составу к жирам женского молока, поэтому они всасываются, минуя переваривание, в желудочно-кишечном тракте ребенка. Подкожный жир в различных частях тела ребенка имеет разный состав, чем и обусловлены своеобразие распределения и порядок накопления или исчезновения жирового слоя при похудении. Так, при накоплении жира отложение его происходит прежде всего на лице, потом на конечностях, туловище и затем на животе (здесь преобладают жидкие жирные кислоты). Исчезает подкожная клетчатка в обратном порядке.
Особенностью детей раннего возраста является наличие у них скоплений бурой жировой ткани в задней шейной области, супраилеоцекальной зоне, вокруг почек, в межлопаточном пространстве, вокруг магистральных сосудов. У доношенного новорожденного ее количество составляет около 1—3 % всей массы тела. Она обеспечивает более высокий уровень теплопродукции за счет так называемого несократительного термогенеза (не связанного с мышечным сокращением).
Малым количеством жировой клетчатки объясняется большая смещаемость внутренних органов у детей до 5-летнего возраста, так как только к этому возрасту увеличивается количество жира в грудной, брюшной полостях, в забрюшинном пространстве. Жировые клетки у детей раннего возраста мельче и содержат ядра, с возрастом они увеличиваются в размере, а ядра, наоборот, уменьшаются. Округлость форм тела у девочек обусловлена тем, что более 70 % жировой ткани приходится на подкожный жир, в то время как у мальчиков — лишь около 50 %.
Функции кожи у ребенка, детей: защитная, дыхательная, резорбционная
Функции кожи многообразны, но главная из них — защитная. У детей эта функция выражена слабо, о чем свидетельствуют легкая ранимость кожи, частая инфицируемость из-за недостаточной кератинизации рогового слоя и его тонкости, незрелости местного иммунитета (детский иммунолог — поликлиника «Маркушка») и обильного кровоснабжения. Эти особенности делают детскую кожу легкоранимой и склонной к воспалениям, в частности при плохом уходе (мокрые, грязные пеленки).
Дыхательная функция кожи у детей раннего возраста имеет большее значение, чем у взрослых. Кожа активно участвует в образовании ферментов, витаминов, биологически активных веществ. Тесно связаны между собой выделительная и терморегулирующая функции, которые становятся возможными лишь к 3—4 мес. при созревании нервных центров. До этого возраста плохая регуляция температуры тела связана с большой относительной поверхностью тела, хорошо развитой сетью сосудов, из-за чего новорожденный ребенок, особенно недоношенный, может легко перегреваться или переохлаждаться при недостаточном уходе.
Резорбционная функция кожи у детей раннего возраста повышена (тонкость рогового слоя, богатое кровоснабжение), в связи с чем следует осторожно применять лекарственные средства в мазях, кремах, пастах, так как накопление их может вызвать неблагоприятный эффект. Кожа является органом с многочисленными и разнообразными рецепторами, обеспечивающими осязательную, температурную, поверхностную болевую чувствительность.
Отеки кожи ребенка, детей
При осмотре кожи ребенка, детей обращается внимание на наличие отеков и их распространенность (на лице, веках, конечностях, общий отек или местный, истинный или слизистый).
Причины генерализованных отеков многообразны. К факторам, влияющим на развитие отеков, относятся: повышение гидростатического давления в сосудистом русле, что способствует усиленному пропотеванию жидкости через сосудистую стенку в межклеточное пространство (сердечная недостаточность — консультации детского кардиолога, портальная гипертензия, слипчивый перикардит, тромбофлебит и др.); снижение онкотического давления, обусловленное уменьшением содержания белка в сыворотке крови (нефротический синдром; общие отеки часто возникают при острых и хронических почечных заболеваниях, при сердечной недостаточности).
Развитию общего отека в случае сердечной недостаточности у детей предшествуют отечность нижних конечностей и увеличение печени. По мере развития декомпенсации отеки становятся более распространенными, сочетаются с накоплением жидкости в серозных полостях (плевральной, перикардиальной, брюшной). В отличие от отеков сердечного происхождения отеки при заболеваниях почек сначала возникают на лице, а затем захватывают все новые и новые участки кожи. Особенно массивные отеки наблюдаются при нефротической форме гломерулонефрита. Общие отеки алиментарного происхождения появляются при недостаточности в рационе белковой пищи (преимущественное питание мучной, углеводистой пищей), при общей дистрофии.
Алиментарные отеки могут появляться при тяжелых хронических заболеваниях (циррозе печени), при расстройствах процессов расщепления и всасывания в кишечнике (целиакии, дисахаридазной недостаточности и др.). Безбелковые отеки зависят от гидростатического давления, то есть более выражены в соответствующих частях тела, например, односторонний легочный отек у лежачих больных при вынужденном или предпочтительном положении.
Своеобразный отек кожи и подкожной жировой клетчатки наблюдается при гипотиреозе. Кожа при этом становится сухой и утолщенной, в надключичных ямках в виде «подушечек» располагаются муцинозные (слизистые) отеки. Стероидные отеки возникают при лечении кортикостероидами и АКТГ в высоких дозах, при синдроме Кушинга.
Распространенные отеки наблюдаются при отечной форме гемолитической болезни новорожденных.
Местные отеки, иногда массивные, наблюдаются после укусов насекомых, змей, особенно в тех случаях, когда ребенок имеет аллергическую настроенность (консультация детский аллерголог поликлиника «Маркушка»). Они возникают также вследствие ангионевротических расстройств, типичным проявлением которых является отек Квинке, локализующийся в любом месте: на губах, веках, ушных раковинах, языке, наружных половых органах и т.д. Реже отек Квинке локализуется в области голосовых связок, что приводит к синдрому острого стеноза гортани.
Изолированные отеки в области лица у детей бывают после приступов кашля при коклюше, после интенсивного растирания глаз. Известно, что локальная инфекция в области придаточных пазух носа, зубов, миндалин может вызвать затруднение оттока и застой лимфы в лимфатических узлах угла нижней челюсти и симулировать односторонний или двусторонний отек лица, который исчезает по мере стихания воспалительного процесса.
К редким причинам отека лица относятся начинающийся дерматомиозит, склеродермия и тромбоз кавернозного синуса. Наиболее часто в детской практике встречаются сердечные и почечные отеки.
Желтуха новорожденных – физиологическое или патологическое состояние, обусловленное гипербилирубинемией и проявляющееся желтушным окрашиванием кожи и видимых слизистых у детей в первые дни их жизни. Желтуха новорожденных характеризуется повышением концентрации билирубина в крови, анемией, иктеричностью кожных покровов, слизистых оболочек и склер глаз, гепато- и спленомегалией, в тяжелых случаях – билирубиновой энцефалопатией. Диагностика желтухи новорожденных основывается на визуальной оценке степени желтухи по шкале Крамера; определении уровня эритроцитов, билирубина, печеночных ферментов, группы крови матери и ребенка и др. Лечение желтухи новорожденных включает грудное вскармливание, инфузионную терапию, фототерапию, заменное переливание крови.
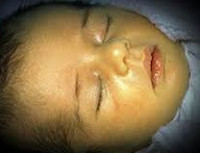
Общие сведения
Желтуха новорожденных – неонатальный синдром, характеризующийся видимой желтушной окраской кожи, склер и слизистых оболочек вследствие повышения уровня билирубина в крови ребенка. По наблюдениям, на первой неделе жизни желтуха новорожденных развивается у 60 % доношенных и 80% недоношенных детей. В педиатрии наиболее часто встречается физиологическая желтуха новорожденных, составляющая 60–70 % всех случаев синдрома. Желтуха новорожденных развивается при повышении уровня билирубина свыше 80-90 мкмоль/л у доношенных и более 120 мкмоль/л у недоношенных младенцев. Длительная или выраженная гипербилирубинемия оказывает нейротоксическое действие, т. е вызывает повреждение головного мозга. Степень токсического воздействия билирубина зависит, главным образом, от его концентрации в крови и длительности гипербилирубинемии.

Классификация и причины желтухи новорожденных
Прежде всего, неонатальная желтуха может быть физиологической и патологической. По происхождению желтухи новорожденных делятся на наследственные и приобретенные. На основании лабораторных критериев, т. е. повышения той или иной фракции билирубина различают гипербилирубинемии с преобладанием прямого (связанного) билирубина и гипербилирубинемии с преобладанием непрямого (несвязанного) билирубина.
К конъюгационным желтухам новорожденных относятся случаи гипербилирубинемии, возникающие вследствие пониженного клиренса билирубина гепатоцитами:
- Физиологическую (транзиторную) желтуху доношенных новорожденных
- Желтуху недоношенных новорожденных
- Наследственные желтухи, связанные с синдромами Жильбера, Криглера-Найяра I и II типов и др.
- Желтуху при эндокринной патологии (гипотиреозе у детей, сахарном диабете у матери)
- Желтуху у новорожденных с асфиксией и родовой травмой
- Прегнановую желтуху детей, находящихся на естественном вскармливании
- Медикаментозную желтуху новорожденных, обусловленную назначением левомицетина, салицилатов, сульфаниламидов, хинина, больших доз витамина К и др.
Гемолитическая желтуха новорожденных характеризуется повышением уровня билирубина вследствие усиленного разрушения (гемолиза) эритроцитов ребенка. К такого вида гипербилирубинемиям относят:
- Гемолитическую болезнь плода и новорожденных
- Эритроцитарные ферменто- и мембранопатии
- Гемоглобинопатию (серповидно-клеточную анемию, талассемию)
- Полицитемию
Механические желтухи новорожденных обусловлены нарушением отведения билирубина с желчью по желчным путям и кишечнику. Они могут возникать при пороках (атрезии, гипоплазии) внутрипеченочных и внепеченочных протоков, внутриутробной желчнокаменной болезни, сдавлении желчных ходов извне инфильтратом или опухолью, закупорке желчных протоков изнутри, синдроме сгущения желчи, пилоростенозе, кишечной непроходимости и пр.
Желтухи смешанного генеза (паренхиматозные) возникают у новорожденных с фетальным гепатитом, обусловленным внутриутробными инфекциями (токсоплазмозом, цитомегалией, листериозом, герпесом, вирусными гепатитами А, В, D), токсико-септическим поражением печени при сепсисе, наследственных заболеваниях обмена веществ (муковисцидозе, галактоземии).
Симптомы желтухи новорожденных
Физиологическая желтуха новорожденных
Транзиторная желтуха является пограничным состоянием периода новорожденности. Сразу после рождения ребенка избыток эритроцитов, в которых присутствует фетальный гемоглобин, разрушается с образованием свободного билирубина. Вследствие временной незрелости фермента печени глюкуронилтрансферазы и стерильности кишечника связывание свободного билирубина и его выведение из организма новорожденного с калом и мочой снижено. Это приводит к накоплению лишнего объема билирубина в подкожно-жировой клетчатке и окрашиванию кожи и слизистых в желтый цвет.
Физиологическая желтуха новорожденных развивается на 2-3 сутки после рождения, достигает своего максимума на 4-5 сутки. Пиковая концентрация непрямого билирубина составляет в среднем 77-120 мкмоль/л; моча и кал имеют нормальную окраску; печень и селезенка не увеличены.
При транзиторной желтухе новорожденных легкая степень желтушности кожных покровов не распространяется ниже пупочной линии и обнаруживается только при достаточном естественном освещении. При физиологической желтухе самочувствие новорожденного обычно не нарушается, однако при значительной гипербилирубинемии может отмечаться вялое сосание, заторможенность, сонливость, рвота.
У здоровых новорожденных возникновение физиологической желтухи связывается с временной незрелостью ферментных систем печени, поэтому не считается патологическим состоянием. При наблюдении за ребенком, организации правильного вскармливания и ухода проявления желтухи стихают самостоятельно к 2-хнедельному возрасту новорожденных.
Желтуха недоношенных новорожденных характеризуется более ранним началом (1–2 сутки), достижением пика проявлений к 7 суткам и стиханием к трем неделям жизни ребенка. Концентрация непрямого билирубина в крови недоношенных выше (137-171 мкмоль/л), его прирост и снижение происходит медленнее. Вследствие более длительного созревания ферментных систем печени у недоношенных детей создается угроза развития ядерной желтухи и билирубиновой интоксикации.
Наследственные желтухи
Наиболее распространенной формой наследственной конъюгационной желтухи новорожденных является конституциональная гипербилирубинемия (синдром Жильбера). Данный синдром встречается в популяции с частотой 2-6%; наследуется по аутосомно-доминантному типу. В основе синдрома Жильбера лежит дефект активности ферментных систем печени (глюкуронилтрансферазы) и, как следствие, - нарушение захвата билирубина гепатоцитами. Желтуха новорожденных при конституциональной гипербилирубинемии протекает без анемии и спленомегалии, с незначительным подъемом непрямого билирубина.
Наследственная желтуха новорожденных при синдроме Криглера-Найяра связана с очень низкой активностью глюкуронилтрансферазы (II тип) или ее отсутствием (I тип). При I типе синдрома желтуха новорожденных развивается уже в первые дни жизни и неуклонно нарастает; гипербилирубинемия достигает 428 мкмоль/л и выше. Типично развитие ядерной желтухи, возможен летальный исход. II тип синдрома, как правило, имеет доброкачественное течение: неонатальная гипербилирубинемия составляет 257-376 мкмоль/л; ядерная желтуха развивается редко.
Желтуха при эндокринной патологии
Обычно возникает у детей с врожденным гипотиреозом в связи с дефицитом гормонов щитовидной железы, нарушающим созревание фермента глюкуронозилтрансферазы, процессы конъюгации и экскреции билирубина. Желтуха при гипотиреозе выявляется у 50-70% новорожденных; проявляется на 2-3-й сутки жизни и сохраняется до 3-5 месяцев. Кроме желтухи, у новорожденных отмечается вялость, пастозность, артериальная гипотония, брадикардия, грубый голос, запоры.
Ранняя желтуха может возникать у новорожденных, матери которых страдают сахарным диабетом, вследствие гипогликемии и ацидоза. Проявляется затяжным желтушным синдромом и непрямой гипербилирубинемией.
Желтуха у новорожденных с асфиксией и родовой травмой
Гипоксия плода и асфиксия новорожденных задерживают становление ферментных систем, следствием чего является гипербилирубинемия и ядерная желтуха. Различные родовые травмы (кефалогематомы, внутрижелудочковые кровоизлияния) могут являться источниками образования непрямого билирубина и его усиленного проникновения в кровь с развитием желтушного окрашивания кожи и слизистых. Выраженность желтухи новорожденных зависит от тяжести гипоксически-асфиксического синдрома и уровня гипербилирубинемии.
Прегнановая желтуха
Синдром Ариеса, или желтуха детей, находящихся на естественном вскармливании, развивается у 1-2% новорожденных. Может возникать на первой неделе жизни ребенка (ранняя желтуха) либо на 7-14 день (поздняя желтуха новорожденных) и сохраняться 4-6 недель. Среди возможных причин прегнановой желтухи новорожденных называют присутствие в молоке материнских эстрогенов, препятствующих связыванию билирубина; неустановившуюся лактацию у матери и относительное недоедание ребенка, вызывающие обратное всасывание билирубина в кишечнике и его поступление в кровяное русло и др. Считается, что факторами риска желтухи у новорожденных, находящихся на грудном вскармливании, служат позднее (позже 12ч жизни) отхождение мекония, задержка пережатия пуповины, стимуляция родов. Течение такого вида желтухи новорожденных всегда доброкачественно.
Ядерная желтуха и билирубиновая энцефалопатия
При прогрессирующем повышении концентрации непрямого билирубина в крови может происходить его проникновение через гематоэнцефалический барьер и отложение в базальных ядрах головного мозга (ядерная желтуха новорожденных), обусловливающее развитие опасного состояния - билирубиновой энцефалопатии.
На первом этапе в клинике преобладают признаки билирубиновой интоксикации: вялость, апатия, сонливость ребенка, монотонный крик, блуждающий взгляд, срыгивания, рвота. Вскоре у новорожденных появляются классические признаки ядерной желтухи, сопровождающиеся ригидностью затылочных мышц, спастичностью мышц тела, периодическим возбуждением, выбуханием большого родничка, угасанием сосательного и других рефлексов, нистагмом, брадикардией, судорогами. В этот период, который длится от нескольких дней до нескольких недель, происходит необратимое поражение ЦНС. В течение последующих 2-3 месяцев жизни в состоянии детей наблюдается обманчивое улучшение, однако уже на 3-5 месяце жизни диагностируются неврологические осложнения: ДЦП, ЗПР, глухота и т. д.
Диагностика желтухи новорожденных
Желтуха выявляется еще на этапе пребывания ребенка в родильном доме врачом-неонатологом или педиатром при посещении новорожденного вскоре после выписки.
Для визуальной оценки степени желтухи новорожденных используется шкала Крамера.
- I степень – желтушность лица и шеи (билирубин 80 мкмоль/л)
- II степень – желтушность распространяется до уровня пупка (билирубин 150 мкмоль/л)
- III степень - желтушность распространяется до уровня коленей (билирубин 200 мкмоль/л)
- IV степень - желтушность распространяется на лицо, туловище, конечности, за исключением ладоней и подошв (билирубин 300 мкмоль/л)
- V - тотальная желтушность (билирубин 400 мкмоль/л)
Необходимыми лабораторными исследованиями для первичной диагностики желтухи новорожденных являются: билирубин и его фракции, общий анализ крови, группа крови ребенка и матери, тест Кумбса, ПТИ, общий анализ мочи, печеночные пробы. При подозрении на гипотиреоз необходимо определение тиреоидных гормонов Т3, Т4, ТТГ в крови. Выявление внутриутробных инфекций осуществляется методом ИФА и ПЦР.
В рамках диагностики механических желтух новорожденным проводится УЗИ печени и желчных протоков, МР-холангиография, ФГДС, обзорная рентгенография брюшной полости, консультация детского хирурга и детского гастроэнтеролога.
Лечение желтухи новорожденных
Для предотвращения желтухи и уменьшения степени гипербилирубинемии все новорожденные нуждаются в раннем начале (с первого часа жизни) и регулярном грудном вскармливании. У новорожденных с неонатальными желтухами частота рекомендуемых кормлений грудью составляет 8–12 раз в сутки без ночного перерыва. Необходимо увеличение суточного объема жидкости на 10-20% по сравнению с физиологической потребностью ребенка, прием энтеросорбентов. При невозможности оральной гидратации проводится инфузионная терапия: капельное введение глюкозы, физ. раствора, аскорбиновой кислоты, кокарбоксилазы, витаминов группы В. С целью повышения конъюгации билирубина новорожденному с желтухой может назначаться фенобарбитал.
Самым эффективным методом лечения непрямой гипербилирубинемии является фототерапия в непрерывном или прерывистом режиме, способствующая переводу непрямого билирубина в водорастворимую форму. Осложнениями фототерапии могут являться гипертермия, дегидратация, ожоги, аллергические реакции.
При гемолитической желтухе новорожденных показано заменное переливание крови, гемосорбция, плазмаферез. Все патологические желтухи новорожденных требуют незамедлительной терапии основного заболевания.
Прогноз желтухи новорожденных
Транзиторная желтуха новорожденных в подавляющем большинстве случаев проходит без осложнений. Однако нарушение механизмов адаптации может привести к переходу физиологической желтухи новорожденных в патологическое состояние. Наблюдения и доказательная база свидетельствуют об отсутствии взаимосвязи вакцинации от вирусного гепатита В с желтухой новорожденных. Критическая гипербилирубинемия может привести к развития ядерной желтухи и ее осложнений.
Дети с патологическими формами неонатальной желтухи подлежат диспансерному наблюдению участкового педиатра и детского невролога.
Пограничные состояния новорожденных – различные транзиторные изменения со стороны кожных покровов, слизистых оболочек и внутренних органов, развивающиеся у ребенка в первые дни после рождения и отражающие физиологическую перестройку организма. К пограничным состояниям новорожденных относятся родовая опухоль, простая и токсическая эритема, шелушение кожи, милии, физиологическая мастопатия, физиологический вульвовагинит, физиологическая желтуха, физиологический дисбактериоз, физиологическая диспепсия, мочекислый инфаркт и др. Пограничные состояния новорожденных наблюдаются неонатологом и не требуют специального лечения.
Общие сведения
Пограничные состояния новорожденных – физиологические реакции, отражающие естественную адаптацию организма новорожденного к внеутробному существованию в неонатальном периоде. В педиатрии пограничные состояния новорожденных расцениваются как переходные, транзиторные, которые сохраняются не дольше 3-х недель (у недоношенных младенцев – 4-х недель) и представляют для этого возраста физиологическую норму. В большинстве случаев пограничные состояния новорожденных самостоятельно исчезают к концу неонатального периода, однако, при нарушении адаптивных возможностей организма ребенка, дефектах ухода, неблагоприятных условиях окружающей среды физиологические процессы могут перерастать в патологические, требующие лечения.
Сразу после рождения ребенок попадает в совершенно иные условия существования, нежели те, что окружали его весь период внутриутробного развития. Организм крохи вынужден адаптироваться к значительно более низкой температурной среде; воспринимать зрительные, слуховые и тактильные раздражители; приспосабливаться к новому типу дыхания, питания и выделения и т. д., что ведет к развитию изменений в различных системах организма, т. е. пограничных состояний новорожденных.
Рассмотрим основные пограничные состояния новорожденных: их причины, проявления и патологические процессы, к которым они предрасполагают. О физиологической желтухе новорожденных подробнее можно прочесть здесь.

Синдром «только что родившегося ребенка»
Данное пограничное состояние новорожденных развивается под воздействием выброса различных гормонов в организме ребенка во время родов и большого количества раздражителей (свет, звук, температура, гравитация – т. н. «сенсорная атака»). Это обусловливает первый вдох, первый крик, сгибательную (эмбриональную) позу новорожденного. В первые минуты после рождения ребенок ведет себя активно: ищет сосок, берет грудь, однако спустя 5-10 минут засыпает.
При неблагоприятных обстоятельствах может развиваться нарушение кардиореспираторной адаптации (кардиореспираторная депрессия) – угнетение жизненно-важных функций в первые минуты и часы жизни.
Физиологическая убыль массы тела
Настоящее пограничное состояние новорожденных отмечается в первые дни и достигает максимальных показателей к 3-4 дню жизни - от 3 до 10% от первоначального веса у здоровых новорожденных. У доношенных детей восстановление массы тела происходит к 6-10 дню (75-80%); у недоношенных – ко 2–3 неделе жизни. Первоначальная потеря массы тела связана с установлением лактации у матери (дефицитом молока), выделением мочи и кала, подсыханием пуповинного остатка у новорожденного и пр. Залогом восстановления и хорошей прибавки массы тела служит раннее прикладывание к груди, естественное вскармливание, кормление «по требованию». При потере более 10% массы тела говорят о гипотрофии у ребенка.
Изменения со стороны кожных покровов
К данной группе пограничных состояний новорожденных относятся простая эритема, токсическая эритема, милии, шелушение кожных покровов.
Под простой эритемой понимают диффузную гиперемию кожных покровов новорожденного, развивающуюся после удаления первородной смазки вследствие адаптации кожи к новым факторам окружающей среды (воздуху, свету и др.). Выраженная гиперемия сохраняется 2-3 дня и полностью исчезает к исходу 1-й недели. По мере исчезновения эритемы развивается мелкопластинчатое или крупнопластинчатое шелушение кожи, более выраженное на груди, животе, ладонях и стопах у детей, рожденных от переношенной беременности. Лечения данных пограничных состояний новорожденных не требуется; на участки обильного шелушения кожи после купания можно наносить стерильное растительное масло или специальную детскую косметику.
Примерно у трети новорожденных на 2-5-й сутки жизни развивается пограничное состояние, расцениваемое как токсическая эритема. При этом на коже появляются эритематозные пятна с пузырьками, содержащими прозрачную серозную жидкость с большим количеством эозинофилов. Излюбленная локализация элементов – кожа в области суставов, груди, ягодиц. Токсическая эритема обычно регрессирует через 2-3 дня, однако может возобновляться в течение первого месяца жизни. Поскольку в основе токсической эритемы лежит аллергическая реакцию на материнские белки, при выраженных проявлениях или затяжном течении педиатр может назначить ребенку обильное питье и прием антигистаминных препаратов.
Милии (милиа, белые угри) после рождения присутствуют у половины новорожденных. Они представляют собой мелкие пузырьки, содержащие молочно-белый или бело-желтоватый секрет. Милии образуются вследствие закупорки выводных протоков сальных желез; чаще располагаются в области носа и лба; исчезают без лечения в течение 1-2 недель.
Неудовлетворительный уход за кожными покровами новорожденного при данных пограничных состояниях может способствовать развитию инфекционных заболеваний кожи.
Гормональный (половой) криз
Эта группа пограничных состояний новорожденных включает физиологический мастит, десквамативный вульвовагинит у девочек, водянку оболочек яичек у мальчиков. Возникновение полового криза у 2/3 новорожденных связано с действием материнских эстрогенов, получаемых плодом в последние месяцы беременности.
Физиологический мастит (мастопатия) – пограничное состояние новорожденных, характеризующееся нагрубанием молочных желез, гиперемий кожи над ними и выделением молозивоподобного секрета. Данное состояние отмечается у большинства девочек и 50% мальчиков; сохраняется с 3-4-го дня до конца 2-3-й недели жизни. Лечение физиологического мастита не проводится; в случае выраженного набухания молочных желез может быть рекомендовано наложение на грудные железы стерильной повязки. Категорически воспрещается надавливание на молочные железы новорожденного из-за опасности развития инфекционного мастита.
Десквамативный вульвовагинит – пограничное состояние новорожденных девочек, сопровождающееся появлением слизистых или кровянистых выделений из половой щели. Выделения отмечаются у 60-70% девочек в первые три дня жизни и продолжаются 1-3 дня. В 5-7% случаев может развиваться метроррагия в объеме, не превышающем 1-2 мл, что связано с прекращением действия эстрогенов матери. Лечение сводится к проведению туалета наружных половых органов девочки.
У 5–10% мальчиков в период новорожденности развивается гидроцеле, которое проходит самостоятельно, без лечения.
Переходные изменения стула
Переходные изменения стула на первой неделе жизни возникают практически у всех новорожденных. К данной группе пограничных состояний новорожденных относятся транзиторный дисбактериоз кишечника и физиологическая диспепсия. После отхождения в первые 1-2 дня мекония (первородного кала), имеющего вид густой вязкой массы темно-зеленого цвета, стул у ребенка становится частым. Переходный стул имеет негомогенную консистенцию с примесью комочков и слизи, окраску с чередованием участков темно-зеленого и желто-зеленого цвета. При исследовании копрограммы обнаруживается большое количество лейкоцитов, слизи, жирных кислот. К концу первой недели стул приобретает гомогенную кашицеобразную консистенцию и более однородную желтую окраску. Одновременно с очищением кишечника происходит его заселение бифидо- и лактофлорой.
Отсутствие выделения мекония может свидетельствовать об атрезии прямой кишки или кишечной непроходимости у новорожденного, что требует немедленной консультации детского хирурга. При нарушении формирования микробного пейзажа кишечника развивается истинный дисбактериоз.
Изменения функции почек
К пограничным состояниям новорожденных, характеризующим адаптацию органов мочевыделительной системы к новым условиям, относят транзиторную олигурию, альбуминурию и мочекислый инфаркт новорожденного.
При транзиторной олигурии, свойственной всем здоровым новорожденным в первые 3 суток жизни, отмечается уменьшение выделения мочи. Причинами данного явления служат снижение поступления в организм жидкости и с особенности гемодинамики.
Отмечаемая альбуминурия (протеинурия) вызвана увеличением проницаемости фильтрационного барьера, капилляров и канальцев почек, усиленным гемолизом эритроцитов.
Патогенез мочекислого инфаркта связан с отложением солей мочевой кислоты в просвете почечных канальцев, что приводит к окрашиваю мочи в красноватый цвет и появлению на пеленках коричнево-красных разводов. При исследовании общего анализа мочи обнаруживаются зернистые и гиалиновые цилиндры, эпителий, лейкоциты. При мочекислом инфаркте необходимо следить за адекватным потреблением жидкости и выделением мочи новорожденным. Если данное пограничное состояние у новорожденного не исчезает самостоятельно, примерно с 10-го дня жизни изменения мочи расцениваются как патологические, требующие консультации детского уролога и проведения УЗИ почек ребенку.
Неблагоприятное протекание данных пограничных состояний новорожденных может послужить основой для последующего развития дисметаболической нефропатии, инфекций мочевыводящих путей, мочекаменной болезни.
Прочие пограничные состояния новорожденных
В числе других пограничных состояний новорожденных, прежде всего, следует рассмотреть транзиторные нарушения теплового обмена – гипотермию и гипертермию. Поскольку рождение ребенка знаменуется переходом в иную окружающую среду, температура которой на 12-15°C ниже внутриутробной, в первый час жизни у новорожденного отмечается транзиторная гипотермия (снижение температуры тела до 35,5-35,8°C и ниже). Через несколько часов температуры тела повышается и стабилизируется.
Кроме этого, к пограничным состояниям новорожденных относят открытый артериальный проток и открытое овальное окно, которые описаны в соответствующих обзорах.
Читайте также:

