Андрогенизация кожи что это
Обновлено: 17.04.2024
Андрогензависимая дерматопатия – это симптомокомплекс воздействия на кожу мужских половых гормонов (андрогенов) при их избыточной продукции в организме. Таким образом, андрогензависимая дерматопатия – это кожные симптомы гиперандрогении, проявляющиеся чаще - гирсутизмом и акне, реже - себореей и алопецией (выпадением волос). Этот симптомокомплекс можно считать не только медицинской, но и социально-экономической проблемой, так как приводит к развитию психоэмоциональных реакций, снижающих качество жизни женщины и, как следствие, ограничения в выборе профессии и трудоустройстве.
Гирсутизм – это избыточный рост волос по мужскому типу, то есть в строго определенных местах - в андрогензависимых участках кожи, характерных для мужчин. В отличие от гирсутизма, равномерный избыточный рост волос по всему телу называется – гипертрихоз. Гипертрихоз никакого отношения к влиянию андрогенов не имеет. Андрогензависимыми считают следующие участки кожи: верхняя губа, бакенбарды, подбородок, окружность сосков, белая линия живота – нижняя часть живота от пупка до лонной кости, грудь, внутренняя поверхность бедер, поясница. Не относится к андрогензависимым областям предплечья и голени, поэтому избыточный рост волос на этих участках рассматривается как гипертрихоз.
Акне – это угревая сыпь, возникающая из-за избыточной продукции кожного сала под влиянием андрогенов, наиболее часто локализованные на коже лица, груди и верхней части спины.
Источником повышенной продукции андрогенов являются яичники и (или) надпочечники, жировая ткань (висцеральная), уменьшение образования половых стероидосвязывающих глобулинов (специальные белки, связывающие половые гормоны в крови) и, как следствие, увеличение уровня свободных биологически активных андрогенов.
Эти симптомы сопровождают нейроэндокринные синдромы и отмечаются с пубертатного возраста – времени активации гормональной функции яичников и надпочечников. У молодых женщин именно эта симптоматика является основной жалобой, которая приводит их к косметологу, а не такие признаки гиперандрогении, как нерегулярный цикл и бесплодие, с которыми нужно обращаться к гинекологу.
Андрогензависимая дерматопатия, как правило, наблюдается при таких нейроэндокринных синдромах, как адреногенитальный синдром (ВДКН), синдром поликистозных яичников (СПКЯ), метаболический синдром (МС), но может быть и следствием генетически обусловленной повышенной чувствительности волосяных фолликулов и сальных желез к нормальному уровню андрогенов, что имеет место у некоторых этнических групп населения (Кавказ, Средиземноморье).
Степень развития андрогензависимой дерматопатии обусловлена не только содержанием в крови андрогенов, но и их периферическим метаболизмом. На рост волос и состояние сальных желез влияет самый активный андроген, метаболит тестостерона, который образуется под влиянием фермента 5а-редуктазы в коже на уровне волосяных фолликулов и рецепторов сальных желез. Андрогены способствуют превращению тонких и светлых пушковых волос в терминальные волосы – более темные и толстые.
Диагностика, как правило, трудностей не представляет. Диагноз устанавливается при осмотре, подтверждается повышенным уровнем андрогенов в крови.
Лечение является достаточно сложной задачей. Это обусловлено не только особенностями роста волос на андрогензависимых участках тела, но и многофакторными причинами гиперандрогении.
Цикл роста волоса длительный, в среднем 6-7 месяцев, поэтому раньше, чем через 3-6 месяцев от начала лечения эффект не очень значительный и характеризуется уменьшением терминальных волос. В начале лечения возможно только предотвратить дальнейший рост волоса, то есть его переход из первородного (пушкового) в терминальный. Положительные результаты в лечении гирсутизма отмечаются у большинства пациенток через 9 месяцев, максимально - в течение 1-2 лет.
Препараты, применяемые для лечения андрогензависимой дерматопатии, действуют на биосинтез, метаболизм и периферическую конверсию (утилизацию) андрогенов на уровне рецепторов кожи.
Механизм их действия:
- уменьшение продукции андрогенов в яичниках;
- уменьшение продукции андрогенов в надпочечниках;
- блокада периферического действия андрогенов;
- блокада рецепторов андрогенов в тканях-мишенях;
- блокада ферментов периферического превращения тестостерона в его метаболит.
Для лечения вышеперечисленных нейроэндокринных синдромов также используется
метаболическая терапия, включающая снижение массы тела и гиперинсулинемии, с помощью препаратов, повышающих чувствительности периферических тканей к инсулину. В комплексном лечении андрогензависимой дерматопатии такая терапия является обязательной у пациенток с СПКЯ и ожирением. Терапия антиандрогенами менее эффективна при ожирении, чем у пациенток с нормальной массой тела. Иногда для лечения используется хирургическое лечение, связанное с уменьшением андрогенсекретирующей ткани яичников, нормализации гонадотропной функции головного мозга и эффективно уменьшает симптомы андрогензависимой дерматопатии у пациенток с СПКЯ.
Для избавления от лишних волос с успехом применяются косметологические процедуры, включающие использование различных методов эпиляции.
Однако, лечение андрогензависимой дерматопатии только у косметолога в большинстве случаев малоэффективно. Правильнее, когда грамотные косметологи направляют таких пациенток на консультацию к гинекологу-эндокринологу для уточнения источника повышенной продукции андрогенов или избыточной чувствительности волосяных фолликулов и сальных желез к нормальному влиянию андрогенов. Коррекция гормонального профиля в сочетании с косметическими процедурами является абсолютно правильным подходом к лечению андрогензависимых дерматопатий.
Применение различных методов эпиляции на фоне медикаментозной терапии дает прекрасный эффект, препятствуя росту новых волос, так как одно медикаментозное лечение гирсутизма направлено на блокаду роста новых волос, но не стабилизирует их рост, поэтому наиболее эффективным является назначение лечения в молодом возрасте и в сочетании с косметическими методами. При выборе препаратов для лечения необходимо учитывать их побочное действие и переносимость, поскольку эффективность повышается соответственно длительности приема тех или иных препаратов.
При объединении усилий двух специалистов: гинеколога-эндокринолога и дерматолога удается добиться наиболее значимого и стойкого эффекта в лечении андрогензависимой дерматопатии.
Проведение коррекции диагностированных нарушений репродуктивной функции у пациенток с гиперандрогенией, с учетом показателей метаболизма андрогенов, позволяет достичь нормализации гормонального профиля, менструальной функции, стойкого восстановления функционального состояния репродуктивной системы, а так же улучшения качества жизни и социально-психологического состояния женщины.
Что такое андрогенная алопеция (облысение у женщин)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Побилат Анны Евгеньевны, дерматолога со стажем в 19 лет.
Над статьей доктора Побилат Анны Евгеньевны работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
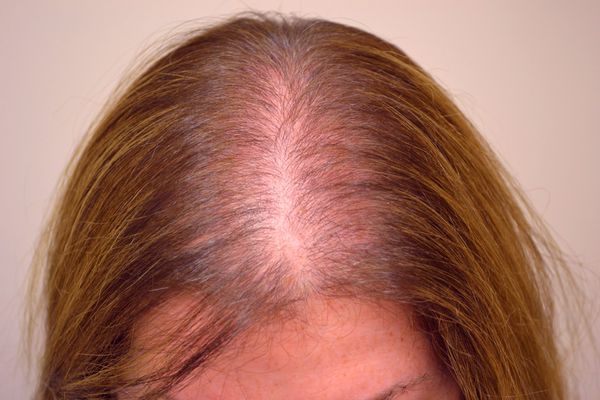
Андрогенетическая алопеция (АГА) — это поредение волос, в основе которого лежит прогрессирующее уменьшение волосяных фолликулов [1] . АГА относится к нерубцовой форме алопеции, при которой отсутствует предшествующее повреждение кожи и рубец в очаге поражения. Это сложное состояние, к которому приводит влияние множества факторов и генов. Андрогенетическая алопеция поражает до 80 % мужчин и 42 % женщин [2] . Вероятность выпадения волос по этому типу у женщин увеличивается с возрастом, достигая у европеоидов к 70 годам 40 % [3] . Развитие заболевания сопровождается интенсивными переживаниями [4] .
Генетическое наследование при андрогенетической алопеции до сих пор остаётся неясным. Вероятнее всего, тип наследования является полигенным (обусловлен влиянием сочетания нескольких генов). Согласно недавним исследованиям, раннее начало заболевания (до 30 лет) связано с геном рецептора андрогена EBA2R на Х-хромосоме [14] . Также изучалось влияние мутации в гене, определяющем работу ароматазы (фермента, который трансформирует андрогены в эстрогены), оно было признано значимым [15] , но не подтвердилось в более позднем исследовании [16] .
Анализ данных репликации (процесса создания дочерних молекул ДНК на основе родительской молекулы ДНК) выявил четыре наиболее значимых локуса (местоположения гена на карте хромосомы) риска для AGA на хромосомах 2q35, 3q25. 1, 5q33.3 и 12p12.1. Самый сильный сигнал был получен для rs7349332 на хромосоме 2q35, который находится в WNT10A. Таким образом, исследования экспрессии в ткани фолликула человеческого волоса показывают, что ген WNT10A играет важную роль в развитии андрогенетической алопеции [18] .
Заболевание может как быть симптомом системной патологии, так и сочетаться с другими состояниями. Оно сопровождает другие кожные или общие признаки гиперандрогении (повышенное содержание мужских половых гормонов), такие как гирсутизм, акне, нерегулярные менструации, бесплодие, галакторею (выделение молока вне периода грудного вскармливания) и инсулинорезистентность. Наиболее распространённой эндокринологической патологией, связанной с АГА, является синдром поликистозных яичников (СПКЯ).
Еще одной важной ассоциацией с АГА является метаболический синдром — нарушенный углеводный обмен, повышающий риск развития патологии сердечно-сосудистой системы. Корейские учёные, изучив 1701 пациентку, доказали положительную статистическую связь между АГА и метаболическим синдромом [28] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы андрогенной алопеции (облысении у женщин)
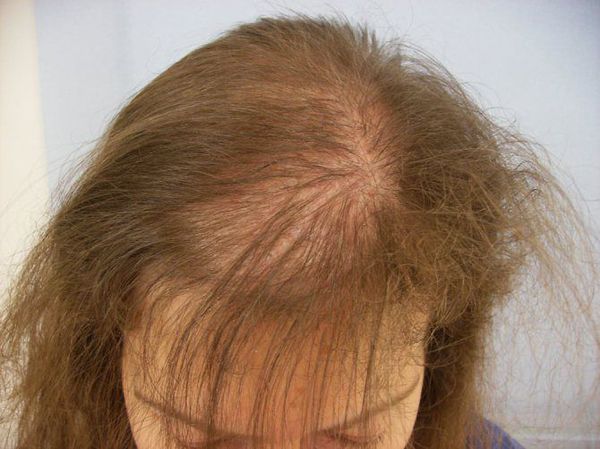
Нормальным считается выпадение 60 – 80 волос в день, при котором они не становятся тоньше и их объём не меняется. При алопеции пациенты жалуются на прогрессивное истончение волос, сокращение их объёма и на непрерывное или скачкообразное выпадение. Заболевание у женщин прогрессирует медленнее, чем у мужчин, и обычно равномерно поражает волосистую часть головы. У женщин алопеция развивается позднее, чем у мужчин, но может начаться и в подростковом возрасте. Первые проявления заболевания почти незаметны [3] .
Патогенез андрогенной алопеции (облысении у женщин)
Волосяные фолликулы постоянно находятся в циклическом процессе смены фаз. Выделяют три фазы:
- анаген — период роста;
- катаген — переход от одной стадии к другой;
- телоген — период покоя.
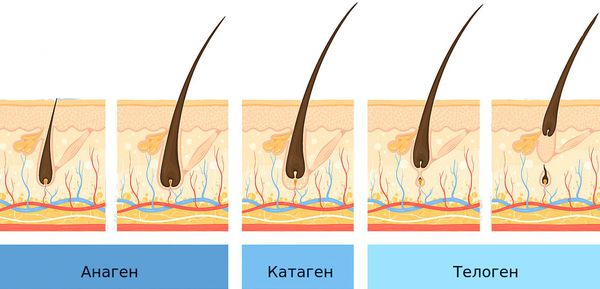
Продолжительность фазы роста (анагена) определяет длину волос. Большинство волос на коже головы (85-90 %) находятся в фазе анагена, которая длится примерно 2-6 лет. Оставшаяся часть волос (10-15 %) находятся в фазе телогена — фазе покоя волосяных фолликулов, которая длится около трёх месяцев. Волос в это время можно сравнить с цветком, который находится в вазе. Он срезан, не растёт, ни сцеплен с вазой, но и не может её оставить. В конце фазы телогена волос покидает фолликул.
Волосы могут различаться по диаметру и длине стержня, выделяют пушковые и терминальные волосы. Пушковые волосы (vellus) тоньше и короче терминальных, лишены пигментации. При заболевании волосяные фолликулы уменьшаются и происходит превращение терминальных фолликулов в веллусоподобные. Эти веллусоподобные фолликулы имеют укороченный цикл волос — фаза анагена у них меньше и они производят короткие и тонкие волосяные стержни.
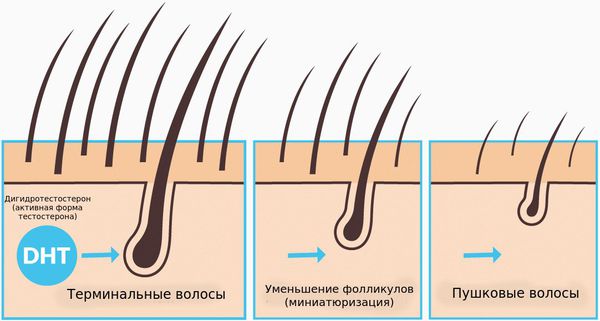
В отличие от мужчин, уменьшение фолликулов у женщин происходит неравномерно и не так интенсивно, поэтому, за исключением редких случаев, у них не появляются области полного облысения [5] .
У некоторых женщин с андрогенетической алопецией выявляют изменённый метаболизм андрогенов, зачастую — избыток, но не во всех случаях. Сывороточный тестостерон у большинства пациенток находится в пределах нормы [6] [7] [8] .
Заболевание у пациенток с нормальным содержанием мужских половых гормонов может возникать из-за повышенной чувствительности волосяного фолликула к нормальному уровню андрогенов. Причина этого может быть в большом количестве рецепторов к андрогенам и сниженной активности ароматазы (фермента, трансформирующего андрогены в эстрогены).
Алопеция также развивается у людей с синдромом нечувствительности к андрогенам или дефицитом 5-альфа-редуктазы (фермента, участвующего в метаболизме стероидов) [9] . Это указывает на то, что андрогенетическая алопеция у женщин, в отличие от мужского выпадения волос, может развиваться даже в отсутствие андрогенов.
Недавнее исследование показало, что лечение андрогенами может улучшить состояние волос у некоторых женщин. В течение года исследовалось влияние подкожных имплантатов тестостерона на частоту развития рака молочной железы у пациенток в пре- и постменопаузе. Большинство женщин (63 %), которые жаловались на истончение волос, сообщили о положительной динамике [10] . Таким образом, гиперандрогения (повышенное содержание мужских половых гормонов — андрогенов) сама по себе не обязательно приводит к андрогенетической алопеции [11] . Механизм воздействия андрогенов на волосы, вызывающий алопецию, связан с преждевременным старением волосяных фолликулов и усилением выработки цитокинов ( белки клеток иммунной системы, которые обеспечивают межклеточные взаимодействия ), сокращающих продолжительность фазы анагена [12] [13] .
Андрогенетическая алопеция усугубляется диффузной телогеновой алопецией, возникающей вследствие приёма некоторых лекарств, стресса, резкой потери веса, гормональной перестройки (например, родов) и терапии препаратами с проандрогенными эффектами, такими как норэтистерон, леворногестрел и тиболон.
Классификация и стадии развития андрогенной алопеции (облысении у женщин)
Андрогенетическая алопеция у женщин протекает иначе, чем у мужчин — сохраняется линия волос в области лба, выпадение равномерное в пределах лобно-теменной зоны и не настолько выраженное [19] .
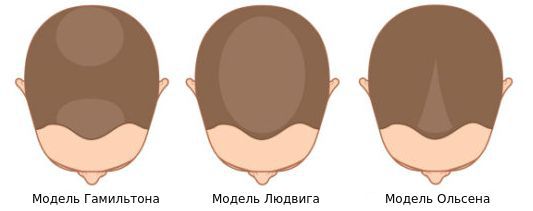
Выделяют три модели андрогенетической алопеции:
- модель Гамильтона — истончение и поредение волос в теменной зоне и расширение лобно-височных углов, скорее характерное для мужчин, которое наблюдается у женщин в менопаузе или с гиперандрогенией;
- модель Людвига — обширное истончение волос в пределах макушки с сохранением линии роста волос в области лба;
- модель Ольсена или "рождественской ёлки" — истончение и поредение волос центральной части головы с поражением линии роста волос в области лба.
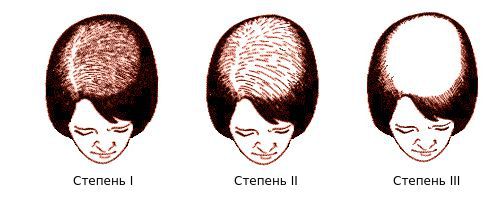
Осмотрев 468 пациенток, немецкий дерматолог Людвиг выделил три степени поредения волос лобно-теменной зоны [20] [21] :
- Заметное истончение волос и расширение пробора.
- Выраженное разрежение волос.
- Волосы полностью утрачены (встречается менее, чем у 5 % женщин).
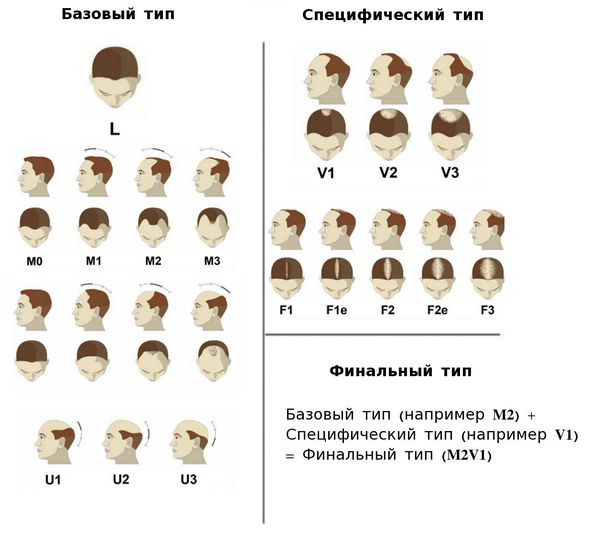
В 2007 году Ли и соавторы предложили базовую и специфическую (BASP) систему классификации, которая представляет собой усовершенствованный вариант классификации Норвуд — Гамильтона и включает четыре базовых типа (L, M, C, U) и два специфических типа (F и V) [22] .
Следует учитывать, что у женщины с паттерном по Людвигу после менопаузы может развиться дополнительно паттерн по Гамильтону, то есть оба типа могут сочетаться [23] .
Осложнения андрогенной алопеции (облысении у женщин)
Основным осложнением при андрогенной алопеции у женщин является полная потеря волос без возможности их естественного восстановления. Потеря волос не приводит к утрате работоспособности, ухудшению общего состояния и не требует длительного нахождения в стационаре. Однако выпадение волос ухудшает эмоциональное состояние пациенток и влияет на качество жизни. Пациентки могут страдать лёгкими формами тревожных, депрессивных и социофобических расстройств.

Диагностика андрогенной алопеции (облысении у женщин)
Диагноз устанавливается на основе клинических признаков. Также проводят тест на вытягивание волос или тракционную пробу. Метод заключается в мягком потягивании волос вдоль скальпа. Проба обычно является положительной в лобно-теменной зоне кожи головы. Положительная тракционная проба со всей поверхности кожи указывает на сочетание андрогенетической алопеции с диффузной телогеновой.
Для раннего выявления и дифференциальной диагностики с другими алопециями проводят дерматоскопию [24] . Дерматоскопическими признаками андрогенетической алопеции является анизотрихоз (вариабельность диаметров более 20 % за счёт истончения волос), перипапиллярные признаки (коричневый ореол вокруг фолликула, жёлтые точки), и увеличение количества веллусоподобных волос [25] [26] .
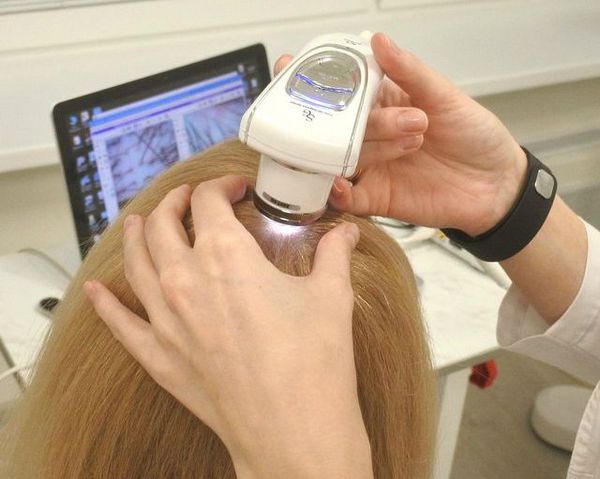
При диагностике важно оценить функцию щитовидной железы, уровень ферритина, цинка, витамина D и пролактина. Это необходимо, чтобы исключить факторы, которые могут увеличить выпадение волос и усугубить заболевание [34] .
Пациенты с нерегулярными менструациями в анамнезе, повышенным индексом массы тела или кожными признаками гиперандрогении должны быть направлены к эндокринологу для выявления возможного СПКЯ (синдрома поликистозных яичников) и ВДКН (врождённой дисфункции коры надпочечников).
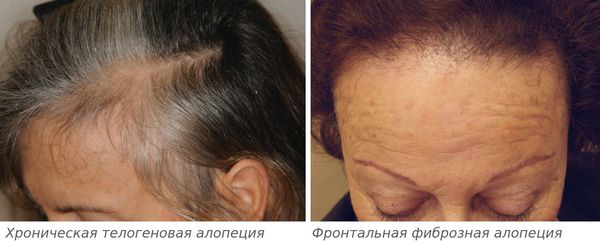
Андрогенетическую алопецию дифференцируют с хронической телогеновой и фронтальной фиброзной, алопецией, вызванной необратимым поражением части волосяных фолликулов химиотерапией, скрытой формой гнездной алопеции:
- для хронической телогеновой алопеции характерно поредение волос в лобно-височной области [30] ;
- алопеция, вызванная химиотерапией, вероятно, связана с поражением стволовых клеток волосяных фолликулов [31] ;
- скрытая форма гнездной алопеции проявляет себя быстро прогрессирующим истончением волос и наличием большого количества жёлтых точек при дерматоскопии [32] ;
- фронтальная фиброзная алопеция — это лимфоцитарная рубцовая алопеция, которая считается вариантом красного плоского лишая.
Лечение андрогенной алопеции (облысении у женщин)
Единственным лекарственным соединением, одобренным FDA ( Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, США) для терапии андрогенетической алопеции, является 2 % местный миноксидил.
Миноксидил усиливает образование новых кровеносных сосудов вокруг фолликула и побуждает фолликулы вступать в фазу анагена, продлевая его продолжительность, увеличивает количество волос [35] .
Первая группа альтернативной терапии — это синтетические антиандрогены, которые используются перорально для блокирования связывания рецепторов андрогенов. Они включают ацетат ципротерона, спиронолактон и флутамид. Назначение ципротерона ацетата оправдано при лабораторно подтверждённой гиперандрогении [37] .
Спиронолактон — это калийсберегающее мочегонное средство, которое снижает выработку тестостерона в надпочечниках и блокирует рецепторы андрогенов в тканях-мишенях. Он эффективен при лечении гирсутизма, связанного с синдромом поликистозных яичников и акне [37] .
Применение флутамида ограничено, поскольку он даже в низких дозировках токсичен для печени [38] .
Вторая группа соединений препятствует воздействию дигидротестостерона. Финастерид уменьшает выпадение волос и стимулирует их отрастание, увеличивая количество волос. Данные об эффективности его применения у женщин в литературе противоречивы, требуются дополнительные контролируемые исследования.
Женщины в пременопаузе должны использовать безопасные методы контрацепции во время лечения финастеридом, так как, если принимать препарат в течение всей беременности, он может вызвать феминизацию мужского плода. Другое возможное побочное действие — это небольшой подъём уровня эстрогенов. По этой причине финастерид не рекомендуется женщинам с семейным или личным анамнезом рака молочной железы, так как может вызвать развитие гормональнозависимой формы рака.
Есть некоторые доказательства того, что световые процедуры могут стимулировать рост волос, но механизм, с помощью которого это происходит, неясен. Lasercomb Hair MaxR — это портативное лазерное устройство, широко продаваемое в качестве средства для отрастания волос. Проведено одно контролируемое исследование у мужчин, показывающее эффективность этой технологии [41] , но исследований, доказывающих его эффективность для женщин, нет.

Латанопрост и биматопрост изначально разработаны для лечения глаукомы, и одним из замеченных побочных эффектов был рост ресниц. Существует одно исследование у 16 мужчин, показывающее, что латанопрост на 0,1 % увеличил плотность волос на коже головы по сравнению с исходным уровнем и плацебо [42] .
При стабильном выпадении волос у пациентов старше 25 лет поможет пересадка волос. Золотой стандарт — это трансплантация фолликулярных единиц, поскольку она даёт хороший результат, который выглядит естественно [43] . Волосяные фолликулы имплантируются индивидуально в соответствии с линией волос пациента. Это многоэтапная процедура, которую должна выполнять опытная хирургическая бригада.
Прогноз. Профилактика
Андрогенетическая алопеция является хроническим заболеванием и без лечения прогрессирует. Официально признанным во всем мире средством для лечения АГА у женщин в настоящий момент является 2 % миноксидил [1] [2] [3] . Если пациентки начинают лечение миноксидилом, то оно должно быть пожизненным, поскольку при прекращении приёма развивается синдром отмены. Также следует знать, что этот препарат, как и большинство антиандрогенных средств, не применяется у беременных и кормящих.
ВГМУ, Профессорская клиника Юцковских, Владивосток
Профессорская клиника Юцковских, Владивосток
Владивостокский государственный медицинский университет
Андрогензависимые синдромы кожи у женщин: роль антиандрогенной терапии на современном этапе
ВГМУ, Профессорская клиника Юцковских, Владивосток
ВГМУ, Профессорская клиника Юцковских, Владивосток
Профессорская клиника Юцковских, Владивосток
Владивостокский государственный медицинский университет
Одной из сложных задач современной дерматологии и косметологии остается лечение андрогензависимых синдромов кожи. Синдромы гиперандрогении (ГА) часто служат причиной психологического дискомфорта и отрицательно влияют на качество жизни женщин. Синдромы ГА у женщин являются частыми причинами психологического дистресса. Внешние проявления избытка андрогенов отмечаются у 10—30% женщин в популяции и становятся существенным косметическим дефектом, отражающимся на нервно-психическом статусе женщины, приводя к раздражительности, депрессивным состояниям, снижая качество жизни и обусловливая социальные проблемы в виде ограничений в выборе профессии и сложностей в трудоустройстве, снижая чувство достоинства женщин. В патогенезе этих процессов большое значение уделяется роли гормонов. Под влиянием избытка андрогенов у женщин развивается синдром ГА, что клинически проявляется себореей, гирсутизмом, андрогензависимой алопецией.
Заболевания, при которых имеются признаки повышенной продукции андрогенов, относятся к междисциплинарной патологии и требуют пристального внимания и знаний не только гинеколога, но и в равной степени затрагивают сферу интересов эндокринологов, дерматологов, косметологов.
Кожа человека является комплексом андрогенчувствительных структур (сальные и потовые железы, волосяные фолликулы). Под влиянием андрогенов находятся многие важные функции кожи: митотическая активность клеток, активность сальных желез, рост волос, выраженность пигментации. Являясь тканью-мишенью для половых стероидных гормонов, например андрогенов, кожа принимает активное участие в метаболизме стероидных половых гормонов, в частности, в экстрагландулярном образовании из стероидов-предшественников.
Источником андрогенов в организме женщины являются яичники и кора надпочечников. Их синтез происходит под стимулирующим действием лютеинизирующего гормона (ЛГ) и адренокортикотропного гормона (АКТГ). Основной андроген надпочечников — дигидроэпиандростерон (ДГЭА) и его сульфат (ДГЭАС), яичников — тестостерон (Т) и андростендион (А). Действие половых гормонов на кожу осуществляется через специфические андрогенные рецепторы (АР) сосочкового слоя дермы, фибробласты, кератиноциты, эпителиальные клетки просвета апокриновых желез и секреторный отдел эккриновых сальных желез, а также в себоцитах и волосяных фолликулах.
Мишенями для половых стероидов в коже являются эпидермис, волосяные фолликулы, сальные железы, меланоциты и фибробласты. Под воздействием андрогенов усиливаются дифференцировка и митотическая активность клеток эпидермиса, увеличивается синтез межклеточных липидов, увеличивается толщина эпидермиса, стимулируется рост и пигментация волос, усиливается продукция кожного сала, снижается синтез глобулина, связывающего половые стероиды (ГСПС) в печени. В то же время под воздействием эстрогенов тормозится рост волос в андрогензависимых зонах, угнетается продукция кожного сала, усиливается синтез ГСПС.
Важным патогенетическим звеном при ГА является нарушение связывания андрогенов со специфическим ГСПС. Связанные с ГСПС стероиды недоступны для соединения с рецепторами в тканях-мишенях и оказания биологического эффекта. Биологический эффект в клетках-мишенях оказывает лишь свободная фракция половых стероидов. Она же ответственна за клинические проявления андрогенного эффекта.
Таким образом, ГА в организме женщины сопровождается избыточной секрецией мужских половых гормонов или повышенной чувствительностью тканей к неизмененному уровню андрогенов. Совокупность признаков поражения кожи и ее придатков, возникающих в результате избытка андрогенов в женском организме (себорея, гирсутизм, андрогензависимая алопеция), можно обозначить термином «гиперандрогенная дермопатия».
ГА может проявляться в виде абсолютного увеличения количества гормонов (абсолютная ГА) или повышенной чувствительностью рецепторов к нормальному или сниженному содержанию андрогенов в организме (относительная ГА).
Акне. В клетках сальных желез — себоцитах тестостерон под действием фермента α5-редуктазы 1-го типа переходит в самый активный метаболит — дигидротестостерон, который служит непосредственным стимулятором роста и созревания себоцитов, образования кожного сала. Основными причинами относительной ГА являются повышенная активность фермента α5-редуктазы 1-го типа, повышенная плотность ядерных дигидротестостероновых рецепторов, увеличение свободной фракции тестостерона в крови. Таким образом, в патогенезе акне ведущая роль принадлежит гормональному фактору, приводящему к гипертрофии и повышенному функционированию сальных желез, фолликулярному гиперкератозу в протоке сально-волосяного фолликула (СВФ), активизации микроорганизмов с последующим воспалением.
Себорея. Себорея — патологическое состояние кожи, обусловленное нарушением функции сальных желез, изменением состава их секрета. Возникновение синдрома ГА — себореи, связано с избытком андрогенов. Проявляется в местах, богатых сальными железами, — на лице, волосистой части головы, верхней части груди, в межлопаточной области. Развитию себореи способствуют нарушения функции половых желез (в частности, нормального соотношения между эстрогенами и андрогенами), надпочечников, щитовидной железы, а также иммунной, пищеварительной, центральной и вегетативной систем. Различают сухую и жирную себорею. У некоторых больных может быть смешанная себорея: на одних участках имеются симптомы сухой, а на других — жирной себореи.
Огромная роль в патогенезе себореи отводится наследственности. Генотип — врожденные качества, заложенные в генах. Структура кожного покрова является врожденной и неизменной на протяжении всей жизни, несмотря на то что поверхность кожи может постоянно меняться — трескаться, шелушиться, менять цвет (тускнеть), стать более грубой, тем не менее структура ее всегда индивидуальная, не меняющаяся.
При повышенном уровне мужских половых гормонов может изменяться тип кожи. Она становится жирной, поры на лице и себорейных участках расширяются, рН достигает 6, появляется склонность к дисхромиям.
Жирную себорею подразделяют на жидкую и густую, в зависимости от консистенции кожного сала, что определяется его физико-химическим составом. Участвуя в формировании водно-липидной мантии, кожное сало оказывает выраженное бактерио- и фунгицидное действие на большинство микроорганизмов. Компоненты липидной пленки на поверхности кожи являются производными сальных желез и эпидермиса и на 60% представлены триглицеридами, на 20—25% — эфирами воска, на 10—15% — скваленом, на 1—3% — эстерифицированными стеролами и на 0,5—2% — свободным стеролом. В увеличенном объеме кожного сала снижается концентрация незаменимой α-линоевой кислоты, которая подавляет экспрессию фермента трансглутаминазы. α-Линоевая кислота является основным регулятором дифференцировки кератиноцитов. Трансглутаминаза участвует в синтезе кератина 1-й и 10-й фракций, белков инволюкрина, лорикрина и филлагрина — основных компонентов цементирующего межклеточного вещества. Уменьшение количества линолевой кислоты приводит к повышению рН кожного сала, в итоге значительно нарушается барьерная функция эпителия и создаются условия для роста микроорганизмов на поверхности кожи и внутри сально-волосяных фолликулов.
Основными критериями оценки типов кожи на приеме у врача-косметолога являются характеристика салообразования — повышенное, пониженное, умеренное; степень расширения пор — расширенные, умеренно-расширенные, точечные; состояние липидной субстанции эпидермиса после умывания — чувство стянутости, дискомфорт, шелушение, покраснение.

Сравнивая различные состояния кожи здоровых пациентов и пациентов с себореей посредством неинвазивных методов морфофункциональной диагностики кожи (себуметрии, корнеометрии, рН-метрии) с применением аппарата SOFT PLUS, CATELLANI GROUP (Италия), мы получили следующие результаты (табл. 1).

Одним из объективных методов оценки состояния кожи является ультразвуковое исследование (УЗИ). У пациента с нормальной кожей при УЗИ видны сглаженность рельефа эпидермиса, равномерное распределение эхосигнала; эпидермис четко отграничен от дермы, дерма дифференцирована на отделы, расположение волокон дермы линейное (рис. 1, а). Рисунок 1. Ультразвуковая картина кожи в норме (а) и у пациента с себореей (б). У пациента с себореей отмечаются изменение эхоструктуры эпидермиса, нарушение его рельефа, протоки сальных желез расширены; отсутствует четкая граница между эпидермисом и дермой, эхогенность субэпидермального отдела дермы снижена (рис. 1, б).
Еще одним симптомом ГА является гирсутизм.

Гирсутизм. Под гирсутизмом (рис. 2) Рисунок 2. Гирсутизм у пациентки (из фотоархива ООО «Профессорская клиника Юцковских»). следует понимать увеличение у женщин количества волос на лице, груди, животе, вокруг сосков, а также на спине и бедрах. При усиленном оволосении женщин еще говорят о гипертрихозе. Между терминами «гирсутизм» и «гипертрихоз» существует разница: первый обозначает мужской тип роста волос у женщин, а второй — количественное увеличение волос на теле. Гирсутизм чаще всего является признаком некоторых эндокринных заболеваний, вызванных поражением гипоталамо-гипофизарной области, коры надпочечников и яичников. Но гирсутизм не всегда связан с нейроэндокринной патологией.
Выделяют следующие формы гирсутизма, не связанные с патологией яичников или надпочечников: конституциональный, экзогенный, идиопатический. Конституциональная форма гирсутизма носит наследственный характер. При этом виде повышенного оволосения продукция андрогенов в норме. К этой форме гирсутизма относится избыточное оволосение у женщин отдельных национальностей (жительницы стран Востока и Средиземноморья). Экзогенная форма гирсутизма возникает в тех случаях, когда приходится вводить андрогены в виде инъекций лекарственных препаратов. Гирсутизм может развиваться при применении таких препаратов, как кортикостероиды, стрептомицин. Предположение об идиопатическом гирсутизме возникает в тех случаях, когда не обнаруживается эндокринная патология и исключается экзогенный и конституциональный гирсутизм. Этот диагноз ставится при нормальном и повышенном содержании свободного тестостерона и невозможности установить причину заболевания. Учитывая, что достаточно часто гирсутизм служит проявлением ГА, целесообразно применение антиандрогенных препаратов. При гирсутизме косметическое устранение волос (эпиляция) эффективно только при условии удаления или угнетения источника повышенной секреции андрогенов.

Алопеция. В развитии андрогенной алопеции (рис. 3) Рисунок 3. Андрогенная алопеция у пациентки (из фотоархива ООО «Профессорская клиника Юцковских»). основная роль принадлежит α5-редуктазе — ферменту, который восстанавливает тестостерон до дигидротестостерона (ДГТ). ДГТ сокращает фазу роста волосяного фолликула, что приводит к его уменьшению и постепенной атрофии. Одновременно сокращается продолжительность жизненного цикла волоса, в результате чего наблюдается усиленное выпадение волос. Исследования показали, что уровень андрогенов у женщин с андрогенной алопецией часто не превышает норму. Это свидетельствует о том, что в патогенезе андрогенной алопеции основную роль играет повышенная чувствительность фолликулов к действию ДГТ. Женская андрогенная алопеция носит диффузный характер и редко приводит к облысению. При андрогенной алопеции на голове всегда остается венчик волос в затылочной и височных областях. Суть феномена состоит в том, что волосяные фолликулы в этих зонах не имеют рецепторов, способных воспринимать действие андрогенов. Поэтому исключается одна из обязательных причин андрогенной алопеции — гормональная активность — и волосы в этих областях генетически «застрахованы» от выпадения.
Современные подходы к лечению различных форм ГА включают назначение системных и наружных препаратов. Выбор методов лечения ГА должен основываться на адекватной клинической оценке степени тяжести синдромов ГА. Следует всегда учитывать состояние эндокринного фона, сопутствующие заболевания и состояния.

По нашим данным, за последние 5 лет значительно увеличилась обращаемость пациентов с синдромами ГА, особенно с такими, как алопеция и гирсутизм (рис. 4). Рисунок 4. Динамика обращаемости пациентов с синдромами гиперандрогении (по данным ООО «Профессорская клиника Юцковских», 2005—2009 гг.).
Механизм антиандрогенного действия КОК заключается в снижении продукции гонадотропинов (ЛГ), редукции уровня циркулирующих андрогенов, увеличении связывания андрогенов, снижении секреции андрогенов надпочечниками, ингибировании α5-редуктазы, связывании андрогенных рецепторов.
Первым КОК антиандрогенного действия был препарат диане-50, созданный на основе синтезированного в 1961 г. ципротерон-ацетата. В 1985 г. были созданы диане-35 (со снижением дозы эстрогенного компонента) и препарат андрокур (10 или 50 мг ципротерона ацетата).
Проведенные в 40 странах Европы два плацебо-контролируемых исследования с участием 1072 женщин в возрасте 14—45 лет с проявлениями акне показали, что применение КОК Джес по сравнению с плацебо к концу 6-го месяца способствует выраженному регрессу как невоспалительных, так и воспалительных акне. К окончанию терапии в среднем по группе акне регрессировали на 56%; состояния клинического излечения удалось достичь у 22% пациенток. Наиболее выраженное улучшение наблюдалось у женщин в возрасте от 14 до 22 лет.
В другом исследовании, посвященном оценке косметических аспектов приема антиандрогенного КОК на основе дроспиренона, к концу 6-го месяца терапии было продемонстрировано уменьшение себореи (на 71%), акне (на 75%) и гипертрихоза (показатель Ферримана—Галлвея — на 43%). При оценке толщины эпидермиса (корнеометрия) выявлено повышение гидратации на 26%, что было обусловлено как влиянием эстрогена в составе КОК, так и снижением концентрации андрогенов и/или их активности. Патоморфологически повышение гидратации эпидермиса обусловлено стимуляцией эстрогенами синтеза гиалуроновой кислоты. Определение снижения уровня испарения жидкости с поверхности кожи (на 35%) с помощью теваметрии (TEWL) также свидетельствовало об улучшении состояния кожи.
Важнейшим преимуществом Джес является хорошая переносимость, в частности, отсутствие влияния на массу тела, а иногда ее снижение. Это объясняется тем, что дроспиренон, входящий в состав препарата, дает антиминералокортикоидный эффект и препятствует задержке жидкости в организме, которая часто служит причиной увеличения массы тела при приеме КОК. Джес эффективно уменьшает проявления предменструального синдрома, в частности, появление акне в период, предшествующий менструации.
Таким образом, патогенетически оправдано и клинически актуально использование для лечения себореи, гирсутизма, андрогензависимой алопеции современных КОК, в частности Джес, которые подавляют секрецию гонадотропинов, стимулируют синтез ГСПС и снижают активность α5-редуктазы. Применение КОК, оказывающих антиандрогенный эффект, может улучшить не только гормональные параметры и классические проявления ГА, но и общее состояние, а также качество кожи, повышая гидратацию и улучшая характеристики, отражающие состояние кожи.
Так как диагностика и лечение различных форм ГА находятся на стыке нескольких специальностей (гинекология, эндокринология, дерматология), то только их объединение позволит добиться высоких результатов в лечении себореи, гирсутизма и андрогензависимой алопеции.

Половые гормоны – незаменимый «пазл» в организме женщины. От их состояния зависит настроение, состояние кожи и репродуктивной системы, общее самочувствие. Более всего отклонение гормонов от нормы отражается на коже. Поэтому каждая представительница прекрасного пола должна знать и понимать, как гормоны определяют состояние кожи. В этом им поможет данная статья.
Всего в женском организме выделяют две группы половых гормонов: андрогены (мужские гормоны) и эстрогены. Последние преобладают в организме женщины.
Самые влиятельные представители группы андрогенов — тестостерон свободный и общий, именно показатели этих двух вариантов гормона исследуются врачами. Воспроизводятся они надпочечниками и яичниками. Для их синтеза требуется холестерин, поступающий с пищей или самостоятельно образующийся в организме.
В организме андрогенам отвели строительную функцию. Они участвуют в развитии скелета и мышц, молочных желез, оволосении по женскому типу, определяют отложение жировой ткани (у женщин она откладывается преимущественно на бедрах, животе и ягодицах.
Влияние на кожу
К андрогенам чувствительны специальные рецепторы, находящиеся в слоях кожи и волосяных фолликулах. Регулируют процесс секреции сальных желез и ороговения кожи.
В момент полового созревания повышается выработка андрогенов. По этой причине железы начинают работать интенсивнее: повышается потливость, жирность кожи, увеличивается скорость ороговения. Меняется и состав кожного сала. В этот период обычно появляются высыпания на коже.
Менструальный цикл и андрогены
Скачок андрогенов приходится на последнюю фазу цикла. За 2-7 дней на коже этот скачок проявляется в виде единичных высыпаний, а если кожа уже больна акне, состояние обостряется, повышается жирность кожи, расширяются поры.
Признаки переизбытка андрогенов:
- Нерегулярный менструальный цикл. Задержка больше 10 дней;
- Раздражительность;
- Сухость кожи;
- Высокая сексуальная активность;
- Оволосение по мужскому типу.
При нехватке андрогенов наблюдается:
- Нерегулярность менструации;
- Чрезмерная жирность кожи;
- Повышенное потоотделение;
- Снижение либидо.
Рекомендации по уходу за кожей, чувствительной к андрогенам
Отказ от агрессивных косметологических процедур (чистки, пилинги, аппаратные процедуры) в начале цикла, поскольку активное деление клеток кожи может вызвать воспаление. Также рекомендуется уделять внимание очищению и регулировать салоотделение в течение дня, используя соответствующие средства.
Андрогенизация — распространенная проблема у женщин, приводящая к множественным нарушениям — от нарушения менструального цикла, бесплодия и гирсутизма до психологических проблем, требующих лечения. Для устранения такой патологии очень важны правильный диагноз и лечение.
Наиболее частыми причинами повышенного уровня андрогенов у женщин являются синдром поликистозных яичников (ПКЯ) и врожденная гиперплазия надпочечников (ВГК).
Синдром поликистозных яичников — андрогенизация яичникового происхождения
СПКЯ поражает примерно 5-7% женщин детородного возраста. Описанный в клинической картине учеными Stein и Loeventhal ещё в 1935 году, синдром включает нарушения менструального цикла (от олигоменореи до аменореи включительно), бесплодие и гирсутизм. Также могут быть другие проблемы андрогенизации, например, прыщи и алопеция.

Нарушение менструального цикла
В классическом определении внимание уделялось двустороннему увеличению яичников. Этот синдром часто сопровождается ожирением, ановуляторными циклами (отсюда и бесплодие), гормональными и метаболическими нарушениями — гиперинсулинемия, нарушения липидного обмена, гиперпролактинемия.
Чаще всего женщины с этой патологией обращаются к гинекологу из-за нарушения менструального цикла, в случае невозможности забеременеть, и все чаще обеспокоены чрезмерным ростом волос. Редко этот синдром связан с первичной аменореей.
Нерегулярные менструальные циклы встречаются примерно у 60-70% пациенток и связаны с возникновением ановуляторных циклов, что связано с отсутствием гормональной активности желтого тела. В этих случаях только от 10 до 40% циклов действительно овулируют, и частота овуляции уменьшается с продолжительностью нарушения. У 20% пациентов развивается аменорея (чаще всего вторичная).
Симптомы андрогенизации возникают особенно у пациентов с ожирением и беспокоят около 60% женщин с поликистозом. Чаще всего это умеренные аномальные волосы.
Увеличение яичников не является постоянным симптомом и встречается примерно у 60% пациентов. При гинекологическом осмотре это трудно определить, особенно в случае часто сопутствующего ожирения. Диагноз затрудняет субъективная оценка, зависящая от опыта врача. Не всегда выявляет увеличение яичников и ультразвуковое исследование.
Наиболее распространенными критериями диагностики синдрома являются критерии, полученные на основании анамнеза, физического осмотра, гормонального обследования и ультразвукового исследования. Но часто решающим является только гистопатологическое исследование .

Гистопатологическое исследование
При опросе пациентки в первую очередь выясняются: нарушения менструального цикла, бесплодие. При обследовании выявляются различные усиленные симптомы андрогенизации, в основном гирсутизм, а также акне и, реже, понижение тона голоса, гипертрофия клитора, изменение формы и пропорций тела, иногда облысение.
- Среди гормональных изменений наиболее важная — усиление секреции ЛГ, который является основной причиной повышенной выработки андрогенов яичниками.
- Помимо повышения уровня ЛГ, наблюдаются также нарушения ритмичности пульсаций ГнРГ (увеличение частоты и амплитуды). Аномальная секреция гонадолиберина наблюдалась у девочек с нарушениями менструального цикла в пубертатном периоде, у которых позже развился синдром ПКЯ.
По словам ученого Йена, причиной нарушений, приводящих к развитию СПКЯ, может быть андрогенная гиперактивность надпочечников в пубертатном периоде, связанная с общепринятыми стрессовыми ситуациями. Повышенные уровни андрогенов стимулируют увеличение секреции ЛГ, и, кроме того, они трансформируются до эстрогенов в периферической жировой ткани.
Эстрогены, в свою очередь, воздействуя на гипоталамус и гипофиз, приводят к нарушениям цикличности секреции ЛГ и ФСГ. Следовательно, повышенная секреция ЛГ приводит к стимуляции текальных клеток яичников и увеличению выработки андрогенов яичниками (в основном андостендиона). Таким образом, круг замыкается. Однако остается неясным, почему не все состояния, связанные с повышенным уровнем андрогенов, приводят к развитию симптомов, характерных для поликистоза.
В настоящее время исследования патогенеза и этиологии синдрома сосредоточены на изучении регуляторных механизмов на уровне яичников, а также роли периферических желез, не связанных напрямую с регуляцией секреции половых гормонов.
Установлено, что в патогенезе синдрома ПКЯ наблюдается нарушение регуляции роста фолликулов яичников и повышенная активность таких факторов роста в яичнике, как:
- TGF-альфа (трансформирующий фактор роста альфа);
- EGF (фактор роста эпителия);
- IGF-1 (инсулиноподобный фактор роста 1;
- bFGF (основной фактор роста фибробластов).
Однако существует разногласие относительно того, происходят ли эти изменения в первую очередь на уровне яичников и затем приводят к дисфункции периферических желез, или же они возникают вторично.
В последние годы большой интерес (в том числе в связи с патогенезом синдрома поликистоза яичников) был сосредоточен на феномене апоптоза. Этот термин описывает процессы и функциональные изменения, связанные с естественной гибелью клеток. Этому явлению подвержены все клетки, и скорость этих процессов зависит от многих факторов.
В яичнике апоптоз, по-видимому, играет роль в атрезии фолликулов и атрофии желтого тела. Благодаря исследованиям на животных и исследованиям фолликулов яичников, полученных в процессе оплодотворения in vitro, были выявлены факторы, увеличивающие выживаемость ооцитов (гонадотропины, эстрогены, IGF1, bFGF, EGF, TGFα) и вызывающие апоптоз (включая GnRH и андрогены).

Апоптоз
Понимание процессов, связанных с апоптозом, позволяет лучше понять процессы, происходящие в яичнике, в том числе и в случае синдрома поликистоза. Понимание механизмов, лежащих в основе выживания фолликулов яичников и их роста, может открыть новую главу в лечении андрогенизации яичников.
Лабораторные тесты при СПКЯ показывают:
- повышение уровня ЛГ;
- повышение уровня тестостерона и андростендиона;
- увеличение сульфата дегидроэпиандростерона.
Уровни ФСГ могут быть в пределах нормы или чаще снижаться, что приводит к сдвигу соотношения ЛГ / ФСГ в пользу ЛГ. Предлагаемое принятие соотношения ЛГ / ФСГ выше 2 в качестве диагностического критерия в настоящее время все чаще ставится под сомнение и не является необходимым для диагностики синдрома СПКЯ.
Белок, связывающий половые гормоны (SHBG), часто снижается, особенно у женщин с ожирением. Также можно наблюдать повышение концентрации гормона роста, пролактина и инсулина. Кроме того, пациенты с поликистозом демонстрируют относительный или абсолютнвй гиперэстрогенизм.
Гормональная картина у пациентов с поликистозом может быть очень разнообразной и однозначных диагностических критериев не существует.
Точно так же неоднозначны критерии ультразвуковой диагностики. Типичная картина маленьких кистозных яичников включает:
- увеличение гонад (чаще всего оценивается площадь поверхности или объем яичников);
- утолщение и увеличение беловатой оболочки;
- повышенная эхогенность стромы яичника.
Важным признаком УЗИ также является наличие большого количества мелких фолликулов, расположенных по периферии или по всему яичнику.
Размер яичников более 10 см 3 (в среднем 12 см 3), площадь более 5,5 мм 2 считается диагностическим признаком синдрома ПКЯ. Предполагается, что количество фолликулов в малом кистозном яичнике больше 10, а их диаметр менее 8 мм или, по мнению некоторых ученых, менее 5 мм.
Ультразвуковой мониторинг овуляции не выявляет выделения и роста доминирующего фолликула — ановуляторные циклы. Однако подчеркивается, что отсутствие типичной картины при ультразвуковом исследовании не исключает наличия синдрома ПКЯ. В тяжелой форме в области неувеличенных яичников могут появиться только единичные крошечные фолликулы.
Большую роль в ультразвуковой диагностике играет индивидуальный опыт врача. Однако следует помнить, что ставить диагноз только на основании ультразвукового исследования — ошибка.

Ультразвуковая диагностика
Из-за большого разнообразия клинических симптомов и неубедительных результатов дополнительных исследований большинство ученых выделяют разные клинические формы, некоторые даже считают, что термин СПКЯ охватывает несколько синдромов заболевания разной этиологии и патогенеза.
Среди прочего выделяют следующие формы: HAIR-AN типа A и B, клинически соответствующие возникновению гиперандрогении, инсулинорезистентности и актинического кератоза.
- Тип A касается молодых девушек с генетически детерминированным снижением количества рецепторов инсулина в периферических тканях;
- Тип B связан с наличием антител к рецепторам инсулина и диагностируется у женщин старшего возраста.
В обеих формах наблюдается увеличение секреции инсулина, который стимулирует IGF-1 в яичниках, стимулируя выработку и высвобождение андрогенов в клетках ткани яичника.
Следует помнить, что метаболические нарушения — гиперлипидемия, неблагоприятный липопротеидный профиль — ЛПВП, ЛПНП — возникают вторично по отношению к гормональным нарушениям при синдроме поликистоза яичников. Вместе с гиперинсулинемией это создает повышенный риск развития сердечно-сосудистых заболеваний.
Относительный избыток эстрогенов и отсутствие гестагенных эффектов (неовуляторные циклы) в течение многих лет могут привести к гиперплазии эндометрия и раку эндометрия в более позднем возрасте, а также вызвать мастопатические изменения в груди. По этим причинам женщины с диагностированным синдромом поликистозных яичников нуждаются в лечении независимо от их желания иметь ребенка или по косметическим причинам.
В зависимости от цели лечения принимаются разные планы лечения. При этом следует помнить, что результаты лечения, независимо от целевого назначения, тем лучше, чем раньше будет поставлен диагноз и проведено лечение. В частности, это касается лечения бесплодия, связанного с СПКЯ, гирсутизма (чем он более продвинутый, тем труднее добиться значительного косметического эффекта), а также профилактики сердечно-сосудистых заболеваний, гиперплазии эндометрия и мастопатических изменений груди.
В случае желания забеременеть используются препараты, вызывающие овуляцию, и лапароскопию. У женщин, которые в настоящее время не планируют потомство, необходимо восстановить нормальный ритм кровотечений путем введения гестагенов или гормональных контрацептивов.
Врожденная гиперплазия надпочечников — андрогенизация надпочечникового происхождения
Поликистоз следует дифференцировать в основном от гиперплазии надпочечников . Врожденная гиперплазия надпочечников (ВГН) связана с наличием ферментативных блоков в пути биосинтеза гормонов коры надпочечников — глюкокортикоидов и минералокортикоидов. Этот синдром генетически детерминирован.

Гиперплазия надпочечников
Наиболее распространенный ферментативный дефицит касается 21-гидроксилазы, реже 17-гидроксилазы, 11-гидроксилазы и 3β-гидроксилдегидрогеназы. Классическая гиперплазия надпочечников проявляется после родов или в детстве и в основном включает симптомы, связанные с электролитными нарушениями, возникновением гипертонии, а также маскулинизацией и гирсутизмом.
Также следует дифференциировать синдром поликистозных яичников в отношении отсроченной или неполной гиперплазии надпочечников (САГ с поздним началом). Патология появляется в более позднем возрасте и не связана с нарушениями концентрации минералокортикоидов. С другой стороны, обнаруживается гирсутизм, олигоменорея, реже гиперплазия клитора и алопеция. У 4-6% пациентов с симптомами андрогенизации врожденная гиперплазия надпочечников возникает поздно.
Гормональные тесты показывают повышение уровня ЛГ и более низкий уровень ФСГ, уровень тестостерона немного повышен или нормален, в то время как уровень свободного тестостерона увеличивается, а уровень ДГЭА может повышаться.
Диагноз ставится на основании уровня 17-гидроксипрогестерона в сыворотке крови. Помогают поставить диагноз значения выше 10 нг / мл.
- Когда значения находятся в диапазоне от 2 до 10 нг / мл, для дифференциации следует провести тест на АКТГ.
- В случае повышения уровня 17-ОН-прогестерона в 3 раза диагностируется гиперплазия коры надпочечников.
Вирилизирующие опухоли надпочечников и яичников встречаются редко и характеризуются внезапным и быстрым началом гирсутизма и маскулинизации. Должно побудить гинеколога искать гормонально активную опухоль в яичниках или надпочечниках повышение концентрации тестостерона выше 2 нг / мл. В этом случае требуется провести определение 17-кетостероидов, 17-гидроксикостероидов, УЗИ яичников и надпочечников.
Источники
- Fruzzetti F. и др.: Влияние яичников на секрецию андрогенов надпочечниками при синдроме поликистозных яичников. Фертильность и бесплодие;
- Rittmaster RS: Клиническая значимость метаболизма тестостерона и дигидротестотерона у женщин, Am. J. Med.;
- Аззиз Р.: Синдром гиперандрогенно-инсулинорезистентного черного акантоза: терапевтический резонанс. Фертильность и бесплодие;
- Ибанез Л. и др.: Локализация источника избытка андрогенов у девочек-подростков. Журнал клинической эндокринологии и метаболизма;
- Barnes RB и др.: Гиперандрогения яичников в результате врожденных нарушений вирилизации надпочечников: данные о перинатальной маскулинизации нейроэндокринной функции у женщин. Журнал клинической эндокринологии и метаболизма;
- Буялос Р.П. и др.: Взаимосвязь между кровообращением, ожирением и гиперинсулинемией на сывороточный белок-1, связывающий инсулиноподобный фактор роста, при синдроме поликистических яичников. Am. J. Obstet. Гинекол;
- Кац Э. и др.: Влияние системной гиперандрогении на реакцию надпочечников на гормон адренокортикотропин. Фертильность и бесплодие;
- Morris RS и др.: Проренин повышен при синдроме поликистозных яичников и может отражать гиперандрогенизм, фертильность и бесплодие;
- Вареник-Шиманкевич А. Синдромы андрогенизации у женщин. Клиническая перинатология и гинекология;
- Янн Р. и др.: Ультразвуковая оценка гипертрофии стромы яичника при гиперандрогении и нарушениях овуляции: визуальный анализ по сравнению с компьютеризированной куантификацией, Фертильность и стерильность.
Читайте также:

