А дерма при экземе
Обновлено: 28.04.2024
Для цитирования: Кассирова Д.А. Применение крема с Дерма–Мембранной Структурой при атопическом дерматите. РМЖ. 2010;12:777.
Атопический дерматит (АтД, атопическая экзема, диффузный нейродермит, конституциональная экзема) – хроническое воспалительное заболевание кожи с рецидивирующим течением, сопровождающееся интенсивным зудом, папулезными высыпаниями, как правило, возникающими на эритематозном фоне, выраженной лихенификацией и симпатергической реакцией кожи.
АтД в типичных случаях начинается в раннем детском возрасте, может продолжаться или рецидивировать и в зрелом возрасте. АтД в большинстве случаев развивается у лиц с наследственной предрасположенностью и часто сочетается с другими аллергическими заболеваниями (бронхиальной астмой, аллергическим ринитом, пищевой аллергией), а также с рецидивирующими кожными инфекциями. Установлено, что АтД клинически манифестирует у 81% детей, если больны оба родителя, у 59% – если болен только один из родителей, а другой имеет аллергическую патологию дыхательных путей, и у 56% – если болен только один из родителей [1,2].
По данным различных источников, АтД является наиболее распространенным кожным заболеванием. Так, в детской дерматологической практике до 90% пациентов, обращающихся за консультацией, страдают теми или иными проявлениями АтД. Отмечается общая тенденция роста числа случаев АтД у населения Земли. Причины увеличения заболеваемости АтД различны и связаны с воздействием аллергенных и неаллергенных экзогенных факторов в тот или иной период жизни пациента. Общая распространенность заболевания в развитых странах составляет 15–20% у детей и 2–10% у взрослых [2,3,4].
Повсеместная распространенность, наследственная предрасположенность, частое начало в детском возрасте, хроническое течение с периодическими обострениями, которые сопровождаются как упорным зудом, так и кожными высыпаниями, нервно–психологическими расстройствами, развивающимися у пациентов на фоне заболевания, – все это делает АтД серьезной медико–социальной проблемой.
Наибольшую ценность в диагностике АтД имеет клиническая картина. Обследование должно включать в себя тщательный сбор анамнеза (отягощенная по атопии наследственность), оценку распространенности и тяжести кожного процесса (белый или смешанный дермографизм, типичная морфология элементов и их локализация), оценку степени психологической и социальной дезадаптации и влияния заболевания на семью пациента. АтД необходимо дифференцировать с чесоткой, себорейным дерматитом, аллергическим контактным дерматитом, иммунодефицитными состояниями, ихтиозом, псориазом, и др. дерматозами.
Классификацию АтД мы приводим из Клинических рекомендаций по дерматовенерологии Российского общества дерматовенерологов (РОДВ), 2008 г. [3]:
1. Возрастные периоды болезни:
• младенческий (до 2 лет);
• детский (от 2 до 13 лет);
• подростковый и взрослый (от 13 лет и старше).
2. Клинико–морфологические формы:
• экссудативная;
• эритематозно–сквамозная;
• эритематозно–сквамозная с лихенификацией;
• лихеноидная;
• пруригинозная.
3. Стадии болезни:
• обострение;
• ремиссия (неполная и полная).
4. Распространенность кожного процесса:
• ограниченный;
• распространенный;
• диффузный.
5. Степень тяжести течения заболевания:
• легкое течение;
• средней тяжести;
• тяжелое течение.
Основной целью терапии АтД должно быть уменьшение выраженности симптомов болезни, обеспечение длительного контроля над заболеванием путем предотвращения или снижения тяжести обострений и изменение естественного течения заболевания. В первую очередь необходимо минимизировать факторы, которые могут спровоцировать обострение заболевания, как например, неблагоприятное воздействие окружающей среды, контактные, ингаляционные и пищевые аллергены, химические раздражители и др. Соблюдение индивидуальной гипоаллергенной диеты также является не менее важным условием коррекции симптомов АтД. По показаниям применяется ультрафиолетовое облучение и психотерапия.
К медикаментозным методам лечения АтД относятся системная и местная лекарственная терапия. В качестве системной терапии используются антигистаминные и гипосенсибилизирующие препараты, седативные и вегетотропные средства, транквилизаторы, иммуномодуляторы и др. Системные глюкокортикостероиды используют для купирования тяжелых обострений АтД.
Наружная лекарственная терапия включает в себя применение топических глюкокортикостероидов, антибиотиков и др. средств. Как известно, особую проблему при АтД представляет возможное присоединение вторичной инфекции на фоне повышенной сухости кожных покровов, особенно в очагах поражения. Происходит это как за счет большого количества микротравм, имеющихся на воспаленной атопичной коже, так и по причине сниженной противомикробной иммунной защиты.
В целом сухость кожи (ксероз) представляет собой серьезную проблему в современной дерматологии, причем в последние годы ее значимость возрастает, и данному состоянию в настоящее время уделяется большое внимание. В основе патогенеза ксероза кожи лежит ряд факторов [5,6], в том числе возникновение сухости кожи обусловлено эндогенной предрасположенностью к АтД или старением (как естественным, так и преждевременным) [7,8,9].
В нормальном состоянии кожный барьер препятствует избыточному испарению влаги через роговой слой, или трансэпидермальной потере воды [10,11]. При атопии в роговом слое дермы уменьшается количество липидов, церамидов, аминокислот и гранул с кератогиалином, сокращается численность ламеллярных телец в межклеточном пространстве [12,13,8]. Вследствие этих изменений способность рогового слоя задерживать воду снижается, а трансэпидермальная потеря воды увеличивается [9,14–17].
На фоне ксероза процесс репарации протекает крайне медленно, а иногда и приостанавливается [5,6,15,18]. В результате дегидратации появляется чувство стягивания, усиливается реакция кожи на действие раздражающих факторов, повышается ее восприимчивость к бактериальным инфекциям [9,10,13,16].
В связи с тем, что у больных АтД нарушена функция кожного барьера, необходимо проведение вспомогательной базисной терапии, заключающейся в регулярном нанесении средств для увлажнения кожи. Т.о., согласно международным и российским рекомендациям, увлажняющие и смягчающие средства входят в стандартную терапию АтД. Они обладают глюкокортикостероид–сберегающим эффектом и используются для достижения и поддержания контроля над симптомами заболевания. В настоящее время наибольшее значение в уходе за кожей больных АтД отводится увлажняющим средствам, содержащим так называемые эссенциальные липиды [3,19].
Восстановление поврежденного гидролипидного слоя эпидермиса при АтД с позиции доказательной медицины было изучено с применением крема Физиогель, в состав которого входят фосфолипиды и церамиды, идентичные эссенциальным липидам кожи [20]. Производство и состав крема Физиогель соответствуют международным правилам для производителей косметики. Крем Физиогель с Дерма–Мембранной Структурой (ДМС) содержит следующие компоненты по Международной номенклатуре косметических ингредиентов (International Nomenclature of Cosmetic Ingredients – INCI): вода, каприлик/каприк–триглицерид, глицерин, пентиленгликоль, масло кокоса, гидрированный лецитин, масло карите, гидроксиэтилцеллюлоза, сквалан, карбомер натрия, ксантиновая камедь, карбомер, церамид–3.
В ниже анализируемом клиническом исследовании крем Физиогель назначали пациентам с атопической экземой нетяжелого течения в качестве монотерапии в течение 4–х недель, а затем анализировали его эффективность [20].
В исследование были включены 50 пациентов с легкой и среднетяжелой атопической экземой, не требующей активного лечения у дерматолога. Из–за неявки 5 пациентов на заключительный осмотр их данные не вошли в окончательный статистический анализ. Основную группу составили 30 пациентов женского и 15 мужского пола в возрасте 1–74 лет (средний возраст 34,7 лет), получавших терапию в амбулаторных условиях. Препарат наносили дважды в день на пораженные участки кожи, а детям – на кожу всего тела. Дополнительное использование других средств для наружного применения не допускалось. За 2 недели до начала исследования отменялись наружные кортикостероиды.
Исследование проводилось с июля по декабрь 2001 г. При непереносимости каких–либо ингредиентов крема Физиогель пациент исключался из когорты испытуемых.
Перед началом лечения и в процессе него пациентов просили классифицировать свои жалобы – ощущение покалывания кожи, жжение, зуд, чувство стягивания – как «отсутствие», «незначительные», «умеренно выраженные», «выраженные». Лечащий врач–дерматолог оценивал объективную симптоматику (покраснение, шелушение, шероховатость кожи) до и после лечения.
Через четыре недели дерматологи и испытуемые независимо друг от друга оценивали эффективность и переносимость крема Физиогель как «неудовлетворительную», «приемлемую», «умеренную», «хорошую» и «высокую».
В ходе исследования врачи и сами пациенты фиксировали любые случаи непереносимости препарата. Пациенты давали оценку субъективным проявлениям до начала лечения и после его завершения.
В результате проведенного исследования были получены следующие данные. Исходно большинство пациентов жаловались на незначительное или умеренно выраженное ощущение покалывания, которое исчезало или оставалось незначительным после нанесения крема Физиогель (рис. 1). То же самое было справедливо и в отношении чувства жжения (рис. 2). При первичном осмотре пациенты жаловались на умеренно выраженное и выраженное ощущение стягивания кожи, тогда как на фоне регулярного использования крема Физиогель эти жалобы либо пропадали совсем, либо были незначительными (рис. 3). Наконец, после четырехнедельного курса нанесения крема кожный зуд, оцениваемый в начале исследования как умеренно выраженный, уменьшался, становясь незначительным (рис. 4).
Объективные признаки (покраснение, шелушение, шероховатость кожи) оценивались лечащим врачом до начала лечения и после его завершения. Исходно кожа у большинства пациентов была умеренно покрасневшей, после завершения терапии сохранялось лишь незначительное покраснение (рис. 5). При первичном осмотре шелушение было выражено незначительно или умеренно, в то время как во время заключительного визита к врачу у подавляющего числа пациентов этот симптом отсутствовал или был выражен незначительно (рис. 6).
Об улучшении состояния кожных покровов на фоне применения крема Физиогель свидетельствует повышение количества баллов в анкетах по оценке клинических симптомов, заполняемых как самими пациентами, так и дерматологами. Во многом мнения испытуемых и врачей совпали: так, эффективность и переносимость препарата были признаны и теми и другими как «хорошие» и «очень хорошие». Практически все испытуемые заявили, что крем имеет приятный запах, легко наносится и экономичен в использовании.
Таким образом, крем Физиогель – это инновационный препарат, в состав которого входят мембранообразующие липиды, восстанавливающие структуру поврежденной кожи. Компоненты крема Физиогель проникают глубоко в кожу, не вызывая ее раздражения [21–23]. Крем полностью повторяет строение здоровой кожи человека благодаря Дерма–Мембранной Структуре (ДМС). Об идентичности липидам межклеточного пространства рогового слоя кожи можно судить по электронным микрофотографиям (рис. 7) [24].
Хорошая переносимость препарата достигается за счет наличия в его составе мембранообразующих липидов растительного происхождения, идентичных собственным липидам кожи. Крем не содержит минеральных масел, силикона, красителей и отдушек, т.е. тех аллергенов, которые могут спровоцировать обострение атопической экземы/дерматита. Благодаря отсутствию в составе крема Физиогель эмульгаторов (технология High Tech Production) в процессе мытья не происходит дополнительного повреждения кожи вследствие эффекта вымывания собственных липидов [21–23]. При использовании крема Физиогель кожа становится гладкой и увлажненной, повышается и ее эластичность [25].
Итак, крем Физиогель – это принципиально новое косметическое средство, прекрасно обеспечивающее уход за сухой и склонной к атопии кожей [21,23]. При помощи крема Физиогель достигается надежный увлажняющий эффект, и данное косметическое средство может быть рекомендовано к широкому применению в лечебной и профилактической дерматологической практике, в частности, как средство базисной терапии при атопическом дерматите/экземе.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

В клинику 5 декабря 2020 года обратился пациент с жалобами на болезненные высыпания и жжение в области ладоней и стоп, болезненность большого пальца правой стопы и изменение ногтей.
Жалобы
Высыпания локализовались на ладонях и стопах. Болезненность умеренная, усиливалась при ходьбе и контакте с водой.
Боль часто усиливалась к концу рабочего дня. Обезболивающие препараты облегчали её на несколько часов, но полностью не устраняли. После сна боль, как правило, снижалась или полностью исчезала.
Анамнез
Впервые высыпания появились в 2001 году. Пациент связывал их со стрессом. Количество обострений не помнит.
Высыпания на стопах появились месяц назад. Боли в области большого пальца правой стопы беспокоят две недели.
Самостоятельно периодически использовал крем Акридерм, который временно оказывал положительный эффект.
Был осмотрен ревматологом и хирургом. Ревматолог поставил диагноз «п сориатический артрит, олигоартритический вариант на фоне очагового псориаза ладоней и подошв » . Хирург предположил, что это псориаз.
Сопутствующие заболевания: гипертоническая болезнь II стадии, алиментарное ожирение II степени, остеохондроз поясничного отдела позвоночника.
Обследование
Патологический процесс расположен на ладонях и подошвах, представлен полиморфной сыпью в виде папул, пустул, чешуек и единичных эритематозно-сквамозных бляшек на локтях и передней поверхности правой голени (см. фото).
На ногтевых пластинах есть углубления, напоминающие ямочки напёрстка. Наблюдается частичный онихолизис (отслоение ногтя от ногтевого ложа) и п одногтевая псориатическая эритема. При такой экземе под ногтями образуются кровоизлияния, выглядящие как красные точки или пятна. Сами ногти толстые, мутные, слоятся, околоногтевой валик кончиков пальцев воспалён.
По результатам МРТ шейного отдела позвоночника выявлены дегенеративные изменения межпозвонковых дисков, дискоэкзофитарные комплексы позвонков С3–С4, С5–С6, С6–С7, спондилёз, спондилоартрозы шейного отдела позвоночника.
По результатам общего анализа крови: СОЭ (скорость оседания эритроцитов) 46 мм/ч, размер, количество лейкоцитов увеличено (13,3 × 10^9/л), С-реактивный белок 30,68, мм/л, ревмофактор 11,3 МЕ/л, мочевая кислота 457 мкм/л, холестерин 5,54 ммоль/л.
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Современные подходы к лечению экземы кистей
Журнал: Клиническая дерматология и венерология. 2011;9(6): 40‑43
Соколовский Е.В., Монахов К.Н., Холодилова Н.А., Домбровская Д.К. Современные подходы к лечению экземы кистей. Клиническая дерматология и венерология. 2011;9(6):40‑43.
Sokolovskiĭ EV, Monakhov KN, Kholodilova NA, Dombrovskaia DK. Modern approaches to the treatment of wrist eczema. Klinicheskaya Dermatologiya i Venerologiya. 2011;9(6):40‑43. (In Russ.).
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Термин «экзема» известен с давних времен. Однако до настоящего времени в разных странах его трактуют по-разному. В последнее время в Европе и Северной Америке термины «дерматит» и «экзема» практически являются синонимами [1, 2]. В то же время никто не отрицает наличия неспецифической патологической реакции кожи, проявляющейся воспалением в эпидермисе и дерме, для которой типично наличие очагового отека шиповатого слоя эпидермиса — спонгиоза. Такая реакция традиционно называется экзематозной и принимает участие в формировании клинической картины многих заболеваний кожи, как инфекционных, так и неинфекционных. В тех случаях, когда после элиминации этиологического фактора проявления заболевания разрешаются полностью, говорят о вторичной экзематизации какого-либо процесса. Это нередко встречается при стрептодермии, микозе стоп, чесотке. В то же время у некоторых пациентов экзематозная реакция возникает первично. Это характерно для контактного аллергического дерматита. В большинстве случаев после устранения аллергена проявления заболевания разрешаются.
В ряде случаев проявления заболевания не разрешаются полностью, а характер его течения становится хронически рецидивирующим. В дальнейшем в качестве провоцирующих обострение болезни выступают различные факторы, действующие как непосредственно на кожу, так и на организм в целом. В таких случаях в России принято говорить об экземе как самостоятельной нозологической единице.
В то же время у значительного количества пациентов имеются указания на проявления атопического дерматита в раннем детском возрасте и на внекожные проявления атопии (атопическая бронхиальная астма, аллергический ринит, поллиноз), выявляется повышение общего и наличие специфических IgE. По-видимому, в таких случаях корректнее говорить об особенном течении атопического дерматита с локализованными экзематозными проявлениями. В настоящее время в специальной литературе вместо термина «атопический дерматит» широко используется термин «атопическая экзема».
Единого понимания термина «экзема кистей» не существует. Однако большинство авторов описывают хроническое поражение кожи кистей, проявляющееся экзематозной реакцией, для которого характерна поливалентная чувствительность, т.е. развитие рецидивов и обострений болезни связывается с различными воздействиями как непосредственно на кожу, так и на организм в целом (химические, физические, метеорологические, психологические стрессы и др.). Заболеваемость экземой, по данным литературы [3, 4], в разных странах составляет 5—20%. Существенную роль в развитии экземы кистей в настоящее время отводят нарушению кожного барьера, что подтверждается, в частности, положительным результатом использования средств базового ухода за кожей [5, 6]. При воспалении в коже нарушаются продукция и секреция липидов кератиноцитами. Следствием этого является увеличение межклеточных промежутков, снижение эластичности кератиноцитов. Повышенная проницаемость кожного барьера приводит к проникновению в кожу как аллергенов, так и ирритантов, еще более усиливающих воспаление. Формирующийся «порочный круг» обеспечивает хронизацию кожного процесса [7, 8].
Многофакторность происхождения экземы кистей в большинстве случаев не позволяет добиться длительной полной ремиссии заболевания и требует подбора постоянной поддерживающей терапии. Многие пациенты без должного врачебного контроля длительно используют топические глюкокортикостероиды (ТГКС), в результате чего формируются местная стероидная зависимость и другие местные побочные эффекты длительного использования препаратов этой группы. Больные другой группы категорически отказываются от применения местных стероидов, позволяя в дальнейшем развиваться бесконтрольному воспалению. Очень часто приходится констатировать, что пациенты с экземой кистей пренебрегают средствами базового ухода за кожей.
Отказ от использования ТГКС значительно удлиняет сроки лечения больных и ухудшает качество их жизни [9].
В настоящее время к препаратам, максимально удовлетворяющим современным требованиям, относится местный стероид мометазона фуроат, обладающий высокой системной безопасностью [10, 11].
Более 10 лет накапливался опыт использования интермиттирующих схем лечения наружными стероидами. Еще в 1999 г. N. Veien и соавт. [12] показали высокую эффективность и безопасность длительной (36 нед) интермиттирующей (препарат назначали по так называемой схеме выходного дня — только в субботу и воскресенье в одной группе и через день — в другой) терапии стероидом для контроля заболевания, особенно при дорсальной локализации проявлений экземы кистей. В более поздних исследованиях было показано, что наиболее хорошие результаты лечения достигаются при сочетании местных ГК и эмолентов [13, 14].
Материал и методы
Под наблюдением находились 34 больных экземой кистей в возрасте от 17 до 62 лет (24 женщины, 10 мужчин; средний возраст 30,45±1,32 года).
Тяжесть проявлений экземы оценивали на основании EASI (Eczema Area Severity Index) по стандартной методике. Если EASI был равен 3—6, то обострение считали нетяжелым, 7—9 — среднетяжелым, 10 и более – тяжелым.
В зависимости от выраженности воспалительных изменений кожи препарат Унидерм (мометазона фуроат 0,1% крем) наносили на пораженные участки кожи 1 раз в сутки до достижения практически полного разрешения высыпаний на коже. В дальнейшем пациентов переводили на интермиттирующую схему использования Унидерма: препарат наносили на пораженные участки кожи в течение 2 дней через 5 сут (2 раза в неделю) на фоне ежедневного использования средств базового ухода (специальный крем или специальную эмульсию для тела Эмолиум). При полном отсутствии проявлений заболевания местно стероиды не наносили, использовали лишь средства базового ухода (крем или эмульсию для тела Эмолиум).
Срок наблюдения за пациентами составил 8 нед. Визиты проводили через 2, 4 и 8 нед лечения.
Результаты и обсуждение
У 25 пациентов были выявлены признаки атопии (начало в раннем детском возрасте, атопические заболевания у кровных родственников, внекожные проявления атопии).
Среди больных экземой кистей без атопии (9 человек) большинство (8) составили пациенты в возрасте 35—62 лет. Среди пациентов данной группы преобладали женщины (8 из 9 человек). Пациентов с тяжелым течением заболевания в этой группе не было, а у абсолютного большинства (у 7 человек, 78%) была диагностирована легкая степень тяжести. В большинстве случаев (у 6 пациентов) заболевание приходилось на острую стадию, характеризующуюся появлением на коже кистей поверхностных сгруппированных микровезикул на фоне гиперемии, мокнутия, сопровождающегося зудом. У оставшихся 3 пациентов экзема была в подострой стадии.
Абсолютное большинство больных (7 человек) отмечали связь развития заболевания с перенесенным психоэмоциональным стрессом (разводом, смертью или болезнью близкого человека, сдачей экзаменов и др.). У 2 пациентов высыпания впервые появились при воздействии экзогенных факторов (строительных материалов, стиральных порошков, щелочных моющих средств с антимикробным действием).
В большинстве случаев экзема кистей с атопией наблюдалась у людей молодого возраста (25—34 лет, средний возраст 29,18±1,4 года). Среди пациентов данной группы также преобладали женщины. В этой группе обострение заболевания расценивалось как тяжелое в 44% случаев, в 29% — средней тяжести и только у 27% пациентов была диагностирована легкая степень тяжести. У 100% больных данной группы была выявлена атопия в анамнезе («детская экзема» или «диатез»). Аллергические заболевания в семейном анамнезе отметил 21 (84%) пациент. Клинически у всех больных были обнаружены признаки атопии, укладывающиеся в общеизвестные критерии J. Hanifin и G. Rajka. У большинства пациентов с экземой кистей с атопией (21 случай) в периоды обострений доминировали симптомы застойной инфильтрации, лихеноидные папулы, лихенификация, выраженная сухость кожи, трещины и шелушение, располагающиеся на тыльной поверхности кожи кистей, тогда как экссудативные проявления с тенденцией к отечности и микровезикуляции были обнаружены лишь у 4 больных. Среди провоцирующих факторов у данной группы больных доминировал психоэмоциональный стресс (в 12 случаях). У 13 пациенток заболевание началось в раннем детстве и по описаниям напоминало младенческую стадию атопического дерматита, затем до определенного возраста у них наблюдалась стойкая ремиссия, и лишь с началом беременности (у 7 женщин) и лактации (5) возник рецидив дерматоза. Обострение заболевания с погрешностями в диете связывали 11 больных, с экзогенными факторами — 2, с профессиональными вредностями — 1, остальные не могли четко указать причину обострений.
Как среди пациентов с экземой кистей без атопии, так и среди больных экземой кистей с атопией, на 1-м месте по частоте встречаемости были заболевания органов желудочно-кишечного тракта (55,6 и 68% случаев соответственно). На 2-м месте у пациентов обеих групп были гинекологические заболевания (22,2 и 32%), на 3-м — заболевания эндокринной системы (11,1 и 12%). Только у 22,2% больных экземой кистей без атопии и у 24% больных экземой кистей с атопией очагов хронических инфекций выявлено не было.
После обследования всем пациентам назначали индивидуальную терапию (системную и наружную) в зависимости от периода заболевания, тяжести патологического процесса, а также от выявленных сопутствующей патологии и провоцирующих факторов. Всем больным были даны общие рекомендации, влияющие на компенсаторные и приспособительные механизмы пациента (диета, режим дня, лечение сопутствующих заболеваний и функциональных расстройств, смена работы, климатолечение и др.). После оценки состояния вегетативной нервной системы назначали вегетокорректоры (длительность приема от 2 нед до 2 мес). При необходимости больные со среднетяжелой и тяжелой степенью тяжести заболевания получали гипосенсибилизирующую и детоксицирующую терапию. Наружно использовали топические глюкокортикоиды. В зависимости от клинической картины заболевания, наличия сопутствующих осложнений крем Унидерм наносили на пораженные участки кожи 1 раз в день не более 14 сут до достижения практически полного разрешения высыпаний на коже. В дальнейшем пациентов переводили на интермиттирующую схему использования ТГКС: препарат наносился на пораженные участки кожи 2 дня подряд с интервалом 5 сут (2 раза в неделю) на фоне ежедневного использования средств базового ухода. При полном отсутствии проявлений заболевания топический стероид не наносили: использовали лишь средства базового ухода.
Как при обострении, так и в период ремиссии заболевания, всем больным экземой кистей были назначены препараты, восстанавливающие целостность кожного барьера (так называемые эмоленты, оказывающие увлажняющее и ожиривающее действие). В нашем исследовании это были косметические средства линии Эмолиум. После курса лечения практически у всех пациентов удалось добиться положительных результатов. У 8 из 9 пациентов с экземой без атопии после достижения ремиссии (для полного разрешения высыпаний потребовалось 4—7 сут непрерывного использования крема Унидерм) и кратковременной (1—2 нед) интермиттирующей терапии полностью удалось отказаться от топических стероидов при условии постоянного использования средств линии Эмолиум. Лишь в одном случае возникла необходимость продолжить интермиттирующую терапию, что можно объяснить контактами с ирритантами в связи с профессиональной деятельностью пациента. В то же время больные, у которых был выявлен атопический фон, оказались более резистентными к проводимому лечению (для разрешения высыпаний потребовалось 6—10 сут ежедневного использования крема Унидерм). Лишь у 13 больных удалось достигнуть стойкой, но неполной ремиссии в течение нескольких недель. В остальных случаях была продолжена интермиттирующая терапия местными стероидами (Унидерм) в течение всего периода наблюдения. Несмотря на проводимое лечение, в 6 случаях не удалось достичь стойкой ремиссии заболевания, что может быть объяснено, в частности, невозможностью полностью устранить провоцирующие факторы.
Таким образом, назначение современного неатрофогенного местного ТГКС Унидерма позволяет быстро подавить гиперергическую реакцию, а интермиттирующая терапия с использованием этого препарата на фоне постоянного применения средств базового ухода за кожей Эмолиум позволяет в большинстве случаев активно бороться с персистирующим воспалением в коже и поддерживать ремиссию экземы кистей. Такая схема лечения может быть рекомендована при длительном течении заболевания с частыми рецидивами.
Выводы
1. Современная терапия экземы кистей должна включать в себя выявление и элиминацию триггерных факторов, активную противовоспалительную терапию даже при минимальных обострениях заболевания и постоянное использование средств базового ухода за кожей.
2. У пациентов с экземой кистей без атопии разрешение кожного процесса происходит быстрее и развивается более стойкая ремиссия, тогда как у пациентов с атопической экземой кистей разрешение высыпаний происходит медленнее и чаще возникают обострения кожного процесса.
3. Интермиттирующая терапия современными местными стероидами (в частности, кремом Унидерм) может быть рекомендована пациентам с длительным течением экземы кистей с частыми рецидивами.
4. Пациенты с экземой кистей нуждаются в постоянном использовании средств базового ухода за кожей.
5. Средства базового ухода за кожей линии Эмолиум соответствуют современным требованиям к этой группе лечебных косметических продуктов.
Для цитирования: Думченко В.В., Орлов М.А., Дорфман И.П. Основные принципы фармакотерапии экземы. РМЖ. 2015;19:1171.
Экзема является распространенным атопическим заболеванием, протекающим с зудом, нарушением сна и качества жизни [31]. Экзема (от греч. еkzeо – вскипаю) – острое или хроническое рецидивирующее аллергическое заболевание кожи, формирующееся под влиянием экзогенных и эндогенных триггерных факторов и характеризующееся появлением полиморфной сыпи, острой воспалительной реакции, обусловленной серозным воспалением кожи, и сильным зудом [21].
Экзема составляет 30–40% всей кожной патологии. Заболевание появляется в любом возрасте, часто протекает остро, реже бывают хронические формы. Острая форма связана с эритемой и отеком. Лихенизация и шелушение – основные черты хронической формы. Это отражает морфологические изменения в коже, происходящие из-за сложного взаимодействия между генетическими и экологическими факторами, что ведет к иммунологическим и биохимическим изменениям, в результате чего появляются воспалительные поражения и зуд [21, 30, 36].
Около 1/3 всех случаев экземы составляет микробная экзема. В последние годы микробная экзема приобрела тенденцию к более тяжелому течению с частыми, продолжительными рецидивами, значительным распространением патологического процесса и характеризуется резистентностью к общепринятым методам лечения [7].
Экзема развивается в результате комплексного воздействия экзогенных и эндогенных факторов, среди которых большое значение имеют генетическая предрасположенность, состояние центральной и периферической нервной системы, наличие сенсибилизации к различным аллергенам, патология внутренних органов, нарушения функции желудочно-кишечного тракта, эндокринной системы, очаги хронической инфекции (холециститы, аднекситы, ЛОР-патология) и др. [8, 11].
Согласно современным представлениям, в механизме развития микробной экземы большую роль играет сенсибилизация к микробным антигенам на фоне изменения иммунной системы. Микробные аллергены обладают достаточно выраженной антигенной активностью, что ведет к сенсибилизации организма. В норме микробная флора кожи является непатогенной и участвует в бактериальной защите кожи за счет подавления патогенных штаммов непатогенными. Микрофлора кожи включает резидентную (Staphylococcus (S.) epidermidis, S. aureus, Micrococcus spp., Sarcina spp., коринеформные бактерии, Propionibacterium spp.) и транзиторную, представленную условно-патогенными и патогенными микроорганизмами [2]. Значительная часть микроорганизмов погибает под действием бактерицидной среды кожи (кислая реакция, жирные кислоты кожного сала, лизоцим) и не проникает через неповрежденный кожный барьер [7]. В связи с нарушением защитной функции кожи и изменением количества и качества липидов кожи у пациентов с экземой может развиваться бактериальная инфекция [27, 30]. Таким образом, ведущую роль в возникновении заболевания на фоне генетически детерминированной наследственной предрасположенности играет изменение микробного пейзажа – преобладание стафилококковой и стрептококковой флоры, а также грибов рода Candida [20].
По данным отечественных исследований, при соскобах с очагов поражения кожи у больных экземой в 80% случаев высевается S. аureus, в 14% – S. haemolyticus, в 40,7% – нелипофильные дрожжи рода Candida [5]. На участках экссудации и мокнутия количество микроорганизмов может достигать 1×107 на 1 см2. Токсины, секретируемые S. aureus (энтеротоксины А и В, токсин синдрома токсического шока), являются суперантигенами, стимулирующими одновременно несколько звеньев иммунного ответа [20]. У 57% больных в сыворотке крови выявлялись антитела к стафилококковым энтеротоксинам А, В, С и токсину синдрома токсического шока. Показано, что наиболее реактогенными свойствами обладает энтеротоксин В, и установлена взаимосвязь между тяжестью поражения кожи и сенсибилизацией к этому токсину [5, 9, 13]. Они связываются с b–цепью Т-клеточного рецептора и молекулой главного комплекса гистосовместимости II класса и активируют целое семейство клонов Т-лимфоцитов, что приводит к повышенной продукции провоспалительных цитокинов и усиливает реакцию аллергического воспаления. Бактериальная колонизация кожи S. aureus и высвобождение им энтеротоксинов – одна из причин формирования резистентности к стероидной терапии [13, 20, 29, 33, 34].
В двойном слепом многоцентровом рандомизированном контролируемом исследовании была продемонстрирована корреляция между тяжестью экземы и колонизацией S. aureus, и установлено, что бактериальная колонизация является важным фактором обострения кожных поражений [25]. Таким образом, микробная сенсибилизация является пусковым, поддерживающим и отягчающим фактором у больных экземой [3].
Лечение экземы проводят комплексно, с учетом формы и стадии заболевания, степени выраженности процесса, эндогенных и экзогенных факторов, лежащих в основе развития болезни [7, 12, 18, 23, 24]. Терапию экземы начинают с ограничения контактов с выявленными и потенциальными аллергенами и ирритантами. При всех формах экземы назначают общую гипосенсибилизирующую терапию, включающую антигистаминные препараты. Основными целями лечения являются предотвращение прогрессирования заболевания, уменьшение зуда, разрешение высыпаний, профилактика рецидивов [21].
Особое место в комплексном лечении микробной экземы занимает наружная терапия. Местное лечение определяется клинической картиной экземы. Наружная терапия проводится длительно и поэтапно, причем на разных стадиях используют различные лекарственные формы. Неизменным остается принцип местной терапии: «на мокрое – мокрое, на сухое – сухое» и «раздраженное не раздражать». Традиционно применяют примочки, влажно-высыхающие повязки. В связи с этим в стадии мокнутия применяются примочки, влажно-высыхающие повязки из антисептических и вяжущих растворов, аэрозоли с кортикостероидами для подавления признаков острого воспаления – гиперемии, отека, экссудации, зуда и болезненности [7, 11].
При обильном мокнутии, которое встречается обычно при истинной экземе (острой или обострении подострой и хронической), назначают примочки или влажно-высыхающие повязки из антисептических растворов, а при необильном, но упорном мокнутии – из вяжущих растворов. К антисептическим относятся растворы борной кислоты (Sol. ac. borici 1%, 2% и 3%), риванола (Sol. rivanoli 1:1000–1:4000), резорцина (Sol. resorcini 1–2%), фурацилина (Sol. furacilini 1:5000), марганцовокислого калия (Sol. Kalii hypermanganici 1:5000). Последний раствор обладает к тому же дезодорирующим свойством. Раствор резорцина выписывают в темном флаконе, т. к. на свету резорцин быстро разлагается. Группу вяжущих растворов составляют свинцовая вода (Aq. plumbi), буровская жидкость (Liq. Burovi; Liq. aluminii acetici 1–2 ст. ложки на 1 стакан воды), раствор ляписа (Sol. Argenti nitrici 0,1–0,25%), гулярдова вода (Ac. borici 6,0; Sp. aethylici 4,0; Aq. plumbi 200,0). Раствор ляписа, как и раствор резорцина, следует выписывать в темном флаконе.
Выбирая раствор для примочки или влажно-высыхающей повязки, необходимо учитывать следующие факторы. При осложнении, вызванном импетигинизацией процесса, показаны антисептические растворы, в первую очередь риванола и фурацилина. В случаях, сопровождающихся сильным зудом, хороший эффект дает гулярдова вода. При мокнущих формах микробной экземы и дисгидротической экземе показаны растворы более крепких концентраций: Sol. ac. borici 3%; Sol. resorcini 3%; Sol. rivanoli 1:1000 и др. Для примочек пожилым и ослабленным больным используют растворы слабых концентраций, т. к. крепкие могут вызывать у них жжение и болезненность. Иногда подобные больные плохо переносят и слабые концентрации. В таких случаях применяют примочки из различных растительных настоев: шалфея, ромашки, череды, чая и др. Что касается вяжущих средств, то обычно их назначают вслед за антисептическими растворами, когда в значительной степени стихли явления воспаления, однако продолжает держаться хотя и необильное, но упорное мокнутие. Наложение примочек из крепких растворов вяжущих средств на обширные очаги мокнутия с выраженными явлениями воспаления может привести к обострению и распространению процесса, что объясняется образованием пленки, препятствующей оттоку серозной жидкости и, следовательно, способствующей ее всасыванию (аутосенсибилизация). Особенно опасны в этом отношении настой коры дуба и раствор танина.
При угасании мокнутия назначают кремы и последовательно мази, содержащие кортикостероидные гормоны. При хронической экземе вне обострений лечение начинают с кремов или мазей. На очаги хронической экземы, покрытые сухими корками и обильными чешуйками, а также на очаги дисгидротической экземы наносят кремы и мази, содержащие и кортикостероидные гормоны, и салициловую кислоту. Салициловая кислота способствует отпадению корок и чешуек и более глубокому проникновению кортикостероидных гормонов в ткани очагов поражения [15].
Эффективность примочек и влажно-высыхающих повязок в острой стадии экземы не вызывает никакого сомнения, однако не всегда больные готовы в домашних условиях делать растворы и проводить методично по несколько раз в день процедуры с применением примочек [11]. Большинство классических растворов, паст, мазей имеют резкий и неприятный запах, пачкают и окрашивают белье и одежду, что ограничивает их применение, особенно в амбулаторной практике. Использование растворов требует применения повязок, которые мешают движению больных, ограничивая их повседневную и профессиональную деятельность. Действие примочек, паст, мазей развивается относительно медленно, требует госпитализации больных и проведения длительного поэтапного лечения [1]. Современный пациент ожидает от наружного лечения не только быстрого облегчения воспалительных и субъективных симптомов заболевания, сокращения сроков болезни, но и удобного и приятного терапевтического воздействия, не ограничивающего его социальную и профессиональную активность, и, как следствие этого, существенного улучшения качества жизни. Поэтому в современной клинической практике значительно возросли требования к лекарственным препаратам, используемым в терапии хронических дерматозов. Препарат должен обладать активным противовоспалительным действием, хорошо переноситься, иметь высокий профиль безопасности, обладать пролонгированным действием, не требующим многократного применения, быть эстетически привлекательным и не ограничивать привычный образ жизни [4, 19].
Во многом этим критериям соответствуют топические кортикостероидные препараты. Наружные глюкокортикостероиды, впервые появившиеся в терапевтическом арсенале дерматологов в середине прошлого века, в настоящее время являются базовой терапией воспалительных дерматозов. До настоящего времени им не существует терапевтической альтернативы по скорости наступления и выраженности (активности) противовоспалительного действия. Топические кортикостероиды обладают высокой противовоспалительной, противоаллергической, иммуносупрессивной активностью, а также сосудосуживающим и антимитотическим эффектом [22, 28]. Эти препараты, обладая мощным патогенетическим воздействием, позволяют быстро уменьшить воспалительные изменения кожи, в короткий срок снизить или устранить субъективные симптомы дерматозов (зуд, жжение).
Улучшение кожного статуса, несомненно, положительно сказывается на психоэмоциональном состоянии пациентов, восстановлении трудоспособности и повседневной активности, что значительно повышает их качество жизни. Успех терапии во многом определяется правильным выбором стероида с учетом его активности и методики применения в зависимости от характера, стадии течения, локализации дерматоза [4]. Согласно Европейской классификации потенциальной активности различают слабые (класс 1), средние (класс 2), сильные (класс 3), очень сильные (класс 4) стероиды. При остром воспалении, характеризующемся отеком, гиперемией, мокнутием, целесообразно использовать средние, сильные, реже – очень сильные топические кортикостероиды (уровни доказательности А, В). По мере уменьшения выраженности воспаления применяют средние и слабые кортикостероиды (уровни доказательности А, В) [16].
Большое значение имеет правильный выбор лекарственной формы препарата, определяющей активность всасывания стероида и рациональность проводимой наружной терапии (табл. 1). Одной из наиболее распространенных ошибок при назначении топических кортикостероидов является выбор препарата без учета топографических и морфофункциональных особенностей кожи, а также активности всасывания наружных средств на различных участках кожного покрова. Всасывание наружных лекарственных средств напрямую зависит от строения (толщины) эпидермиса. Сравнительные исследования выявили существенные различия всасывания одного и того же лекарственного препарата, наносимого на разные области кожи. Таким образом, одним из критериев выбора наружного стероида является локализация очага воспаления. На участки тонкой кожи (лица, половых органов, сгибательных поверхностей) предпочтительнее нанесение стероидов умеренной потенции. Следует учитывать, что наносить препараты, содержащие сильные стероиды, на вышеуказанные области кожи, относящиеся к зонам повышенной чувствительности к глюкокортикостероидам, крайне нежелательно, т. к. это может привести к высокому риску развития как местных побочных эффектов (атрофии, телеангиэктазии и др.), так и системных, а также активизации инфекционных агентов [4].
С учетом важной роли инфекционных агентов в патогенезе экземы, в частности микробной экземы, перед врачом стоит задача в максимально короткие сроки не только снять воспаление и субъективные симптомы, но и подавить сенсибилизацию к бактериальным и грибковым антигенам, нормализовать количество и состав микрофлоры кожи [7]. Инфекционные агенты могут не только способствовать развитию заболевания, но и осложнять его течение. В связи с этим в плане наружной терапии к топическим глюкокортикостероидам нужно присоединять препараты с антимикробными и противогрибковыми свойствами. Можно использовать последовательно несколько препаратов, но более предпочтительным является наружное применение комбинированных средств, которое обладает противовоспалительным, антибактериальным и противогрибковым действием [20].
Что касается антимикробного компонента, то необходимо отметить, что традиционно назначаемые комбинированные наружные глюкокортикостероиды содержат такие действующие вещества, как гентамицин, тетрациклин, клотримазол, натамицин, к которым многие возбудители бактериально-грибковых инфекций оказываются малочувствительными. В настоящее время неэффективность применения традиционных схем терапии дерматозов сочетанной этиологии в первую очередь связана с развитием устойчивости возбудителей к назначаемым препаратам [6]. Так, по данным проведенного в России микологического исследования чувствительности нозокомиальных штаммов S. aureus к длительно используемым в клинической практике антибиотикам, выявилась резистентность к гентамицину у 31% выделенных штаммов и к тетрациклину – у 37%. Таким образом, более чем у 1/3 пациентов применение этих препаратов в качестве антимикробной терапии не дает ожидаемого лечебного эффекта [14, 17]. В другом исследовании [32] у 87% больных хронической экземой и атопическим дерматитом при посевах с очагов поражения были обнаружены MRSА (methicillin-resistant S. aureus – метициллин-устойчивый золотистый стафилококк) штаммы. Группу риска по обсемененности MRSА составили больные с длительным течением дерматоза, пожилые пациенты, отягощенные соматическими заболеваниями (сахарный диабет, хронические инфекции легких и ЛОР-органов), а также часто и длительно пребывающие на стационарном лечении. При этом у женщин активность бактериального обсеменения кожи MRSA была выше, однако тяжелее инфекция протекала у мужчин [5]. По данным микробиологических исследований [10], устойчивость к гентамицину MRSA-штаммов составляет 56%. При выборе комбинированного глюкокортикостероида следует ориентироваться прежде всего на противоинфекционную эффективность его действия. Нерациональный выбор препарата приводит к дальнейшему повышению резистентности микроорганизмов, отсутствию эффекта от терапии и ухудшению течения кожного процесса [5].
Учитывая, что у 90% пациентов основным бактериальным агентом является S. aureus [25], к тому же в большинстве случае выделяются MRSА-штаммы, также резистентные к гентамицину, необходимо использовать препарат, обладающий достаточной антибактериальной активностью против таких возбудителей. Фузидовая кислота является сильным антибактериальным препаратом и ингибирует почти все штаммы золотистого стафилококка, включая S. aureus, S. epidermidis и метициллин-резистентные штаммы, стрептококков и других патогенных микроорганизмов. Препарат действует как ингибитор синтеза белка в бактериальной клетке, обладает бактериостатическим или бактерицидным действием в зависимости от размера инокулята. Местное применение фузидовой кислоты является безопасным и эффективным в лечении бактериальных инфекций кожи [17, 26, 30]. Развитие устойчивости к ней в целом остается низким или непродолжительным и может быть сведено к минимуму, если ограничить терапию курсом не более 14 дней [35]. Перекрестной резистентности, так же, как и перекрестной чувствительности, к фузидовой кислоте нет, т. к. это единственный антибиотик в своей группе. Лечебная эффективность при местном применении фузидовой кислоты обусловлена уникальной способностью глубоко проникать в кожу и накапливаться в дозировке, в разы превышающей минимальную терапевтическую.
Фузидовая кислота успешно использовалась вместе с кортикостероидами (бетаметазоном и гидрокортизоном). Гидрокортизона ацетат – мягкий кортикостероид его предпочтительнее применять при легкой степени поражения. Бетаметазон относится к группе сильных глюкокортикостероидов (группа III), что позволяет назначать его при выраженном воспалении [17]. Данные препараты особенно эффективны в лечении микробной экземы, т. к. их действие направлено на лечение как воспаления, так и инфекции. Использование антибиотиков и кортикостероидов как по отдельности, так и в фиксированных комбинациях дает хороший терапевтический эффект при экземе и также снижает колонизацию золотистого стафилококка. Раннее начало комбинированной топической терапии является необходимым для пациентов с экземой средней и тяжелой степени и уменьшает необходимость использования антибиотиков на более поздних стадиях заболевания [25]. Назначение одного лекарственного препарата, обладающего широким терапевтическим диапазоном, заменяющего несколько медикаментозных средств, позволяет исключить полипрагмазию, избежать побочных действий и нежелательных взаимодействий между препаратами, уменьшить затраты и повысить комплаентность пациентов [4].
Комплексный подход в терапии экземы позволит уменьшить выраженность воспаления, сопровождающегося зудом и экссудацией, причиняющими больному значительные страдания, и тем самым окажет благоприятное влияние на качество жизни пациентов.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
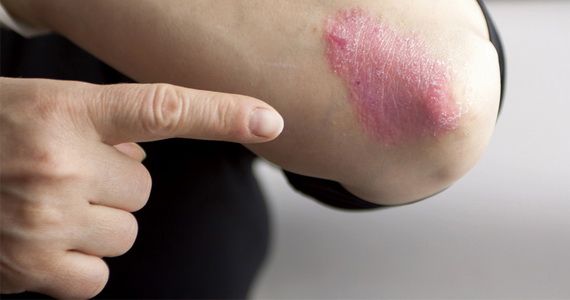
Рассматривая, какие мази применяют при дерматите, стоит сразу сказать, что они делятся на две большие группы: гормональные и негормональные. Они отличаются не только составом, но также степенью эффективности и безопасности.
Мазь считают лучшей от дерматита на коже у конкретного пациента, если она отвечает ряду требований:
- эффективно снимает жжение и зуд;
- купирует острые и хронические воспалительные процессы;
- увлажняет кожу;
- снижает выраженность болевых ощущений;
- препятствует проникновению в очаги воспалений вирусов, грибков и бактерий (об этом говорит отсутствие вторичных присоединившихся инфекций).
Какими негормональными мазями можно лечить дерматит
Негормональные мази считают более безопасными, поскольку они имеют относительно натуральный состав. Это позволяет использовать наружное средство в течение длительного времени без какого-либо вреда для здоровья.
Именно негормональные мази считают лучшими при атопическом дерматите у ребенка. У взрослых в большинстве случаев в начале лечения врачи тоже стараются назначать именно такие мази. По принципу действия они делятся на несколько групп:
- Антисептические. Действие направлено на то, чтобы обеззаразить кожу и исключить проникновение бактерий через образующиеся язвочки.
- Противовоспалительные. Направлены на снятие зуда и раздражения, устранение воспалительных процессов.
- Увлажняющие. Косвенно способствуют выздоровлению за счет восстановления водного баланса кожи.
- Регенерирующие. Их основное действие – стимуляция процессов заживления за счет активации естественной регенерации кожного покрова.
Поскольку средства с одним основным веществом могут снимать только один симптом, врачи часто назначают комбинированные мази. Они за счет нескольких активных компонентов могут оказывать не одно, а несколько эффектов. Примеры негормональных препаратов, претендующих на роль самой хорошей мази от дерматита:
- Бепантен,
- Пантенол,
- Цинковая мазь,
- Радевит,
- Видестим,
- Левосин,
- Фенистил,
- Топикрем.
Из плюсов негормональных мазей особое значение имеет минимум побочных эффектов. Еще большинство из них разрешены к применению у детей, беременных и кормящих женщин.
Главным минусом негормональных мазей часто выступает недостаточная эффективность. Из-за этого лечение может затянуться на несколько недель, месяц и даже дольше. При этом курс нельзя прерывать, иначе предыдущая терапия может оказаться неэффективной. В результате врачу все-таки приходится назначать более сильные гормональные средства.
Выбирая, какая мазь лучше от дерматита, нельзя игнорировать и другие недостатки негормональных мазей:
- могут вызывать аллергию у людей, склонных к аллергическим проявлениям;
- проявляют свое действие не при всех видах дерматита, чаще при контактном и аллергическом.
То есть при длительном лечении мазь вызывает аллергию, но при этом может не давать нужного эффекта.
Гормональные мази
Когда отсутствует положительная динамика от применения негормональных мазей, специалисты прибегают к гормональным препаратам. В их составе основным компонентом выступают глюкокорстикостероиды – гормоны, которые в теле человека вырабатываются надпочечниками. В основе механизма действия таких препаратов лежит влияние на обмен белков и углеводов. Гормональные мази восстанавливают уровень кортизона, при недостатке которого организм становится неспособен справляться с воспалительными процессами.
В зависимости от степени воздействия на кожу гормональные мази делятся на несколько категорий:
- слабые,
- средние,
- сильные,
- очень сильные.
Последние используют только при самых тяжелых формах дерматита, поэтому первыми их никогда не назначают. Примеры гормональных мазей:
- Гидрокортизоновая,
- Целестодерм,
- Акридерм,
- Адвантан,
- Элоком,
- Дермовейт,
- Фуцикорт.
Главные недостатки гормональных мазей при лечении дерматита:
- Привыкание. Самый главный минус, который заключается в том, что со временем мазь перестает быть эффективной для лечения конкретного пациента. Одни и те же активные компоненты гормональных мазей вызывают привыкание.
- Побочные эффекты. Ввиду гормональной природы такие мази имеют множество неприятных побочных действий. Они проявляются при неправильном или слишком долгом применении. В тяжелых случаях может развиться атрофия кожи и даже недостаточность надпочечников.
- Наличие синдрома отмены. Как и в случае с негормональным, при использовании гормональных мазей нельзя прерывать курс и пропускать нанесение. Особенно сильно синдром отмены проявляется при резком отказе от гормонального средства. Это проявляется в том, что симптомы дерматита могут внезапно вернуться. По этой причине гормональные средства отменяют постепенно, уменьшая дозу и количество нанесений.
- венерические заболевания;
- туберкулез;
- беременность и лактацию;
- герпес;
- бактериальные или грибковые поражения кожи.
Какую же мазь использовать
Как видно из обзора мазей от дерматита, и гормональные, и негормональные средства нельзя назвать идеальными для лечения такого заболевания. Клиника «ПсорМак» предлагает в качестве альтернативы и эффективную, и безопасную мазь. Она создана по собственной рецептуре и показывает свою эффективность уже в течение более 25 лет.

В составе мази отсутствуют гормоны. Вместо них только натуральные природные компоненты, которые делают мазь безопасной для детей, беременных и кормящих. Мазь не вызывает побочных эффектов, не приводит к аллергии и обострению симптомов.
Кроме того, мы комплексно подходим к лечению заболевания, прибегая к всесторонней работе с пациентом путем психотерапии, игло- и гирудотерапии. Еще мы разрабатываем для пациентов индивидуальную диету. Такой подход позволяет добиться стойкой ремиссии до 6 лет, что подтверждают отзывы и результаты лечения наших пациентов.
Читайте также:

